Основные аспекты патогенеза преждевременного разрыва плодных оболочек (ПРПО) как при доношенной, так и при недоношенной беременности пока до конца не изучены; нет четкого представления, едины ли механизмы ПРПО при недоношенной и доношенной беременности или это разные процессы. Детализация звеньев патогенеза ПРПО при доношенной беременности позволит разработать эффективные стратегии для коррекции данного осложнения, в том числе и при преждевременных родах. Важную роль в разрыве плодных оболочек играет дисбаланс иммунологических показателей, которые участвуют как в реализации инфекционно-воспалительного процесса, так и в развитии асептического воспаления при физиологических родах [1]. При ПРПО и доношенной беременности доказаны: повышение уровня провоспалительных цитокинов в сыворотке крови [2] и околоплодных водах, рецепторов врожденного иммунитета [3, 4]; активация экспрессии матриксных металлопротеиназ и снижение их ингибиторов [5, 6], увеличение сосудистых факторов роста [7]. Продукция цитокинов, как правило, кратковременна и регулируется различными стимулами на уровне транскрипции и трансляции, а радиус их действия обычно ограничен небольшими участками [8]; соответственно, изучение уровня цитокинов с помощью иммуноферментного анализа из отдаленных от плодных оболочек локусов менее информативно, чем их локальное определение. Внедрение современных молекулярно-биологических методов исследования, основанных на полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР), мРНК генов непосредственно в изучаемом очаге, позволяет иначе взглянуть на изменения иммунологических параметров при различных патологических и физиологических процессах.
Цель исследования: оценить уровни экспрессии мРНК генов провоспалительных (интерлейкин (ИЛ)-1β, ИЛ-6, ИЛ-8, ИЛ-17А, ИЛ-18, ИЛ-23, фактор некроза опухоли (TNF)α, интерферон (IFN)-γ) и противовоспалительных (ИЛ-4, ИЛ-10, трансформирующий фактор роста (TGF)β) цитокинов в плодных оболочках при их преждевременном разрыве при доношенной физиологически протекающей беременности.
Материалы и методы
В ходе исследования на клинической базе ФГБОУ ВО СамГМУ Минздрава России (CГКБ №1 им. Н.И. Пирогова) обследованы 40 беременных с доношенной беременностью: 24 из них вошли в основную группу и 16 – в группу сравнения.
Критерии включения в основную группу: срок беременности 37,0–41,0 недели, ПРПО, наличие показаний к кесареву сечению (неправильное положение/предлежание плода и/или рубец на матке после операции кесарева сечения).
Критерии включения в группу сравнения: беременность 37,0–41,0 недели без отхождения околоплодных вод – плановое кесарево сечение (неправильное положение/предлежание плода и/или рубец на матке после операции кесарева сечения).
Критерии исключения: беременные, относящиеся к группе высокого риска (согласно Порядку оказания медицинской помощи по профилю «акушерство и гинекология» (приказ Минздрава России от 1 ноября 2012 г. № 572н)) с соматическими или акушерскими осложнениями: сахарный и гестационный диабет, повышенное артериальное давление, задержка внутриутробного развития, вагинальное кровотечение, предлежание плаценты, подозрение на макросомию плода, внутрипеченочный холестаз, многоплодная беременность, мекониальное окрашивание околоплодных вод, признаки острой инфекции и обострения хронической инфекции, наличие кольпита.
Методом количественной ОТ-ПЦР в режиме реального времени выполнено определение уровней экспрессии мРНК генов провоспалительных (ИЛ-1β, ИЛ-4, ИЛ-6, ИЛ-8, TNFα, ИЛ-17А, ИЛ-18, ИЛ-23, IFN-γ) и противовоспалительных (ИЛ-4, ИЛ-10, TGFβ) цитокинов плодных оболочек у всех обследованных на базе лаборатории молекулярно-генетических методов ООО «ДНК-Технология» согласно инструкциям производителя («ДНК-Технология», Россия). Образцы плодных оболочек забирались интраоперационно в стерильных условиях в пределах операционного поля с помощью конхотома с диаметром рабочей поверхности 9,4 мм посередине между плацентой и внутренним зевом. Полученные образцы помещались в пробирки типа «эппендорф» с транспортной средой («Проба-НК» производства ООО «НПО ДНК-Технология»). Нормировка уровня экспрессии генов выполнена с использованием метода сравнения индикаторных циклов (метод ΔCq) по одному референсному гену B2M, в относительных единицах (ОЕ), отражающих представленность транскрипта относительно нормировочного фактора. В качестве меры центральной тенденции количественных признаков выбрана медиана (Me), а в качестве интервальной оценки – верхний (Q1) и нижний (Q3) квартили.
Перед началом исследования у всех обследованных получено письменное согласие; исследование проведено через комитет по биоэтике ФГБОУ ВО СамГМУ Минздрава России (протокол №207 от 19 мая 2017 г.). Расчет гестационного срока выполнялся по первому ультразвуковому исследованию или по первому дню последней менструации.
Статистический анализ
Для оценки результатов исследования применены программы Statistica 10.0, SPSS 13. Количественные данные представлены в виде среднего (M) и стандартного отклонения (SD) при условии соответствия нормальному распределению, при несоответствии нормальному распределению – в виде медианы (Ме) и верхнего (Q1) и нижнего (Q3) квартилей. Оценка соответствия нормальному распределению выполнена с помощью критерия Шапиро–Уилка. Для сравнения количественных переменных, не соответствующих нормальному распределению, применен непараметрический U-критерий Манна–Уитни для несвязанных совокупностей. Для расчета статистической значимости различий качественных признаков применяли критерий χ² Пирсона, в случае четырехпольной таблицы – с поправкой Йейтса. Статистически значимыми считали различия при уровне значимости p<0,05.
Результаты
Клинико-демографические характеристики обследуемых представлены в таблице 1.
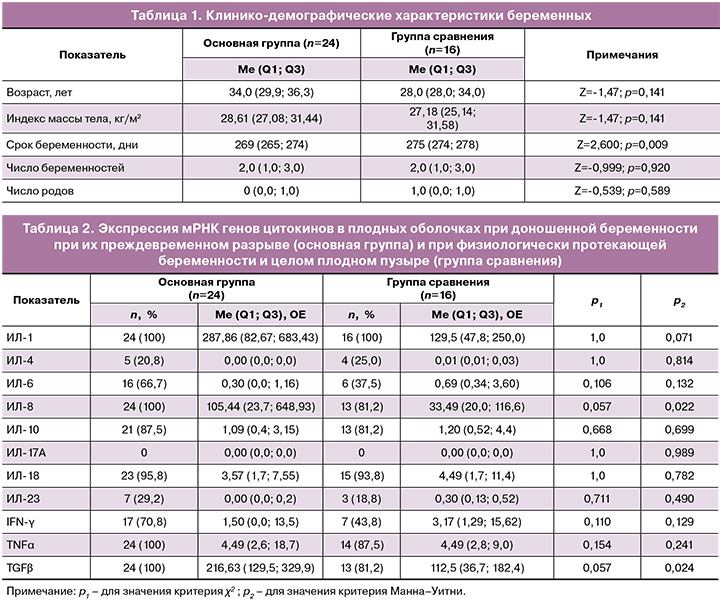
Группы были сопоставимы между собой по возрасту, конституциональным особенностям; беременных с индексом массы тела более 30 кг/м2 в основной группе было 8/24 (33,3%) и 6/16 (37,5%) – в группе сравнения (р=0,946). Срок беременности в основной группе к моменту родоразрешения был значимо меньше по сравнению с группой сравнения, что вполне объяснимо: на плановое родоразрешение пациентки группы сравнения поступали после достижения 39 недель, а в основной группе момент отхождения околоплодных вод регламентировал более ранние сроки родоразрешения. По паритету беременностей и родов значимых различий в группах выявлено не было. Частота первых родов в основной группе составила 16/24 пациенток (66,7%), в группе сравнения – 7/16 (43,8%), р=0,267.
Анализ особенностей экспрессии мРНК генов цитокинов на плодных оболочках представлен в таблице 2.
Из таблицы видно, что по частоте экспрессии мРНК генов цитокинов значимых различий для исследуемых показателей выявлено не было. Экспрессия мРНК генов большинства провоспалительных цитокинов (ИЛ-1β, ИЛ-8, ИЛ-18, TNFα) наблюдалась практических у всех обследованных обеих групп, за исключением экспрессии мРНК гена ИЛ-17, который не определялся ни у одной пациентки; ИЛ-23 выявлен только у 7/24 (29,2%) пациенток основной группы и у 3/16 (18,8%) – группы сравнения в крайне низком количественном соотношении. Экспрессия мРНК генов ИЛ-6 и IFN-γ наблюдалась несколько чаще: у 16/24 (66,7%) и 17/24 (70,8%) – в основной группе; у 6/16 (37,5%) и 7/16 (43,8%) – в группе сравнения соответственно. Из исследованных противовоспалительных цитокинов наиболее часто представлена экспрессия мРНК генов ИЛ-10 – 21/24 (87,0%) и 13/16 (81,2%) в основной группе и в группе сравнения соответственно и TGFβ – 24/24 (100,0%) и 13/16 (81,2%) соответственно. Экспрессия мРНК гена ИЛ-4 нехарактерна для плодных оболочек и выявлена только у 5/24 (20,8%) и 4/16 (25,0%) на крайне низком уровне.
Значимые различия в группах были получены только для экспрессии мРНК генов универсального хемоаттрактанта ИЛ-8 – 105,44 (23,7; 648,93) ОЕ и 33,49 (20,0; 116,6) ОЕ и противовоспалительного цитокина TGFβ – 216,63 (129,5; 329,9) ОЕ и 112,5 (36,7; 182,4) ОЕ в основной группе и группе сравнения соответственно.
Для остальных изучаемых показателей полученные различия были статистически не значимы.
Обсуждение
Плодные оболочки играют важную роль в обеспечении коммуникаций между клетками миометрия и плодом, т.к. являются гораздо большей по площади рецепторной поверхностью по сравнению с плацентой и участвуют в поддержании гомеостаза амниотической жидкости. В исследовании Hadley E.E. et al. (2018) было показано, что экзосомы эпителиальных клеток амниона приводят к усилению воспалительной реакции в децидуальной оболочке матки, тогда как клетки плаценты проявляют рефрактерность. Экзосомы эмбриональных клеток могут сигнализировать о родах, усиливая асептическое воспаление в децидуальной оболочке и запуская процесс родов [8]. Важная роль в процессах асептического воспаления отводится TGFβ, принадлежащему к противовоспалительным цитокинам и представляющему собой белок, который контролирует пролиферацию, клеточную дифференцировку и другие функции в большинстве клеток [9]. По данным литературы, TGFβ запускает эпителиально-мезенхимальный переход, который ослабляет прочность фетальных мембран в норме в первом периоде родов при доношенной беременности и преждевременно – при различных патологических состояниях [10]. Эпителиально-мезенхимальный переход в амнионе чаще происходит по мере увеличения срока беременности, а также в ответ на выработку провоспалительных цитокинов или окислительный стресс, который усиливает ремоделирование и приводит к механическому ослаблению фетальных мембран [11, 12]. Более того, мезенхимальные клетки амниона более чувствительны к провоспалительным стимулам, что еще больше способствует разрыву мембраны и выработке утеротонических факторов, включая простагландины. Таким образом, контролируемые и правильно рассчитанные по времени изменения фенотипа клеток амниона имеют решающее значение как для поддержания беременности, так и для запуска родов. Считается, что эпигенетические события (например, оксидативный стресс, провоспалительные стимулы, ишемия плаценты и плодных оболочек), влияющие на паттерны экспрессии генов за счет модификации гистонов и снижения экспрессии микроРНК, способствуют гестационной трансформации по типу провоспалительного фенотипа клеток амниона и децидуальной оболочки [10, 13]. В нашем исследовании наблюдалось увеличение экспрессии мРНК генов TGFβ в плодных оболочках при их преждевременном разрыве, практически в 2 раза превышающее экспрессию мРНК генов TGFβ в группе сравнения, что можно считать важным элементом патогенеза ПРПО при доношенной беременности.
Ряд авторов демонстрируют повышение экспрессии мРНК генов ряда провоспалительных цитокинов как в реализации процесса родовой деятельности, так и в разрыве фетальных мембран [1, 14]. Нами продемонстрировано, что при доношенной беременности, независимо от целостности плодного пузыря, наблюдается постоянный уровень экспрессии мРНК генов следующих провоспалительных цитокинов: ИЛ-1β, ИЛ-18, TNFα и противовоспалительного ИЛ-10; однако значимых различий в группах выявлено не было. Экспрессия мРНК генов ИЛ-6 наблюдалась далеко не у всех пациенток в нашем исследовании (16/24 (66,7%) – в основной группе и 6/16 (37,5%) – в группе сравнения, р=0,106). Большинство источников свидетельствует, что ИЛ-6 является в большей степени маркером септического процесса и к ключевым участникам родового акта и разрыва плодных оболочек не относится [1, 15, 16], что косвенно подтверждают полученные результаты. Пациентки не имели родовой деятельности, экспрессия мРНК генов ИЛ-6 значимо не отличалась в группах и, вероятно, являлась маркером субклинического воспалительного процесса в плодных оболочках; однако никаких клинических признаков ни у матери, ни у новорожденного выявлено не было.
Согласно литературным источникам, в патогенезе ПРПО при доношенной беременности важную роль играет ИЛ-8 в фетальных мембранах [17], что подтверждено результатами нашего исследования: при ПРПО наблюдалось повышение экспрессии мРНК гена ИЛ-8, определяющего миграцию нейтрофилов, макрофагов. ИЛ-8 усиливает экспрессию матриксных металлопротеиназ в мембранах плода. В своей работе мы наблюдали повышение уровня экспрессии мРНК гена ИЛ-8, который, вероятно, активировал экспрессию матриксной металлопротеиназы 8, разрушающей внеклеточный матрикс, что вело к расслоению плодных оболочек и их разрыву.
При доношенной неосложненной беременности экспрессия мРНК гена ИЛ-17 не характерна для плодных оболочек, а также не участвует в патогенезе ПРПО; экспрессия мРНК гена ИЛ-17 продемонстрирована в исследованиях преэклампсии и задержки роста плода [14]. Доказано, что ИЛ-17, как и некоторые другие провоспалительные цитокины (TNFα и IFN-γ), обладает эмбриотоксическим и антитрофобластным действиями [15]. ИЛ-17 активируется в присутствии липополисахаридов (компонентов клеточной стенки бактерий) либо при аутоиммунных процессах [16].
Заключение
Вне зависимости от целостности плодного пузыря, в плодных оболочках выявлена высокая частота экспрессии мРНК генов ИЛ-1, ИЛ-8, ИЛ-18, TNFα (100%); отсутствовала экспрессия мРНК гена ИЛ-17, и крайне редко в низких титрах наблюдалась экспрессия мРНК гена ИЛ-4. При ПРПО на плодных оболочках происходит активация экспрессии мРНК гена ИЛ-8, являющегося хемоаттрактантом для нейтрофилов и макрофагов и активатором металлопротеиназ, в 3,1 раза (р=0,022), а также активация экспрессии мРНК гена TGFβ, способствующего эпителиально-мезенхимальному переходу в плодных оболочках, – в 1,9 раза (р=0,024), что делает их более чувствительными к воздействию провоспалительных цитокинов и простагландинов и, соответственно, приводит к их истончению и ослаблению.



