ВВЕДЕНИЕ
Расширение показаний к проведению дентальной имплантации, в частности, у больных с аутоиммунной патологией, ревматоидными заболеваниями в анамнезе, повышает риск возникновения осложнений при выборе метода стоматологического лечения с помощью дентальных имплантатов, а также увеличивает вероятность проявления аллергических реакций, особенно при сопутствующем, не выявленном ранее аллергоанамнезе у пациента.
Очевидно, что воспаление, связанное с аутоиммунными заболеваниями и хронической интоксикацией металлическими наночастицами, является инициирующим событием, приводящим к дегенерации и дисфункции тканей. Воспалительные моноциты и нейтрофилы системно циркулируют и проникают в воспаленную ткань, а фармакологическое воздействие на эти клетки существенно не улучшает результаты и приводит к возникновению осложнений [1].
При анализе литературы обнаружены противоречивые данные об отрицательном действии металлических нано- и микрочастиц TiO2 (НРМЧ) на слизистую оболочку полости рта в эксперименте [1, 2].
Ранее в наших работах было показано, что НРМЧ – пусковой фактор для возникновения хронического иммунопатологического воспаления в тканях костного ложа и слизистой полости рта. Их накопление в тканях до критической массы, названной «критическая доза НРМЧ» (Critical Dose of NanoMetall Particles, CDNanoMP), вызывает раннюю гибель клеток иммунной системы, что, очевидно, становится триггером для накопления наночастиц и формирования их комплексов до микронных размеров на фоне хронического иммунопатологического воспаления [3].
Периимплантит – это воспалительное заболевание твердых и мягких тканей вокруг остеоинтегрированных дентальных имплантатов, сопровождающееся прогрессирующим повреждением альвеолярной кости. Микроорганизмы полости рта могут формировать биопленки ко всем типам поверхностей за счет выработки множества адгезивных факторов. Присущие материалам свойства будут влиять не только на количество микроорганизмов, но и на их профиль и силу адгезии к поверхности материала. В этой перспективе стратегии снижения адгезии патогенных микроорганизмов к дентальным имплантатам и их компонентам должны быть исследованы в рамках современных концепций реабилитации в имплантологической стоматологии. На сегодняшний день разработано несколько видов обработки поверхности с помощью нанесения металлических наночастиц для уменьшения роста патогенных бактерий. Однако основными недостатками этих подходов являются потенциальная токсичность и накопительный эффект металлов с течением времени [4].
В связи с риском развития периимплантита после установки дентальных имплантатов на основе ретроспективного, открытого, когортного исследования была проанализирована 4591 единица дентальных имплантатов, установленных в условиях частной практики, с последующим наблюдением от 5 до 10 лет. Кроме того, была оценена распространенность мукозита и периимплантита среди исследуемой когорты пациентов. Установлено, что к факторам риска убыли костной ткани в пришеечной зоне дентальных имплантатов относятся аутоиммунные заболевания, интенсивное курение, терапия бисфосфонатами, расположение имплантата, его диаметр и конструкция, а также наличие костного дефекта в месте проведения дентальной имплантации. Распространенность мукозита в области остеоинтегрированных дентальных имплантатов равнялась 38,6% через 6–7 лет использования дентальных имплантатов в качестве опор для ортопедических конструкций. Распространенность периимплантита через 6–7 лет применения дентальных имплантатов составила 4,7% [5].
В настоящее время одна из ведущих ролей в формировании биопленки на поверхности дентальных имплантатов, способствующей разрушению костной ткани, отводится бактериальным штаммам, в частности Staphylococcus aureus; это обстоятельство учитывается при оценке антибактериального эффекта в экспериментах по разработке новых антибактериальных покрытий для дентальных имплантатов [6].
Существует противоречие с результатами клинических исследований в оценке роли S. aureus в качестве бактериального штамма, ассоциированного с убылью костной ткани при периимплантите.
При проведении микробиологических исследований у пациентов с диагнозом «периимплантит» были выделены следующие штаммы бактерий: Staphylococcus epidermidis и специфические пародонтопатогены: Porphyromonas gingivalis, Tannerella forsythia, Treponema denticola, Fusobacterium nucleatum и Prevotella intermedia. В ходе оценки результатов 12 микробиологических исследований у 1233 человек с установленными 1513 дентальными имплантатами выявлено, что развитие периимплантита было ассоциировано с наличием S. epidermidis (отношение шансов, ОШ 10,28; 95% доверительный интервал, ДИ: 1,26–83,98), F. nucleatum (ОШ 7,83; 95% ДИ: 2,24–27,36), T. denticola (ОШ 6,11; 95% ДИ: 2,72–13,76), T. forsythia (ОШ 4,25; 95% ДИ: 1,71–10,57), P. intermedia (ОШ 3,79; 95% ДИ: 1,07–13,35) и P. gingivalis (ОШ 2,46; 95% ДИ: 1,21–5,00). И наоборот, присутствие Aggregatibacter actinomycetemcomitans (ОШ 3,82; 95% ДИ: 0,59–24,68), S. aureus (ОШ 1,05; 95% ДИ: 0,06–17,08) и Campylobacter rectus (ОШ 1,48; 95% ДИ: 0,69–3,17) не было связано с периимплантитом [7].
Было сделано предположение и получены доказательства того, что НРМЧ, расположенные в окисном слое дентальных имплантатов, имеют свойство эмиссии и накопления в тканях костного ложа под воздействием механической нагрузки [8].
В результате проведенных исследований по изучению иммунологических и нанотехнологических аспектов остеоинтеграции и дезинтеграции дентальных имплантатов впервые были получены супернатанты, содержащие металлические НРМЧ в составе бидистиллированной воды, с поверхностей окисного слоя сертифицированных медицинских изделий [9]. Была изучена особенность взаимодействия НРМЧ, полученных с поверхности дентальных имплантатов в составе супернатантов, при совместном культивировании с различными штаммами бактерий, в частности с S. aureus в присутствии интактной и инактивированной сыворотки. Установлена роль системы комплемента в формировании биопленки в присутствии НРМЧ [10].
Возникает вопрос, можно ли рассматривать накопительный эффект НРМЧ в присутствии симбионтной микрофлоры полости рта при наличии аллергостатуса у пациента как этиологический комплекс для возникновения местного аутовоспаления? Чтобы попытаться найти ответ, представляем разбор клинического случая.
МАТЕРИАЛ И МЕТОДЫ
Рентгеновская микротомография
Для выявления инородных включений в исследуемых образцах, которые представляли собой части десны, прилегающей к балочной конструкции, а также для определения их расположения и размера использовался метод рентгеновской абсорбционной микротомографии. Томографические исследования образцов выполнялись на рентгеновском микротомографе ТОМАС [11]. В данных измерениях применялся кристалл-монохроматор из пиролитического графита (размер пучка на объекте около 1 см). Измерения делались при помощи рентгеновской трубки с молибденовым анодом (энергия 17,5 кэВ).
Геометрия проведенных экспериментов была следующая: расстояние «источник – образец» 1,2 м, расстояние «образец – детектор» 0,02 м. Условия зондирования: ускоряющее напряжение 40 кВ, ток 40 мА. С целью томографических исследований выполнялось вращение образцов относительно фиксированной вертикальной оси, при этом измерялось 400 проекций с шагом 0,5 градуса и экспозицией 3,5 с на кадр. При проведении измерений использовался высокоразрешающий рентгеновский детектор XIMEA-xiRay11 с разрешением 9 мкм при поле зрения 36 на 24 мм. Реконструкция выполнялась алгебраическим методом.
Для количественной оценки содержащихся в образцах микровключений была применена процедура обработки полученных 3D-изображений, включающая пороговую фильтрацию, бинаризацию, маркирование. В результате анализа полученных трехмерных реконструкций определялись расположение, размеры (эквивалентный диаметр, объем) и средние коэффициенты поглощения обнаруженных инородных включений в биологических тканях. Эквивалентный диаметр включения EqD, представляющий собой диаметр сферы того же объема Volume, рассчитывался по формуле:
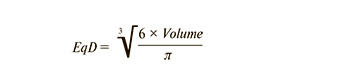
Рентгенофлуоресцентный анализ
Элементный состав образцов (части десны, прилегающей к балочной конструкции) определяли методом рентгенофлуоресцентного анализа на рентгеновском микротомографе с использованием детектора-спектрометра X-123SDD (Amptek, США). Источником излучения служила рентгеновская трубка с молибденовым анодом, излучение монохроматизировалось при помощи однократного отражения от высокосовершенного симметричного кристалла кремния, ориентацией (111). Энергия излучения соответствовала характеристической линии Kα1 молибдена и равнялась 17,47 кэВ. Нижний предел измерений был ограничен параметрами чувствительного элемента детектора и составлял ~1 кэВ. Энергетическое разрешение отснятых от исследуемого образца спектров флуоресцентного излучения находилось на уровне ~150 эВ.
Геометрия проведенных экспериментов была следующая: расстояние «источник – образец» около 1 м, расстояние «образец – детектор» около 0,02 м. Размер зондирующего пучка на образце был ~1 мм по горизонтали и ~5 мм по вертикали. Условия зондирования: ускоряющее напряжение 40 кВ, ток 40 мА. Экспозиция составляла 600 с.
Электронная микроскопия
Для исследования качества покрытия имплантатов и визуализации их структуры под покрытием были получены шлифы поперечных сечений, которые готовили в несколько этапов: заливка имплантата смолой, резка, механическая шлифовка, ионная полировка. Резка имплантата осуществлялась c помощью универсальной системы прецизионной резки Leica EM TXP. Механическая шлифовка проводилась с использованием шлифовальных дисков при последовательном уменьшении размера частиц абразива от 15 до 0,5 мкм. На последнем этапе мы применяли метод ионного травления поверхности образца в установке Hitachi IM4000plus, которая позволяет осуществить травление поверхности образца широким пучком ионов Ar+ с энергией до 6 кВ, легко устраняет дефекты резки, обеспечивает получение неискаженных поперечных сечений большой площади (до 5 мм2) без приложения механического напряжения к образцу.
Структуру поверхности балки и имплантатов изучали посредством растровой электронной микроскопии (РЭМ), просвечивающей растровой микроскопии (ПРЭМ) с z-контрастом, электронной дифракции и энергодисперсионного (ЭД) анализа с использованием растрового электронного микроскопа Scios (режим вторичных электронов, детектор Эверхардта – Торнли) при ускоряющих напряжениях 2–20 кВ, просвечивающего электронного микроскопа с полевой эмиссией TermoFisher Scientific Osiris при ускоряющем напряжении 200 кВ. Просвечивающий электронный микроскоп оборудован специальной системой детекторов, позволяющих получать карты распределения химических элементов большой площади за несколько минут.
Для исследования на просвет (просвечивающая электронная микроскопия) образцы подготавливали диспергированием имплантатов, помещенных в дистиллированную воду, в ультразвуковой ванне. Супернатант с НРМЧ наносили на медные сетки с тонкой подложкой из аморфного углерода для исследования в просвечивающем электронном микроскопе.
Базофильный тест
Мы исследовали супернатанты, содержащие НРМЧ, полученные с поверхности медицинских изделий, при взаимодействии с венозной кровью пациента в процессе постановки базофильного аллерготеста (последний проводился методом проточной цитометрии). Балочная конструкция и дентальные имплантаты были удалены из полости рта пациента. Балочная конструкция стерилизовалась в автоклаве, а затем в ламинарных условиях погружалась в чашку Петри с бидистиллированной водой. Стерильную балочную конструкцию инкубировали в течение 5 дней в CO2-инкубаторе при температуре 37,2 °C. Впоследствии получали супернатанты, содержащие НРМЧ, способом, описанным в патенте [9]. Супернатанты, включающие НРМЧ с поверхностей двух систем дентальных имплантатов, изготовленных на основе сплава TiO2 Sky и Astra Tech, получали тем же способом. Полученные супернатанты, содержащие НРМЧ, были далее использованы для выполнения базофильного теста в качестве модификации реагентов.
В работе был проведен базофильный тест («Тест-система для определения аллергии», Beckman Culter, США), чтобы увидеть активацию и дегрануляцию базофилов при взаимодействии с молекулами CD203, CD294 на поверхности клеток с использованием моноклональных антител при совместном культивировании венозной крови пациента с полученными НРМЧ в составе супернатантов. Совместную инкубацию супернатантов, содержащих НРМЧ, и венозной крови пациента осуществляли в течение 15 мин. Активацию базофилов или ее отсутствие фиксировали методом проточной цитофлуориметрии (проточный цитометр FC-500). На основании полученных результатов рассчитывался индекс активации базофилов [9].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Клинический случай – пациентка Ж., 80 лет
На кафедру пропедевтики хирургической стоматологии стоматологического факультета Научно-образовательного института стоматологии им. А.И. Евдокимова ФГБОУ ВО «Российский университет медицины» Минздрава России поступила пациентка с жалобами на резкие боли в области слизистой оболочки полости рта, наличие покраснения, белого налета, невозможность использовать условно-съемный протез, фиксируемый на балочной конструкции с опорой на дентальные имплантаты системы Sky, установленные 10 лет назад в проекции отсутствующих зубов 32, 42 и съемного пластиночного протеза на верхней челюсти (рис. 1, 2). Со слов пациентки, балочная конструкция была изготовлена из металлического сплава на основе TiO2.
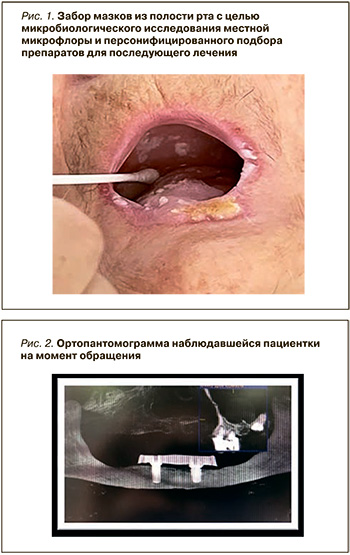
Данные анамнеза указывали на наличие хронического гастрита, катаракты правого глаза, глаукомы левого глаза, непереносимость металлов при ношении бижутерии (гноетечение, боль, покраснение кожных покровов в месте контакта).
Со слов пациентки, впервые жалобы на указанные выше симптомы со стороны слизистой оболочки полости рта появились у нее через месяц после окончания ортопедического лечения. На протяжении 10 лет она наблюдалась и проходила лечение в профильных медицинских учреждениях г. Москвы без какого-либо эффекта.
На момент обращения изменений со стороны конфигурации лица не отмечалось, лимфатические узлы головы и шеи не пальпировались, открывание рта было свободным, но болезненным в области красной каймы губ, где наблюдались признаки хронического хейлита.
На левой половине нижней губы в области красной каймы имелся участок гиперкератоза размером 1,5–2 см с переходом на внутреннюю поверхность слизистой оболочки нижней губы, контактирующей непосредственно с металлической поверхностью балки.
На поверхности слизистой оболочки языка, щек и твердого нёба наблюдался белый налет, не снимающийся шпателем, в виде бляшек, что указывало на возможность микотического поражения слизистой изолятами грибов рода Candida. Для исключения бактериального и грибкового поражения был сделан забор мазков с поверхности щек, языка и твердого нёба с последующим культивированием в чашках Петри на питательных средах и подбором к выявленным штаммам и изолятам необходимых медикаментозных препаратов.
В связи с предположением о возможной аллергии к компонентам сплава балочной конструкции, а именно гиперчувствительности замедленного типа, было принято решение об удалении металлической балки в день обращения пациентки и фиксации формирователей десны.
Балочная конструкция подверглась стерилизации в условиях автоклава, в последующем были изучены ее структура, элементный состав НРМЧ окисного слоя, и проведены иммунологические исследования с супернатантами, полученными с поверхности металлической балки и дентальных имплантатов системы Sky и Astra Tech.
Мы взяли биоптаты слизистой оболочки полости рта в проекции ранее фиксированной балочной конструкции и дентальных имплантатов до их удаления. Были получены супернатанты, содержащие НРМЧ с поверхностей новых дентальных имплантатов системы Sky, для выполнения лабораторных иммунологических исследований с целью выявления аллергии на компоненты сплава металлов.
При осмотре полости рта выявлено втяжение на боковых поверхностях языка в проекции отсутствующих седьмых моляров нижней челюсти. По словам пациентки, данные изменения носили характер дефектов после удаления доброкачественных новообразований в виде папиллом, что подтвердило проведенное постоперационное гистологическое исследование и обозначило вирусоносительство ВПЧ (вирус папилломы человека) с 2018 г.
По результатам гистологического исследования была получена микроскопическая картина, соответствующая хроническому воспалению слизистой оболочки полости рта.
Полная санация полости рта с удалением как зубов, так и дентальных имплантатов под прикрытием комплексной медикаментозной терапии дала положительный эффект (рис. 3).
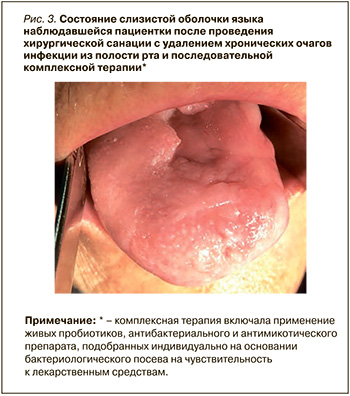
Через 2 мес. у пациентки произошел рецидив грибкового поражения с усугублением течения клинических симптомов, в том числе боли в области корня языка, что потребовало консультаций смежных специалистов, в частности лор-врача.
На сегодняшний день по результатам обследования и биопсии слизистой оболочки корня языка выставлен диагноз «плоскоклеточная папиллома спинки языка без признаков озлокачествления».
Рентгенологические исследования
На рисунке 4 представлены результаты томографических исследований образцов, которые описаны в разделе «Рентгеновская микротомография» и представляют собой части десны (образцы 1–3), прилегающей к балочной конструкции.
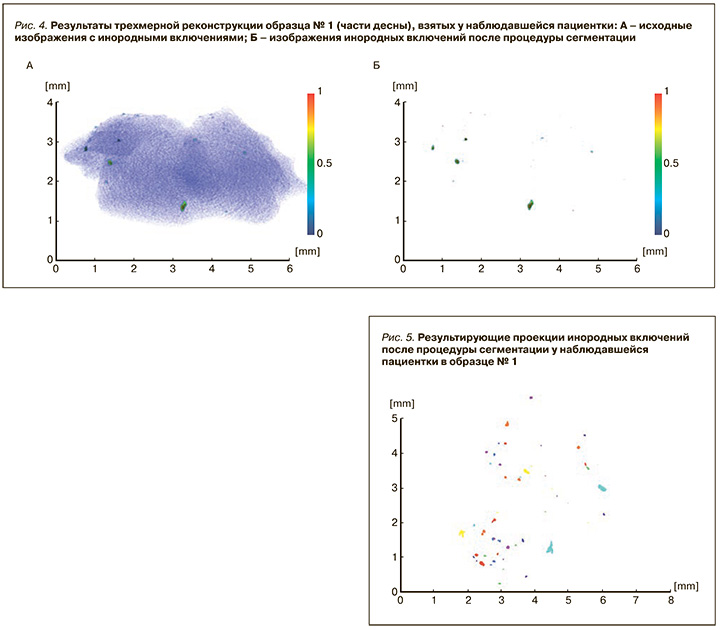
Результирующие проекции всех включений после применения подхода, указанного в разделе «Рентгеновская микротомография», представлены на рисунке 5. В ходе анализа полученных трехмерных реконструкций были определены расположение, размеры (эквивалентный диаметр, объем) и средние коэффициенты поглощения (табл. 1) инородных включений, обнаруженных в биологических тканях.
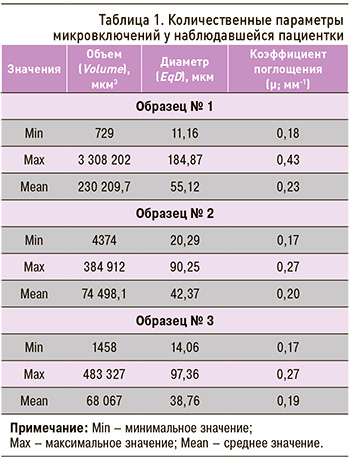
Таким образом, во всех образцах частей десны (1–3), прилегающей к балочной конструкции, были обнаружены инородные микровключения размерами от ~11 до 185 мкм с коэффициентами поглощения (µ) от ~0,17 до 0,43 мм-1.
На рисунке 6 представлен рентгенофлуоресцентный спектр, типичный для всех исследованных образцов в силу идентичности их элементного состава.
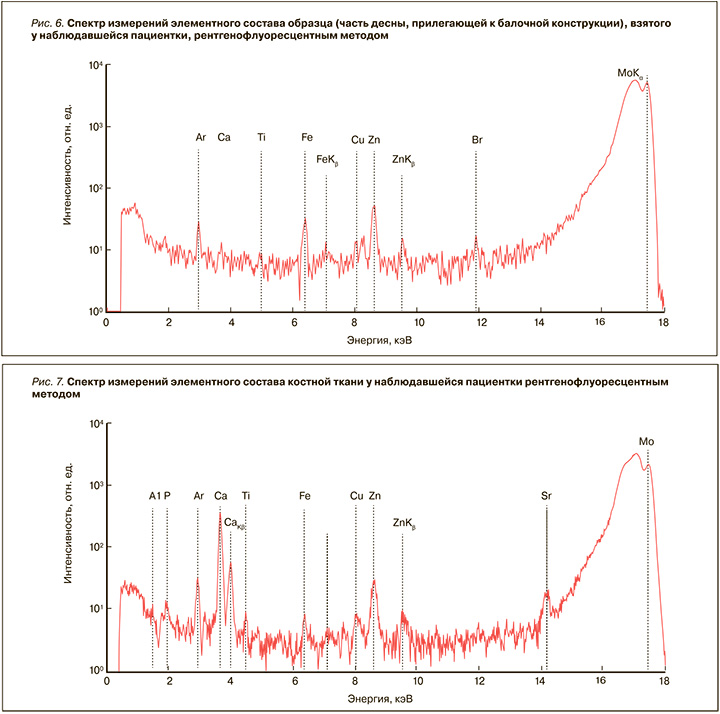
Расшифровка полученных спектров позволила выявить наличие в исследуемых образцах следующих элементов: Ca, Ti, Fe, Cu, Zn, Br. Пики от Ar (воздух) и Mo (анод рентгеновской трубки) – аппаратные.
Кроме того, методом рентгенофлуоресцентного анализа был определен элементный состав костного биоптата размером около 1 мм, взятого в месте контакта с титановым имплантатом системы Sky. На рисунке 7 представлен рентгенофлуоресцентный спектр кости.
Расшифровка полученного спектра выявила наличие в исследуемом образце следующих элементов: Al, P, Ca, Ti, Fe, Cu, Zn, Sr. Пики от Ar (воздух) и Mo (анод рентгеновской трубки) – аппаратные.
Состав дентальных имплантатов системы Sky, заявленный производителем, представлен в таблице 2.
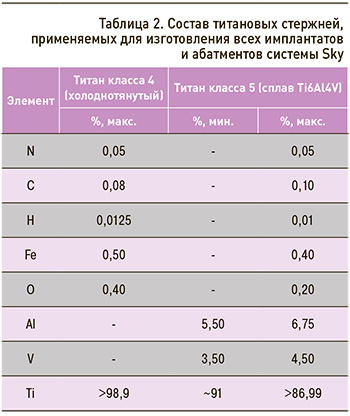
Таким образом, методами рентгеновской микротомографии и рентгенофлуоресцентного анализа были идентифицированы импрегнированные металлические НРМЧ в структуру патологических участков тканей с наличием хронического воспалительного процесса. Выявлена их идентичность с составом титановых стержней, применяемых при изготовлении дентальных имплантатов и абатментов системы Sky (см. рис. 5–7, табл. 2).
Электронная микроскопия
На поверхности балки обнаружены участки со следами коррозии, что можно видеть на рисунках 8–9, где представлены РЭМ-изображения фрагмента балки и одной из кромок. Кроме того, на поверхности обнаружены области со светлым контрастом (рис. 8А). ЭД-спектры не показали явных различий по основному химическому составу для этих областей и прилегающих мест с более темным контрастом. При большем увеличении можно заметить трещины и нарушения сплошности поверхностного слоя, отслоения (рис. 9А). Из спектра и карт распределения химических элементов видно, что основным химическим элементом сплава балки является титан, также в нем присутствуют алюминий, кислород (рис. 9Б). Таким образом, наиболее вероятный материал балки – сплав ВТ5 (хотя нельзя исключить и ВТ6). На поверхности балки имеются частицы окиси кремния, кальций, фосфор. Никель и цинк в составе сплава не обнаружены.
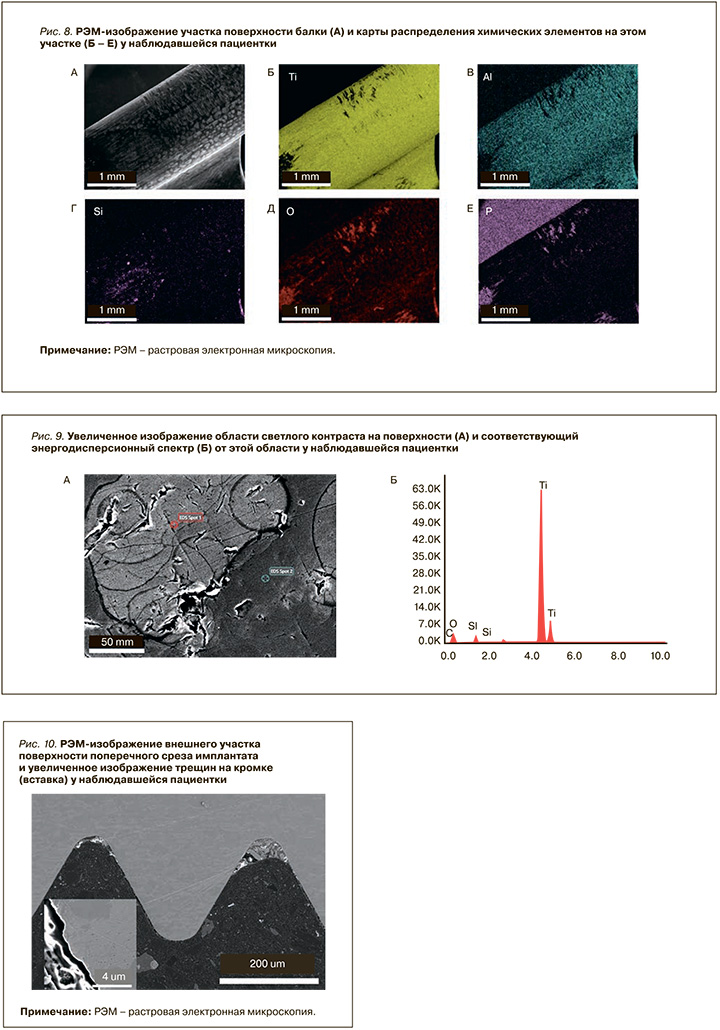
РЭМ-изображения участков шлифа поперечного среза дентального имплантата представлены на рисунках 10, 11. Следует отметить, что внешняя поверхность имплантата не гладкая (см. рис. 10), во многих местах наблюдаются значительная шероховатость поверхности порядка 2–3 мкм, трещины, в то время как шероховатость внутренней поверхности в основном не превышает 0,5 мкм (см. рис. 11).
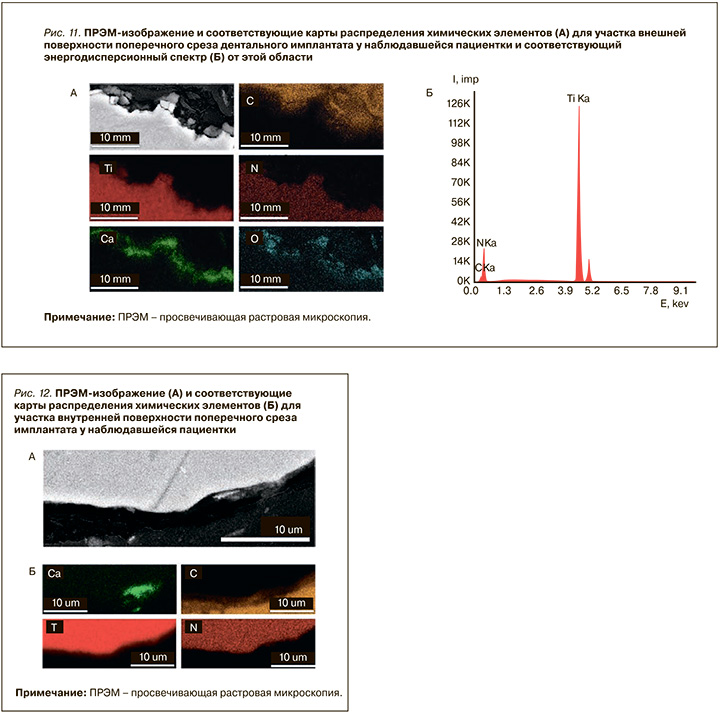
Результаты ЭД-анализа поверхности поперечного среза имплантата приведены на рисунках 11, 12. Сплав содержит титан и азот, а на поверхности присутствует в основном оксид кальция. Аналогичные результаты получены и для участков внутренней поверхности имплантата.
При анализе частиц в растворе (в составе супернатантов) методами просвечивающей растровой микроскопии (ПРЭМ) и ЭД-анализа в нем в основном были найдены частицы размером до 1–2 микрон. По ЭД-спектру можно было заключить, что конгломерат частиц содержит преимущественно окислы алюминия и титана, а также магний, кремний. По-видимому, это частицы самого имплантата. Кальций оказался распределен равномерно по площади сканирования, однако он может встречаться и в виде отдельных частиц.
На картах распределения химических элементов были видны окислы железа, кремния и алюминия округлой формы размером 0,5–1,0 мкм, а также частицы меди, встречавшиеся почти в каждом поле зрения. Обычно пики меди появляются в спектрах из-за того, что частицы нанесены на медные сетки с углеродной подложкой, однако в данном случае по картам распределения можно было сделать вывод о наличии также и медьсодержащих частиц.
Наряду с характерными частицами, включающими кальций, серу, алюминий, железо, были обнаружена единичная частица размером около 1 мкм, содержащая барий, кислород, серу (возможно, сульфат бария).
Результаты модифицированного базофильного теста с использованием метода проточной цитометрии, где в качестве реагентной базы применялись супернатанты, содержащие металлические НРМЧ, полученные с поверхностей исследуемых медицинских изделий
Необходимо отметить, что по результатам проточной цитометрии общее количество Th-2 типа лимфоцитов составило 3,92 при норме 0–1,5. В данном случае это служило подтверждением аллергостатуса пациентки.
На рисунке 13 приведены данные базофильного теста с использованием супернатантов, полученных с поверхностей исследуемых металлических изделий и прокультивированных совместно с венозной кровью пациентки в лабораторных условиях. По результатам такой совместной культивации мы можем наблюдать реакцию базофилов в ответ на взаимодействие с НРМЧ, полученными в составе супернатантов и использованными в качестве модифицированных реагентов. Эта методика модификации базофильного теста описана в патенте [9].
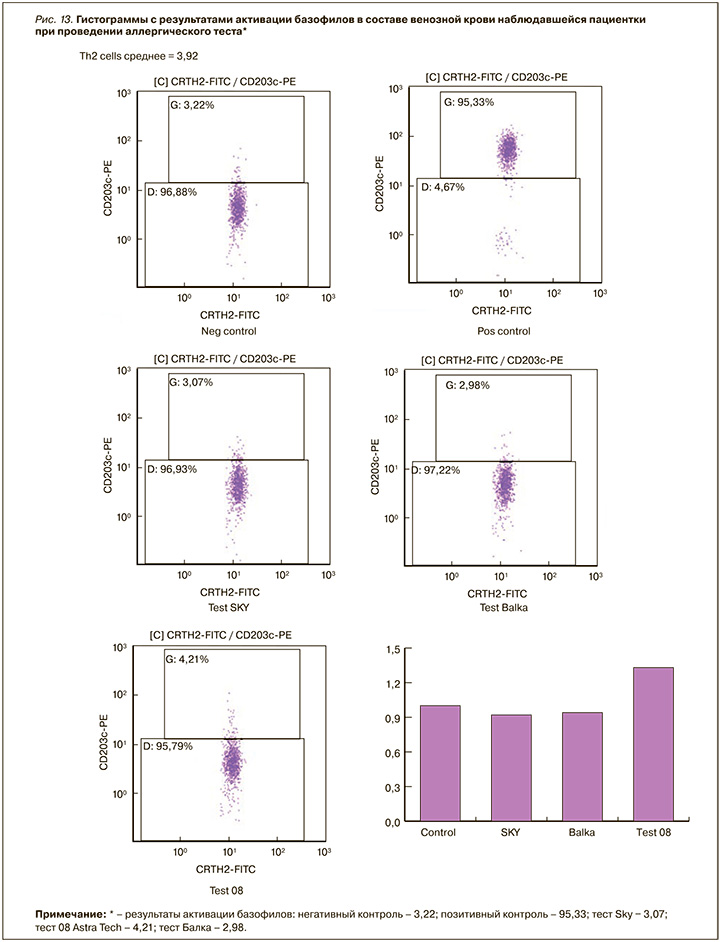
Результаты теста на аллергию выявили снижение активации базофилов, что исключает в данном конкретном случае возможность гиперчувствительности к элементам сплава на основе TiO2 как к дентальному имплантату системы Sky, так и к балочной ортопедической металлической конструкции. Нами был изучен элементный состав самих медицинских изделий и супернатантов, полученных с их поверхностей. Расшифровка полученного спектра НРМЧ в составе супернатантов выявила наличие большого количества окислов алюминия и титана, а также магний, кремний, железо в составе как самих изделий, так и биоптатов, полученных в области костного ложа, а также в области слизистой оболочки полости рта пациентки.
ЗАКЛЮЧЕНИЕ
Проведенные исследования демонстрируют возможность развития эффектов НРМЧ в тканях у пациентов после проведения стоматологической реабилитации методом дентальной имплантации.
Выполнение ортопедического этапа дентальной имплантации с использованием балочных конструкций и появлением функциональной нагрузки способствует выходу металлических НРМЧ и формированию микрочастиц в прилежащих тканях. Роль этих частиц в развитии патологических процессов в слизистой оболочке и тканях костного ложа остается неизученной. Необходимо помнить, что функционирование мукозального иммунитета в полости рта служит защитой от возможного проявления осложнений, связанных с эффектом частиц эмиссии металлических НРМЧ. К сожалению, в ряде клинических случаев на фоне имеющихся вторичных нарушений иммунной системы, обусловленных индивидуальной чувствительностью к компонентам сплава металлов, можно ожидать возникновение аллергической реакции замедленного типа, которая при несвоевременной верификации способствует переходу в аутовоспаление [12]. Подключение микробиоты полости рта как вторичного звена в инициации хронического воспалительного процесса усугубляет его течение, переводя его в хроническое аутовоспалительное заболевание. На этом фоне мы можем наблюдать как грибковое поражение слизистой оболочки и манифестацию вирусной инфекции в виде ВПЧ, так и поражение в виде очагов веррукозной лейкоплакии, отягощенной глоссалгией.
Для исключения аллергического компонента в развитии аутовоспалительного процесса необходимо исключить гиперчувствительность замедленного типа к компонентам сплавов металла в полости рта пациента. С помощью методики получения супернатантов, содержащих металлические НРМЧ, которая описана в патенте [9], возможно проведение базофильного теста с применением реагентов, полученных непосредственно из тех изделий, что были уставлены в полости рта пациента.
В нашем клиническом случае использование базофильного теста показало отсутствие активации базофилов в ответ на супернатанты, содержащие металлические НРМЧ, полученные с поверхности как балочной конструкции, так и дентальных имплантатов системы Sky и Astra Tech. Такой результат говорит об отсутствии аллергической реакции на микроэлементы, входящие в состав металлического медицинского изделия.
Подобные исследования [13] по изучению влияния НРМЧ на ткани и органы человека являются современной тенденцией, позволяющей расширить ракурс видения проблемы идиопатических состояний и понять природу их возникновения.
Информированное согласие
От пациентки было получено письменное добровольное информированное согласие на публикацию фотографий, результатов обследования и лечения.



