ВВЕДЕНИЕ
Для оценки состояния печени используется широкий спектр биохимических тестов, которые обозначаются хотя и неточным, но прочно вошедшим в клиническую практику термином «функциональные пробы печени» (ФПП) и отражают не только функциональное состояние печени, но и характер повреждения ее основных структур. ФПП обычно применяют для выявления заболеваний печени, а также свойственных им основных патогенетических синдромов. Правильная интерпретация ФПП способна помочь построить алгоритм обследования для определения этиологии болезни, определить тяжесть, характер течения и прогноз заболевания, а также оценить эффективность терапии. В то же время следует учитывать, что нарушения хотя бы одного теста встречаются более чем у 20% обследуемых пациентов: с одной стороны, у многих из них не выявляются заболевания печени, а с другой – у значительной части больных с доказанной патологией печени результаты ФПП остаются в пределах референсных значений [1–3].
Перечень используемых биохимических показателей при заболеваниях печени чрезвычайно широк, и они подразделяются на скрининговые (обязательные для исследования при всех заболеваниях печени) и дополнительные (уточняющие), которые проводятся по определенным показаниям. К скрининговым тестам относится исследование аланиновой трансаминазы (АЛТ), аспарагиновой трансаминазы (АСТ), щелочной фосфатазы (ЩФ), гамма-глютамилтрансферазы (ГГТ), общего, конъюгированного и неконъюгированного билирубина, протромбинового времени (ПТВ), протромбинового индекса (ПТИ), международного нормализованного отношения (МНО), общего белка и белковых фракций. Сопоставление результатов клинико-морфологических исследований с лабораторными данными при заболеваниях печени позволили классифицировать эти заболевания с выделением патогенетических синдромов, среди которых основными являются цитолитический, холестатический, мезенхимально-воспалительный, синдром печеночно-клеточной недостаточности.
СИНДРОМ ЦИТОЛИЗА
Морфологическим субстратом синдрома цитолиза выступает некроз гепатоцитов, которому предшествует повышение проницаемости наружной и цитоплазматических клеточных мембран. При нарушении их целостности внутриклеточные ферменты выходят из цитоплазмы клетки в межклеточную жидкость и кровь. Уровень внутриклеточных ферментов в сыворотке крови находится в прямой пропорциональной зависимости от объема поврежденных клеток печени. Цитолиз гепатоцитов – признак активности и прогрессирования патологического процесса в печени. Основные патогенетические механизмы гепатоцеллюлярных повреждений, которые косвенно можно оценить по результатам лабораторных тестов, включают формирование оксидативного стресса (алкогольные, лекарственные, метаболические поражения печени), иммунопатологические реакции (вирусные, бактериальные, аутоиммунные поражения печени), гидростатические нарушения (билиарная гипертензия, гипертензия в системе печеночных вен), гипоксию печени (синдром шоковой печени, сепсис и др.), нутритивные расстройства, связанные с резким дефицитом энергетической ценности пищи или дефицитом отдельных компонентов питания [4].
Основной биохимический маркер гепатоцеллюлярного повреждения – повышение уровня АЛТ или АЛТ и АСТ [5–9]. АЛТ локализована в цитозоле, а АСТ – как в цитозоле (20%), так и в митохондриях (80%) гепатоцитов. Период полувыведения из крови АЛТ и АСТ равен 47 и 17 ч соответственно. Помимо печени, АСТ присутствует в цитоплазме и митохондриях скелетных мышц, сердечной мышце, почках, головном мозге, поджелудочной железе, легких, лейкоцитах и эритроцитах и повышается в сыворотке крови при поражении этих органов и тканей. Повышенный уровень АЛТ является наиболее чувствительным индикатором некрозов гепатоцитов. Изолированное увеличение уровня АСТ имеет место при алкогольных поражениях печени с наличием дефицита витамина В6, участвующего в синтезе АЛТ, но чаще связано с внепеченочными заболеваниями: инфарктом миокарда, миокардитом, острым панкреатитом, гемолизом эритроцитов, острым нефритом, заболеваниями мышц, обширными ранениями, тяжелыми физическими нагрузками, заболеваниями нервной системы, патологией щитовидной железы. Уровень сывороточных АЛТ и АСТ может быть повышен и у здоровых лиц вследствие формирования макроэнзимов, которые представляют собой крупномолекулярные соединения (иммунные комплексы), состоящие из антигена (фермент) и антител, обладающих высоким молекулярным весом, что резко увеличивает период их полувыведения.
УРОВЕНЬ АМИНОТРАНСФЕРАЗ В ОЦЕНКЕ СТЕПЕНИ АКТИВНОСТИ ЗАБОЛЕВАНИЙ ПЕЧЕНИ
В зависимости от величины превышения верхней границы нормы (ВГН) АЛТ или АСТ выделяют три степени активности патологического процесса в печени:
- низкую активность – повышение уровня АЛТ или АСТ до 3 ВГН;
- умеренную активность – от 3 до 5 ВГН;
- высокую активность – повышение уровня АЛТ или АСТ > 5 ВГН либо > 3 ВГН в сочетании с возрастанием уровня общего билирубина > 2 ВГН в отсутствие холестаза (при нормальном уровне ЩФ).
Повышение уровня аминотрансфераз свыше 6 мес. служит биохимическим признаком хронического патологического процесса в печени.
УРОВЕНЬ АМИНОТРАНСФЕРАЗ В ОЦЕНКЕ ЭТИОЛОГИИ ЗАБОЛЕВАНИЙ ПЕЧЕНИ
Нормальный уровень аминотрансфераз или их повышение до 3 ВГН наблюдается у пациентов с компенсированным циррозом печени, хроническим вирусным гепатитом (В или С), неалкогольной жировой болезнью печени (НАЖБП). Возрастание уровня АЛТ и/или АСТ > 5 ВГН при этих патологиях указывает на сопутствующее острое повреждение печени другой этиологии.
Повышение уровня AСT < 8 ВГН и AЛT < 5 ВГН характерно для заболеваний печени алкогольной этиологии. Уровни АСТ и/или АЛТ > 25 ВГН с возрастанием уровня общего и конъюгированного билирубина типичны для острых вирусных и токсических гепатитов. Самые высокие уровни АСТ и АЛТ (до >50 ВГН) свойственны ишемическим поражениям печени, таким как шоковая печень, ишемический гепатит, поражения печени при сепсисе и др. [1, 10–12].
При гепатоцеллюлярном поражении уровень АЛТ обычно превышает значения АСТ, и только при массивных некрозах гепатоцитов с разрушением митохондрий уровень АСТ становится выше АЛТ в связи с поступлением в сыворотку крови не только цитозольной, но и митохондриальной АСТ.
ДИАГНОСТИЧЕСКАЯ ЗНАЧИМОСТЬ КОЭФФИЦИЕНТА ДЕРИТИСА
Для оценки тяжести гепатоцеллюлярного поражения, дифференциального диагноза острых и хронических поражений печени и внепеченочного повышения ферментов используется коэффициент ДеРитиса – отношение АСТ к АЛТ (рис. 1). Расчет этого показателя целесообразен только при повышении уровня АЛТ и/или АСТ [7].
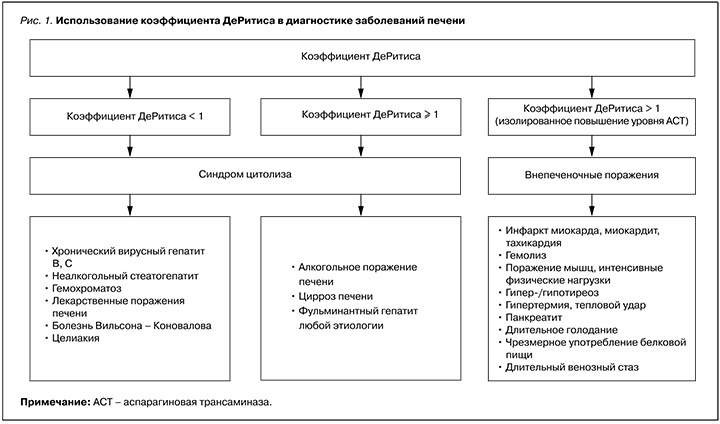
Преобладание уровня АЛТ или повышение АЛТ при нормальном уровне АСТ (коэффициент ДеРитиса < 1) характерно для следующих заболеваний:
- хронического вирусного гепатита В, С;
- неалкогольного стеатогепатита;
- гемохроматоза;
- лекарственных поражений печени;
- болезни Вильсона – Коновалова;
- целиакии.
Коэффициент ДеРитиса > 1, свидетельствующий о тяжелом поражении печени и более серьезном прогнозе заболевания, наблюдается при:
- алкогольных поражениях печени;
- фульминантном гепатите любой этиологии;
- циррозе печени любой этиологии.
Относительно низкий уровень AЛT при алкогольных поражениях печени может быть связан с дефицитом пиридоксина (витамина B6), который используется в качестве кофермента в синтезе как АСТ, так и АЛТ. При воздержании от употребления алкоголя нормализация коэффициента ДеРитиса происходит в течение 30–90 дней в отсутствие цирроза печени. Значения этого показателя > 2 определяются при алкогольных и злокачественных поражениях печени, > 4 – при фульминантном гепатите.
Возрастание уровня АСТ при нормальных значениях АЛТ указывают на внепеченочные поражения, включая инфаркт миокарда, миокардит, тахикардию, гемолиз, поражения мышц, гипер-/гипотиреоз, интенсивные физические нагрузки, гипертермию, тепловой удар, длительное голодание, панкреатит, чрезмерное употребление белковой пищи, длительный венозный стаз.
ГАММА-ГЛЮТАМИЛТРАНСФЕРАЗА КАК МАРКЕР ЦИТОЛИЗА
ГГТ – микросомальный фермент, который обнаруживается в мембранах гепатоцитов и холангиоцитов, эпителии почечных канальцев, поджелудочной железе, тонкой кишке, сердце, легких, селезенке, слюнных железах, костном мозге, тимусе и головном мозге и отсутствует в мышцах, костях и эритроцитах. Это ключевой фермент в метаболизме глутатиона, транспортирующего пептиды через клеточную мембрану.
Повышение уровня ГГТ связано с двумя причинами. Первая обусловлена индукцией синтеза новых молекул как в результате токсического действия на гепатоцит ксенобиотиков (алкоголя, лекарств и других химических субстанций), так и вследствие процессов клеточной регенерации после перенесенных острых гепатитов, даже когда нормализовался уровень АЛТ и АСТ. Как правило, в этих ситуациях уровень ГГТ не превышает 3 ВГН.
Вторая причина – повреждение клеточных мембран гепатоцитов и холангиоцитов. Тестирование уровня ГГТ при заболеваниях печени важно проводить в двух ситуациях:
- при соотношении АСТ/АЛТ > 2, когда повышенный уровень ГГТ свидетельствует об алкогольном поражении печени и может использоваться для мониторинга воздержания от алкоголя (уровень ГГТ возвращается к норме после 2–6 нед. прекращения употребления спиртного);
- для диагностики холестаза при заболеваниях печени. Одновременное увеличение ЩФ и ГГТ подтверждает наличие холестаза. Следует отметить, что активность этого фермента снижается при приеме женских половых гормонов [1, 9].
Изолированное увеличение уровня ГГТ выявляется как при заболеваниях печени, так и внепеченочной патологии, в том числе заболеваниях поджелудочной железы, инфаркте миокарда, почечной недостаточности, хронических обструктивных заболеваниях легких, сахарном диабете, правожелудочковой сердечной недостаточности, ожирении, никотиновой зависимости и опухоли мозга. В случае доказанной патологии печени изолированное повышение уровня ГГТ может быть обусловлено как регенеративными процессами после прекращения некрозов гепатоцитов при острых гепатитах, циррозе печени, развитии гепатоцеллюлярной карциномы, так и с интралобулярным (гепатоцеллюлярным) холестазом [7, 13].
Таким образом, возрастание уровня ГГТ при заболеваниях печени может быть маркером некрозов и регенерации гепатоцитов, холестаза, опухолевого роста в печени, интоксикации алкоголем и лекарствами. Повышение ГГТ рассматривается как «сигнал тревоги», но не указывает однозначно на природу заболевания печени и требует поиска причины такого повышения. Исследование ГГТ необходимо в качестве «отсеивающего» теста и контроля за течением установленного патологического процесса в печени.
СИНДРОМ ХОЛЕСТАЗА
Холестаз представляет собой вариант нарушения эндогенного клиренса физиологических метаболитов и в частности компонентов желчи на всем протяжении билиарного тракта: гепатоцитов, каналикул, внутрипеченочных и внепеченочных желчных протоков. Патологический процесс при холестазе может локализоваться во внутрипеченочном отделе билиарного тракта, включающем синусоидальные и каналикулярные мембраны гепатоцита, внутридольковые каналикулы, экстралобулярные желчные протоки портальных трактов, и во внепеченочном отделе билиарной системы, к которому относятся правый, левый и общий печеночный проток, общий желчный проток (холедох), большой дуоденальный сосок.
В зависимости от локализации поражения выделяют внутрипеченочный и внепеченочный холестаз. Первый из них подразделяется на интралобулярный (гепатоцеллюлярный и каналикулярный) и экстралобулярный (дуктулярный) холестаз. Гепатоцеллюлярный холестаз обусловлен повреждением билиарного полюса гепатоцита с нарушением выведения компонентов желчи в каналикулы. Каналикулярный холестаз связан с повреждением не только билиарного полюса гепатоцита, представляющего стенку холангиол, но и холангиоцитов вставочных внутридольковых канальцев. В свою очередь, экстралобулярный (дуктулярный, холангиоцеллюлярный) холестаз развивается в результате поражения и гиперрегенерации холангиоцитов внутрипеченочных междольковых желчных протоков портальных трактов, сопряженных с развитием обструктивно-воспалительных и гранулематозных процессов в портальных трактах.
Внепеченочный холестаз вызывается поражением внепеченочного отдела билиарной системы. Он может быть синдромом при острых и хронических поражениях печени (гепатитах, циррозах различной этиологии, метаболических расстройствах, опухолевых процессах печени и др.) или же самостоятельным заболеванием печени (первичным билиарным холангитом/циррозом, первичным склерозирующим холангитом, лекарственным холестазом, доброкачественным рецидивирующим семейным холестазом, холестазом беременных и др.).
Лабораторные маркеры, которые используются в оценке синдрома холестаза, включают скрининговые (билирубин общий и конъюгированный, ЩФ, ГГТ) и дополнительные (уточняющие) показатели (холестерин, лейцинаминопептидаза, 5-нуклеотидаза, желчные кислоты, медь) [7, 14, 15].
ОБЩИЙ БИЛИРУБИН И ЕГО ФРАКЦИИ В ДИАГНОСТИКЕ ХОЛЕСТАЗА
Билирубин образуется в клетках ретикулоэндотелиальной системы (в системе мононуклеарных фагоцитов) из гемоглобина старых эритроцитов и ряда гемсодержащих белков и, поступая в кровоток, связывается с альбумином, превращаясь в так называемый непрямой (свободный, неконъюгированный) билирубин. Дальнейший метаболизм билирубина включает три процесса:
- транслокацию билирубина с альбумина в гепатоцит;
- конъюгацию с глюкуроновой кислотой при участии фермента глюкуронозилтрансферазы с образованием растворимого в воде прямого (конъюгированного, связанного) билирубина;
- секрецию прямого билирубина в желчь.
Уровень в крови общего билирубина составляет приблизительно 3,4–20,5 мкмоль/л. При этом на долю непрямого билирубина приходится 75%, прямого – 25% от общего билирубина. Данное соотношение может изменяться в зависимости от принятых в конкретной лаборатории референсных значений.
Исследование уровней общего, конъюгированного (прямого) и неконъюгированного (непрямого) билирубина используют для дифференциальной диагностики желтухи (рис. 2).
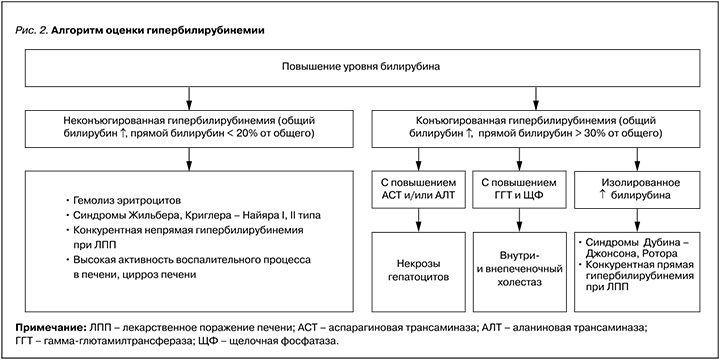
Для конъюгированной (прямой) гипербилирубинемии характерны повышение общего билирубина свыше ВГН и конъюгированного (прямого) билирубина более 30% от общего билирубина, а также наличие билирубина в моче. Неконъюгированной (непрямой) гипербилирубинемии сопутствуют повышение общего билирубина свыше ВГН при содержании конъюгированного (прямого) билирубина менее 20% от общего билирубина и увеличение содержания уробилиногена в моче [1, 7, 16, 17].
Возрастание в крови общего и конъюгированной фракции билирубина наблюдается при следующих состояниях:
- некрозах гепатоцитов (одновременно повышается уровень АЛТ, АСТ);
- внутрипеченочном и внепеченочном холестазе (одновременно повышается уровень ГГТ, ЩФ);
- наследственной патологии: синдроме Дубина – Джонсона, синдроме Ротора (моносимптом);
- печеночно-клеточной дисфункции (конкурентная конъюгированная гипербилирубинемия) при лекарственных поражениях печени (моносимптом).
Уровень конъюгированного билирубина служит маркером состояния выделительной функции печени и может применяться для прогнозирования течения и исхода заболеваний печени.
Повышение в крови общего и неконъюгированного билирубина наблюдается при следующих состояниях:
- гемолизе эритроцитов;
- синдроме Жильбера, синдроме Криглера – Найяра I, II типа (связаны со снижением активности глюкуронилтрансферазы);
- печеночно-клеточной дисфункции (конкурентная неконъюгированная гипербилирубинемия) при лекарственных поражениях печени;
- высокой активности острого процесса в печени или циррозе печени в результате уменьшения количества печеночных клеток и, как следствие, падения конъюгационной способности оставшихся гепатоцитов [9, 16].
Ложноположительный подъем уровня общего билирубина наблюдается при голодании более 24 ч и интенсивной мышечной нагрузке.
К причинам низкого уровня билирубина в крови относятся негемолитические анемии, тяжелая сердечно-сосудистая патология, почечная недостаточность, туберкулез, низкокалорийная диета, применение витамина С, фенобарбитала, интенсивные солнечные инсоляции, прием кофе перед исследованием. Большинство этих причин обусловлено индукцией перемещения билирубина из мест связывания с альбумином на фармакологические субстанции и ксенобиотики, что приводит к транслокации его в ткани и снижению в крови.
Признаком внутри- или внепеченочного желтушного холестаза является повышение в крови общего и конъюгированного билирубина в сочетании с повышением ГГТ и ЩФ.
МЕТАБОЛИТЫ БИЛИРУБИНА В МОЧЕ И КАЛЕ В ДИАГНОСТИКЕ ХОЛЕСТАЗА
Основные метаболиты прямой фракции билирубина желчи – уробилиноген, уробилин, стеркобилин – образуются в кишечнике с участием кишечной микробиоты. Они экскретируются с калом и только незначительная их часть (<2%) всасывается, поступает в общий кровоток и выделяется с мочой. В норме билирубин в моче не определяется. Наличие его в этом биосубстрате свидетельствует о повышении в крови конъюгированного билирубина > 30 мкмоль/л. В норме в моче содержатся следы уробилиноидов (уробилин + уробилиноген), их отсутствие служит признаком холестаза (отсутствует поступление желчи в желудочно-кишечный тракт (ЖКТ). Увеличение содержания уробилиноидов в моче отмечается при гемолитической желтухе, токсических поражениях печени. Стеркобилин в кале определяется в норме, тогда как его отсутствие, сопровождающееся обесцвечиванием (ахолией) кала, – признак холестаза (нет поступления желчи в ЖКТ).
ЩЕЛОЧНАЯ ФОСФАТАЗА КАК МАРКЕР ХОЛЕСТАЗА
ЩФ входит в семейство металлоферментов цинка, которые локализуются в высокой концентрации в микроворсинах холангиоцитов, а также в некоторых других тканях (костях, кишечнике, плаценте, лактирующей молочной железе). Физиологическое повышение ЩФ наблюдается во время интенсивного роста (у подростков до 15 лет) за счет костного изофермента ЩФ, у женщин в III триместре беременности при участии плацентарного изофермента ЩФ и нередко у женщин в возрасте старше 65 лет. Костный изофермент ЩФ повышается в пределах 3–10 ВГН при миеломной болезни, рахите, первичном гиперпаратиреоидизме, деформирующей остеодистрофии, остеомиелите, переломах, остеогенной саркоме, метастазах в кости. Кроме того, возрастание ЩФ отмечается в случае аутоиммунных васкулитов, заболеваний почек, опухолей, гипертиреоидизма, целиакии, интестинальной ишемии, гиперлипидемии, саркоидоза и ряда других патологий. Снижение активности этого фермента выявляется при врожденной гипофосфатаземии, гипотиреозе, кахексии, пернициозной анемии, фульминантном гепатите, связанным с болезнью Вильсона– Коновалова, дефиците цинка и магния и других состояниях.
Уровень ЩФ повышается при холестазе, в основе которого лежат повреждение и последующая гиперрегенерация холангиоцитов внутрипеченочной билиарной системы с формированием внутрипеченочного холестаза на уровне каналикул и желчных протоков, а также при обструкции внепеченочных желчевыводящих путей. Повышение ЩФ при холестазе ассоциировано с индукцией ее синтеза вновь регенерирующими холангиоцитами и не зависит от нарушения ее экскреции в желчь. При обструкции внутрипеченочных и внепеченочных желчевыводящих путей уровень ЩФ превышает ВГН в ≥ 3 раза. Самый высокий ее уровень обнаруживается у пациентов с билиарной обструкцией, обусловленной злокачественными новообразованиями, при сепсисе, системных инфекциях. После разрешения билиарной обструкции нормализация уровня ЩФ может занять несколько дней, поскольку период ее полураспада составляет 7 дней [1, 18].
Принимая во внимание большое количество причин, приводящих к повышению ЩФ, исследовать ее необходимо одновременно с другими маркерами холестаза, в первую очередь с ГГТ. Одновременное возрастание уровней ГГТ и ЩФ свидетельствует о наличии холестаза. Стойко повышенные ЩФ и ГГТ при отсутствии обструкции желчевыводящих путей требуют определения антимитохондриальных антител, которые являются высокоспецифичными в отношении первичного билиарного холангита/цирроза печени [19].
ГАММА-ГЛЮТАМИЛТРАНСФЕРАЗА КАК МАРКЕР ХОЛЕСТАЗА
ГГТ практически всегда повышается при внутри- и внепеченочном холестазе, поскольку локализуется преимущественно в холангиоцитах, повреждение которых лежит в основе формирования холестаза. Исключение из этого правила – семейный внутрипеченочный холестаз, когда сохраняется нормальный уровень ГГТ [20].
ГГТ – высокочувствительный (95%) индикатор гепатобилиарных заболеваний, включая холестатические: в диагностике холестаза ее чувствительность в 6 раз выше, чем ЩФ [21]. При доказанной патологии печени изолированное повышение ГГТ свыше 3 ВГН рассматривается как признак внутрипеченочного гепатоцеллюлярного холестаза. В то же время для уточнения причины повышения ГГТ и локализации холестаза необходимо оценивать уровень ГГТ вместе с показателями ЩФ. В отличие от ЩФ ее содержание остается нормальным при заболеваниях костей, беременности и др. Одновременное увеличение уровня ЩФ и ГГТ подтверждает наличие холестаза, а также его локализацию и клинический вариант.
При холестазе как самостоятельном заболевании печени целесообразно выделять три клинических варианта патологии:
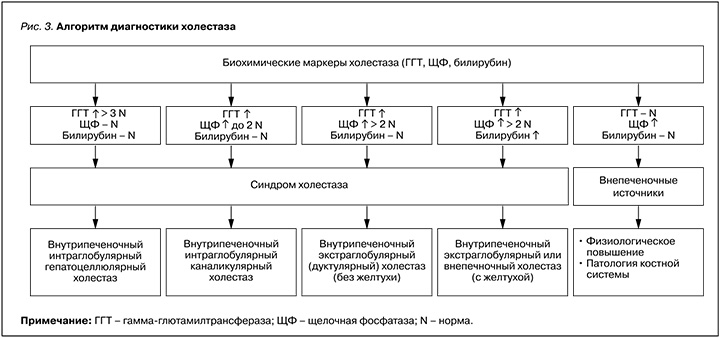
- внутрипеченочный интралобулярный гепатоцеллюлярный холестаз. Лабораторная формула для его определения: нормальный уровень АЛТ, АСТ, ЩФ + повышение ГГТ > 3 ВГН;
- внутрипеченочный интралобулярный каналикулярный холестаз. Лабораторная формула: нормальный уровень АЛТ, АСТ + повышение ГГТ до любого уровня + повышение ЩФ ≤ 3 ВГН;
- внутрипеченочный экстралобулярный (дуктулярный) холестаз. Лабораторная формула: нормальный уровень АЛТ, АСТ + повышение ГГТ до любого уровня + повышение ЩФ ≥ 3 ВГН + нормальный либо повышенный уровень общего и прямого билирубина.
Если же внутрипеченочный холестаз выступает синдромом, сопровождающим острые и хронические заболевания печени, то в лабораторной формуле при указанных трех его клинических вариантах имеет место повышение уровня АЛТ и АСТ. Об алкогольной этиологии заболевания печени с наличием холестаза свидетельствует активность ГГТ, превышающая в 2,5 раза активность ЩФ. Алгоритм диагностики холестаза обобщен на рисунке 3.
СИНДРОМ ПЕЧЕНОЧНО-КЛЕТОЧНОЙ НЕДОСТАТОЧНОСТИ
В основе синдрома печеночно-клеточной недостаточности лежит снижение массы функционирующей паренхимы печени вследствие некрозов гепатоцитов или ее замещения соединительной тканью с развитием цирроза. Синдром печеночно-клеточной недостаточности может развиваться как при острых, так и хронических заболеваниях. Основными лабораторными показателями (маркерами) в оценке синдрома печеночно-клеточной недостаточности являются общий белок, альбумин, ПТВ, ПТИ, общий, прямой и непрямой билирубин [1, 5, 6, 9].
Альбумин – основной белок плазмы крови, который синтезируется исключительно гепатоцитами. Снижение альбумина при патологии печени обусловлено уменьшением их количества и, как следствие, развитием печеночно-клеточной недостаточности. При анализе этого показателя как маркера синдрома печеночно-клеточной недостаточности следует учитывать два факта.
1. Альбумин имеет длительный период полувыведения (14–20 дней), поэтому при острых и даже фульминантных заболеваниях печени, когда полностью прекращается синтетическая функция гепатоцитов, его нормальная концентрация в плазме может сохраняться в течение длительного времени. Вместе с тем при хронических заболеваниях печени гипоальбуминемия служит высокочувствительным маркером печеночно-клеточной недостаточности.
2. Существуют внепеченочные причины гипоальбуминемии, которые необходимо иметь в виду при анализе этого показателя: это вегетарианские диеты, голодание, потеря альбумина (нефротический синдром, мальабсорбция различного генеза, экссудативная энтеропатия), новообразования, аутоиммунные заболевания. Кроме того, следует учитывать, что высокий уровень гамма-глобулинов, который вносит свой вклад в повышение онкотического давления, оказывает депрессивный эффект в отношении синтеза альбумина [7, 9].
ФАКТОРЫ СВЕРТЫВАЮЩЕЙ СИСТЕМЫ КРОВИ В ОЦЕНКЕ ПЕЧЕНОЧНО-КЛЕТОЧНОЙ НЕДОСТАТОЧНОСТИ
Печень синтезирует I, II, V, VII, IX и X факторы свертывающей системы крови. Наиболее часто в клинической практике для подтверждения печеночно-клеточной недостаточности, особенно ее роли в развитии геморрагического синдрома, выполняется исследование протромбина (фактор II), реже – фибриногена (фактор I) и проконвертина (фактор VII).
Для оценки уровня протромбина используются следующие показатели:
- ПТВ – характеризует активность протромбинового комплекса (факторов V, VII, X и собственно протромбина – фактора II). Результат исследования (время свертывания плазмы крови) выражают в секундах. При печеночно-клеточной недостаточности время свертывания удлиняется;
- ПТИ – отношение ВГН ПТВ здорового человека к ПТВ больного в процентах. При печеночно-клеточной недостаточности значение этого показателя снижается;
- МНО – отношение ПТВ больного к стандартному ПТВ. Косвенно отражает результаты ПТВ и ПТИ. При печеночно-клеточной недостаточности величина этого параметра также уменьшается [22].
СИНДРОМ ИММУННОГО ВОСПАЛЕНИЯ (МЕЗЕНХИМАЛЬНО-ВОСПАЛИТЕЛЬНЫЙ СИНДРОМ)
Синдром иммунного воспаления обусловлен реакцией иммунной системы на антигенные стимулы – вирусные и бактериальные антигены или аутоантигены. Персистирующая антигенная стимуляция вызывает стойкую активацию ретикулогистиоцитарной системы, пролиферацию лимфо-, моноцитарных ростков и их перемещение в печеночные дольки и/или портальные тракты. Гистологический маркер синдрома иммунного воспаления – наличие лимфо-, плазмо-, моно-, гистиоцитарной портальной и/или внутридольковой инфильтрации.
Лабораторными маркерами синдрома иммунного воспаления служат неспецифические показатели воспаления (лейкоцитоз, повышение скорости оседания эритроцитов, С-реактивного белка, фибриногена), повышение в сыворотке крови общего белка, иммуноглобулинов класса (Ig) G, M, A, наличие аутоантител при аутоиммунных заболеваниях. Общий белок состоит из 5 фракций, из которых 4 (за исключением гаммаглобулинов) синтезируются преимущественно гепатоцитами. Уровень общего белка возрастает в основном при аутоиммунных поражениях печени. Гиперпротениемия, как правило, обусловлена гипергаммаглобулинемией. Гамма-глобулины включают антитела к вирусам и бактериям, а также аутоантитела к структурам гепатоцитов и/или холангиоцитов. Повышение уровня гамма-глобулинов до 1,5 ВГН расценивается как иммунопатологическая реакция при поражениях печени, а свыше 1,5 ВГН – как включение в патогенез некрозов гепатоцитов или холангиоцитов аутоиммунных механизмов.
Уровень Ig G, М, А при заболеваниях печени повышается, при этом наблюдаются некоторые различия в зависимости от этиологии заболевания. IgG выполняют в организме защитные функции по отношению к патогенным микроорганизмам, вирусам и токсинам в сосудистом русле и экстраваскулярном пространстве, их концентрация увеличивается при хроническом активном гепатите преимущественно вирусной этиологии. IgM оказывают протективное действие в сосудистом русле на ранней стадии бактериемии, виремии, их содержание возрастает на фоне первичного билиарного холангита и других холестазов. IgA осуществляют защиту слизистых оболочек от патогенных микроорганизмов и потенциальных аутоаллергенов, содержатся в различных секретах (слюна, мокрота, желчь и других секретах ЖКТ) и повышаются преимущественно при алкогольных поражениях печени.
При аутоиммунных заболеваниях печени имеет место увеличение уровня Ig всех классов [7].
В настоящее время большой интерес вызывают неинвазивные методы диагностики заболеваний печени, в частности наиболее распространенной гепатопатологии – НАЖБП, а также фиброза печени, основанные на измерении и оценке клинических параметров и содержания биомаркеров в сыворотке крови. Ниже представлены наиболее известные клинико-биохимические шкалы и индексы в диагностике стеатоза, фиброза и цирроза печени [23–26].
ОСНОВНЫЕ НЕИНВАЗИВНЫЕ МЕТОДЫ СКРИНИНГА СТЕАТОЗА ПЕЧЕНИ
Шкала HAIR (Hypertension, ALT and Insulin Resistance) позволяет прогнозировать НАЖБП у пациентов с морбидным ожирением (индексом массы тела не менее 35 кг/м2). Метод основан на оценке трех показателей: артериальной гипертензии (АГ) – 1 балл; АЛТ > 40 Ед/л – 1 балл; индекса резистентности к инсулину > 5,0 – 1 балл. Присутствие минимум двух указанных параметров имеет высокую диагностическую чувствительность (80%) и специфичность (89%) в отношении НАЖБП. Наличие всех трех факторов позволяет уверенно говорить о наличии НАЖБП у пациента.
Индекс стеатоза печени FLI (Fatty Liver Index) включает оценку уровня триглицеридов и гамма-глутамилтрансферазы в сыворотке крови, индекс массы тела (ИМТ), объем талии. Формула для расчета этого индекса построена на сложных логарифмических вычислениях, поэтому для удобства можно использовать соответствующие онлайн-калькуляторы (например, https://www.mdapp.co/fatty-liver-index-fli-calculator-356/). Значение FLI < 30 исключает (чувствительность метода 87%), а показатель ≥ 60 подтверждает (специфичность 86%) наличие стеатоза печени.
Индекс стеатоза печени НIS (Hepatic Steatosis Index) рассчитывается исходя из оценки отношения АЛТ/АСТ, ИМТ, пола, наличия сахарного диабета по следующей формуле: 8 × (АЛТ/АСТ) + ИМТ + 2 (если пациент – женщина) + 2 (если имеется сахарный диабет). Пороговое значение HSI > 36,0 свидетельствует в пользу наличия стеатоза печени с чувствительностью 93,1% и специфичностью 92,4%.
ОСНОВНЫЕ НЕИНВАЗИВНЫЕ МЕТОДЫ СКРИНИНГА ФИБРОЗА ПЕЧЕНИ
При выраженном фиброзе соотношение АСТ/АЛТ превышает 1. Этот параметр применяется в ряде многокомпонентных моделей диагностики НАЖБП и фиброза печени.
Шкала BARD (BMI, AST/ALT Ratio and Diabetes Score) включает анализ суммы баллов трех показателей: соотношение АСТ/АЛТ ≤ 0,8 – 2 балла; ИМТ ≥ 28 кг/м2 – 1 балл; наличие сахарного диабета 2-го типа – 1 балл. Количество баллов 0–1 с высокой вероятностью указывает на отсутствие выраженного фиброза печени (прогностическая ценность отрицательного результата 96%). Результат ≥ 2 баллов свидетельствует о минимальной вероятности III–IV стадии фиброза.
Шкала NFS (Nonalcoholic Fatty Liver Disease Fibrosis Score) учитывает возраст, уровень глюкозы в крови, ИМТ, количество тромбоцитов, уровень альбумина и соотношение АСТ/АЛТ. Расчет проводится по формуле: -1,675 + 0,037 × возраст (годы) + 0,094 × ИМТ (кг/м2) + 1,13 × гипергликемия или сахарный диабет (да = 1, нет = 0) + 0,99 × АСТ/АЛТ - 0,013 × тромбоциты (×109/л) - 0,66 × альбумин (г/дл). Для определения значений индекса по шкале NFS можно использовать онлайн-калькулятор (https://nafldscore.com/). Величина индекса менее -1,455 с чувствительностью 90% и специфичностью 60% говорит о минимальной вероятности фиброза F3 и F4, тогда как показатель более 0,676 (чувствительность 67% и специфичность 97%) указывает на выраженный фиброз печени.
Индекс фиброза по шкале APRI (AST / Platelet Ratio Index) вычисляется по формуле: АСТ (Ед/л) / (верхний предел нормы АСТ в Ед/л) × 100 / тромбоциты (109/л). Если показатель не превышает 0,5, то вероятность фиброза печени низка (отрицательное прогностическое значение 83%), если же превышает 1,5, то с высокой вероятностью можно констатировать фиброз печени (положительное прогностическое значение 68,4%).
Шкала FIB-4 (Index for Liver Fibrosis-4) включает оценку возраста, АСТ, АЛТ, количества тромбоцитов по формуле: возраст × АСТ (Ед/л) / тромбоциты (×109/л) × √АЛТ (Ед/л). Значение > 2,67 говорит в пользу фиброза F3 и F4, < 1,3 – о минимальной вероятности этого состояния.
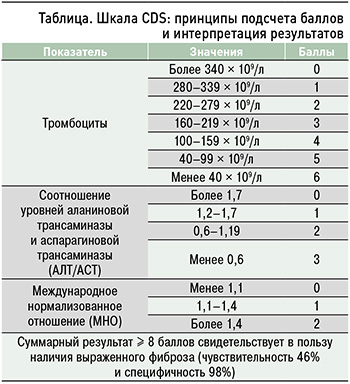
При применении Шкалы CDS (Cirrhosis Discriminant Score) в расчет берутся уровень тромбоцитов в крови, отношение АЛТ/АСТ и показатель свертываемости крови (МНО); значения полученных показателей выражаются в баллах (табл.).
Шкала MELD (Model for End-Stage Liver Disease) применяется с целью объективной оценки тяжести состояния больного и прогнозирования течения заболевания печени. Показатель по этой шкале определяется с использованием формулы: 10 × [0,957 ln (креатинин в мкмоль/л / 88,4)] + 0,378 ln (общий билирубин в мкмоль/л / 17,1) + 1,12 (МНО) + 6,43. Для расчета результата по MELD также можно использовать соответствующий онлайн-калькулятор (https://www.mayoclinic.org/medical-professionals/model-end-stage-liver-disease/meld-model). При значениях > 35 баллов летальный исход прогнозируется в 80%, 20–34 баллов – в 10–60% случаев. Если результат составляет < 8 баллов, то пациент относительно стабилен и может находиться на амбулаторном лечении.
ЗАКЛЮЧЕНИЕ
Таким образом, применение и правильная интерпретация скрининговых биохимических проб печени позволяет врачу решить ряд важных клинических задач: выявить патологию печени, предположить ее этиологию и патогенетические механизмы прогрессирования, определить степень активности, наличие фиброза, разработать оптимальный подход к лечению пациента и мониторировать его эффективность, избегая при этом выполнения биопсии печени. Дополнительное использование представленных расчетных шкал и индексов дает возможность не только уточнить диагноз заболевания, но и определить степень тяжести патологического процесса, прогнозировать выживаемость пациентов и определить показания для трансплантации печени.



