Одним из основных клинических проявлений эндометриоза является тазовая боль. Согласно данным литературы, почти 95% женщин с эндометриозом сообщают о наличии у них хотя бы одного из проявлений болевого синдрома [1]. Спектр эндометриоз-ассоциированных болевых симптомов широко варьирует от наиболее часто встречающихся – дисменореи до менее распространенных, таких как хроническая тазовая боль (ХТБ), диспареуния, дисхезия, дизурия, миалгии, мигрень и другие. Однако степень выраженности болевого синдрома не всегда коррелирует с распространенностью эндометриоза, визуализируемой при лапароскопии, а хирургическое иссечение эндометриоидных очагов в ряде случаев не уменьшает тяжесть тазовой боли [2, 3]. Следует отметить, что природа эндометриоз-ассоциированной тазовой боли многокомпонентная; в ее генезе играют роль не только активация ангио- и нейрогенеза, но и центральная сенситизация (ЦС), способствующая хронизации болевого синдрома и даже персистенции его после радикального хирургического лечения [4, 5]. На качество жизни пациентов с ХТБ при эндометриозе могут влиять сопутствующие ему состояния, ассоциированные с ЦС, такие как интерстициальный цистит, синдром раздраженного кишечника (СРК), миалгия, вульводиния [6].
Несмотря на разноречивость данных литературы о взаимосвязи степени распространенности эндометриоза и интенсивности болевого синдрома [3, 7–9], прослеживается тенденция к ассоциации выраженности клинических симптомов с их множественностью. Так, примерно каждая 2-я пациентка с эндометриозом предъявляет жалобы на сочетание дисменореи, диспареунии и ХТБ [10, 11]. Кроме того, единичные исследования демонстрируют, что для эндометриоидных кист яичников (ЭК) не характерен болевой синдром, а наличие тазовой боли чаще сопряжено с сопутствующими другими формами – перитонеальным (ПЭ) и глубоким эндометриозом (ГЭ) [12, 13].
В клинической практике степень выраженности тазовой боли оценивают по 11-балльной визуальной аналоговой шкале (ВАШ). Так, например, вероятность наличия эндометриоза увеличивается при интенсивности дисменореи ≥6 баллов, ХТБ≥2 баллов и диспареунии ≥3 баллов по ВАШ [14, 15]. Было установлено, что клиническое значение имеет не только степень выраженности симптомов, но и их сочетание друг с другом с учетом вышеуказанных пороговых значений [14]. В настоящее время продолжается поиск клинических предикторов эндометриоза для его своевременной диагностики. Одними из основоположников данного направления можно считать Ballard K.D. et al., которые в 2008 г. выявили взаимосвязь риска развития эндометриоза с увеличением числа сопутствующих симптомов и коморбидных состояний [16]. В свою очередь, коллектив ученых из Франции предложил онлайн-опросник из 21 пункта, созданный на базе результатов собственных исследований и опросника ENDOPAIN-4D, позволяющих оценить вероятность наличия эндометриоза на основании различных характеристик болевого синдрома и ряда других его клинических проявлений [17]. В литературе имеются и другие публикации по созданию прогностических моделей риска эндометриоза, основанные на данных анамнеза пациенток, их семейной отягощенности, степени выраженности тазовой боли и наличия эндометриоз-ассоциированных сопутствующих заболеваний [18, 19]. Однако предложенные прогностические модели несовершенны, и все еще ведется поиск значимых предикторов развития эндометриоза.
В связи с этим целью настоящего исследования явилась оценка болевого синдрома у пациенток с различными формами наружного генитального эндометриоза (НГЭ) и определение значимости ЦС и нейропатического компонента в генезе боли при эндометриозе.
Материалы и методы
Одномоментное исследование проводилось на базе ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» МЗ РФ в период с 2021 г. по 2023 г.; были включены 200 женщин в возрасте от 18 до 49 лет (средний возраст 32,03 (7,15) года, средний индекс массы тела – 21,35 (3,35) кг/м2). Всем пациенткам с подозрением на генитальный эндометриоз были проведены экспертное ультразвуковое исследование (УЗИ) и магнитно-резонансная томография органов малого таза (МРТ ОМТ). У 54% пациенток НГЭ был лапароскопически и гистологически верифицирован: у 63/200 (31,5%) – во время предшествующего оперативного вмешательства до момента включения в исследование, у 45/200 (22,5%) – при последующей первой плановой операции.
Критерии исключения: отсутствие признаков НГЭ по данным МРТ, онкологические заболевания женской репродуктивной системы в настоящий момент или в анамнезе, тяжелые соматические заболевания, требующие стационарного лечения, беременность и лактация, прием супрессивной гормонотерапии как минимум за 3 месяца до момента включения в исследование. Алгоритм формирования выборки пациенток представлен на рисунке 1, итоговое количество женщин, включенных в исследование, составило 200, что является репрезентативной выборкой в целом и для каждой из подгрупп в отдельности.
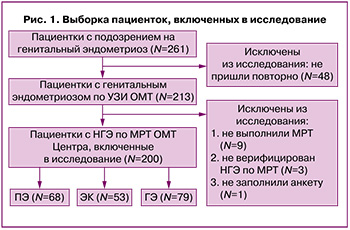
МРТ ОМТ выполнялось с помощью МРТ-аппаратов GE Signa Excite 1.5T и GE Signa Architect 3.0T, использование контрастного усиления проводилось в случаях необходимости дифференциальной диагностики эндометриоза, а также как вспомогательный инструмент визуализации экстрагенитальных форм эндометриоза. При МРТ выполнялась оценка интенсивности сигналов на Т1- (Т1ВИ) и Т2-взвешенных изображениях (Т2ВИ), выполненных в сагиттальной, аксиальной и корональной плоскостях, а также на диффузионно-взвешенных изображениях с использованием толщины среза 0,3 см и поля зрения 32–42 см. Визуальная диагностика ЭК, ГЭ и экстрагенитального эндометриоза осуществлялась согласно рекомендациям Европейского общества урогенитальной радиологии [20]. Предполагаемый диагноз ПЭ устанавливался при наличии в области малого таза МР-признаков эндометриоидных гетеротопий с пикулообразными неоднородными контурами размерами менее 0,5 см, с гипоинтенсивным сигналом на Т2ВИ, локализованными по серозному покрову матки, на связочном аппарате, включая крестцово-маточные связки, а также брюшине и пузырно-маточной, параметриальной клетчатке [21–25]. В зависимости от предполагаемой формы эндометриоза, выявленной по данным МРТ, пациентки были распределены на 3 группы: с ПЭ, ЭК и ГЭ; при сочетанной патологии включение в ту или иную группу осуществлялось по наиболее тяжелой форме эндометриоза.
Всем женщинам проводились сбор анамнеза с учетом данных о наличии негинекологических заболеваний, ассоциированных с болевым синдромом, а также анкетирование. ХТБ определялась как наличие ациклической боли внизу живота, не связанной с менструацией, овуляцией или половым актом, на протяжении как минимум 6 месяцев. Оценка диспареунии и расчет индекса тазовой боли (ИТБ) проводились только среди женщин, живущих половой жизнью. Бесплодие определялось как отсутствие наступления беременности при регулярной половой жизни без предохранения в течение 12 месяцев; его оценка проводилась только среди женщин, планирующих беременность.
Оценка степени выраженности дисменореи, диспареунии, ХТБ, дисхезии и дизурии осуществлялась с помощью 11-балльной ВАШ, рассчитывался ИТБ, где Д1 – дисменорея, Д2 – диспареуния, Д3 – дисхезия, Д4 – дизурия, 5 – число показателей:
Для определения уровня ЦС было проведено анкетирование с использованием опросника Central Sensitization Inventory (шкала ЦС); наличие нейропатического компонента боли оценивалось по опроснику PainDetect; для оценки уровня качества жизни использовали анкету SF-12; для оценки сексуальной функции – 5-балльную шкалу Лайкерта [26–28]. Точка отсечения, определяющая наличие симптомов ЦС – ≥40 баллов, нейропатического компонента – ≥19 баллов. Интерпретация полученных результатов шкал проводилась врачом-неврологом. Перед проведением расчета полученного материала все данные были полностью обезличены. Исследование одобрено этическим комитетом ФГБУ «НМИЦ АГП им. академика В.И. Кулакова» МЗ РФ.
Статистический анализ
Для количественных показателей были рассчитаны: среднее значение (М), среднеквадратическое отклонение (SD), медиана (Ме), интерквартильный интервал (Q1; Q3). Для качественных и порядковых показателей – частоты (%). Все полученные количественные параметры были проверены на соответствие нормальному распределению с помощью критерия Шапиро–Уилка. Числовые параметры, имеющие нормальное распределение, представлены в формате М (SD). Параметры, имеющие распределение, отличное от нормального, представлены в формате Ме (Q1; Q3). Сравнение двух независимых выборок (количественные признаки) проводилось по критерию Манна–Уитни. Для попарного сравнения групп по категориальным признакам проводили с помощью точного критерия Фишера. Как для одного, так и для другого критерия использовали поправку Бонферрони. Для оценки порогового значения балла ИТБ использовался ROC-анализ с определением показателя AUC (Area Under Curve, или площадь под кривой) с указанием доверительного интервала. Анализ данных проводился в программе IBM SPSS Statistics (v.26). Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Результаты
В структуре НГЭ, визуализированного с помощью МРТ ОМТ, ПЭ был верифицирован у 68/200 (34%), ЭК – у 53/200 (26,5%), ГЭ – у 79/200 (39,5%) пациенток. В каждом 4-м случае ГЭ сопутствовал колоректальный эндометриоз (КРЭ) (22/79, 27,8%), у 7,6% женщин – экстрагенитальный эндометриоз других локализаций (мочевого пузыря, рубца, аппендикса, легких). Изолированные ЭК наблюдались лишь в 4,5% случаев, в 22% – сочетались с ПЭ и в 2,5% – с ГЭ. Наличие всех 3 форм НГЭ отмечалось у каждой 5-й пациентки (рис. 2). В дальнейшем пациентки была разделены на группы в соответствии с наиболее тяжелой формой НГЭ на ПЭ (n=68), ЭК (n=53) и ГЭ (n=79).
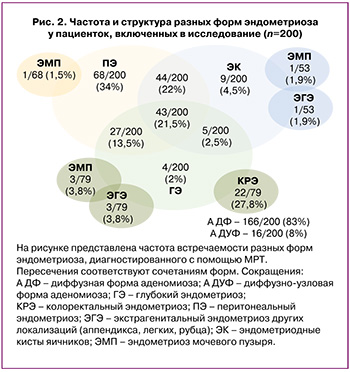
Пациентки всех трех групп были сопоставимы по своим клиническим характеристикам, за исключением более старшего возраста и большей частоты предшествующего оперативного лечения, в том числе – неоднократного, при ГЭ в сравнении с ПЭ и ЭК (табл. 1). Так, если при наличии ПЭ ранее была оперирована каждая 4-я, при ЭК – каждая 3-я, то при ГЭ – практически каждая 2-я женщина.
Каждая 2-я пациентка до момента включения в исследование уже получала гормонотерапию; статистически-значимой разницы между группами выявлено не было. Каждая 5-я женщина имела семейную отягощенность по эндометриозу; каждая 2-я из числа планирующих беременность предъявляла жалобы на бесплодие.
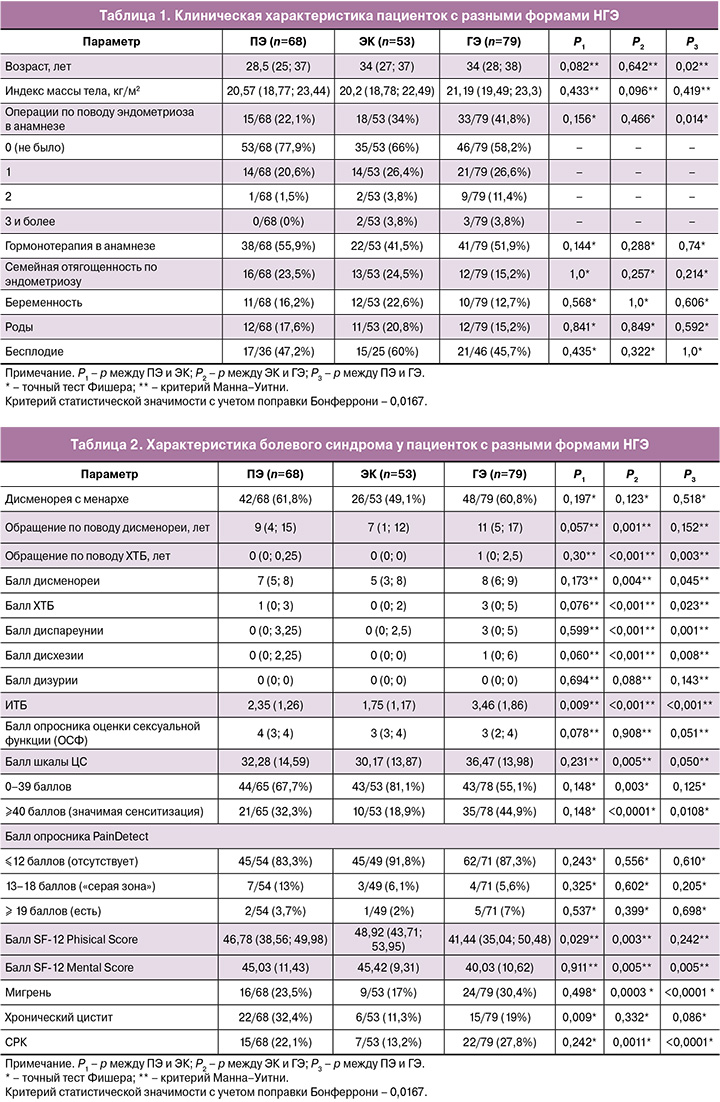
Данные, представленные в таблице 2, иллюстрируют статистически значимую разницу по всем показателям болевого синдрома между группами. Пациентки с ЭК имели менее выраженную тазовую боль в отличие женщин с ПЭ и ГЭ, что наглядно демонстрирует ИТБ: 3,46 (1,86) балла – при ГЭ, 2,35 (1,26) балла – при ПЭ, и лишь 1,75 (1,17) балла – при ЭК (р<0,001). Кроме того, данная группа женщин преимущественно характеризовалась наличием дисменореи средней степени выраженности, в то время как с ПЭ и ГЭ – высокой интенсивности.
Пациентки с ГЭ характеризовались статистически значимо более высоким средним баллом по шкале ЦС. Процент значимой сенситизации (≥40 баллов) был установлен практически у каждой 2-й женщины с ГЭ, у каждой 3-й – с ПЭ и лишь у каждой 5-й – с ЭК. При парном сравнении групп отмечалось, что при ГЭ статистически значимо чаще отмечалось наличие сенситизации в сравнении с пациентками с ЭК (р<0,0001) и ПЭ (р=0,0108). Схожая тенденция прослеживалась и в отношении коморбидных эндометриозу негинекологических заболеваний, ассоциированных с ЦС. При попарном сравнении было показано, что наличие сопутствующей мигрени и СРК в большей степени характерно для пациенток с ГЭ в сравнении с ПЭ (р<0,0001 в обоих случаях сравнения) и ЭК (р=0,0003 и р=0,0011 для мигрени и СРК соответственно) (табл. 2).
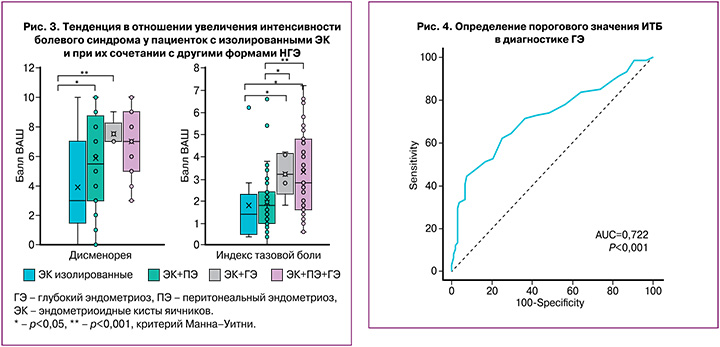
При более детальном анализе полученных данных была установлена тенденция в отношении наименьшей степени выраженности болевого синдрома по показателям дисменореи и ИТБ при изолированных ЭК и их сочетании с ПЭ с увеличением интенсивности тазовой боли при сочетании кист с ГЭ и при наличии всех 3 форм НГЭ (рис. 3).
Результаты опросника PainDetect продемонстрировали, что высокая вероятность нейропатического компонента боли отмечалась лишь у 5% пациенток с эндометриозом, а 8% пациенток находились в так называемой «серой зоне», характеризующейся как неопределенный результат, означающий возможное присутствие нейропатического компонента.
В ходе опроса пациенток, имеющих соответствующие жалобы, было установлено, что в общей когорте женщин с эндометриозом среднее время от момента возникновения дисменореи до верификации диагноза составило 10 (3,5; 15) лет, а от момента возникновения ХТБ – лишь 1 (0; 3) год. Пациентки с ЭК имели статистически значимо меньший интервал до постановки диагноза, составляющий 7 (1; 12) лет, что, вероятно, связано с тем, что эндометриомы многократно чаще выявляются с помощью УЗИ ОМТ, в отличие от других форм эндометриоза. Несмотря на выраженную дисменорею при ГЭ, составляющую в среднем 8 (6; 9) баллов по ВАШ, это не способствовало уменьшению времени до постановки диагноза; в то время как ХТБ явилась более значимым симптомом и поводом для более быстрого обращения за медицинской помощью.
С целью улучшения диагностики НГЭ с помощью ROC-анализа был произведен расчет порогового значения ИТБ. Было установлено, что при ИТБ≥3,8 балла можно предполагать наличие ГЭ с чувствительностью 44,59% и специфичностью 92,52% (AUC 0,722 (0,04) [95% ДИ 0,651;0,786], р<0,001) (рис. 4).
Обсуждение
Одним из основных принципов ранней диагностики эндометриоза, направленной на снижение риска его прогрессирования в более тяжелые формы, остается адекватная оценка симптомов заболевания. Однако спектр клинических проявлений эндометриоза разнообразен и часто не ограничивается «классическими» проявлениями – дисменореей, диспареунией, ХТБ и бесплодием; а вопрос о связи этих симптомов со степенью распространенности эндометриоза остается дискуссионным. Так, в исследовании Ashkenazi et al. с участием 2964 пациенток с различными стадиями эндометриоза по классификации Американского общества по репродуктивной медицине (ASRM) было показано, что менструально-ассоциированная боль в большей степени связана с I стадией заболевания; в то время как ХТБ, напротив, наблюдалась преимущественно при II, III и IV стадии; наличие других «не классических» болевых ощущений и частота бесплодия положительно коррелировали со стадией заболеваний [29]. Zhao H. et al. на основе логистического регрессионного анализа показали, что при наличии болевого синдрома интенсивностью ≥4 баллов по ВАШ и болезненности при пальпации в области крестцово-маточных связок можно предполагать у пациентки IV стадию заболевания с чувствительностью 87,2% и специфичностью 71,0% (AUC 0,760 [95% ДИ 0,677; 0,842]) [7]. В настоящем исследовании было показано, что пациентки с ГЭ, в отличие от пациенток с ПЭ и ЭК, имеют более выраженную дисменорею, диспареунию, ХТБ и дисхезию, а также статистически значимо более низкие баллы опросника оценки здоровья SF-12 как по физической, так и по психической его шкале, что, вероятно, напрямую связано с более выраженным болевым синдромом у данной группы женщин.
В сравнении с определением степени выраженности только дисменореи или ХТБ, которые не всегда коррелируют с тяжестью и распространенностью НГЭ, более информативным показателем можно считать ИТБ, который учитывает и другие, не столь распространенные проявления болевого синдрома – дизурию и дисхезию. Так, несмотря на полученную статистическую значимость между сравниваемыми группами, нельзя четко разграничить ПЭ и ГЭ по степени выраженности дисменореи, составившей 7 (5; 8) и 8 (6; 9) баллов по ВАШ соответственно; в то время как средняя величина ИТБ при ГЭ оказалась в 1,5 раза выше в сравнении с ПЭ, в 2 раза выше – в сравнении с ЭК (ИТБ 3,46 (1,86) балла при ГЭ; 2,35 (1,26) балла при ПЭ; 1,75 (1,17) балла при ЭК). По результатам ROC-анализа было показано, что при ИТБ≥3,8 балла можно предполагать наличие ГЭ с чувствительностью 44,59% и специфичностью 92,52% (AUC 0,722 (0,04) [95% ДИ 0,651;0,786], р<0,001).
Высоковероятный нейропатический компонент боли отмечался лишь у 5% пациенток с эндометриозом. Однако не было установлено значимых отношений между баллом опросника PainDetect и степенью выраженности дисменореи, ХТБ и других проявлений болевого синдрома. Konrad L. et al. в своем исследовании продемонстрировали сопоставимые результаты на схожей по количеству выборке пациенток; доля женщин с эндометриозом и наличием нейропатического компонента боли составила лишь 4,2% при отсутствии статистически значимой разницы с группой контроля (1,1%). В связи с этим было сделано заключение, что нейропатическая боль не является основной при эндометриозе [30]. Однако в исследовании был получен статистически значимо больший балл PainDetect при тяжелом эндометриозе, чего не наблюдалось по данным настоящего исследования. Согласно данным литературы, нейропатический компонент боли может быть связан с активацией малых сенсорных волокон в эндометриоидных очагах, которая в совокупности с воспалением приводит к возникновению смешанного болевого синдрома [31, 32], а также может быть следствием изменений в центральной нервной системе, а именно ЦС [33].
Известно, что ЦС играет важную роль в формировании ХТБ, в том числе – при эндометриозе. По результатам настоящего исследования, значимая сенситизация отмечалась у каждой 3-й пациентки с НГЭ; балл шкалы ЦС статистически значимо разнился в зависимости от формы эндометриоза: баллы ≥40 отмечались у каждой 2-й пациентки с ГЭ, у каждой 3-й – с ПЭ и лишь у каждой 5-й – с ЭК. Это может иметь значение при направлении пациенток с болевым синдромом на оперативное лечение, поскольку при более высоком балле шкалы ЦС может не наблюдаться значимого уменьшения имеющейся клинической симптоматики [34]. Кроме того, при более тяжелой форме НГЭ – ГЭ, в сравнении с женщинами с ПЭ и ЭК, статистически значимо чаще встречаются сопутствующие заболевания, ассоциированные с ЦС, такие как мигрень и СРК. В более раннем исследовании было показано, что у женщин с эндометриозом и мигренью чаще встречаются дисменорея, ХТБ, диспареуния и дисхезия, а также более высокие средние значения ИТБ, чем при эндометриозе без сопутствующей мигрени [33].
Заключение
В диагностике эндометриоза на амбулаторном этапе обследования более важную роль играет оценка степени выраженности болевого синдрома, чем факт его наличия. Выделение женщин группы риска по развитию эндометриоза позволяет своевременно проводить комплексное обследование, включая МРТ ОМТ, направленное на выявление более тяжелых форм эндометриоза уже на первичном амбулаторном приеме. На основании расчета значений ИТБ можно предполагать наличие ГЭ. Такой подход в перспективе может позволить сократить время до постановки диагноза с последующим персонифицированным решением вопроса о тактике ведения пациенток.
Результаты проведенного исследования позволяют сделать заключение о том, что существенный вклад в генез болевого синдрома у пациенток с НГЭ вносит ЦС, в то время как нейропатический компонент не является столь значимым.



