ВВЕДЕНИЕ
На сегодняшний день наблюдается высокая распространенность неалкогольной жировой болезни печени (НАЖБП), которая, наряду с метаболическим синдромом и ожирением, часто ассоциируется с другими часто встречающимися кардиометаболическими заболеваниями, такими как сахарный диабет (СД) 2-го типа и хроническая болезнь почек (ХБП) [1, 2].
В последнее время большое внимание уделяется роли висцерального жира в развитии и прогрессировании НАЖБП. Клинические и эпидемиологические исследования показывают прямую корреляцию между содержанием жира в печени и висцеральным жиром. Площадь висцерального жира имеет тесную связь с метаболическими нарушениями и служит более точным маркером абдоминального ожирения, чем индекс массы тела (ИМТ) и окружность талии (ОТ) [3]. Высокий уровень липопротеина (а) (Лп(а)) – фактор риска заболеваний сердечно-сосудистой системы, таких как атеросклероз, инфаркт миокарда и инсульт, однако данные о его ассоциации с НАЖБП на сегодняшний день довольно противоречивы [4].
Большинство лиц с НАЖБП, особенно молодого возраста, не имеют симптомов, поэтому важную роль играет скрининг на начальной стадии болезни. Вопрос о том, является ли рутинный скрининг на стеатоз печени у бессимптомных пациентов из группы высокого риска практичным или экономически эффективным, остается предметом споров, поскольку у преобладающей их части течение заболевания, скорее всего, будет неосложненным и непрогрессирующим [5]. Однако его выявление имеет важное клиническое значение, поскольку стеатотическая болезнь печени, которая когда-то считалась относительно доброкачественной и имела благоприятный прогноз, сопряжена с повышенным риском общей смертности и смертности, связанной с заболеваниями печени [6].
Цель исследования – разработать модель прогнозирования НАЖБП у лиц молодого возраста.
МАТЕРИАЛ И МЕТОДЫ
В исследование «случай – контроль» было включено 100 человек, разделенных на две группы и сопоставимых по полу: группа 1 («случаи») – пациенты с НАЖБП (n = 50); группа 2 («контроли») – лица без НАЖБП (n = 50).
Критерии включения в исследование: молодой возраст (18–44 лет), подписанное информированное согласие на участие в исследовании.
Критерии невключения: эндокринологические заболевания, включая СД 1-го и 2-го типа, острые и хронические заболевания печени, ассоциированные клинические состояния (инсульты, инфаркты), ХБП С3б–С5 стадии, инфекционные, онкологические заболевания, постоянный прием лекарственных средств на момент включения в исследование (антигипертензивных, гиполипидемических, сахароснижающих препаратов, у женщин – комбинированных гормональных контрацептивов), беременность и период лактации.
Проводились сбор жалоб и анамнеза, анкетирование, измерение артериального давления (АД), антропометрических показателей – веса и роста для расчета индекса массы тела (ИМТ, кг/м2), окружности талии и бедер (с помощью гибкой узкой неэластичной ленты). Окружность талии (ОТ) определялась посередине между нижними ребрами и гребнем подвздошной кости, окружность бедер (ОБ) – по наибольшей окружности вокруг ягодиц.
Биохимические показатели (глюкоза плазмы крови, инсулин, общий холестерин, холестерин липопротеидов высокой плотности, холестерин липопротеидов низкой плотности и триглицериды, уровни аланинтрансаминазы, аспарагинтрансаминазы в сыворотке крови) измерялись после 8-часового ночного голодания.
Инсулинорезистентность оценивалась с использованием индекса оценки инсулинорезистентности (HOMA-IR).
Выполнялось определение уровня сывороточных адипокинов (лептина, адипонектина, ингибитора активатора плазминогена 1-го типа).
Уровень Лп(а) устанавливался с использованием набора реагентов AssayMax Human Lp (a) ELISA. Метод основан на иммуноферментном анализе типа «сэндвич», время анализа составляет около 4 ч.
Состояние композиционного состава тела анализировалось при помощи биоэлектрического импеданса (Inbody 370). Комплексная оценка состава тела включала измерение ИМТ, процентного содержания жира тела, индекса ОТ/ОБ, а также уровня висцерального жира (в кг) как наиболее опасной разновидности жира в человеческом организме (именно он, накапливаясь между органами в брюшной полости, повышает риск развития кардиометаболических заболеваний).
Диагноз НАЖБП подтверждался на основании проведения ультразвуковой эластографии сдвиговой волной (Aixplorer, Франция) с оценкой эластичности и жесткости печени.
Статистическая обработка данных осуществлялась с помощью пакета программ MedCalc (2023). В рамках анализа количественных показателей в случае значений, отличных от нормального распределения, использовался критерий Манна – Уитни, при нормальном распределении – средние величины со стандартным отклонением. Для оценки качественных категорий применялись χ2 Пирсона и точный тест Фишера. Разработка диагностической модели НАЖБП у лиц молодого возраста выполнялась посредством метода логистической регрессии.
В ходе использования диагностической модели рассчитывался показатель р для определения вероятности наличия НАЖБП у пациентов молодого возраста: при logit(p) ≥ 0,04 у пациента определялась высокая вероятность наличия НАЖБП, при logit(p) < 0,04 – низкая. Результаты считались статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Общая характеристика исследованных групп представлена в таблице 1. Средний возраст пациентов с НАЖБП составил 38 [34–40] лет, участников из группы контроля – 34,5 [28–38] года (p = 0,004).
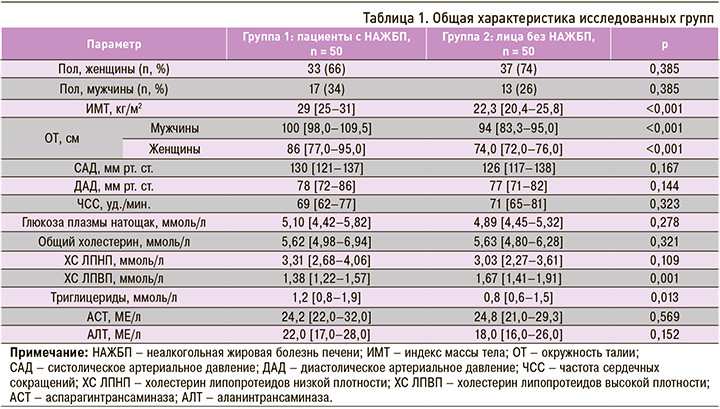
Различий по полу в группах сравнения получено не было. Величины ИМТ и ОТ оказались выше среди пациентов с НАЖБП в сравнении с контролем. Кроме того, у участников 1-й группы выявлялись более высокие уровни триглицеридов (ТГ) и более низкие концентрации холестерина липопротеидов высокой плотности (ХС ЛПВП). Систолическое, диастолическое АД, частота сердечных сокращений, равно как и лабораторные показатели глюкозы крови, общего холестерина, холестерина липопротеидов низкой плотности (ХС ЛПНП), аланинтрансаминазы (АЛТ) и аспарагинтрансаминазы (АСТ), в группах значимо не отличались.
Результаты оценки композиционного состава тела представлены в таблице 2. При его исследовании статистически значимые различия были получены по всем изучавшимся параметрам.
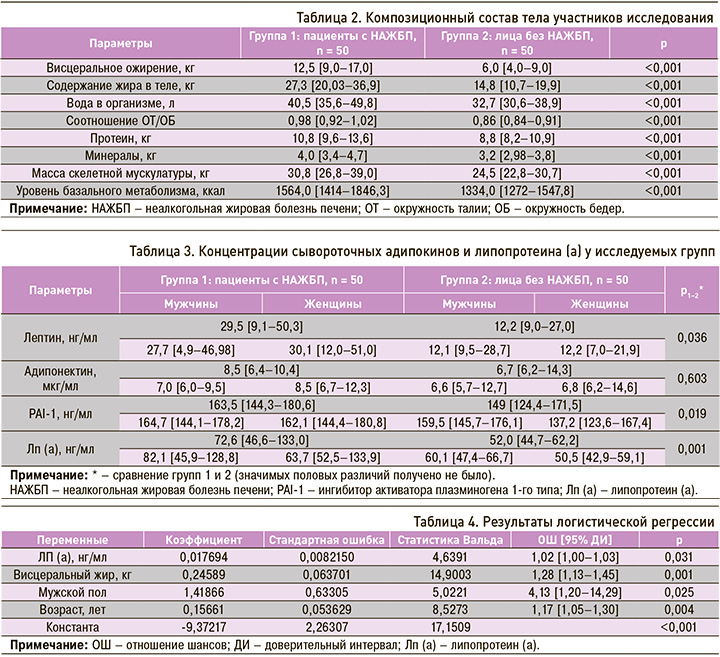
Результаты измерения сывороточных адипокинов и Лп(а) приведены в таблице 3.
У пациентов с НАЖБП отмечались наиболее высокие концентрации лептина, ингибитора активатора плазминогена 1-го типа и Лп(а), при этом в ходе сравнения мужчин и женщин были выявлены половые различия по уровню адипонектина, хотя в связи с малочисленностью групп, разделенных по полу, эти различия не были достоверными.
Модель логистической регрессии была построена для прогнозирования развития НАЖБП с использованием оптимального набора параметров в полном наборе исследований (табл. 4). Полученная регрессионная модель оказалась статистически значимой (p < 0,0001). Коэффициент детерминации Найджелкерка составил 55,14%.
Согласно модели, уравнение логистической регрессии выглядит следующим образом:
logit(p) = -9,37 + 0,02 × Лп(а) (нг/мл) + 0,25 × висцеральный жир (кг) + 1,42 × мужской пол (1/0) + 0,16 × возраст (лет).
Для дополнительной оценки качества модели мы провели ее ROC-анализ. Качество ROC-анализа оценивалось исходя из площади под ROC-кривой: AUC составила 0,89 (95% доверительный интервал: 0,81–0,94), чувствительность – 80%, специфичность – 82% в точке отсечения logit(p) = 0,04.
Разработанный нами способ диагностики НАЖБП у лиц молодого возраста далее был независимо апробирован на 60 пациентах молодого возраста в 2021–2022 гг. Чувствительность метода составила 81%, специфичность – 81%.
ОБСУЖДЕНИЕ
Прогностические модели в медицине представляют собой сложные инструменты, объединяющие две и более характеристики (параметра) исследуемых пациентов. Они имеют потенциальную ценность при принятии сложных клинических решений (назначение инвазивных методов диагностики, отбор пациентов для включения в клинические исследования, выбор вариантов лечения с учетом предпочтений пациента и т. д.). Вместе с тем в клинической практике обычно используются лишь немногие из таких моделей. В последние десятилетия большое значение приобрели неивазивные методы выявления НАЖБП у бессимптомных пациентов. Попытки разработать неинвазивные подходы для стратификации лиц с этим заболеванием привели к появлению различных диагностических панелей, индексов и методов визуализации, которые можно было бы применять вместо биопсии печени. На сегодняшний день разработано несколько моделей верификации стеатоза печени. Для неинвазивной диагностики и стадирования НАЖБП берутся в расчет такие параметры, как антропометрические данные, биохимические показатели липидного и углеводного обмена, уровни печеночных ферментов.
Не первый год обсуждается и изучается более весомая роль висцерального ожирения в развитии НАЖБП по сравнению с общим содержанием жира в организме [3]. В то же время существующие модели прогнозирования, даже с учетом висцерального жира, применялись лишь в отношении взрослых пациентов старше 40 лет, уже имеющих сердечно-сосудистые заболевания [7]. Поскольку продолжительность воздействия инсулинорезистентности, вероятно, является ключевым фактором в развитии НАЖБП, разумно предположить, что проведение скрининга среди бессимптомных молодых людей может быть полезно как для ранней диагностики этой болезни, так и для более эффективного выявления поздних ее стадий в молодом возрасте.
В настоящее время доступны неоднородные сообщения об ассоциации Лп(а) с различными кардиометаболическими заболеваниями [8]. Так, эпидемиологические и клинические исследования подтвердили причинно-следственную связь между его повышенными концентрациями и риском сердечно-сосудистых патологий [9]. В то же время Gudbjartsson D.F. et al. продемонстрировали обратную связь между уровнем Лп(а) и риском развития СД 2-го типа [10]. В нескольких исследованиях оценивалась взаимосвязь концентраций этого биомаркера и хронических заболеваний печени, таких как НАЖБП, цирроз и гепатоцеллюлярная карцинома. Исходя из их результатов, было сделано предположение, что уровень циркулирующего Лп(а) снижается при гепатодепрессии [11]. В нашем исследовании значения данного показателя оказались выше у молодых пациентов с НАЖБП по сравнению с лицами без этого заболевания, особенно среди мужчин.
Метод логистической регрессии представляет собой классический способ прогнозирования, применявшийся в тысячах исследований для комплексной оценки различных факторов в качестве предикторов. В нашей модели использовались различные параметры, которые можно получить во время плановых медицинских осмотров независимо от состояния здоровья обследуемых лиц. Несмотря на то что измерение Лп(а) не относится к рутинным методам диагностики, мы считаем, что при однократном определении он может представлять ценность как один из элементов оценки общего сердечно-сосудистого риска и как ранний биомаркер для прогнозирования НАЖБП у лиц молодого возраста. Следовательно, разработанная нами модель уникальна, поскольку мы впервые представили модель прогнозирования НАЖБП в молодом возрасте с применением клинических, лабораторных и инструментальных параметров.
Несмотря на все сказанное, наше исследование имеет определенные ограничения. Во-первых, это небольшая выборка включенных пациентов, которая не позволяет широко транслировать полученные результаты на общую популяцию; с учетом этого обстоятельства для дальнейшего подтверждения эффективности модели и стабильности полученных с ее помощью данных необходимы лонгитюдные и перекрестные исследования. Во-вторых, наши результаты могут быть спроецированы только на европейскую популяцию. Следовательно, для возможности клинического использования разработанной модели требуется дальнейшая ее проверка на большем количестве разнообразных этнических групп населения. В-третьих, мы не учитывали генетические факторы, влияющие на уровень Лп(а), что также могло сказаться на полученных данных.
ЗАКЛЮЧЕНИЕ
Разработанная нами прогностическая модель для ранней неинвазивной диагностики НАЖБП у лиц молодого возраста может помочь клиницистам в выявлении пациентов с повышенным кардиометаболическим риском, подлежащих дальнейшей диагностической оценке. Таким пациентам могут рекомендованы определенные вмешательства, основанные на коррекции образа жизни.



