ИСТОРИЯ ИЗУЧЕНИЯ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ
Интерес к исследованию вегетативной нервной системы (ВНС) восходит ко временам Древней Греции. Греческие врачи разделяли организм на две подсистемы – «животную» и «органическую». Во II в. н. э. римский хирург, анатом и философ Гален проследил ход блуждающего нерва до грудной и брюшной полостей. Им было выдвинуто предположение о наличии «шестого черепного нерва», в который, по современным представлениям, входят 3 черепно-мозговых нерва – языкоглоточный, блуждающий и добавочный. Гален оставил свой след в изучении автономной нервной системы в самом первом описании верхнего и нижнего шейного ганглиев [1].
В Новое время также неоднократно предпринимались попытки подробного описания ВНС анатомами из разных стран: Везалиус, который, основываясь на своих трудах и работах Галена, представил визуальную анатомию ВНС; Евстахий и Этини исправили ошибку Галена, отделив симпатический ствол от блуждающего нерва; британский врач Уиллис (Велизий) представил изображение солнечного сплетения [2]. Ключевым моментом в истории изучения ВНС стало первое появление термина nervus sympaticus в работе 1732 г., который лег в основу понятия симпатической нервной системы [3]. Французский анатом Биша с помощью микроскопа описал, что симпатический ствол представляет собой не единый нерв, а соединенные между собой отдельные ганглии [1]. Его последователь Рейл впервые предложил наименование «вегетативная нервная система» [4]. Ремак, живший в первой половине XIX в., показал, что вегетативные нервы являются немиелинизированными, в отличие от двигательных и чувствительных [5]. Позже Бернаром было сделано открытие, позволившее судить о связи между ВНС и центральной нервной системой [1], а Броун-Секаром описано явление вазоконстрикции при возбуждении симпатических волокон [5]. В XX в. силами Гаскелла и Лангли были введены в научный оборот понятия «автономной нервной системы» и «парасимпатической нервной системы» [6].
ГИПОТАЛАМУС КАК ГЛАВНЫЙ ЦЕНТР ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ
Все упомянутые исследования были посвящены периферической части ВНС. Хотя некоторыми учеными и была отмечена связь между эмоциональным состоянием человека и работой внутренних органов, однако она рассматривалась, скорее, как восходящее влияние от внутренних органов на эмоциональное состояние, а не наоборот [6]. Так было до XX в., пока несколькими группами исследователей не было открыты функции гипоталамуса как главного центра вегетативной регуляции [4]. Гипоталамус – это отдел головного мозга, формирующий нижнюю часть третьего желудочка. Он лежит кзади от перекреста зрительных нервов и кпереди от ножек мозга. Гипоталамус служит не только главным центром регуляции функции автономной нервной системы, но и частью лимбической системы, отвечающей за реакции на эмоциональные стимулы. Ее функция неотъемлемо связана с формированием памяти, вниманием, сексуальным влечением, поведением [7].
Гипоталамус оказывает свое влияние как на парасимпатическую, так и симпатическую части ВНС. Получая афферентные сигналы от висцеральных органов, он регулирует работу внутренних органов двумя путями: непосредственным контактом с симпатической и парасимпатической нервными системами через гипоталамо-спинальный тракт (симпатическая часть) и дорсальный продольный пучок (парасимпатическая часть). Другим путем регуляции работы организма являются эндокринные функции гипоталамуса, включающие выработку таких биологически активных веществ, как тиреотропин-рилизинг гормон, соматотропин-рилизинг гормон, соматостатин, гонадотропин-рилизинг гормон, кортикотропин-рилизинг гормон, окситоцин и вазопрессин [8].
При обсуждении роли гипоталамуса в регуляции функции ВНС следует упомянуть его участие в формировании пищевого поведения, регуляции артериального давления (АД), функционировании внутренних органов, полового поведения. За формирование пищевого поведения отвечают хвостатое, паравентрикулярные ядра и латеральное гипоталамическое ядро. В хвостатом ядре сходятся афферентные волокна от желудочно-кишечного тракта (грелин, глюкагоноподобный пептид-1, холецистокинин), поджелудочной железы (инсулин) и жировой ткани (лептин). Стимуляция хвостатого ядра грелином через некоторые нейрональные взаимодействия приводит к ингибирующему воздействию на префронтальную кору, отвечающую за прекращение потребления пищи [9]. При потреблении пищи гипоталамус посредством воздействия на ядра блуждающего нерва через дорсальный продольный пучок стимулирует моторику желудочно-кишечного тракта (ЖКТ), а через стимуляцию верхнего и нижнего слюноотделительных ядер вызывает слюноотделение [10]. В данном процессе активны по большей части холинорецепторы. Стимуляция адренорецепторов, расположенных на тех же органах-мишенях, вызывает снижение интенсивности моторики ЖКТ и слюноотделения, обеспечивая реакцию со стороны симпатической нервной системы [11].
Роль гипоталамуса в поддержании АД осуществляется за счет выделения вазопрессина – гормона, участвующего в поддержании объема циркулирующей крови. Механизм его действия заключается во влиянии на каналы аквапорин-2 в почках, что приводит к увеличению резорбции в канальцах [12]. В данном случае афферентным волокнами поставляется информация в гипоталамус от барорецепторов и осморецепторов [13]. Другой путь влияния на уровень АД – симпатическая активация мозгового вещества надпочечников через гипоталамо-спинальный тракт. При этом в мозговом веществе надпочечников увеличивается секреция адреналина и норадреналина, которые посредством воздействия на адренорецепторы в стенках сосудов и сердце увеличивают артериальный тонус и частоту сердечных сокращений (ЧСС) [14]. Описанные функции гипоталамуса как центрального регулятора ВНС иллюстрируют его ключевую роль в процессах жизнедеятельности организма.
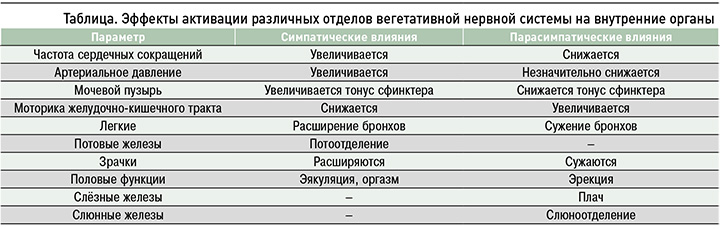
По современной классификации, ВНС делится на периферическую часть, разделенную на симпатическую и парасимпатическую, и центральную, включающую ядра гипоталамуса, нейроны боковых рогов и крестцовых отделов спинного мозга. ВНС отвечает за непроизвольные реакции организма, в связи с чем ее называют еще автономной (в дальнейшем мы будем использовать эти понятия как синонимы): уровень АД и ЧСС, терморегуляцию за счет потоотделения и механизмов мышечной дрожи, моторику ЖКТ; сокращение мышц мочевого пузыря, аккомодацию, сужение/расширение глазной щели. Эффекты симпатической и парасимпатической активации на внутренние органы представлены в таблице.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ НАРУШЕНИЯ ДЕЯТЕЛЬНОСТИ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ
Клиническое значение имеет степень нарушения деятельности ВНС. В соответствии с уровнем поражения различают вегетативные (автономные) невропатии, вегетативные (автономные) расстройства с вовлечением спинного мозга и вегетативные (автономные) расстройства с вовлечением головного мозга.
Проведение возбуждения в периферической автономной нервной системе происходит по тонким, или немиелинизированным волокнам. Данная особенность строения делает эти нервные волокна одной из самых чувствительных «целей» при воздействии метаболических и токсических факторов. Поражения периферической части ВНС разделяют на острые и хронические. Чаще всего врачу приходится сталкиваться именно с хронической автономной невропатией. Данное состояние можно наблюдать у больных с сахарным диабетом (СД) как 1-го, так и 2-го типа. Вегетативная невропатия обнаруживается у 90% людей с СД, а тяжесть ее проявления зависит от длительности заболевания [15]. Нарушения функции парасимпатического отдела ВНС при СД встречаются чаще (в 65% случаев), чем дисфункции симпатической нервной системы (24% случаев) [16]. Один из наиболее ранних симптомов автономной невропатии при этом заболевании – нарушение трофики кожи и выпадение волос, что является следствием как повреждения микроциркуляции, так и нарушения функции потовых желез [17]. Поскольку при СД чаще затрагиваются парасимпатические нервные волокна, клиническая симптоматика представлена склонностью к запорам, эректильной дисфункцией, тахикардией и артериальной гипотонией. Осложнением парасимпатической денервации сердечной мышцы выступает увеличение риска внезапной смерти у таких больных в 5- и 10-летнем периоде на 27 и 56% соответственно [18]. Вагусная денервация сердца приводит к выраженной компенсаторной тахикардии даже в состоянии покоя. С прогрессированием невропатии присоединяются и проявления недостаточности симпатической иннервации, что вызывает ортостатическую гипотензию ввиду недостаточной вазоконстрикции в сосудах нижних конечностей, снижение толерантности к физическим нагрузкам и даже безболевую форму ишемии миокарда [19].
Другой причиной развития функции периферического отдела ВНС выступает развитие автономной невропатии на фоне хронического злоупотребления алкоголем. Наиболее важным фактором, определяющим развитие этой формы дизавтономии, является общая доза этанола. Среди жалоб, наиболее часто предъявляемых при этой форме вегетативной недостаточности, лидирует эректильная дисфункция, в то время как жалобы на ортостатическую гипотензию отмечаются редко [20]. В то же время при объективизации функции ВНС у больных хроническим алкоголизмом выявлялось снижение вариабельности ритма сердца в ходе холтеровского мониторирования (у 26% людей) на фоне симпатической недостаточности [21].
К развитию клинически выраженной дизавтономии могут приводить не только экзогенные факторы. С увеличением возраста повышается риск возникновения этого состояния вследствие гиперактивности симпатической нервной системы [22]. Механизм развития возрастзависимых автономных невропатий остается неизвестным; существуют теории, связывающие повышение уровня лептина с активацией ренин-ангиотензин-альдостероновой системы, а также с интенсификацией процессов нейровоспаления в периферической нервной системе на фоне клеточного старения [23]. Предполагается роль центральной нейродегенерации в развитии дизавтономий пожилого возраста. Относительная симпатическая гиперактивация при возрастной дизавтономии становится результатом не только повышения активности самой этой системы, но и снижения активности парасимпатического отдела ВНС. Было установлено, что с возрастом у животных увеличивается степень вагусной денервации сердца, что, возможно, происходит и у человека [24].
ДИАГНОСТИКА И ЛЕЧЕНИЕ ПЕРИФЕРИЧЕСКОЙ ВЕГЕТАТИВНОЙ НЕДОСТАТОЧНОСТИ
Выявление периферической вегетативной недостаточности происходит на основании опроса пациента, данных физикального обследования и исследования вегетативных функций. К наиболее характерным жалобам при дизавтономиях относятся сухость глаз и во рту, повышенная чувствительность к свету, усталость, запоры или диарея, раннее чувство насыщения, эректильная дисфункция, снижение либидо, снижение переносимости температуры, нарушения урологических функций. Среди методов верификации вегетативной недостаточности следует выделить выявление реакции зрачков на свет, определение поверхностной температуры тела и ее реакции на жаропонижающие средства (аспириновая проба). Для объективизации деятельности ВНС используются такие инструментальные методы обследования, как анализ вариабельности ритма сердца, кардиоинтервалография при ортостатической пробе и пробе Вальсальвы, исследование кожных симпатических потенциалов, конфокальная микроскопия роговицы. В некоторых случаях для подтверждения поражения вегетативных нервов требуется проведение биопсии кожи [17].
Выделяют три подхода к лечению вегетативной дизавтономии:
- лечение и контроль основного заболевания;
- поведенческая терапия и диетотерапия;
- симптоматическое фармакологическое лечение.
Тактика поведенческой терапии и коррекции диеты зависит от того, какие именно симптомы вегетативной недостаточности необходимо скорректировать. Так, при ортостатической гипотензии эффективны методики постепенного вставания, когда, прежде чем принять вертикальное положение из горизонтального, человек 2–3 мин. находится в положении сидя. Эффективными оказались рекомендации ношения компрессионных чулок и повышения потребления воды и соли (до 5 г/ сут.). При стойких запорах могут быть результативными коррекция диеты путем обогащения рациона растительной пищей, увеличение физической активности, тренировка мышц тазового дна. Последняя методика может принести пользу и при неполном опорожнении мочевого пузыря.
Одновременно с этим применяются и лекарственные средства, направленные на симптоматическое лечение вегетативной дисфункции. При ортостатической гипотензии эффективным препаратом является флудрокортизон – синтетический аналог гормонов коры надпочечников, конечный эффект которого заключается в увеличении реабсорбции в почечных канальцах и повышении АД. Препарат применяется в дозировке от 0,1 мг/сут. до 0,1 мг 3 р./сут. [25]. Для лечения запоров возможно назначение слабительных разнообразного спектра действия.
ЦЕНТРАЛЬНЫЕ НАРУШЕНИЯ ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ
Вегетативная недостаточность симптоматического характера часто развивается при таких нейродегенеративных заболеваниях, как болезнь Паркинсона, мультисистемная атрофия (МСА), деменция с тельцами Леви (ДТЛ), прогрессирующий надъядерный паралич (ПНП), кортикобазальная дегенерация и др., которые объединяются термином «экстрапирамидные расстройства» [26]. Наиболее часто среди ее проявлений присутствуют ортостатическая гипотензия и неполное опорожнение мочевого пузыря. Существует и другая группа центральных дизавтономий, характеризующаяся первичным поражением гипоталамуса. Ее составляют такие разнородные заболевания, как синдром Вернике – Корсакова, диэнцефальный синдром, серотониновый синдром, фатальная семейная инсомния, несахарный диабет, идиопатическая гипер- и гипотермия, расстройства сексуального поведения, булимия и анорексия [27].
На протяжении длительного времени было распространено убеждение о существовании синдрома вегетативной дистонии (СВД) – идиопатической дисфункции центральных вегетативных центров. Родоначальником этого направления стал американский врач Б. Оппенгеймер, который ввел в 1918 г. термин «нейроциркуляторная дистония». В 1950-х гг. Н.Н. Савицкий предложил термин «вегетососудистая дистония», включающий загрудинные боли, головокружения, синкопальные состояния, стрессовые реакции и др. А.М. Вейн рассматривал СВД как синдром, представленный перманентными или пароксизмальными нарушениями вегетативных функций локального характера в сочетании с эмоциональными расстройствами [28]. Клинический симптомокомплекс СВД описывался такими неспецифическими и часто трудно верифицируемыми проявлениями, как головные боли, несистемные головокружения, общая слабость, ощущение сердцебиения или перебоев в работе сердца, учащенное мочеиспускание, повышенная тревожность, эмоциональная лабильность и нарушения сна. Концепция СВД строилась на разграничении перманентной и пароксизмальной форм, в рамках последней выделяли симпатоадреналовый и вагоинсулярный приступы. Симпатоадреналовый пароксизм проявляется тахикардией, страхом смерти, ощущением озноба, он объяснялся избыточным выбросом норадреналина и адреналина. Вагоинсулярный пароксизм сопровождался несистемным головокружением, ощущением недомогания и расстройством функции ЖКТ в виде тошноты и/или диареи.
Выделяли 7 причин возникновения СВД:
- генетические;
- гормональные перестройки (пубертат, климактерический период, беременность);
- патологию висцеральной и/или эндокринных систем;
- патологию сегментарной нервной системы из-за «сдавления» вегетативных ганглиев;
- органические поражения головного мозга;
- психофизиологические реакции;
- невротические и психические расстройства.
Сам А.М. Вейн признавал необходимость мультидисциплинарного подхода к лечению СВД с участием специалистов соответствующего профиля. Если в жалобах преобладал гипервентиляционный синдром, то пациента обучали дыхательным гимнастикам; при периодическом ощущении тахикардии назначались бета-адреноблокаторы, для купирования приступов тошноты – прокинетики, в случае несистемного головокружения – вестибулолитики.
До сих пор СВД остается одним из популярных диагнозов в практике отечественных терапевтов и неврологов. Такой диагноз ставился хотя бы один раз в жизни 64% людей [29]. Однако со временем выяснилось, что под маской СВД скрываются эмоциональные расстройства, неразрывно связанные с вегетативными нарушениями, поскольку гипоталамус является одной из ключевых структур лимбической системы. В 2010 г. было показано, что до 90% пациентов с СВД имеют клинические и субклинические признаки депрессии [30]. Под маской диагноза СДВ могут скрываться и такие состояния, как тревожные расстройства, панические атаки, хронические ежедневные головные боли или их сочетание [31]. В настоящее время СВД рассматривается как проявление одного из расстройств психической сферы. В том случае, когда очевидный психопатологический синдром не выявлен, рекомендуется использовать термин «соматоформная дисфункция вегетативной нервной системы».
В настоящее время становится понятно, что лечение СДВ должно заключаться не в компенсации вегетативных расстройств, а лечении первичного психического расстройства, вызвавшего соматоформную дисфункцию. В зависимости от основного диагноза применяются препараты из групп антидепрессантов, нейролептиков или антипсихотиков. Эффективным неспецифическим способом лечения данных расстройств является психотерапия, препятствующая развитию «катастрофизации» из-за переоценки пациентом значимости своих симптомов [32]. При сочетании лекарственной терапии и психотерапевтических методик стойкого терапевтического эффекта удается достичь у 72% пациентов. Лекарства, обладающие ноотропным или седативным и вегетостабилизирующим эффектами (в том числе соответствующие фитопрепараты), также могут рассматриваться в качестве дополнительных средств, повышающих эффективность лечения данного состояния.
Остается открытым вопрос о том, кто же должен лечить больного с проявлениями СВД? Учитывая тот факт, что вегетативные расстройства развиваются на фоне нарушений психической деятельности, наилучшим выбором было бы направление пациента к психиатру. Однако в большей части случаев пациенты отказываются от помощи психиатра и единственным вариантом помощи со стороны врача общей практики или даже невролога становится назначение в качестве симптоматического лечения препаратов с седативным, анксиолитическим и «вегетотропным» (т. е., по сути, с тем же седативным) действием.



