ВВЕДЕНИЕ
Снижение мышечной силы, уменьшение мышечной массы и ухудшение функционального состояния мышц составляют суть синдрома, получившего название саркопения (СП). Данный термин был предложен Rosenberg I.H. в 1989 г. для определения возрастной потери мышечной ткани [1]. Европейский консенсус по СП был впервые принят в 2010 г., когда это состояние было определено как «синдром, характеризующийся прогрессирующей и генерализованной потерей скелетной мышечной массы и силы, который приводит к повышению риска развития таких неблагоприятных событий, как снижение физических возможностей и качества жизни, а также к преждевременной смерти человека» [2]. В 2016 г. СП был присвоен код М62.84, относящийся к XIII классу «Болезни костно-мышечной системы и соединительной ткани» Международной классификации болезней 10-го пересмотра (МКБ-10) [3].
С учетом появившегося большого количества научных работ, посвященных этой проблеме, в 2018 г. Европейская рабочая группа по изучению СП у пожилых людей 2-го созыва (European Working Group on Sarcopenia in Older People 2, EWGSOP2) представила пересмотренный консенсус, согласно которому СП определяется как «прогрессирующее и генерализованное заболевание скелетных мышц, связанное с повышенной вероятностью неблагоприятных исходов, включая падения, переломы, ограничение физических возможностей и смертность» [4].
СП вследствие увеличения риска падений и переломов является одной из основных причин развития локомотивного синдрома – состояния, характеризующегося хроническим нарушением мобильности и потребностью в постороннем, в том числе профессиональном, уходе [5].
ЭПИДЕМИОЛОГИЯ
Распространенность СП, согласно разным источникам, широко варьирует, что связано с различными критериями включения, а также с особенностями исследуемых групп. При обследовании российской когорты лиц старше 65 лет частота СП составила 26,5%, причем при стратификации пациентов по возрасту было отмечено увеличение этого показателя в два раза в группе людей старше 85 лет [6]. В работах, изучавших СП у пациентов с различными заболеваниями, показано, что ее распространенность колеблется от 1,8 до 53%. Например, у пациентов с сердечно-сосудистыми заболеваниями она находится в пределах 19,9–53% [7, 8]. У больных, перенесших острое нарушение мозгового кровообращения, СП выявлялась в 29,9% случаев [9]. У пациентов с хронической обструктивной болезнью легких ее частота варьирует от 14,5 до 44,1% [10, 11], при сахарном диабете 2-го типа в среднем составляет 18% [12], у лиц, находящихся на гемодиализе или перенесших трансплантацию почки, достигает 26–30,3% [13–15]. В среднем 2 из 5 пациентов с хроническим панкреатитом или прогрессирующими болезнями печени имеют СП [16, 17].
В исследованиях по изучению СП у лиц с ревматическими заболеваниями, проведенных в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой», она регистрировалась у 34,8% женщин с системной склеродермией, у 29,8% – с ревматоидным артритом (РА) и у 1,8% – с остеоартритом (ОА), при этом средний возраст пациентов равнялся 60 годам [18]. В то же время при обследовании пациентов с ОА более старшего возраста (74 ± 6 лет) частота СП по критериям EWGSOP 2 составила 28,9% [19].
Различия в распространенности СП могут быть обусловлены не только возрастом и наличием коморбидности, но также этнической принадлежностью обследуемых лиц и гендерными факторами. Так, систематический обзор и метаанализ эпидемиологических популяционных исследований, опубликованный в 2017 г., продемонстрировал, что у мужчин частота СП колебалась от 1 до 26% среди азиатов и от 2 до 23% у лиц не азиатской расы, а среди женщин – от 1 до 34% и от 0 до 44% соответственно [20]. С учетом темпов старения населения в ближайшие 30 лет ожидается дальнейший рост заболеваемости СП.
ЭТИОЛОГИЯ
СП разделяют на первичную, связанную только с возрастными изменениями мышечной ткани, и вторичную, развивающуюся на фоне различных заболеваний. СП может быть вызвана гиподинамией, возникшей по любым причинам, а также приемом ряда лекарственных средств. У части пациентов, как правило, в более молодых возрастных группах, можно определить единственную причину развития СП. В то же время у многих пожилых людей имеет место многофакторная этиология ее возникновения, что не позволяет установить единственно правильный диагноз.
В настоящее время рассматривается наличие генетической предрасположенности к СП. Доказана связь некоторых генов, в том числе кодирующих ангиотензинпревращающий фермент, миостатин, инсулиноподобный фактор роста-1 (ИФР-1), интерлейкин 6 (ИЛ-6) и рецепторы витамина D, с силой мышц и/или мышечной массой. Взаимосвязь наследственных факторов и некоторых показателей силы и массы мышц может достигать 80% [21].
МЕХАНИЗМЫ РЕГУЛЯЦИИ МАССЫ СКЕЛЕТНЫХ МЫШЦ
Мышечная масса определяется балансом между путями, способствующими синтезу и распаду белка. Наиболее изученный анаболический путь включает активацию серин/треониновой киназы Akt, которая приводит к последующей амплификации мишени рапамицина (mTOR), что, в свою очередь, влечет увеличение синтеза мышечного белка [22]. Большинство мышечных анаболических факторов, в частности ИФР-1, а также аминокислоты с разветвленной цепью (например, лейцин), физические упражнения и тестостерон активируют этот путь [23]. Атрофия скелетных мышц сопровождается распадом мышечного белка при активации пути убиквитиновых протеасом и каспаз под контролем транскрипционных факторов forkhead O (Fox-O) и ядерного фактора (NF)-κB.
Другим важным катаболическим механизмом служит миостатиновый путь. Миостатин секретируется миоцитами, циркулирует в крови и действует локально как отрицательный регулятор мышечной массы, подавляя путь Akt/mTOR и уменьшая количество сателлитных клеток [23]. Между этими путями синтеза и деградации мышечной ткани существует перекрестная связь, при нарушении баланса между ними может возникать атрофия мышечных волокон, приводящая к СП. Кроме этого, развитие мышечной атрофии могут вызывать усиление мышечного апоптоза [24], аутофагии [25], снижение функции митохондрий [26] и сателлитных клеток, которые имеют большое значение для восстановления мышц [27].
ПАТОГЕНЕЗ
СП характеризуется атрофией мышечных волокон, особенно волокон типа II (быстрых), уменьшением количества двигательных единиц и накоплением жира в мышцах [28]. Гиподинамия и неподвижность также выступают важной движущей силой патофизиологических изменений, приводящих к потере мышечной массы. С возрастом снижается синтетическая способность мышц, называемая анаболической резистентностью [29]. Как упоминалось ранее, тестостерон, инсулин и ИФР-1 являются мощными активаторами пути Akt, способствующими увеличению синтеза мышечного белка и снижению его деградации за счет ингибирования FoxO. Тестостерон также стимулирует миобласты, ингибирует миостатин и увеличивает количество клеток-сателлитов, которые помогают в восстановлении миоцитов [30]. Старение организма сопряжено с более низкими уровнями тестостерона, ИФР-1 и развитием резистентности к инсулину, что влечет за собой уменьшение синтеза белка. Хотя с возрастом наблюдается увеличение циркулирующих маркеров воспаления, таких как ИЛ-6, остается спорным вопрос, связано ли такое повышение исключительно с возрастным фактором или же еще и с сопутствующими заболеваниями [31]. Отметим, что воспалительные пути, включающие NFκB, обычно не активируются при СП.
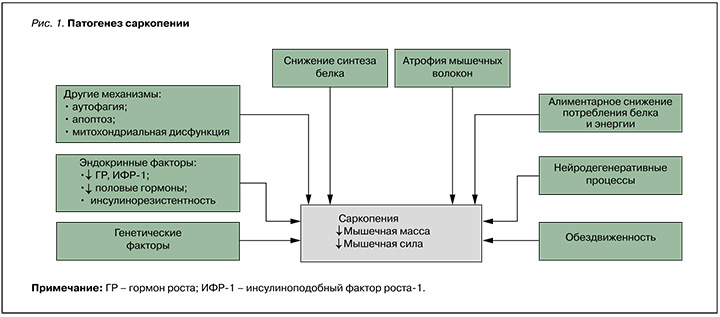
Генетический потенциал, дефицит питательных веществ и потеря нижних мотонейронов – все это играет роль в развитии рассматриваемого синдрома у пожилых людей [32, 33]. Наряду с этим на животных моделях можно наблюдать нарушение мышечной аутофагии и увеличение апоптоза при СП. Интересно, что эти изменения предотвращаются ограничением калорий [25]. Наконец, в мышцах с увеличением возраста развивается митохондриальная дисфункция, также относящаяся к патофизиологическим механизмам СП [26] (рис. 1).
ДИАГНОСТИКА
Заподозрить СП бывает достаточно сложно, особенно на ранних ее этапах, поскольку жалобы пациентов неспецифичны или могут отсутствовать вовсе. Вот почему практикующему врачу необходимо знание путей диагностического поиска, направленного на активное выявление пациентов с этим синдромом.
Потребность в простой и универсальной методике, позволяющей клиницистам заподозрить СП, привела к созданию алгоритма, предложенного экспертами EWGSOP2 (рис. 2). Этот алгоритм условно разделен на скрининг и собственно диагностику СП: Find – Assess – Confirm – Severity (FACS) – «Найти – Оценить – Подтвердить – Тяжесть СП».

Сначала рекомендуется скрининг лиц с подозрением на наличие СП при помощи простого опросника Sarcopenia Fast (SARC-F), в который входит всего 5 вопросов для определения затруднений при выполнении простых бытовых действий (табл. 1). Диагностически значимым является результат 4 балла и более [34].
По аналогии с инструментом FRAX для оценки риска остеопоротических переломов, который используется при скрининге кандидатов для проведения остеоденситометрии, итогом опроса по представленной анкете SARC-F является определение круга лиц, нуждающихся в дальнейшем обследовании для диагностики СП. Однако применение опросника SARC-F ограничено у пациентов с различными поражениями опорнодвигательного аппарата. В частности, в работе по оценке диагностических возможностей опросника SARC-F у женщин с РА его чувствительность и специфичность составили всего 30 и 42% соответственно [35].
На следующем этапе предлагается оценить мышечную силу посредством простых в использовании тестов, не требующих сложного оборудования. Рекомендуется определять силу кистевого сжатия с помощью динамометра и время, необходимое для выполнения теста «Встать со стула» (5-кратное вставание со стула без помощи рук; табл. 2). Но даже такие простые тесты оценки мышечной силы затруднены для выполнения у пациентов с двигательными нарушениями, например, после перенесенного инсульта или при заболеваниях опорно-двигательного аппарата. Так, у женщин с РА диагностическая точность кистевой динамометрии и теста «Встать со стула» была лишь 48 и 28% соответственно [35].
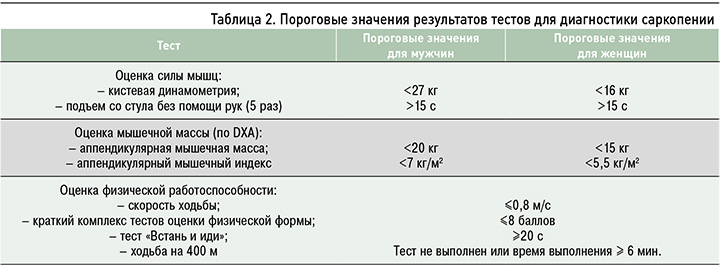
При выявлении сниженной мышечной силы диагностируется «вероятная СП», требующая дальнейшего обследования для определения содержания мышечной массы. С целью подтверждения наличия СП применяются инструментальные методы оценки мышечной массы – биоимпедансный анализ (БИА) или двуэнергетическая рентгеновская денситометрия (Dual X-ray Absorptiometry, DXA) всего тела.
Метод БИА представляет собой быстрый и доступный инструментальный способ оценки мышечной ткани. При его проведении нет необходимости в специальных условиях для оборудования, так как полностью отсутствует лучевая нагрузка. В то же время точность БИА и воспроизводимость результатов зависят от многих факторов, связанных как с состоянием самого пациента, так и с окружающей средой, техническими характеристиками и математическими алгоритмами, используемыми в аппаратах [36]. Эти недостатки отсутствуют при исследовании состава тела с помощью DXA, которая обеспечивает быструю неинвазивную количественную оценку содержания мышечной массы [37].
На основании определения мышечной массы с помощью DXA всего тела рассчитывается аппендикулярный мышечный индекс (АМИ) – отношение суммарной мышечной массы верхних и нижних конечностей (аппендикулярная мышечная масса, АММ) к квадрату роста пациента: АМИ (кг/ м2) = АММ (кг) / рост2 (м2). Если показатели АММ и/или АМИ ниже пороговых значений, диагностируется «подтвержденная СП» (см. табл. 2).
На заключительном этапе диагностического поиска выполняется оценка физической работоспособности скелетных мышц. Для этого могут применяться различные тесты; низкие результаты любого из них свидетельствуют о снижении функционального состояния мышц (см. табл. 2). В этом случае у пациента диагностируется «тяжелая СП» [4].
Наиболее полно функциональное состояние мышц отражает краткий комплекс тестов оценки физической формы (ККТ ОФФ; Short Physical Performance Battery, SPPB), включающий оценку баланса в вертикальном положении при постановке стоп вместе, полупоследовательно и последовательно, измерение времени для прохождения расстояния 4 м и для выполнения теста «Встань со стула». Вместе с тем для практикующих врачей эта методика имеет существенное ограничение: выполнение всего набора тестов требует значительно бóльших временных затрат, чем только оценка скорости ходьбы на 4 м или выполнение теста «Встань и иди» (оценка времени, необходимого для подъема со стула, прохождения дистанции 3 м и возвращения в исходное положение). Кроме того, проведение SPPB затруднено у больных с тяжелой сердечно-сосудистой патологией, у лиц с нарушениями равновесия и снижением когнитивных функций [4].
ОСТЕОСАРКОПЕНИЯ
СП может быть как самостоятельным заболеванием, так и сочетаться с остеопорозом (ОП). Одновременное наличие у пациента СП и сниженной минеральной плотности кости (МПК) получило название «остеосаркопения». Поскольку в старших возрастных группах существует повышенный риск развития СП и ОП, пожилым пациентам необходимо проводить оценку состояния как мышечной, так и костной ткани.
Развитию остеосаркопении, помимо возраста, способствуют генетические факторы, эндокринные нарушения (сахарный диабет, нарушения функции щитовидной железы), дефицит витамина D, хронические иммуновоспалительные заболевания. Также на развитие остеосаркопении влияют прием глюкокортикоидов, алиментарная недостаточность и ожирение. Мышечная и костная ткань обладают взаимными механическими и биохимическими воздействиями, функционируя на макроуровне как основные ткани, составляющие органы опорно-двигательного аппарата, и на микроуровне как органы эндокринной и паракринной регуляции за счет выработки различных перекрестно действующих цитокинов.
Риск переломов у пациентов с остеосаркопенией превышает таковой у лиц с нормальной МПК и без СП в 3,5 раза, в то время как только СП или только ОП увеличивает его в 2,3 и в 2,4 раза соответственно [38]. Показано, что смертность в течение года после перелома бедра среди лиц 60 лет и старше зависела от наличия как ОП, так и СП. Например, у пациентов с ОП она равнялась 5%, с СП – 10,3%, а при остеосаркопении достигала 15,1% [39]. При оценке 10-летней вероятности основных остеопоротических переломов у женщин в постменопаузе с РА высокий риск переломов выявлялся у 34,0% лиц без ОП и СП, у 42,9% пациенток с СП и у 92,3% – с остеосаркопенией (р < 0,001). Кроме того, частота падений в течение года, предшествовавшего опросу, составила 22,4% у лиц без СП и ОП, 40,0% у пациенток с СП и 61,5% – с остеосаркопенией (р < 0,05). В проспективном наблюдении частота падений в этих группах также различалась – 10,3, 50,0 и 53,8% соответственно (р < 0,001). Установлено, что СП и остеосаркопения увеличивали риск падений в 9,3 и 13,3 раза соответственно по сравнению с лицами без ОП и СП [40].
ПРОФИЛАКТИКА САРКОПЕНИИ
С целью профилактики СП и остеосаркопении используются методы как немедикаментозной, так и лекарственной терапии. В качестве основных профилактических мероприятий применяют лечебную физкультуру и нормализацию питания с достаточным поступлением белка и витамина D.
Физические упражнения доказали свое позитивное влияние на массу, силу и функцию мышц. В 2017 г. были опубликованы несколько метаанализов, в одном из которых продемонстрировано, что у пациентов с СП через 3 мес. от начала выполнения физических упражнений и приема продуктов с адекватным содержанием белка улучшились мышечная сила и физическая работоспособность [41]. В другом метаанализе авторы показали, что физические упражнения и прием пищевых добавок с белками и аминокислотами способствовали увеличению мышечной массы и силы скелетных мышц [42]. В более позднем метаанализе (2019) авторы пришли к выводу, что у пациентов с СП после 12-недельной тренировки отмечалось значимое увеличение мышечной массы и функции скелетных мышц по сравнению с лицами, не выполнявшими физических упражнений [43].
Увеличение потребления белка – еще одно вмешательство, которое имеет потенциальную терапевтическую пользу у пациентов с СП. Диетический белок оказывает прямое влияние на ключевые регуляторные протеины и факторы роста, участвующие в здоровье мышц и костей, увеличивая абсорбцию кальция, подавляя выработку паратиреоидного гормона и увеличивая секрецию ИФР-1 [44].
Включение в рацион белка (в основном животного происхождения), богатого незаменимыми аминокислотами, в пропорции свыше 0,8 г на килограмм массы тела в день усиливает анаболизм мышечного белка и защищает от возрастной потери мышечной массы [45]. У пациентов 70–79 лет потребление белка в дозе 1,1 г на килограмм массы тела в день приводило к меньшей потере мышечной массы при трехлетнем наблюдении [46]. Кроме того, было установлено, что потребление белка в сочетании с физическими упражнениями усиливает синтез мышечного белка и положительно влияет на состав тела, способствуя потере жира, увеличению или поддержанию мышечной массы и сохранению костной ткани [44, 45].
В настоящее время рекомендуется достаточное потребление белка с пищей (1,0–1,2 г на килограмм массы тела в сутки). Возможно увеличение его количества до 1,5 г на килограмм массы тела в день и больше при тяжелых заболеваниях и травмах [47]. Однако в целом для белковой пищи в рекомендуемых количествах результаты исследований неоднозначны, так как получены противоречивые данные по влиянию потребляемого белка на мышечную силу, массу и функцию, что связано с различным дизайном исследований, плохим мониторированием приема белка и затрудненной оценкой комплаентности пациентов [48].
При недостаточном поступлении белка с пищей можно рассмотреть возможность применения аминокислотных и белковых пищевых добавок, хотя доказательств, подтверждающих их значимое влияние на мышечную массу и функцию, пока недостаточно [49].
В этом плане определенные надежды возлагались на возможность дополнительного приема β-гидрокси-β-метилбутирата, но к настоящему моменту не получено однозначных данных о его позитивном влиянии на массу, силу и функцию мышц [50]. В отдельных работах продемонстрирован дополнительный прирост мышечной массы и силы в группе лиц, занимавшихся физическими упражнениями, и улучшение функционирования мышц на фоне приема добавок с креатином [51]. Обзор исследований по применению других пищевых добавок (зеленого чая, оксида магния, соевых изофлавоноидов, обогащенных витаминами и минералами молочных продуктов, фруктов, катехинов зеленого чая) не выявил дополнительного их влияния на массу и силу мышц ни в одной из представленных работ. В то же время наблюдалось улучшение выполнения функциональных тестов в группе, получавшей дополнительно оксид магния или чайный катехин [52].
Витамин D участвует в анаболических процессах мышечных белков и поэтому может играть важную роль в профилактике СП и ее исходов, таких как падения и переломы. Существуют два типа препаратов витамина D – нативные формы и его активные метаболиты. Для достижения адекватного уровня витамина D используются только нативные препараты [53]. Эффективность коррекции дефицита витамина D в увеличении мышечной функции показана в двух метаанализах. В первой работе лечение витамином D при исходном уровне 25(ОН)D менее 30 нмоль/л (12 нг/мл) способствовало увеличению мышечной силы у лиц старше 65 лет по сравнению с людьми моложе 65 лет, однако не было обнаружено влияния терапии этим витамином на мышечную массу в обеих группах (р = 0,52) [42]. В более позднем метаанализе оценивалось влияние терапии витамином D и физических упражнений в течение 3 мес. на мышечную силу и физическую работоспособность у людей старше 65 лет. В нем было выделено две группы пациентов: в одной все участники выполняли комплекс физических упражнений, в другой принимали витамин D. Согласно результатам этого метаанализа, у лиц, выполнявших комплекс упражнений, отмечалось значительное увеличение мышечной силы относительно тех, кто принимал только витамин D. В то же время в группе пациентов, получавших витамин D, результаты тестов физической работоспособности (SPPB и «Встань и иди») оказались существенно лучше по сравнению с группой, которая занималась физическими упражнениями [54].
Еще в двух исследованиях изучались эффекты комбинированного применения физических упражнений и витамина D на силу и функцию мышц [55, 56]. В работе Bunout D. еt al., применявших витамин D в дозе 400 МЕ/сут. в течение 9 мес., не было выявлено влияния упражнений и их комбинации с витамином D на мышечную массу, однако продемонстрировано значимое увеличение силы мышц как в группе, применявшей только упражнения, так и в группе с дополнительным приемом витамина D. Также было продемонстрировано значимое увеличение скорости выполнения теста «Встань и иди» в группе комбинированного лечения, но не получено различий по общему баллу SPPB [55]. В работе Binder E.F. сообщалось об улучшении балансировки тела на фоне физических упражнений без дополнительного положительного влияния приема витамина D у пожилых лиц с деменцией, проживающих в доме престарелых [56].
В ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» проведено пилотное исследование, в котором пациенты в одной группе получали витамин D в сочетании с кальцием и делали изометрические физические упражнения, а в другой группе только принимали витамин D и кальций. Через 3 мес. в группе женщин, выполнявших рекомендованный комплекс упражнений в сочетании с приемом препаратов кальция и витамина D, отмечалось улучшение функциональной работоспособности скелетных мышц, оцененной с помощью тестов SPPB (р = 0,043), а также уменьшение времени выполнения тестов «Встань и иди» (р = 0,025) и «Встать со стула» (р = 0,017).
В арсенале врачей сегодня есть не только нативные формы витамина D, но и его активные метаболиты, такие как альфакальцидол и кальцитриол, которые обладают доказанным положительным влиянием на мышечную ткань, обусловливающим снижение риска падений. У пожилых пациентов с дефицитом витамина D 6-месячное использование альфакальцидола привело к увеличению мышечной силы четырехглавой мышцы бедра и физической работоспособности [57]. При сравнении эффектов альфакальцидола и нативного витамина D у пациентов с РА, остеопенией и дефицитом 25(ОН)D наблюдалось существенное повышение мышечной силы на 60% при приеме альфакальцидола, тогда как на фоне применения 1000 МЕ нативного витамина D она стала больше только на 18% [58].
Альфакальцидол также показал свою эффективность в плане уменьшения риска падений. Так, рандомизированное клиническое исследование, выполненное в Швеции, продемонстрировало значимое уменьшение как числа падений на 54%, так и количества падавших лиц на 55% среди пожилых людей, получавших 1 мкг альфакальцидола и более 500 мг кальция ежедневно, по сравнению с группой плацебо [59]. Более выраженное влияние на риск падений и физическую работоспособность при приеме альфакальцидола отмечено у пожилых людей со сниженной функцией почек (клиренс креатинина менее 65 мл/ мин.) [60]. В то же время не было получено данных о влиянии на мышечную массу при приеме как нативного витамина D, так и его активных метаболитов.
В настоящее время не зарегистрировано ни одного лекарственного средства для лечения СП. Исследуемые препараты, на которые возлагались большие надежды, например антитела к миостатину, блокатор рецептора активина 2B, тестостерон, гормон роста и ИФР-1, либо имели побочные реакции, либо не продемонстрировали эффективности в улучшении функции скелетных мышц [61, 62].
Таким образом, на сегодняшний день можно говорить только о профилактике СП, включающей достаточное потребление белка с продуктами питания, поддержание нормального уровня витамина D, регулярные физические упражнения и контроль основного заболевания при вторичной СП. Перспективным направлением в дальнейшем изучении данного синдрома является создание новых лекарственных препаратов в соответствии с требованиями доказательной медицины на основе результатов последующих исследований этиопатогенеза СП.
ЗАКЛЮЧЕНИЕ
СП – распространенный синдром, который встречается как у пожилых людей, так и в более молодом возрасте на фоне различных хронических заболеваний. Она отягощает течение любой соматической патологии и ухудшает качество жизни пациента. Знание клинических и патоморфологических аспектов этой проблемы врачами практически всех специальностей имеет значение для более раннего выявления лиц, предрасположенных к СП, с целью ее первичной и вторичной профилактики.



