Синдром Бругада является редким, генетически обусловленным заболеванием, ассоциированным с высоким риском внезапной смерти. В настоящее время выявлено 16 генов, кодирующих натриевые, калиевые и кальциевые каналы, мутации в которых могут быть причиной данного заболевания [1].
Представленный нами случай демонстрирует принципиально новое направление для неинвазивного электрокардиографического картирования сердца, направленное на поиск аритмогенного субстрата у пациентов с синдромом Бругада.
Пациент П., 1964 г.р. с диагнозом: синдром Бругада 1-го типа.
Состояние после клинической смерти с успешной реанимацией на фоне фибрилляции желудочков (ФЖ; 2006).
Пароксизмальная желудочковая тахикардия (ЖТ). Имплантация кардиовертера-дефибриллятора GemIIIVR от 2006 г., реимплантация кардиовертера-дефибриллятора LumaxDR от 2012 г.
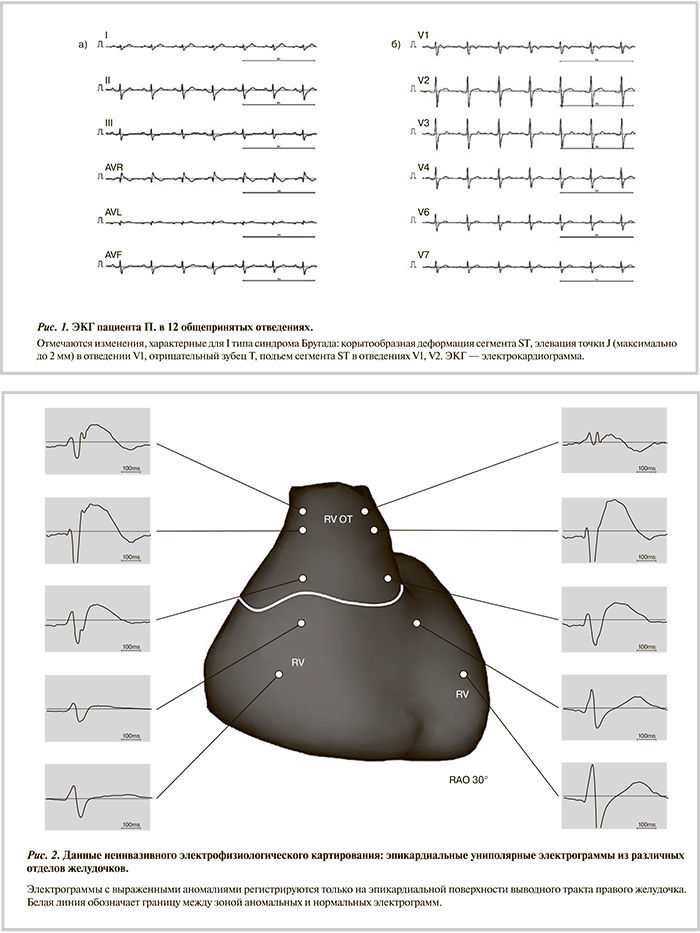
На стандартной электрокардиограмме (ЭКГ) регистрировался синусовый ритм. Вертикальное положение электрической оси сердца. Отмечались типичные для 1-го типа синдрома Бругада изменения в правых грудных отведениях: корытообразная деформация сегмента ST, подъем точки J (максимально до 2 мм) в отведении V1, отрицательный зубец Т, подъем сегмента ST в отведениях V1, V2 (рис. 1).
При генетическом исследовании выявлена мутация p.E553X в гене SCN5A, ответственном за α-субъединицу натриевого мембранного канала. Данная мутация ассоциирована с развитием синдрома Бругада. В 2014 г. в РНЦХ им. акад. Б.В. Петровского пациенту было выполнено неинвазивное трехмерное картирование сердца при помощи комплекса AMYCARD 01 К (EPsolutions, SA), которое позволяет реконструировать локальные униполярные электрограммы на эпикарде и эндокарде и визуализировать паттерны возбуждения миокарда [2].
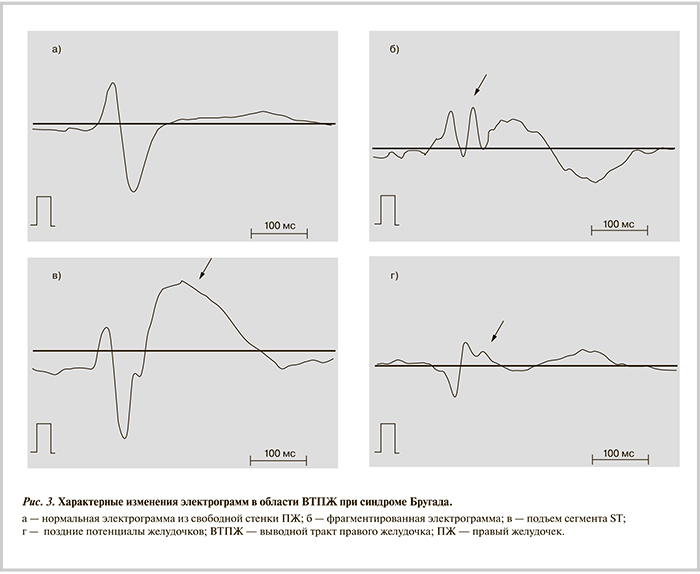
Электрограммы с выраженными аномалиями регистрируются только на эпикардиальной поверхности выводного тракта правого желудочка. Белая линия обозначает границу между зонами аномальных и нормальных электрограмм.
Последовательность активации желудочков, в том числе выводного тракта правого желудочка (ВТПЖ) у обследованного пациента не имела клинически значимых особенностей. Однако униполярные электрограммы в области ВТПЖ характеризовались следующими особенностями: 1) выраженная фрагментация комплекса QRS и снижение его амплитуды; 2) поздние потенциалы в конечной части желудочкового комплекса; 3) подъем сегмента ST (см. рис. 2; рис. 3).
Данные изменения отмечались только в области передней стенки эпикардиальной поверхности ВТПЖ и практически отсутствовали на эндокарде. При неинвазивном картировании сердца у пациентов без синдрома Бругада подобные находки не встречались.
Специфический подъем сегмента ST локальных униполярных электрограмм в области ВТПЖ соответствует аналогичным изменениям стандартных ЭКГ в правых грудных отведениях. Фрагментация и поздние желудочковые потенциалы наблюдаются только на локальных электрограммах, а на поверхностной ЭКГ, как правило, не выявляются.
Впервые фрагментация локальных электрограмм выявлена у пациентов с синдромом Бругада во время инвазивного электрофизиологического исследования с использованием системы CARTO в исследовании K. Nademanee и соавт. [3]. Наше наблюдение подтверждает эти данные.
В настоящее время существует две основные теории, объясняющие изменения ЭКГ при синдроме Бругада [4]: замедление распространения возбуждения в области свободной стенки ВТПЖ и преждевременная реполяризация миокарда в эпикардиальных слоях ВТПЖ, приводящая к градиенту электрического потенциала между эпикардом и эндокардом.
Можно предположить, что поздние желудочковые потенциалы и подъем сегмента ST обусловлены вторым механизмом. Фрагментация электрограмм, вероятно, связана с дисперсией скоростей и направлений деполяризации на клеточно-тканевом уровне, не проявляющихся в виде клинически значимых изменений последовательности активации желудочков на макроскопическом уровне. Кроме того, фрагментация электрограмм может свидетельствовать о наличии локальных фиброзных изменений в миокарде [3].
Основным механизмом развития ЖТ и ФЖ у пациентов с синдромом Бругада считается возникновение re-entry во второй фазе потенциала действия, которое обусловлено критическим снижением амплитуды потенциала действия в I фазу. Подъем сегмента ST, отражающий снижение амплитуды потенциала действия в I и II фазы в кардиомиоцитах эпикардиальных слоев миокарда, является предиктором возникновения угрожающих жизни аритмий [4].
Хорошо известно, что фрагментированные желудочковые электрограммы также ассоциированы с риском возникновения ЖТ и ФЖ [5]. Можно предположить, что фрагментация электрограмм указывает на возможность возникновения у пациентов с синдромом Бругада ЖТ и ФЖ по иному механизму. Однако роль фрагментированных электрограмм как предиктора опасных для жизни аритмий у пациентов с синдромом Бругада нуждается в тщательном изучении.
Представленный клинический случай демонстрирует, что неинвазивное электрофизиологическое картирование сердца открывает новые перспективы изучения патофизиологического субстрата аритмий при наследственных каналопатиях. Возможно, дальнейшее изучение вопроса поможет подойти к решению проблемы лечения этого заболевания, предложив новые стратегии, включая катетерную аблацию.



