Введение
Ожирение – это хроническое метаболическое заболевание, характеризующееся избыточным отложением жировой ткани в организме и индексом массы тела (ИМТ), больше или равным 30 кг/м2 [1]. Эта дефиниция актуальна для всех возрастных групп и полов населения европеоидной расы [1], если не указано иное для определенных групп населения [2, 3]. Ожирение приводит к осложнениям, служит фактором риска ряда заболеваний (сахарного диабета 2 типа [СД2], сердечно-сосудистых заболеваний, дислипидемии, апноэ во сне, депрессии и др.), снижающих качество жизни, приводящих к инвалидности, увеличивающих летальность, что имеет огромную медико-социальную значимость [4]. Отчет Всемирной организации здравоохранения (ВОЗ) о распространенности ожирения в Европе вызвал беспокойство, поскольку в нем говорится, что более 50% граждан либо страдают ожирением, либо имеют избыточный вес [5]. Это побудило международные научные ассоциации и общества, занимающиеся проблемами ожирения, разработать клинические рекомендации, в которых подчеркивалась бы необходимость раннего скрининга этого заболевания и раннего активного вмешательства, направленного на снижение веса [6, 7].
Кроме того, известно, что с возра-стом увеличивается распространенность такого фенотипа ожирения, как саркопеническое ожирение (СО), характеризующееся повышенным накоплением жировой ткани и снижением массы, силы, функции скелетной мускулатуры [8–10].
Проблема изучения СО актуальна для современной медицины [9, 11, 12]. Представляет научно-практический интерес ассоциация нарушений композиционного состава тела с полиморбидной патологией, кардиометаболическими заболеваниями, СД2 [13]. Так, M. Pellegrini et al. (2022) показали, что у пациентов с СО во время программ по снижению веса были более высокие кардиометаболические риски и шансы развития дислипидемии, гипертонии, СД2 и нарушения качества жизни, связанного со здоровьем (HRQoL), по сравнению с группой, страдающей только от ожирения. Кроме того, у этих больных были также худшие результаты снижения веса, более высокие показатели отказа от лечения и раннего его прекращения, больше трудностей с поддержанием сниженного веса в долгосрочной перспективе [14]. В связи с этим пациенты с СО требуют особого внимания, особенно в вопросах контроля веса [15].
В настоящее время описан новый фенотип, сочетающий ожирение, снижение мышечных массы, силы, функции и низкой костной массы, получивший название «остеосаркопеническое ожирение» (ОСО) [16, 17]. Однако вокруг ОСО ведется много споров вплоть до того, что одни исследователи утверждают о его существовании, тогда как другие утверждают обратное [18, 19]. Это связано, по-видимому, с недостаточным количеством исследований, отсутствием ясности в вопросе о взаимосвязи СО с костной плотностью. В связи с этим целью нашего исследования стало изучение взаимосвязи между СО и плотностью костной ткани у людей пожилого возраста.
Методы исследования
В одномоментное исследование вошли 568 человек пожилого возра-ста (средний возраст – 66,5±5,6 года), обратившихся в поликлинику к участковому терапевту в плановом порядке, страдавших ожирением, подписавших добровольное информированное согласие на участие. У всех участников исследования проводили сбор жалоб, анамнеза, определяли антропометрические показатели (рост, вес, индекс массы тела [ИМТ]). Состав тела измеряли с помощью биоимпедансного анализа на аппарате АВС-02 («Медасс», Россия). Исследовали следующие параметры: жировую массу (кг), долю жировой массы (%), индекс аппендикулярной скелетно-мышечной массы (ИАСММ), безжировую массу (кг), долю безжировой массы (%). Силу хвата кисти измеряли ручным кистевым динамометром (ДК-50, Россия) в положении сидя с согнутой в локте рукой под углом 90° и нейтральным положением предплечья. Скорость ходьбы по ровной горизонтальной поверхности пола, покрытой нескользким покрытием, на расстоянии 4 метров измерялась по стандартной методике [20]. СO определяли как наличие ожирения, низкий силы хвата кисти (ниже 27 кг для мужчин и ниже 16 кг для женщин), соотношение массы аппендикулярных скелетных мышц (АСММ) (кг) и ИМТ (кг/м2) (АСММ/ИМТ) меньше 0,789 кг/м2 для мужчин и меньше 0,512 кг/м2 для женщин, а также низкой физической работоспособности (низкой скорости ходьбы – меньше 0,8 м/с) [21]. Пациенты по наличию или отсутствию СО были разделены на две группы: с СО, без СО. Содержание минеральных веществ в кости (BMD) определяли с помощью двухэнергетической рентгеновской абсорбциометрии (DEXA) на аппарате Norland XR-46 [22]. Наконец, OСO было определено как сочетание СO и низкого BMD [18]. Критерии исключения: возраст младше 60 лет и старше 75 лет; прием лекарственных препаратов, влияющих на состав тела (анаболические гормоны, L-тироксин, инсулин); заболевания, связанные с потерей веса; тяжелые когнитивные нарушения, деменция, выраженные сенсорные дефициты, тяжелая саркопения, делающие невозможным участие; наличие острой сердечно-сосудистой патологии, онкологических заболеваний; анамнестических данных о наследственной патологии системы гемостаза; выраженная печеночная недостаточность (наличие цирроза печени, повышение активности печеночных трансаминаз более чем в 5 раз), терминальная почечная недостаточность (СКФ менее 30 мл/мин/1,73 м2 по CKD-EPI), хроническая сердечной недостаточность III стадии.
Статистический анализ проводили с помощью SPSS версии 21.0 (SPSS Inc., США). Нормальность распределения переменных оценивали с помощью теста нормальности Колмогорова–Смирнова. Описательная статистика для непрерывных переменных представлена как среднее значение±стандартное отклонение (M±SD). Групповые различия количественных переменных сравнивались с помощью дисперсионного анализа (ANOVA) с использованием апостериорного критерия Тьюки. Категориальные переменные выражались в процентах и сравнивались с использованием критерия хи-квадрат. Модели бинарной логистической регрессии использовали для расчета вероятности низкого BMD при наличии СО. Потенциальными искажающими факторами были вес и процент жировой массы. Значения p<0,05 считались статистически значимыми.
Результаты
В исследование вошли 568 участников (средний возраст – 66,5±5,6 года) со средним ИМТ 33,87±2,73 кг/м2, из них 57% женщин (n=325). Лица с СО (197 человек, 34,7%) были значительно старше (р<0,001), преимущественно женщины (51,6 против 48,4%) с более высокими ИМТ (р<0,001), жировой массой (р=0,015) и долей жировой массы (р<0,001) по сравнению с группой без СO (табл. 1).
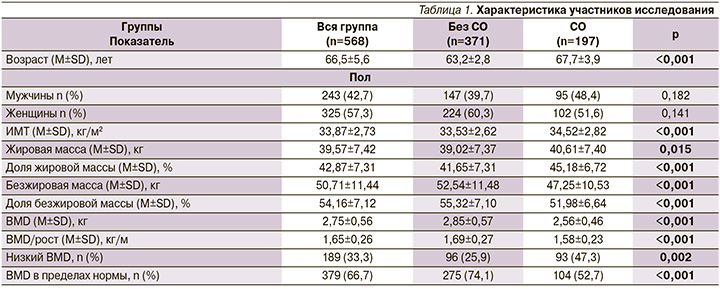
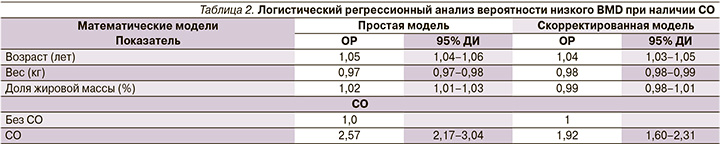
Более того, у группы с СО наблюдались более низкие средние значения BMD (р<0,001) и BMD/рост (р<0,001) по сравнению с лицами без него (табл. 1). В группу СО входило больше участников с низким BMD (47,3 против 25,9%), чем в группу без СО. Логистический регрессионный анализ выявил почти удвоенный риск низкого BMD (ОР=2,57; 95% ДИ: 2,17–3,04; p<0,05) в группе СO (табл. 2). Ассоциация сохранялась после поправок на возраст, вес и процент жировой массы, что отражало почти двукратный более высокий риск низкого BMD при наличии СO (ОР=1,92; 95% ДИ: 1,60–2,31; p<0,05). Было выявлено, что из общей выборки 93 (16,4%) пациента имели ОСО.
Обсуждение результатов
Наша работа показала, что встречаемость СО среди пожилых пациентов, обратившихся с ожирением в поликлинику к участковому терапевту в плановом порядке, составляет 34,7%, что соответствует данным, полученным в ряде исследований [8, 14, 23]. В то же время, по литературным данным, имеет место широкий диапазон распространенности СО, который варьируется от 0 до 100% в зависимости от используемого метода определения СО [10]. О более высокой распространенности обычно сообщается в исследованиях, в которых определялся состав тела, а более низкая распространенность отмечается при использовании ИМТ. Низкая распространенность также может быть объяснена использованием методов, которые в первую очередь были разработаны на основе исследований на пожилых когортах и не могут быть применимы к более молодым [10].
Мы обнаружили более низкий средний BMD в группе с СО по сравнению с группой без СО (р<0,001). При этом в группу СО входило больше пациентов с низким BMD (47,3%) по сравнению с участниками без СО (25,9%).
В связи с этим можно предположить, что наличие СO тесно связано с увеличением риска снижения костной массы. Механизм, лежащий в основе этих событий, до сих пор неясен; однако, видимо, существует двунаправленное взаимодействие между ожирением, хроническим воспалением, низкой костной массой и саркопенией [24–26].
Ожирение опасно своими осложнениями и сопутствующей коморбидной патологией. Действительно, в работе А.Ф. Вербового и соавт. (2022) отмечено, что рост распространенности ожирения имеет негативные последствия, т.к. избыточная масса тела относится к факторам риска сердечно-сосудистой патологии, СД и других заболеваний, что в конечном итоге увеличивает риск неблагоприятных исходов [27].
Мы предполагаем, что сочетание ожирения и саркопении (т.е. СО) может иметь синергический эффект и наблюдаемое при этом хроническое воспаление является общим триггером снижения МПК. Возможно, что воспаление может играть важную роль в ремоделировании костной ткани, усугубляя резорбцию и приводя к уменьшению костной массы [28].
Как известно, хроническое воспаление является одним из общих механизмов патогенеза ожирения и метаболического синдрома [29], а также увеличивает риск прогрессирования сердечно-сосудистых осложнений [30].
Встречаемость OСO, включающего ожирение, саркопению и низкую костную массу, в нашем исследовании составляет 16,4%. Этот результат частично согласуется с данными J.H. Chung et al. (2015) [31], обнаружившими сильную связь между СО и снижением костной массы, но более низкую распространенность ОСО – всего 5% по сравнению с нашей работой (16,4%). Причину разной частоты ОСО между нашими данными и исследованием J.H. Chung et al. (2015) можно объяснить несколькими факторами. Прежде всего наблюдались различия в изученных выборках по этнической принадлежности, возрастным группам [31]. Более того, мы использовали разные критерии для определения СО, а также разные показатели оценки костной массы. Это означает, что эти результаты следует интерпретировать с осторожностью, особенно те, которые связаны с встречаемостью ОСО, поскольку мы имеем дело с новым фенотипом, четкого определения которого на сегодняшний день нет [32].
Тем не менее наше исследование имеет определенные сильные стороны. Во-первых, это одна из немногих работ, посвященных изучению связи между СО и низкой костной массой у пожилых с ожирением, а также оценке встречаемости ОСО. Во-вторых, состав тела измерялся с помощью биоимпедансного анализа, а костная плотность с помощью «золотого стандарта» диагностики – DЕXA. Однако наше исследование также имеет определенные ограничения. Прежде всего при определении OСO мы полагались на сочетание СO и низкой костной массы, однако на сегодняшний день точного определения этой новой нозологии не существует. Это особенно важно отметить, т.к. использование термина OСO является дискуссионным, поскольку ряд исследователей все еще спорят о его существовании и о том, можно ли считать его новым отдельным фенотипом с конкретными клиническими характеристиками, а не простым сочетанием его составляющих (ожирение, саркопения и низкая костная масса) [19]. С другой стороны, многие исследователи рекомендуют рассматривать ОСО как отдельную клиническую единицу [3, 17, 18]. Кроме того, наше исследование, как и ряд других, не изучало связи между OСO и кардиометаболическими заболеваниями, маркерами воспаления, факторами образа жизни, что, по нашему мнению, остается вопросом, требующим дальнейшей разработки.
Выводы
1. Встречаемость остеосаркопенического ожирения в нашем исследовании составляет 16,4%.
2. Логистический регрессионный анализ выявил увеличенный в 2,5 раза риск низкого BMD (ОР=2,57; 95% ДИ: 2,17–3,04; p<0,05) в группе СO. Ассоциация сохранялась после поправок на возраст, вес и процент жировой массы, что отражало почти двукратный более высокий риск низкого BMD при наличии СO (ОР=1,92; 95% ДИ: 1,60–2,31; p<0,05).
3. Для формирования индивидуального комплекса лечебно-профилактических и реабилитационных мероприятий пациентам пожилого возраста с ожирением необходимо проведение исследования состава тела и костной плотности.



