В разработке V Московских соглашений принимали участие ведущие специалисты России и стран СНГ: Л.Б. Лазебник, Е.И. Ткаченко, Д.И. Абдулганиева, Р.А. Абдулхаков, С.Р. Абдулхаков, Е.Б. Авалуева, М.Д. Ардатская, В.А. Ахмедов, Д.С. Бордин, С.Г. Бурков, М.А. Бутов, В.Ю. Голофеевский, В.Б. Гриневич, Е.В. Голованова, Е.В. Денисова, Г.С. Джулай, В.П. Добрица, О.П. Дуданова, Е.Ю. Еремина, А.Б. Жебрун, Т.Н. Жигалова, Н.В. Захарова, И.В. Зверков, И.О. Иваников, В.А. Исаков, А.Н. Казюлин, А.В. Калинин, И.В.Козлова, Е.А. Корниенко, Н.В. Корочанская, И.А. Комиссаренко, С.А. Курилович, Ю.А. Кучерявый, Е.Д. Ли, И.А. Ли, С.В. Левченко, М.А. Ливзан, А.Ф. Логинов, И.Д. Лоранская, И.В. Маев, В.А. Максимов, Д.А. Миллер, О.Н. Минушкин, О.М. Михеева, А.А. Низов, Л.С. Орешко, М.Ф. Осипенко, А.И. Пальцев, В.Д. Пасечников, Е.М. Приходько, В.Г. Радченко, М.Н. Рустамов, О.А. Саблин, В.Э. Сагынбаева, Р.Г. Сайфутдинов, А.А. Самсонов, А.С. Сарсенбаева, П.В. Селиверстов, В.И. Симаненков, С.И. Ситкин, Б.Д. Старостин, А.Н. Суворов, Г.Н. Тарасова, Л.В. Тарасова, А.В. Ткачев, Н.М. Хомерики, С.Г. Хомерики, В.В. Цуканов, В.В. Чернин, А.Л. Чернышев, О.О. Шархун, М.А. Шевяков, П.Л. Щербаков, А.В. Яковенко, Э.П. Яковенко.
Список сокращений
- АСК – ацетилсалициловая кислота
- ГЭР – гастроэзофагеальный рефлюкс
- ГЭРБ – гастроэзофагеальная рефлюксная болезнь
- ЖКТ – желудочно-кишечный тракт
- ИПП – ингибитор протонной помпы
- ФД – функциональная (неязвенная) диспепсия
- ПЦР – полимеразная цепная реакция
- НПВП – нестероидные противовоспалительные препараты
- ФОС – фруктоолигосахариды
- ХГ – хронический гастрит
- ЭГДС – эзофагогастродуоденоскопия
- Hp – Helicobacter pylori
ГАСТРОЭЗОФАГЕАЛЬНАЯ РЕФЛЮКСНАЯ БОЛЕЗНЬ
(шифр по МКБ-10: гастроэзофагеальный рефлюкс (ГЭР) – К 21, ГЭР с эзофагитом – К 21.0, ГЭР без эзофагита – К 21.9)
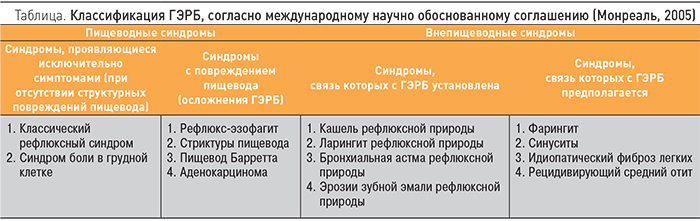
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) – хроническое рецидивирующее заболевание, характеризующееся забросом в пищевод желудочного и/или дуоденального содержимого, возникающим вследствие нарушений моторно-эвакуаторной функции эзофагогастродуоденальной зоны и проявляющимся симптомами, беспокоящими больного, и/или развитием осложнений. Наиболее характерными симптомами ГЭРБ являются изжога и регургитация, а наиболее распространенным клинико-эндоскопическим проявлением – рефлюкс-эзофагит. Классификация ГЭРБ представлена в таблице.
Методы диагностики гастроэзофагеальной рефлюксной болезни
- Клинически наиболее распространен классический рефлюксный синдром (эндоскопически негативная форма ГЭРБ), проявляющийся исключительно беспокоящими больного симптомами – изжогой и/или регургитацией. Диагноз выставляется клинически и базируется на верификации и оценке жалоб больного, при условии одинаковой трактовки симптомов врачом и больным. Национальное определение изжоги, принятое VII Съездом НОГР (2007): «Изжога – чувство жжения за грудиной и/или «под ложечкой», распространяющееся снизу вверх, индивидуально возникающее в положении сидя, стоя, лежа или при наклонах туловища вперед, иногда сопровождающееся ощущением кислоты и/или горечи в глотке и во рту, нередко связанное с чувством переполнения в эпигастрии, возникающее натощак или после употребления какого-либо вида твердых или жидких пищевых продуктов, алкогольных или неалкогольных напитков или акта табакокурения». Под регургитацией понимают попадание содержимого желудка вследствие рефлюкса в ротовую полость или нижнюю часть глотки (Монреаль, 2005). Нередко изжога и регургитация сочетаются со стенокардическими загрудинными болями (ночными, в положении лежа, после еды или при наклоне туловища вперед), что требует проведения дополнительных мероприятий для диагностики сопутствующей ишемической болезни сердца и правильного построения лечебного процесса. Исследование МЭГРЕ показало, что больные с верифицированной ГЭРБ чаще обращаются к кардиологу, нежели к гастроэнтерологу.
- Терапевтический тест с одним из ингибиторов протонной помпы (ИПП) в стандартной дозе в течение 7–10 дней (чувствительность – 80%, специфичность – 57%). Устранение симптома (-ов) подтверждает связь с рефлюксом и является критерием диагноза. Однако сохранение симптома не позволяет отказаться от диагноза ГЭРБ.
- Альгинатный тест – оценка эффекта однократного приема разовой дозы альгината при изжоге (чувствительность – до 97%, специфичность – до 88%). Купирование изжоги при однократном приеме альгината является дополнительным критерием диагноза ГЭРБ.
- Эндоскопическое исследование позволяет выявить и оценить изменения в дистальном отделе пищевода, прежде всего рефлюкс-эзофагит. При подозрении на метаплазию пищевода (пищевод Барретта) и злокачественное поражение проводится множественная биопсия и морфологическое исследование. Выявление характерных повреждений дистального отдела пищевода (эрозий, обнаруживаемых как при обычной эндоскопии, так и при использовании более современных методов, например, эндоскопии в режиме NBI) подтверждает диагноз ГЭРБ (эрозивная форма). Отсутствие изменений у больного с клиническими проявлениями заболевания, обусловленными рефлюксом, не свидетельствует против диагноза.
- Суточный рефлюкс-мониторинг пищевода (pH-мониторинг, комбинированный многоканальный импеданс-рН-мониторинг) для выявления и количественной оценки патологического гастроэзофагеального рефлюкса, определения его связи с симптомами болезни, а также для оценки эффективности терапии. Суточный рН-мониторинг позволяет выявить патологический кислый рефлюкс (pH<4,0). Импеданс-pH-мониторинг дает возможность также выявлять слабокислые, щелочные и газовые рефлюксы. Выявленный патологический ГЭР или доказательство связи ГЭР с типичными или атипичными симптомами подтверждают диагноз ГЭРБ. Отсутствие этих находок не позволяет отказаться от диагноза.
- Манометрия пищевода – для оценки моторики пищевода (перистальтика тела, давление покоя и расслабление нижнего и верхнего пищеводных сфинктеров), дифференциальной диагностики с первичными (ахалазия) и вторичными (склеродермия) поражениями пищевода. Манометрия помогает правильно установить зонд при рН-мониторинге пищевода (на 5 см выше проксимального края нижнего пищеводного сфинктера). Перед фундопликацией рекомендуется как обязательное предоперационное исследование.
- Рентгеноскопическое исследование верхних отделов желудочно-кишечного тракта (ЖКТ) в положении больного стоя и лежа для диагностики и дифференциальной диагностики пептических язв и/или пептических стриктур пищевода и/или грыж пищеводного отверстия диафрагмы.
- По показаниям проводится оценка нарушений эвакуаторной функции желудка (электрогастрография и другие методы).
- При выявлении внепищеводных синдромов и при определении показаний к хирургическому лечению ГЭРБ – консультации специалистов (кардиолог, пульмонолог, отоларинголог, стоматолог, психиатр и др.).
Медикаментозная терапия гастроэзофагеальной рефлюксной болезни
Лечение должно начинаться с соблюдения рекомендаций по изменению стиля жизни и диеты с исключением продуктов или блюд, провоцирующих симптомы заболевания. Пациенту следует отказаться от табакокурения и употребления алкогольных напитков, доказанно вызывающих изжогу. При избыточной массе тела рекомендуется плавное ее снижение; при ночных симптомах заболевания – сон в положении на левом боку или с приподнятым на 15–20 см головным концом кровати.
Для контроля симптомов и лечения осложнений ГЭРБ (рефлюкс-эзофагит, пищевод Барретта) наиболее эффективны ИПП (омепразол 20 мг, лансопразол 30 мг, пантопразол 40 мг, рабепразол 20 мг или эзомепразол 20 мг), назначаемые 1–2 раза/сут за 30–60 мин до приема пищи. Длительность основного курса терапии составляет не менее 6–8 нед. У пожилых больных с эрозивным рефлюкс-эзофагитом, а также при наличии внепищеводных синдромов его продолжительность увеличивается до 12 нед. Эффективность всех ИПП при длительном лечении ГЭРБ сходна. Особенности метаболизма в системе цитохромов P450 обеспечивают наименьший профиль лекарственных взаимодействий рабепразола, эзомепразола и пантопразола, что делает лечение наиболее безопасным при необходимости приема препаратов для терапии синхронно протекающих заболеваний (дигоксин, нифедипин, фенитоин, теофиллин и др.). При необходимости синхронного применения антиагрегантов и нестероидных противовоспалительных препаратов (НПВП) пантопразол может быть средством выбора.
Для большинства ИПП характерен определенный латентный период, что не всегда удобно для быстрого купирования симптомов. Для быстрого облегчения изжоги следует использовать антациды и препараты альгиновой кислоты (альгинаты). В начале курса терапии ГЭРБ рекомендуется комбинация ИПП с альгинатами или антацидами до достижения стойкого контроля симптомов (изжоги и регургитации).
При выявлении нарушений эвакуаторной функции желудка и выраженном дуоденогастроэзофагеальном рефлюксе показано назначение прокинетиков (итоприда гидрохлорид, метоклопрамид, домперидон). Длительный прием метоклопрамида (более 2 нед) – нежелателен, особенно у пожилых пациентов, поскольку вызывает экстрапирамидные нарушения (мышечный гипертонус, спазм лицевой мускулатуры, гиперкинезы). Домперидон следует с осторожностью назначать пациентам с сердечно-сосудистой патологией при обязательном контроле ЭКГ (возможность развития внутрисердечного нарушения проводимости) и в минимальной (10 мг) дозе.
По показаниям (непереносимость, недостаточная эффективность, рефрактерность к ИПП, наличие ночных кислотных «прорывов») возможно применение антагонистов Н2-рецепторов гистамина (фамотидин), как правило, курсами 10 дней.
При неэффективности стандартной дозы ИПП возможно назначение удвоенной дозы или комбинации ИПП с альгинатами, антацидами и/или прокинетиками. Антациды или альгинаты могут быть добавлены к базисной терапии ИПП в качестве адъювантной терапии на всех этапах лечения ГЭРБ.
Критерии эффективности терапии: достижение клинико-эндоскопической ремиссии (отсутствие симптомов или значительное уменьшение их выраженности при условии существенного улучшения самочувствия и качества жизни больного при эндоскопически негативной форме заболевания; отсутствие признаков рефлюкс-эзофагита при эзофагогастродуоденоскопии (ЭГДС)).
Необходимо отметить, что течение ГЭРБ, как правило, непрерывно-рецидивирующее, и у большинства больных при отмене антисекреторной терапии симптомы рефлюкс-эзофагита достаточно быстро рецидивируют.
Варианты ведения пациентов с гастроэзофагеальной рефлюксной болезнью после стойкого устранения симптомов и рефлюкс-эзофагита
- При рецидивирующем эрозивно-язвенном рефлюкс-эзофагите, пищеводе Барретта – непрерывная поддерживающая терапия ИПП (омепразол 20 мг, лансопразол 30 мг, пантопразол 40 мг, рабепразол 20 мг или эзомепразол 20 мг) 1–2 раза/сут.
- При часто рецидивирующей эндоскопически негативной ГЭРБ, ГЭРБ с рефлюкс-эзофагитом, ГЭРБ у пожилых больных – непрерывная поддерживающая терапия ИПП в минимальной, но эффективной дозе (подбирается индивидуально).
- При классическом рефлюксном синдроме для быстрого устранения симптомов терапия альгинатами, комплексными средствами с антацидными свойствами или ИПП «по требованию» под контролем симптомов с обязательным продолжением плановой терапии.
Лечение гастроэзофагеальной рефлюксной болезни у беременных
Лечение должно начинаться с соблюдения рекомендаций по изменению стиля жизни и диеты. Показано дробное питание (5–7 раз/сут), малыми порциями, без переедания. Необходимо избегать запоров.
Перед назначением любого лекарственного препарата обязательное изучение инструкции по применению с целью исключения возможности повреждающего воздействия на организм матери, плода или новорожденного.
Для купирования изжоги во всех триместрах назначают невсасывающиеся антациды (в том числе алюминия фосфат) и альгинаты. Применение алюминийсодержащих невсасывающихся антацидов в большинстве случаев ограничено возможностью развития запора. Алюминия фосфат практически не имеет таких ограничений (запоры развиваются редко, в основном у лежачих пациентов) и может назначаться по показаниям в терапевтических дозах. Препарат не следует принимать длительно без назначения врача.
Альгинаты безопасны, ограничений не имеют. При недостаточной эффективности антацидов и альгинатов возможно назначение Н2-блокаторов (категории безопасности FDA – B), наибольшая доказательная база безопасности – у ранитидина. При тяжелых поражениях пищевода во II и III триместрах беременности возможно назначение ИПП, поскольку развитие нежелательных эффектов в отношении матери и плода при их использовании в терапевтических дозах не получило подтверждения.
Гастроэзофагеальная рефлюксная болезнь и Helicobacter pylori
В ряде исследований показано, что распространенность Helicobacter pylori (Hp) у больных ГЭРБ ниже, чем в популяции, однако характер этой отрицательной взаимосвязи не имеет убедительного объяснения. Наличие Hp не влияет на тяжесть симптомов, частоту рецидивов и эффективность лечения ГЭРБ. Эрадикация Hp не усугубляет существующую ГЭРБ и не влияет на эффективность лечения.
На фоне значительного и длительного подавления кислотопродукции происходит распространение Hp из антрального отдела на тело желудка (транслокация Hp). При этом могут ускоряться процессы потери функций специализированных желез желудка, ведущие к развитию атрофического гастрита и, возможно, рака желудка. Поэтому больным ГЭРБ, нуждающимся в длительной антисекреторной терапии, необходимо провести диагностику Hp, при выявлении – провести эрадикацию.
Для диагностики Hp у больных, получающих лечение ИПП, необходима их отмена за 2 нед до проведения исследования (культурального, гистологического, быстрого уреазного теста, уреазного дыхательного теста или выявления антигена в кале). Если отмена ИПП невозможна, допустимо проведение валидированного серологического теста с IgG, но только у тех больных, у которых эрадикация Hp ранее не проводилась.
Эрадикация Hp у больных, длительно получающих ИПП, способствует уменьшению выраженности гастрита и предотвращает его прогрессирование в атрофический гастрит, уменьшая вероятность развития метапластических процессов и предупреждая развитие рака желудка (см. раздел «Медикаментозная терапия язвенной болезни желудка и 12-перстной кишки, ассоциированной с Hp»).
Для достижения большего эрадикационного эффекта целесообразно:
- выявить генотип больного по отношению к метаболизму ИПП – быстрый, усредненный или медленный (более эффективны ИПП у медленных метаболизаторов (метаболайзеров));
- увеличить рекомендуемую дозу ИПП в 2 раза;
- убедиться в биоэквивалентности или качестве лекарственного препарата (ИПП или иного, включенного в схему эрадикационной терапии) данного производителя, сверившись с официальной документацией.
Хирургическое лечение гастроэзофагеальной рефлюксной болезни
Рекомендуется дифференцированный отбор больных ГЭРБ для проведения хирургического лечения – лапароскопической фундопликации. Точные показания для хирургического лечения ГЭРБ остаются спорными, а отдаленные результаты не гарантируют полного отказа от ИПП. Проведение лапароскопической фундопликации часто сопровождается развитием дисфагии, летальность, как правило, не превышает 1%.
Предоперационное обследование должно включать ЭГДС (при подозрении на пищевод Барретта – с множественной биопсией и морфологическим исследованием), оценку степени анемизации, рентгенологическое исследование пищевода, желудка и 12-перстной кишки, манометрию пищевода и 24-часовой pH-мониторинг (импеданс-pH-мониторинг). Оптимально принятие решения об операции консилиумом, включающим гастроэнтеролога, хирурга, при необходимости, кардиолога, пульмонолога, оториноларинголога, психиатра и др. специалистов.
Показания к хирургическому вмешательству:
- сохраняющиеся или постоянно возникающие симптомы, несмотря на оптимальную терапию;
- отрицательное воздействие на качество жизни из-за зависимости от приема медикаментов или в связи с их побочными эффектами;
- наличие тяжелых осложнений ГЭРБ (пищевод Барретта, рефлюкс-эзофагит III или IV степени (LA C-D), язва пищевода, стриктура);
- ограничения качества жизни или наличие осложнений, обусловленных грыжей пищеводного отверстия диафрагмы.
ЯЗВЕННАЯ БОЛЕЗНЬ, АССОЦИИРОВАННАЯ С HELICOBACTER PYLORI
(шифр по МКБ-10: язва желудка – К 25, язва 12-перстной кишки – К 27)
Язвенная болезнь – хроническое рецидивирующее заболевание, основным морфологическим проявлением которого является язва желудка или двенадцатиперстной кишки, как правило, развивающаяся на фоне хронического гастрита, ассоциированного с Hp.
Методы диагностики язвенной болезни
- Клинический.
- Эндоскопический, при язве желудка в обязательном порядке для исключения малигнизации – прицельная биопсия (5–7 фрагментов) дна и краев язвы.
- Рентгенологический – для выявления осложнений (пенетрация, перфорация, стеноз, малигнизация).
- По показаниям – определение кислотообразующей и кислотонейтрализующей функций желудка (внутрижелудочная pH-метрия).
Методы диагностики инфекции Helicobacter pylori
1. Биохимические методы:
1.1. быстрый уреазный тест (определение активности уреазы в биоптате слизистой оболочки желудка);
1.2. уреазный дыхательный тест с 13С-мочевиной;
1.3. аммиачный дыхательный тест (Хелик-тест).
2. Морфологические методы:
2.1. гистологический метод – выявление Hp в биоптатах слизистой оболочки антрального отдела и тела желудка;
2.2. цитологический метод – выявление Hp в слое пристеночной слизи желудка.
3. Бактериологический метод с выделением чистой культуры и определением чувствительности к антибиотикам.
4. Иммунологические методы:
4.1. выявление антигена Hp в кале (слюне, зубном налете, моче) с применением моноклональных антител;
4.2. валидированный серологический тест с IgG.
5. Молекулярно-генетические методы – полимеразная цепная реакция (ПЦР) (для изучения биоптатов слизистой оболочки желудка). ПЦР проводится не столько для выявления Hp, сколько для верификации штаммов Hp (генотипирование), в том числе молекулярно-генетических особенностей, определяющих степень их вирулентности и чувствительности к кларитромицину или другим антибиотикам.
Методы диагностики Hp должны использоваться в зависимости от целей:
- первичная диагностика: гистологический или цитологический методы, быстрый уреазный тест;
- контроль эффективности терапии: дыхательные тесты (13C или Хелик-тест) или определение антигена Hp в кале;
- первичный скрининг: серологический (антитела к Hp, иммуноблот) или дыхательные тесты (13C или Хелик-тест);
- оценка антибиотикорезистентности Hp: ПЦР (мутации 23S рРНК при резистентности к макролидам), бактериологический метод с определением чувствительности Hp к антибиотикам с помощью Е-теста.
Для первичной диагностики Hp может использоваться любой метод при условии отсутствия лечения ИПП, Н2-блокаторами, антибиотиками или препаратами висмута в течение месяца перед проведением теста. Если у больного не предполагается проведение ЭГДС, предпочтение отдается неинвазивным тестам (13С-дыхательный тест, определение антигена Hp в кале). Диагностика Hp на фоне приема указанных препаратов возможна путем выявления антител к Hp в крови (IgG), при условии, что ранее эрадикация Hp у больного не проводилась. Для первичной диагностики Hp необходимо использовать минимум два метода, например, цитологический + быстрый уреазный тест (или Хелик-тест).
Контроль эффективности эрадикации проводится не ранее чем через месяц после завершения приема лекарств (ИПП, Н2-блокаторы, антибиотики, препараты висмута). Для этого может быть использован любой метод за исключением определения антител к Hp в крови, предпочтительны дыхательные тесты. Оценка антибиотикорезистентности проводится в случае неэффективности двух курсов эрадикационной терапии.
Медикаментозная терапия язвенной болезни желудка и 12-перстной кишки, ассоциированной с Helicobacter pylori
Выбор варианта лечения зависит от наличия индивидуальной непереносимости больными тех или иных препаратов, а также чувствительности штаммов Hp к препаратам. Применение стандартной тройной терапии на основе кларитромицина и ИПП возможно в регионах, где резистентность к нему менее 15–20%. Схемы тройной терапии с метронидазолом не рекомендуются из-за высокой распространенности резистентных штаммов Hp в популяции. В этой ситуации применение других рекомендованных антибиотиков делает их средством выбора.
Проведенные в последние годы исследования свидетельствуют о том, что распространенность резистентных к кларитромицину штаммов Hp в разных регионах России отличается и составляет по различным источникам от 7,6 до 40%.
При неосложненной язвенной болезни 12-перстной кишки прием ИПП после завершения эрадикационной терапии может быть прекращен. При язвенной болезни желудка и осложненной язвенной болезни 12-перстной кишки рекомендуется продолжение приема ИПП до заживления язвенного дефекта.
Эрадикационную терапию больному с состоявшимся язвенным кровотечением следует начинать сразу после возобновления питания через рот.
Антациды могут применяться как в комплексной терапии в качестве симптоматического средства, так и в виде монотерапии – до проведения диагностики Hp и pH-метрии.
Лечение должно начинаться с соблюдения рекомендаций по изменению стиля жизни и соблюдения диеты с исключением продуктов, вызывающих или усиливающих неприятные ощущения.
После хирургического вмешательства по поводу острой или хронической патологии желудка или 12-перстной кишки возможно считать целесообразным исследование на наличие геликобактериоза и при его выявлении – проведение антихеликобактерной терапии.
Первая линия антихеликобактерной терапии
Первый вариант. Один из ИПП в стандартной дозировке (омепразол 20 мг, лансопразол 30 мг, пантопразол 40 мг, эзомепразол 20 мг, рабепразол 20 мг 2 раза/сут) и амоксициллин (1000 мг 2 раза/сут) в сочетании с кларитромицином (500 мг 2 раза/сут), или джозамицином (1000 мг 2 раза/сут), или нифурателем (400 мг 2 раза/сут) в течение 10–14 дней. Использование высоких доз ИПП (двойная доза 2 раза/сут) повышает эффективность трехкомпонентной терапии.
Наиболее высокая эффективность и безопасность антихеликобактерной терапии проявляется на фоне пребиотической или пробиотической терапии.
Добавление пребиотиков, содержащих комбинацию ди-, олиго- и полисахаридов (фруктоолигосахариды (ФОС), гуммиарабик, лактитол), к стандартной антихеликобактерной терапии в стандартных дозах в течение 1 мес улучшает переносимость терапии, повышает эффективность эрадикации Hp и комплайенс.
Добавление пробиотиков Saccharomyces boulardii к стандартной антихеликобактерной терапии в стандартной дозе в течение 10–14 дней и более улучшает переносимость антибиотиков, повышает эффективность эрадикации Hp и комплайенс пациентов.
Добавление пробиотиков, содержащих некоторые штаммы Lactobacillus acidophilus и/или Bifidobacterium spp., например, Lactobacillus acidophilus LA-5 и Bifidobacterium animalis subsp. lactis BB-12, к стандартной антихеликобактерной терапии в стандартных дозах в течение 1 мес улучшает переносимость антибиотиков, повышает эффективность эрадикации Hp и комплайенс.
Второй вариант (четырехкомпонентная терапия). Препараты, используемые при первом варианте (один из ИПП в стандартной дозировке, амоксициллин в сочетании с кларитромицином, или джозамицином, или нифурателем) с добавлением четвертого компонента – висмута трикалия дицитрата 120 мг 4 раза/ сут или 240 мг 2 раза/сут продолжительностью 10–14 дней.
Третий вариант (модифицированная гибридная терапия). Рабепразол 10 мг 4 раза/сут в течение 14 дней, амоксициллин 500–750 мг 4 раза/ сут в течение 14 дней, пребиотический комплекс, содержащий ФОС, гуммиарабик, лактитол, 5 г 2 раза/сут в течение 28 дней. С 8-го дня лечения дополнительно – кларитромицин 500 мг 2 раза/ сут и тинидазол 500 мг 2 раза/сут в течение 7 дней.
Примечание. Четырехкратный прием рабепразола повышает эффективность антихеликобактерной терапии, позволяя проводить лечение безотносительно к генетическому полиморфизму CYP2C19, IL-1β, гликопротеина Р и антимикробной чувствительности. Четырехкратный прием амоксициллина повышает эффективность эрадикационной терапии за счет поддержания необходимой бактерицидной концентрации.
Четвертый вариант (при аллергии к препаратам пенициллинового ряда) – классическая квадротерапия. Один из ИПП в стандартной дозировке, висмута трикалия дицитрат по 120 мг 4 раза/сут, метронидазол по 500 мг 3 раза/сут (или нифураксозид 200 мг 4 раза/сут), тетрациклин 500 мг 4 раза/сут в течение 10–14 дней.
Пятый вариант (рекомендуется только в ситуациях, при которых полноценная терапия невозможна – поливалентная аллергия к антибиотикам, сопутствующая патология гепатобилиарной системы и категорический отказ пациента от приема антибиотиков):
А. Висмута трикалия дицитрат по 120 мг 4 раза/ сут (или 240 мг 2 раза/сут) за 30–40 мин до приема пищи и на ночь в течение 28 дней. При наличии болевого синдрома – короткий курс ИПП.
Б. Один из ИПП в стандартной дозировке в сочетании с 30% водным раствором прополиса (100 мл 2 раза/сут натощак) в течение 14 дней.
В. Один из ИПП в стандартной дозировке в сочетании со щелочной углекислой хлоридной-гидрокарбонатной натриевой или хлоридной-натриевой питьевой минеральной водой (по 150–200 мл 3 раза/сут за 90 мин до приема пищи в дегазированном и подогретом до 38°C виде) и пробиотиками, содержащими некоторые штаммы Lactobacillus acidophilus и Bifidobacterium spp., в стандартных дозах в течение 1 мес. Примечание: прием щелочной углекислой хлоридной-гидрокарбонатной натриевой или хлоридной натриевой питьевой минеральной воды в течение 1 мес возможен и в качестве адъювантной терапии к стандартной эрадикационной схеме.
Г. Один из ИПП в стандартной дозировке в сочетании с пробиотиками, содержащими некоторыми штаммы Lactobacillus acidophilus и Bifidobacterium spp. в стандартных дозах в течение 1 мес.
Шестой вариант (при наличии атрофии слизистой оболочки желудка с ахлоргидрией, подтвержденной при внутрижелудочной рН-метрии). Амоксициллин (1000 мг 2 раза/сут) в сочетании с кларитромицином (500 мг 2 раза/сут), или нифурателем (400 мг 2 раза/сут), или нифураксозидом 200 мг 4 раза/сут, или джозамицином (1000 мг 2 раза/сут) и висмута трикалия дицитрат (120 мг 4 раза/сут или 240 мг 2 раза/сут) продолжительностью 10–14 дней.
Вторая линия антихеликобактерной терапии
Проводится при отсутствии эрадикации Hp после лечения больных одним из вариантов терапии первой линии.
Первый вариант (классическая квадротерапия). Один из ИПП в стандартной дозировке, висмута трикалия дицитрат по 120 мг 4 раза/сут, метронидазол по 500 мг 3 раза/сут, тетрациклин 500 мг 4 раза/сут в течение 10–14 дней.
Второй вариант. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза/сут или 1000 мг 2 раза/сут) в сочетании с нитрофурановым препаратом: нифурателем (400 мг 2 раза/ сут), нифуроксазидом (100 мг или 200 мг 4 раза/сут) или фуразолидоном (100 мг 4 раза/ сут) и висмута трикалия дицитрат (120 мг 4 раза/ сут или 240 мг 2 раза/сут) продолжительностью 10–14 дней.
Третий вариант. Один из ИПП в стандартной дозировке, амоксициллин (500 мг 4 раза/сут или 1000 мг 2 раза/сут), левофлоксацин (500 мг 2 раза/сут) в течение 10–14 дней.
Третья линия антихеликобактерной терапии
При отсутствии эрадикации Hp после лечения препаратами второй линии рекомендуется подбор терапии только после определения чувствительности Hp к антибиотикам.
Особые указания
При сохранении язвенного дефекта по результатам контрольной ЭГДС на 10–14-й день от начала лечения рекомендовано продолжить цитопротективную терапию висмута трикалия дицитратом (120 мг 4 раза/сут или 240 мг 2 раза/сут) и/или ИПП в половинной дозе в течение 2–3 нед. Пролонгированная терапия висмута трикалия дицитратом показана также в целях улучшения качества послеязвенного рубца и скорейшей редукции воспалительного инфильтрата.
Проведение эрадикации Hp беременным не показано.
Медикаментозная терапия язвенной болезни желудка и 12-перстной кишки, не ассоциированной с Helicobacter pylori
Отсутствие Hp должно быть подтверждено двумя методами при обязательном условии отсутствия терапии ИПП, Н2-блокаторами, антибиотиками или препаратами висмута в течение месяца перед проведением теста.
Антисекреторные препараты: один из ИПП (омепразол 20 мг 2 раза/сут, лансопразол 30 мг 1–2 раза/сут, пантопразол 40 мг 1–2 раза/ сут, эзомепразол 20–40 мг 1–2 раза/сут, рабепразол 20 мг 1–2 раза/сут) или блокаторы Н2-рецепторов (фамотидин 20 мг 2 раза/сут) в течение 2–3 нед.
Гастропротекторы: висмута трикалия дицитрат 120 мг 4 раза/сут, сукральфат по 0,5–1,0 г 4 раза/сут.
Антациды могут применяться в комплексной терапии в качестве симптоматического средства и в монотерапии (до проведения рН-метрии и диагностики Hp).
ХРОНИЧЕСКИЙ ГАСТРИТ
(шифр по МКБ-10: хронический гастрит – К 29.6)
Хронический гастрит (ХГ) – группа хронических заболеваний, которые морфологически характеризуются наличием воспалительных и дистрофических процессов в слизистой оболочке желудка, прогрессирующей атрофией, функциональной и структурной перестройкой с разнообразными клиническими признаками.
Самой частой причиной ХГ является Hp, что связано с высокой распространенностью этой инфекции.
Методы диагностики хронического гастрита
- Эндоскопический с морфологической оценкой биоптатов.
- Диагностика Hp (см. выше).
- Определение кислотообразующей и кислотонейтрализующей функций желудка (внутрижелудочная рН-метрия).
- Рентгенологический.
Принципы лечения хронического гастрита
Терапия ХГ осуществляется дифференцированно, в зависимости от клиники, этиопатогенетической и морфологической формы заболевания.
Хронический антральный гастрит, ассоциированный с Hp (тип В). Основной принцип лечения данного типа ХГ – эрадикация Hp (см. раздел «Медикаментозная терапия язвенной болезни желудка и 12-перстной кишки, ассоциированной с Hp»).
Хронический химический (реактивный) гастрит (рефлюкс-гастрит, тип C). Причиной гастрита C является заброс (рефлюкс) дуоденального содержимого в желудок. При дуоденогастральном рефлюксе повреждающее воздействие на слизистую оболочку желудка оказывают желчные кислоты и лизолецитин. Повреждающие свойства желчных кислот зависят от pH желудка: при pH<4 наибольшее воздействие на слизистую оболочку желудка оказывают тауриновые конъюгаты, а при pH>4 – неконъюгированные желчные кислоты.
При лечении рефлюкс-гастрита используют:
- висмута трикалия дицитрат (120 мг 4 раза/сут или 240 мг 2 раза/сут в течение 28 дней);
- сукральфат (500–1000 мг 4 раза/сут) наиболее эффективно связывает конъюгированные желчные кислоты при pH=2, при повышении pH этот эффект снижается, поэтому нецелесообразно его одновременное назначение с антисекреторными препаратами;
- препараты урсодезоксихолевой кислоты (10 мг/кг/сут) в течение 1–1,5 мес;
- для нормализации моторной функции – прокинетики, регуляторы моторной функции, спазмолитики (итоприда гидрохлорид, метоклопрамид, домперидон, тримебутин, мебеверин, альверина цитрат, гиосцина бутилбромид).
Понятие «хронический гастрит», особенно в странах СНГ, тесно связано с понятием «функциональная диспепсия» (ФД). Многие пациенты с диагнозом ФД оказываются инфицированными Hp, но не страдают при этом язвенной болезнью. Эрадикация Hp приводит к длительному улучшению примерно у 1 из 12 инфицированных пациентов, страдающих ФД.
HELICOBACTER PYLORI И НПВП-ГАСТРОПАТИЯ
НПВП-гастропатия – патология верхних отделов пищеварительного тракта, возникающая в хронологической связи с приемом НПВП и характеризующаяся повреждением слизистой оболочки (развитием эрозий, язв и их осложнений – кровотечения, пенетрации, перфорации).
Инфекция Hp ассоциирована с повышением риска возникновения неосложненных и осложненных гастродуоденальных язв у пациентов, принимающих НПВП и низкие дозы ацетилсалициловой кислоты (АСК). Эрадикация Hp снижает риск возникновения неосложненных и осложненных гастродуоденальных язв, ассоциированных с приемом НПВП и низких доз АСК.
Методы диагностики НПВП-гастропатии
- Клинический (изучение жалоб, сбор анамнеза заболевания, выявление факта и длительности приема НПВП, АСК, оценка факторов риска развития НПВП-гастропатии).
- Общий анализ крови (концентрация гемоглобина, число эритроцитов, гематокрит), биохимический анализ крови (показатели обмена железа), анализ кала на скрытую кровь для выявления кровотечения.
- Эндоскопический (с морфологической оценкой биоптатов).
- Диагностика Hp (см. выше).
- Определение кислотообразующей и кислотонейтрализующей функций желудка (внутрижелудочная рН-метрия).
- Рентгенологический.
Факторы риска НПВП-гастропатии
1. Со стороны пациента:
- возраст >60 лет;
- язвенная болезнь или желудочно-кишечные кровотечения в анамнезе.
2. Обусловленные особенностями применения НПВП:
- применение относительно более токсичных НПВП;
- высокие дозы НПВП (или сочетанное применение 2 и более НПВП);
- сочетанное применение антикоагулянтов и/или кортикостероидов.
3. Вероятные факторы риска:
- длительность применения НПВП;
- женский пол;
- ишемическая болезнь сердца;
- инфекция Hp;
- табакокурение;
- злоупотребление алкоголем;
- диспепсия на фоне приема НПВП в прошлом.
Медикаментозное лечение НПВП-гастропатии
Для медикаментозного лечения повреждений желудка и 12-перстной кишки, ассоциированных с приемом НПВП, целесообразно отменить прием НПВП и использовать Н2-блокатор (фамотидин) или ИПП в стандартных дозировках. Может быть рекомендована комбинация ИПП и висмута трикалия дицитрата продолжительностью 4 нед. Возможно назначение мизопростола в дозе 200 мкг 4 раза/сут во время еды и на ночь в течение 14–28 дней (противопоказан при беременности).
Если прием НПВП нельзя отменить, целесообразно назначение сопутствующей терапии ИПП на весь период приема НПВП.
Если больному с НПВП-гастропатией показано продолжение приема НПВП, целесообразно назначение селективных ингибиторов ЦОГ2. Однако такое лечение не исключает развития осложнений НПВП-гастропатии и не отменяет необходимости приема антисекреторных препаратов или гастропротекторов по показаниям.
Как альтернативна НПВП в качестве противовоспалительной терапии у больных с остеоартритом возможно назначение препарата на основе экстракта имбиря по 1 капсуле 2 раза/ сут продолжительностью 30 дней.
Обязательной является диагностика Hp, при выявлении которого должна быть проведена эрадикационная терапия с использованием схем, представленных в разделе «Медикаментозная терапия язвенной болезни желудка и 12-перстной кишки, ассоциированной с Hp».
Эрадикация Hp целесообразна перед началом лечения НПВП. Она обязательна у пациентов с язвенным анамнезом. Однако только одна эрадикация Hp не уменьшает риск развития гастродуоденальных язв у пациентов, длительно принимающих НПВП. Продолжение приема ИПП у таких пациентов так же необходимо, как и сама эрадикация Hp. У пациентов с язвенным анамнезом, принимающих АСК, необходимо проводить диагностику Hp.
Профилактика НПВП–гастропатии у разных категорий пациентов
Пациентам с риском развития НПВП-гастропатии (прием высоких доз НПВП, комбинация 2 и более НПВП, комбинация НПВП и АСК, антитромбоцитарных препаратов, антикоагулянтов или кортикостероидов, язвенная болезнь в анамнезе, наличие множественных факторов риска, возраст старше 65 лет) показан профилактический прием ИПП в стандартных дозах 1–2 раза/сут.
HELICOBACTER PYLORI И MALT-ЛИМФОМА
MALT-лимфома – экстранодальная В-клеточная лимфома из клеток маргинальной зоны, которая поражает лимфоидную ткань слизистых оболочек. Она относится к группе В-клеточных новообразований низкой степени злокачественности. Встречается в любом возрасте, может локализоваться в органах ЖКТ, щитовидной, слезных, слюнных и молочных железах, а также в бронхах. При эндоскопии определяется картина гастрита или язвенный дефект слизистой оболочки с нетипичными для обычной язвы солидными структурами.
Эрадикация Hp является первой линией терапии MALT-лимфомы низкой степени злокачественности.
HELICOBACTER PYLORI И КИШЕЧНАЯ МЕТАПЛАЗИЯ
Имеются доказательства, что после эрадикации Hp функция тела желудка улучшается. Однако остается не ясным, связано ли это с регрессией атрофического гастрита. Нет данных о том, что эрадикация Hp может привести к редукции кишечной метаплазии.
HELICOBACTER PYLORI И ВНЕЖЕЛУДОЧНЫЕ ЗАБОЛЕВАНИЯ
Имеются доказательства связи Hp с этиопатогенезом железодефицитной анемии, идиопатической тромбоцитопенической пурпуры и дефицитом витамина В12. При этих заболеваниях необходимо выявлять и проводить эрадикацию Hp.
Не подтверждено какой-либо причинной связи между Hp и сердечно-сосудистыми и неврологическими заболеваниями, а также протективного или ухудшающего воздействия Hp в отношении развития или течения астмы, аллергии и ожирения.
После проведения эрадикационной терапии биодоступность тироксина и L-изомера дигидроксифенилаланина (L-ДОФА) возрастает.
HELICOBACTER PYLORI И ИНГИБИТОРЫ ПРОТОННОЙ ПОМПЫ
Длительное применение ИПП у Hp-позитивных пациентов ускоряет процесс потери специализированных желез и ассоциировано с развитием атрофического гастрита тела желудка. Эрадикация Hp у пациентов, длительно принимающих ИПП, предотвращает развитие атрофического гастрита, однако еще не приведено доказательств, что это снижает риск развития рака желудка.



