По заключению экспертов Организации Объединенных Наций, Всемирной организации здравоохранения и Всемирного банка, программы по решению проблемы злоупотребления алкоголем в России относятся к приоритетным [1]. Показатели, характеризующие здоровье и демографическую ситуацию в России в целом, в значительной степени зависят от потребления алкоголя [2, 3].
Неблагоприятные медицинские и социальные последствия злоупотребления алкоголем представляют серьезную проблему современного общества. Алкоголизм является одной из наиболее значимых причин повышения смертности населения, а также заболеваемости и снижения трудоспособности. Существует прямая зависимость между долей потребления крепких алкогольных напитков в общем объеме потребления этанола и средней продолжительностью жизни мужчин и женщин в различных странах, причем особенно велик разрыв между продолжительностью жизни мужчин и женщин в странах с высоким потреблением крепких алкогольных напитков [4]. Риск возникновения и тяжесть алкоголь-ассоциированных соматических и психических расстройств связаны как с объемом употребляемого этанола, так и с абсолютной или относительной частотой злоупотребления [5]. Продемонстрирована связь между средними показателями потребления алкоголя на душу населения и смертностью в популяции [6]. Средняя дневная доза на уровне 35‒45 г «чистого алкоголя», или 245‒315 г в неделю, увеличивает риск смерти, а возрастание риска различных хронических заболеваний имеет место уже при употреблении 25 г алкоголя в день, или 175 г в неделю [7]. Эти объемы соответствуют объемам потребления алкоголя со средним и высоким уровнями риска, установленным ВОЗ [8]. По данным ВОЗ, злоупотребление алкоголем ассоциируется с развитием примерно 200 заболеваний и занимает пятое место среди причин преждевременной смерти (5,9% всех случаев смерти), приводя к 3 млн летальных исходов ежегодно [9]. Злоупотребление алкоголем сокращает продолжительность жизни в среднем на 30 лет [10]. Снижение дозы алкоголя (особенно с уровня высокого риска) приводит к уменьшению показателей смертности, что рассматривается как новая стратегия решения этой проблемы [11, 12].
В Российской Федерации серьезное положение в связи с чрезмерным потреблением алкоголя сложилось в начале 90-х гг. ХХ в., когда резко возросла смертность от болезней, связанных с алкоголизмом [13]. В России среди граждан в возрасте от 15 до 54 лет 52% смертей вызваны злоупотреблением алкоголем [14].
Среди ургентных пациентов многопрофильного соматического стационара четвертая часть поступающих имеет диагноз зависимости от алкоголя, при этом алкоголизация является существенным фактором риска срочной госпитализации, утяжеления состояния больных и ухудшения прогноза заболевания [15].
Потребление алкоголя может влиять на параметры здоровья как прямо, через повышение частоты отравлений, травматизма, так и косвенно, опосредуя развитие целого ряда соматических заболеваний. Алкоголь-ассоциированные расстройства включают панкреатит и цирроз печени [5], поражения сердца и сосудов, в том числе нарушения сердечного ритма, ишемическую болезнь сердца, алкогольную кардиомиопатию, инфекционные и опухолевые заболевания (рак верхних отделов желудочно-кишечного тракта и рак печени), неврологические и коморбидные психические расстройства (депрессия, алкогольные психозы) [16]. Поражение различных органов и систем организма в результате хронической алкогольной интоксикации входит в понятие алкогольной болезни [17]. К наиболее распространенным причинам алкогольной смертности относят несчастные случаи, дорожно-транспортные происшествия и случаи насильственной смерти, алкогольное отравление и ишемическую болезнь сердца.
Систематическое или редкое, но массивное злоупотребление алкоголем неизбежно приводит к поражению центральной нервной системы. Алкогольное поражение периферической нервной системы является наиболее частым осложнением хронической алкогольной интоксикации, которое развивается на поздних стадиях заболевания и отмечается в 5 раз чаще, чем поражение центральной нервной системы [18].
Алкогольная полинейропатия (АПНП; G62.1) выявляется у злоупотребляющих алкоголем людей любого возраста и пола (с незначительным преобладанием у женщин), вероятность ее развития не зависит от расы и национальности. Частота алкогольной полинейропатии достигает 12,5–29,6% у больных алкоголизмом [19‒21]. В то же время ее латентные бессимптомные формы обнаруживаются у 97–100% больных алкоголизмом [22].
К сожалению, ввиду редкой своевременной обращаемости больных алкоголизмом за медицинской помощью, а также вследствие нередко бессимптомного течения АПНП типичной является поздняя диагностика этого заболевания.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ АЛКОГОЛЬНОЙ ПОЛИНЕЙРОПАТИИ
Клинические признаки АПНП и их связь с чрезмерным потреблением алкоголя были описаны еще в 1787 г. Lettsom и в 1822 г. Jackson. АПНП относится к группе экзогенно-токсических поражений нервной системы; она возникает у злоупотребляющих алкоголем лиц на поздних стадиях развития алкоголизма (при наличии алкогольной зависимости в течение ≥5 лет) вследствие непосредственного влияния этанола и его метаболитов на периферические нервы и последующего нарушения обменных процессов в нервных волокнах.
Около 76% случаев заболевания спровоцировано реактивностью организма. Имеют значение аутоиммунные процессы, а пусковым фактором служат определенные вирусы и бактерии. АПНП развивается в результате переохлаждения и других провоцирующих факторов у женщин чаще, чем у мужчин. Предрасполагает к развитию АПНП дисфункция печени. Условием развития тяжелой формы заболевания является повышенная уязвимость нервной ткани, сформировавшаяся в результате наследственной предрасположенности [23].
Отмечается связь развития АПНП с оксидативным стрессом и избыточным образованием свободных кислородных радикалов, поражающих эндотелий и вызывающих эндоневральную гипоксию [24]. Нервная система чувствительна к свободным радикалам, образующимся в ходе перекисного окисления липидов, избыточное образование которых в условиях хронической алкогольной интоксикации при сниженной активности антиоксидантных систем приводит к развитию окислительного стресса [25]. Показано снижение содержания α-токоферола в крови при алкоголизме, что свидетельствует о несостоятельности эндогенной антиоксидантной системы [26].
Прямое токсическое действие этанола и его метаболитов на нейроны обусловлено индуцированием глутаматной нейротоксичности, снижением выработки белка нейрофиламентов и нарушением быстрого аксонального транспорта [27].
Определенную роль в нарушении синтеза белков миокарда и скелетных мышц играет основной метаболит этанола – ацетальдегид. В случаях хронической алкогольной интоксикации в связи со снижением активности альдегиддегидрогеназы в печени концентрация ацетальдегида в крови значительно повышается [24, 25].
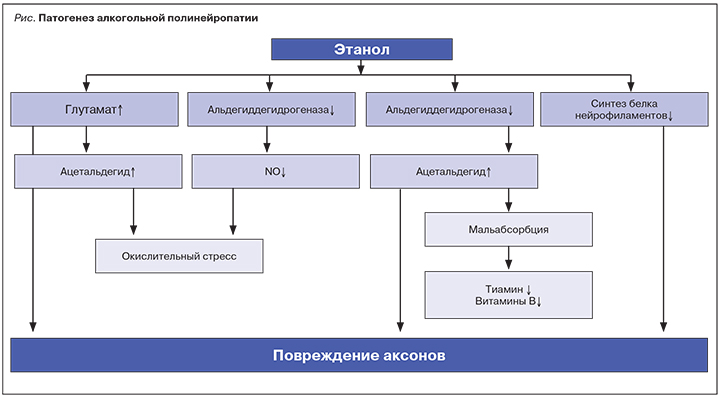
На развитие двигательной и смешанной форм АПНП оказывает влияние дефицит в организме тиамина (витамина В1) [28, 29]. Алкоголизм – наиболее частая причина тиаминдефицитного состояния у населения развитых стран, что обусловлено недостаточным питанием и/или нарушением под влиянием алкоголя и ацетальдегида всасывания тиамина в тонкой кишке (синдромом мальабсорбции). Гиповитаминоз тиамина при алкоголизме также может быть обусловлен угнетением процессов фосфорилирования, в результате чего нарушается превращение тиамина в тиамина пирофосфат, который является коферментом (катализатором) в катаболизме сахаров и аминокислот. Инфекционные болезни, кровотечения и ряд других повышающих энергетические потребности организма факторов усугубляют дефицит витамина. Гиповитаминоз тиамина и недостаточное образование тиамина пирофосфата вызывает снижение активности ряда ферментов, участвующих в катаболизме углеводов, биосинтезе некоторых элементов клетки и синтезе предшественников нуклеиновых кислот. В организме тиаминдефицитное состояние сопровождается различными изменениями метаболизма глюкозы. В результате снижается встраивание липидов в миелин; нарушается биосинтез и метаболизм нейромедиаторов; образуются зоны с лактатацидозом и внутриклеточным накоплением кальция, которые способствуют проявлению нейротоксических эффектов алкоголя (рис.).
Токсическое воздействие алкоголя подтверждается прямой зависимостью между тяжестью АПНП и количеством потребляемого этанола [13, 30].
АПНП относится к числу первичных аксонопатий, но по мере прогрессирования заболевания развивается также и демиелинизация. В настоящее время принято разделять полинейропатии на аксонопатии, в основе патогенеза которых лежит первичное повреждение осевых цилиндров нервов, и миелинопатии, характеризующиеся нарушением функции проводимости вследствие поражения миелиновых оболочек. Однако разделение характера поражения на первично аксональный или демиелинизирующий возможно лишь на ранних стадиях патологического процесса. Больные алкоголизмом чаще оказываются в поле зрения врача на отдаленных стадиях полинейропатии с выраженным функциональным дефектом.
КЛИНИЧЕСКАЯ КАРТИНА
АПНП представляет собой нарушение функций множества периферических нервов. Основными симптомами АПНП являются парестезии, боль и/или жжение в стопах и кистях, прогрессивно нарастающая слабость стоп и кистей, нарушения походки.
Динамика заболевания
Выделяют хронический вариант течения АПНП, который отличается медленным (более года) прогрессированием патологических процессов (встречается часто); острый и подострый варианты (развиваются в течение месяца и наблюдаются реже).
Первые симптомы АПНП проявляются в виде парестезии и слабости мышц. В половине случаев нарушения первоначально затрагивают нижние конечности, а через несколько часов или дней распространяются на верхние. Иногда руки и ноги пациентов поражаются одновременно. Часто уже в дебюте заболевания отмечаются болезненные мышечные спазмы (крампи) в ногах. У большинства больных наблюдаются диффузное снижение тонуса мышц; резкое снижение, а затем и отсутствие сухожильных рефлексов. Возможны нарушения со стороны мимической мускулатуры, а при тяжелых формах заболевания – задержка мочеиспускания. Эти симптомы сохраняются на протяжении 3‒5 дней, а затем исчезают.
Возникают парестезии в дистальных отделах конечностей, болезненность нервных стволов и икроножных мышцах во время пальпации. В дальнейшем развиваются слабость и парез или паралич конечностей. Сначала поражаются дистальные отделы нижних конечностей. Самыми выраженными являются симптомы поражения малоберцового нерва с выпадением функции разгибателей стопы и пальцев, что предопределяет перонеальную, «петушиную» походку ‒ степпаж (фр. steppage). Быстро развиваются гипотония, атрофия парализованных мышц. Сухожильные рефлексы сначала могут быть повышенными, а в дальнейшем снижаются или выпадают. Чувствительность страдает меньше, чем двигательная сфера. В одних случаях возникают явления чувствительной ирритации в виде гиперестезии, гипералгезии, иногда с гиперпатическими чертами, в других – преобладают симптомы выпадения чувствительной функции по дистальному типу в виде гипестезии, анестезии, иногда в сочетании с гиперестезиями. Расстройства проприоцептивной чувствительности приводят к развитию сенситивной атаксии. Атактические нарушения сочетаются с выпадением коленных и ахилловых рефлексов и напоминают клиническую картину спинной сухотки. Такая сенситивно-атактическая, в том числе с поражением vasa nervorum, форма АПНП получила название периферического псевдотабеса (pseudotabes peripherica). Очень часто наблюдаются вазомоторные, трофические и секреторные расстройства: гипергидроз, отек дистальных отделов конечностей, нарушение их нормальной окраски, изменение температуры кожи. Из черепных нервов нередко поражаются глазодвигательные, значительно реже блуждающий и диафрагмальный нервы, что сопровождается нарушением функции сердечно-сосудистой системы, расстройствами дыхания. Характерной особенностью АПНП является ее сочетание с амнестическим синдромом, который проявляется потерей памяти на текущие события, конфабуляциями, дезориентацией во времени и пространстве (Корсаковский синдром). Период нарастания симптомов может продолжаться недели и месяцы.
Для тяжелых случаев заболевания характерны ослабление дыхательной мускулатуры, требующее проведения искусственной вентиляции легких; выраженное поражение суставно-мышечной и вибрационной глубокой чувствительности (20‒50% больных); поражение вегетативной нервной системы (синусовая тахикардия или брадикардия, аритмия, падение артериального давления).
Прогноз для жизни может быть серьезным при вовлечении в процесс ветвей блуждающего нерва, иннервирующих сердце, и диафрагмального нерва.
Патогенетические формы алкогольной полинейропатии
С учетом патогенетических факторов развития нейропатии при алкоголизме оправданным является выделение АПНП без дефицита тиамина и АПНП с его дефицитом, различающихся по клиническим проявлениям [28].
АПНП без дефицита тиамина представляет собой медленно прогрессирующую дистальную симметричную сенсорную (в большинстве случаев) или сенсорно-моторную полинейропатию с преимущественным поражением нижних конечностей. Для токсической формы, связанной с прямым повреждающим действием этанола, характерны повреждение тонких волокон, хроническое прогрессирование. Это приводит к избирательной потере болевой или температурной чувствительности, парестезиям, дизестезиям, спонтанным болям при отсутствии парезов, нормальных сухожильных рефлексов. Развивается сенсорная или моторно-сенсорная нейропатия, в 25‒45% случаев сопровождающаяся болевым синдромом [23].
АПНП с дефицитом тиамина представляет собой дистальную симметричную сенсорно-моторную или моторно-сенсорную полинейропатию, развивающуюся на фоне длительного запойного приема алкоголя, дефицита питания и сопровождающуюся значительным снижением массы тела. При алиментарной форме страдают тонкие и толстые волокна, что сопровождается острым или хроническим прогрессированием. Поражаются волокна глубокой чувствительности, что ведет к развитию сенситивной атаксии. Боль наблюдается в 10‒20% случаев [28].
Клинические формы алкогольной полинейропатии
В зависимости от клинической картины заболевания выделяют несколько форм АПНП.
Для сенсорной формы характерны болевые ощущения в дистальных отделах конечностей, как правило, нижних; чувство зябкости, онемения или жжения; судороги икроножных мышц, болезненность в области крупных нервных стволов. Для ладоней и стоп характерны повышенная или пониженная болевая и температурная чувствительность по типу «перчаток и носков», возможны сегментарные нарушения чувствительности. Сенсорные нарушения в большинстве случаев сопровождаются вегетативно-сосудистыми нарушениями (гипергидроз, акроцианоз, мраморность кожи на ладонях и стопах).
Двигательную форму характеризуют периферические парезы различной степени и легкая степень сенсорных нарушений в нижних конечностях. Наблюдаются нарушения подошвенного сгибания стоп и пальцев, вращения стопы внутрь, ходьбы на носках или функции разгибателей стопы и пальцев, мышечная атрофия и гипотония в области стоп и голеней («когтистая стопа»).
Смешанная форма предполагает наличие как двигательных, так и сенсорных нарушений: вялые парезы, паралич стоп или кистей, боль или онемение по ходу крупных нервных стволов, повышенная или пониженная чувствительность в области пораженных участков, причем поражение затрагивает как нижние, так и верхние конечности (страдают в основном разгибатели). Мышцы кистей и предплечий атрофируются.
Атактическая форма представлена нарушениями глубокой чувствительности: сенситивная атаксия (нарушенная походка и координация движений), онемение в ногах, пониженная чувствительность дистальных отделов конечностей, отсутствие ахилловых и коленных рефлексов, боль при пальпации в области нервных стволов.
ДИАГНОСТИКА АЛКОГОЛЬНОЙ ПОЛИНЕЙРОПАТИИ
АПНП диагностируется комплексно.
Клинические методы включают неврологическое обследование и специальные шкалы (ВАШ, Мак-Гилла, Общей оценки симптомов нейропатии ‒ NTSS). Диагностически значимыми клиническими критериями являются прогрессирующая слабость мышц более чем в одной конечности, относительная симметричность поражений, наличие сухожильной арефлексии, чувствительных нарушений, быстрое нарастание симптомов и прекращение их развития на 4-й неделе заболевания.
Нейрофизиологические методы (электромиография, количественное сенсорное тестирование) позволяют обнаружить признаки аксональной дегенерации и разрушения миелиновой оболочки.
Лабораторные методы включают определение уровней аспартатаминотрансферазы, аланинаминотрансферазы, γ-глутамилтрансферазы, иммуноглобулина А, активности транскетолазы; жидкостную хроматографию тиамина пирофосфата. Анализ спинномозговой жидкости и биопсия нервных волокон осуществляются для исключения диабетической и уремической полинейропатии. В сомнительных случаях для исключения других заболеваний проводят магнитно-резонансную или компьютерную томографию. Морфологические методы включают биопсию нерва, кожи, мышцы.
Указанный комплекс методов позволяет диагностировать АПНП на ранней (субклинической) стадии, когда функциональные нарушения периферического нейромоторного аппарата преобладают над структурными и имеют потенциально обратимый характер, что является важным фактором успешного лечения.
ЛЕЧЕНИЕ АЛКОГОЛЬНОЙ ПОЛИНЕЙРОПАТИИ
Терапия АПНП должна быть комплексной и предусматривать воздействие на причину заболевания. Полное прекращение приема алкоголя с восстановлением полноценного сбалансированного питания и возмещением необходимых витаминов, преимущественно тиамина, а также пиридоксина, цианокобаламина, фолиевой кислоты относится к обязательным условиям лечения. Перед началом терапии желательно определение уровня тиамина в крови или оценка транскетолазной активности эритроцитов.
Лечение АПНП включает физиотерапевтические процедуры (электростимуляция нервных волокон и спинного мозга); магнитотерапию и иглорефлексотерапию; лечебную физкультуру и массаж, позволяющие восстановить мышечный тонус.
При медикаментозном лечении применяют симптоматическую (антиконвульсанты, антидепрессанты), патогенетическую (α-липоевая кислота ‒ АЛК, комплекс витаминов группы В) или комбинированную терапию [31].
В терапии АПНП используют витамин С; улучшающий микроциркуляцию пентоксифиллин или цитофлавин; улучшающие утилизацию кислорода и повышающие устойчивость к кислородной недостаточности антигипоксанты; улучшающий нервно-мышечную проводимость ипидакрин; для уменьшения болей — противовоспалительные нестероидные препараты (диклофенак); для устранения стойких чувствительных и двигательных расстройств — антихолинэстеразные препараты; улучшающие возбудимость нервных волокон церебральные ганглиозиды и препараты нуклеотидов. При наличии токсических поражений печени применяют гепатопротекторы. Болевой синдром при АПНП имеет характер нейропатического, поэтому для его купирования широко используются антиконвульсанты (карбамазепин, габапентин) и антидепрессанты (трициклические — амитриптилин; селективные ингибиторы обратного захвата серотонина — флуоксетин, пароксетин; ингибиторы обратного захвата серотонина и норадреналина — венлафаксин, дулоксетин) [32]. Лечение следует начинать с минимальных терапевтических доз, постепенно повышая их до достижения эффекта или развития побочных эффектов.
Часто требуется комбинированная терапия с применением препаратов с различными механизмами действия и по возможности неперекрывающимся спектром побочных эффектов [33]. Комплексное применение препаратов для симптоматической и патогенетической терапии АПНП повышает эффективность лечения и улучшает клиническое состояние пациентов [34].
Была продемонстрирована безопасность и эффективность клинического применения в лечении больных АПНП комбинации цитидина монофосфата, уридина трифосфат и гидроксокобаламина (производное витамина В12) [35].
При наличии полидефицитарного состояния показана заместительная терапия витаминами группы В, в первую очередь тиамином, препаратами фолиевой кислоты. При лечении в течение 12 нед комплексом витаминов группы В отмечали улучшение вибрационной чувствительности и функции проведения по чувствительным волокнам, уменьшение выраженности боли [36]. Эффект комплексного препарата связывают с прямым нейротропным действием. В систематическом обзоре Cochrane 2008 г. отмечена хорошая переносимость витаминов группы В, однако был сделан вывод, что количество рандомизированных исследований недостаточно для подтверждения их высокой эффективности [37].
Основным элементом патогенетической терапии АПНП считается применение антиоксидантов, в том числе наиболее активного из них АЛК или тиоктовой кислоты [38]. Согласно современным представлениям, АЛК представляет собой витаминоподобное вещество, биологическая роль которого определяется его участием в окислительном декарбоксилировании пировиноградной кислоты и α-кетокислот. АЛК является коферментом митохондриальных мультиферментных комплексов и играет важную роль в энергетическом балансе организма. Наличие тиоловых (сульфгидрильных) групп в молекуле АЛК придает ей свойства антиоксиданта. Препараты АЛК не только уменьшают проявления оксидантного стресса, но и способствуют увеличению содержания в нерве нейротрофических факторов, в том числе фактора роста нерва, нормализуют аксональный транспорт и восстанавливают мембрану нервной клетки. Антиоксидантный эффект АЛК способствует более эффективной репарации молекул ДНК после повреждения в результате окислительного стресса. Как эндогенный антиоксидант АЛК участвует в регулировании липидного и углеводного обмена, оказывает липотропный эффект, влияет на обмен холестерина, улучшает функцию печени, оказывает дезинтоксикационное действие при различных интоксикациях. Влияние на углеводный обмен выражается в снижении концентрации глюкозы в крови и увеличении содержания гликогена в печени. В целом препараты АЛК улучшает трофику нейронов. Доказано прямое детоксикационное воздействие АЛК при этанол-обусловленной нейротоксичности in vivo [39]. Также АЛК позитивно действует на сенсорные и моторные симптомы полиневропатии, оказывает умеренный анальгетический эффект [40].
На фоне лечения препаратами АЛК происходит уменьшение выраженности невропатической боли, парестезий, крампи. Установлен дозозависимый эффект АЛК. Наиболее отчетливый результат терапии отмечен у больных с преимущественно сенсорными проявлениями АПНП, получавших АЛК. Значимых различий в динамике симптомов при применении указанных доз выявлено не было, что позволяет считать оптимальной дозировку 600 мг/сут [38].
В настоящее время в медицинской практике используются различные препараты АЛК, различающиеся дозировкой, количеством активного вещества в таблетированной или инъекционной форме. Патогенетическая терапия с использованием АЛК приводит к уменьшению зоны расстройств чувствительности, повышению силы в ногах при хорошей переносимости препарата и отсутствии побочных эффектов [42].
В зависимости от клинических особенностей течения АПНП препарат АЛК назначается либо парентерально, либо перорально. Эти лекарственные формы различаются по времени наступления эффекта и скорости снижения выраженности болевой симптоматики. Как правило, в клинической практике используют ступенчатую схему терапии. Целесообразно начинать лечение с внутривенного введения АЛК в дозе 600 мг/ сут в течение 2 нед с последующим переходом на пероральный прием в этой же дозе в течение 6‒8 нед (капсулы по 300 мг 2 раза в сутки) [43]. Следует отметить, что препарат АЛК и в ампулах , и в таблетках выпускается в дозировках 300 и 600 мг.
Препараты АЛК эффективны у 70% пациентов с АПНП.
ПРОГНОЗ
Ранее считалось, что даже при длительном ежедневном употреблении алкоголя (100 г этилового спирта в сутки в течение 5–10 лет) его отмена приводит к регрессу клинических проявлений АПНП. Однако в случаях тяжелой алкогольной нейропатии даже через 5 лет ремиссии алкоголизма не происходит регресса клинических и морфологических признаков заболевания.
ЗАКЛЮЧЕНИЕ
Распространенность АПНП время весьма высока, она стала не только медицинской, но и социальной проблемой. Предполагается участие двух основных патогенетических факторов: токсического действия этанола и его метаболитов и недостаточного питания с дефицитом витаминов группы В, в частности тиамина. При формировании терапевтической стратегии следует учитывать индивидуальные особенности пациента, выраженность основного заболевания, болевой симптоматики, степень неврологического дефицита, наличие сопутствующих заболеваний. Терапевтические мероприятия наиболее эффективны на субклинической стадии поражения, когда повреждение периферических нервов имеет обратимый характер. Это указывает на необходимость ранней, субклинической диагностики АПНП, так как проведение адекватной терапии на асимптомной стадии поражения периферических нервов может привести к их структурному и функциональному восстановлению. Следует отметить необходимость длительной терапии АПНП.



