Несмотря на то что хроническая сердечная недостаточность (ХСН) не является самостоятельной нозологической единицей и может осложнять течение практически всех сердечно-сосудистых заболеваний (ССЗ), внимание к ней продолжает оставаться крайне высоким, что обусловлено значительным ее вкладом в структуру госпитализаций и смертности, а также высокими затратами на лечение [1]. ХСН страдают приблизительно 1–2% взрослой популяции в развитых странах, а в возрастной группе старше 70 лет – более 10%. Риск развития ХСН у пациентов 55 лет и старше составляет 33% для мужчин и 28% для женщин [2]. В России распространенность ХСН с 1998 по 2014 г. выросла почти в 2 раза и, по данным Российских эпидемиологических исследований, достигла в общей популяции 7%; при этом встречаемость клинически выраженной ХСН составляет 4,5%, увеличиваясь от 0,3% в возрастной группе 20–29 лет до 70% у лиц старше 90 лет [3].
Высокая распространенность и тяжесть ХСН обусловливают высокую частоту госпитализаций. ХСН становится причиной более чем 16,8% всех случаев поступлений в стационар. При этом пациенты, госпитализированные по поводу декомпенсации сердечной недостаточности, в 62,5% случаев повторно госпитализируются в течение года после выписки [4].
До 1990-х гг. 60–70% пациентов с ХСН умирали в течение 5 лет. Несмотря на то что современные методы терапии позволили уменьшить как количество повторных госпитализаций в связи с декомпенсацией ХСН, так и смертность, результаты лечения зачастую остаются неудовлетворительными. Данные пилотных исследований Европейского общества кардиологов (ESC) демонстрируют, что уровень смертности от всех причин у госпитализированных и амбулаторных пациентов с ХСН за 12-месячный период составил 17 и 7%, а частота госпитализаций – 44 и 32% соответственно [2]. В России средняя годовая смертность среди пациентов с ХСН I–IV функциональных классов (ФК) составляет 6%, а среди пациентов с клинически выраженной симптоматикой достигает 12% [3].
В действующих клинических рекомендациях в зависимости от состояния насосной функции сердца, определяемой по показателю фракции выброса (ФВ) левого желудочка (ЛЖ), выделяют группы пациентов с ХСН и низкой ФВ (<40%; СНнФВ), ХСН и промежуточной ФВ (40–49%; СНпФВ) и ХСН с сохраненной ФВ (≥50%; СНсФВ). Количество больных СНсФВ, по разным данным, варьирует от 22 до 78%, однако смертность у пациентов с СНнФВ выше, чем при СНсФВ [2, 3].
ПРИНЦИПЫ ФАРМАКОТЕРАПИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ С НИЗКОЙ ФРАКЦИЕЙ ВЫБРОСА ЛЕВОГО ЖЕЛУДОЧКА
Поиск новых методов эффективного лечения сердечной недостаточности остается крайне актуальной проблемой. В настоящее время основными задачами лечения пациентов с ХСН являются:
- устранение симптомов (одышки, отеков и др.);
- улучшение качества жизни;
- снижение количества госпитализаций;
- улучшение прогноза.
Снижение смертности и числа госпитализаций служат главными критериями эффективности терапевтических мероприятий. При этом недопустимо недооценивать важность уменьшения клинических проявлений и улучшения самочувствия, поскольку повышение качества жизни больного, помимо гуманистической составляющей, содержит потенциал позитивного влияния на прогноз через повышение приверженности к лечению.
Общепринятые медикаментозные методы лечения СНнФВ включают ингибиторы ангиотензинпревращающего фермента (ИАПФ), ингибитор ангиотензиновых рецепторов и неприлизина (АРНИ) сакубитрил/валсартан, бета-адреноблокаторы, блокаторы рецепторов к ангиотензину II (БРА), петлевые диуретики, антагонисты минералкортикоидных рецепторов (АМКР), блокатор If-каналов ивабрадин и изосорбида динитрат в комбинации с гидралазином. За исключением петлевых диуретиков, все эти группы лекарственных средств в той или иной степени доказали свою эффективность в улучшении симптомов, сокращении числа госпитализаций и/или увеличении выживаемости [2, 3, 5]. Алгоритм лечения пациентов с СНнФВ представлен на рисунке.
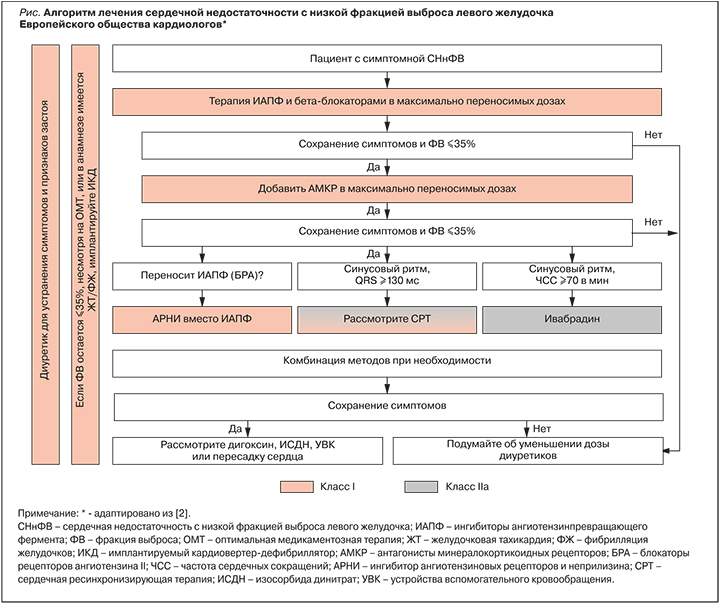
ИАПФ при отсутствии противопоказаний рекомендованы всем пациентам с симптомной СНнФВ для снижения риска смерти и госпитализации по причине сердечной недостаточности, а также пациентам с бессимптомной систолической дисфункцией ЛЖ и инфарктом миокарда в анамнезе для профилактики развития симптомов заболевания [2, 3].
Бета-адреноблокаторы дополнительно к ИАПФ рекомендованы всем пациентам со стабильной симптомной СНнФВ для снижения риска смерти и госпитализации по поводу сердечной недостаточности. Также бета-блокаторы показаны бессимптомным пациентам после перенесенного инфаркта миокарда с наличием систолической дисфункции ЛЖ для снижения риска смерти и профилактики развития симптомов сердечной недостаточности [2].
АМКР (спиронолактон или эплеренон) рекомендованы всем пациентам с сохраняющимися, несмотря на применение ИАПФ и бета-адреноблокаторов, симптомами сердечной недостаточности и показателем ФВ ЛЖ ≤35% с целью снижения риска смерти и госпитализации по поводу этого заболевания [2]. Согласно российским клиническим рекомендациям, АМКР показаны всем пациентам с ХСН II–IV ФК и ФВ ЛЖ ≤40% с аналогичными целями [3].
Применение БРА рекомендовано пациентам с ХСН и ФВ ЛЖ ≤40% для уменьшения количества госпитализаций и смерти по сердечно-сосудистой причине только в случае непереносимости ИАПФ. Применение комбинации ИАПФ/БРА следует ограничить кругом пациентов с симптомной СНнФВ, которые находятся на терапии бета-адреноблокаторами и имеют непереносимость АМКР [2, 3].
Комбинацию ингибитора неприлизина сакубитрила и БРА валсартана рекомендуется применять для снижения риска смерти и госпитализаций по причине сердечной недостаточности вместо ИАПФ/БРА у пациентов с симптомной СНнФВ и сохраняющимися симптомами заболевания, несмотря на оптимальную терапию ИАПФ/БРА, бета-адреноблокаторами и АМКР [2, 3].
Диуретики рекомендованы для уменьшения признаков и симптомов задержки жидкости у пациентов с СНнФВ, но их влияние на смертность и заболеваемость не было изучено в рандомизированных клинических исследованиях. Метаанализ из базы Cochrane показал, что у пациентов с ХСН, принимающих петлевые и тиазидные диуретики, наблюдается уменьшение риска смерти и ухудшения течения сердечной недостаточности, а также улучшение переносимости физических нагрузок [2, 3].
Прием ивабрадина показан пациентам с синусовым ритмом, ФВ ЛЖ ≤35%, симптомами ХСН II–IV ФК и уровнем частоты сердечных сокращений (ЧСС) ≥70 ударов в минуту, находящимся на подобранной терапии рекомендованными (или максимально переносимыми) дозами бета-адреноблокаторов, ИАПФ/БРА/АРНИ и АМКР для снижения госпитализаций и смертности по причине сердечной недостаточности, а также в случае невозможности назначения бета-адреноблокаторов [2].
Использование сердечных гликозидов у пациентов с ХСН в настоящее время ограниченно. Из существующих препаратов этой группы рекомендован дигоксин; эффективность и безопасность других сердечных гликозидов при ХСН изучена недостаточно. Назначение дигоксина пациентам с ХСН не улучшает их прогноз, но снижает количество госпитализаций по поводу заболевания, улучшает его симптомы и качество жизни [5]. Следует отметить, что в рандомизированных клинических исследованиях (РКИ) влияние дигоксина на исходы пациентов с СНнФВ и фибрилляцией предсердий (ФП) не изучалось. Результаты метаанализов недавних нерандомизированных, в том числе наблюдательных, исследований оказались противоречивыми [2]. Сегодня дигоксин рекомендован только для лечения больных СНнФВ и ФП с ускоренной частотой сокращения желудочков, когда нет возможности использовать другие варианты терапии. Также можно рассмотреть назначение дигоксина пациентам с ХСН II–IV ФК, ФВ ЛЖ ≤40%, с синусовым ритмом и сохраняющимися симптомами сердечной недостаточности, несмотря на терапию ИАПФ/БРА/АРНИ, бета-адреноблокаторами и АМКР, для снижения риска госпитализаций [2, 3].
Комбинация изосорбида динитрата с гидралазином (последний не зарегистрирован в России) рекомендована ESC для снижения риска смерти и госпитализации по поводу ХСН пациентам негроидной расы с ФВ ЛЖ ≤45% при наличии дилатированного ЛЖ и сохраняющимися, несмотря на терапию ИАПФ/БРА/АРНИ, бета-адреноблокаторами и АМКР, симптомами III–IV ФК сердечной недостаточности. Также применение этой комбинации может быть рассмотрено у пациентов с симптомной СНнФВ в случаях противопоказаний или непереносимости ИАПФ/БРА [2]. Отечественные клинические рекомендации предлагают в такой ситуации рассмотреть назначение изосорбида динитрата без гидралазина [3, 5].
Препараты омега-3 полиненасыщенных жирных кислот (ПНЖК), содержащие 850–882 мг эйкозапентаеновой и докозагексаеновой кислоты в виде этиловых эфиров, могут рассматриваться в качестве дополнительной терапии для улучшения прогноза у пациентов с симптомной СНнФВ, которые уже находятся на оптимизированной рекомендованной терапии ИАПФ/БРА, бета-блокаторами и АМКР [2, 3].
Помимо медикаментозной терапии, у пациентов с СНнФВ могут использоваться методы хирургического лечения, такие как имплантация кардиовертеров-дефибрилляторов, многокамерных электрокардиостимуляторов (сердечная ресинхронизирующая терапия), устройств вспомогательного кровообращения, и трансплантация сердца [2, 3].
РОЛЬ И МЕСТО ИНГИБИТОРОВ SGLT2 В ТЕРАПИИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ С НИЗКОЙ ФРАКЦИЕЙ ВЫБРОСА ЛЕВОГО ЖЕЛУДОЧКА
Ингибиторы натрий-глюкозного котранспортера 2‑го типа (SGLT2) представляют собой группу препаратов, вызывающих гипогликемический эффект за счет усиления глюкозурии. Реабсорбция глюкозы почти на 90% осуществляется в проксимальных извитых канальцах за счет участия белка SGLT2 – обладающего низким сродством переносчика с большой транспортной способностью, а оставшаяся часть подвергается обратному всасыванию за счет взаимодействия с более прочно связывающим субстрат протеином SGLT1, расположенным дистальнее [6].
Первым веществом, являющимся конкурентным неселективным блокатором SGLT2 и SGLT1, стал выделенный еще в 1835 г. из коры яблони флоризин, обладающий эффектами хинина. Долгое время его пытались использовать в качестве жаропонижающего средства, в том числе при малярии. В 1980-е гг. на лабораторных моделях был показан гипогликемический эффект флоризина, сопровождавшийся снижением инсулинорезистентности. Это дало импульс к разработке и изучению новых субстанций, обладающих большей селективностью к SGLT2 и лучшей биодоступностью [7, 8]. Неудивительно, что первоначальной сферой применения данной группы препаратов стал сахарный диабет (СД) 2-го типа: в 2012 г. с целью его лечения у взрослых пациентов в Европе был одобрен дапаглифлозин, в 2014 г. – эмпаглифлозин, а в США первым на рынок в 2013 г. поступил канаглифлозин. В России, помимо этих трех препаратов, в настоящее время также доступны ипраглифлозин и эртуглифлозин. Особенностью данного класса препаратов, помимо гипогликемического эффекта, стало влияние на снижение массы тела и, что важно, очень низкий риск развития гипогликемии.
Новая эра в применении ингибиторов SGLT2 началась в 2015 г., когда были опубликованы результаты исследования EMPA-REG OUTCOME. Они показали, что прием эмпаглифлозина позволяет снизить относительный риск госпитализации по причине сердечной недостаточности на 35%, а относительный риск сердечно-сосудистой смерти – на 38%. При этом снижение сердечно-сосудистой смертности и частоты госпитализаций по поводу сердечной недостаточности было одинаково выражено как у пациентов, исходно имевших признаки заболевания, так и у лиц без его анамнеза, а величина эффекта эмпаглифлозина была сопоставима с препаратами основных классов для лечения ХСН. Более того, вероятность смерти от кардиоваскулярных осложнений была ниже при приеме эмпаглифлозина вне зависимости от исходного риска развития сердечной недостаточности. Наибольшая абсолютная разница по данному показателю (снижение на 4,9%) в сравнении с плацебо регистрировалась у лиц с высокой вероятностью развития сердечной недостаточности [9]. Более поздний анализ повторных событий исследования EMPA-REG OUTCOME продемонстрировал, что в сопоставлении с плацебо эмпаглифлозин в дополнение к стандартной терапии у пациентов с СД 2-го типа и ассоциированными кардиоваскулярными заболеваниями предотвращал общее количество событий: 3P-MACE (3 основные нежелательные сердечно-сосудистые события) и 4P-MACE (4 основные нежелательные сердечно-сосудистые события), сердечно-сосудистой смерти, коронарных событий, инфаркта миокарда (на 21%), госпитализаций по причине сердечной недостаточности и госпитализаций по любой причине [10].
В другом многоцентровом международном исследовании – CANVAS – канаглифлозин снизил частоту сердечно-сосудистых событий (MACE) на 14%, но не приводил к снижению общей и сердечно-сосудистой смертности [11]. Для еще одного представителя группы ингибиторов SGLT2 – дапаглифлозина – в рамках исследования DECLARE-TIMI 58 совокупная частота возникновения случаев сердечно-сосудистой смерти и госпитализации по поводу сердечной недостаточности была значимо ниже (4,9%) по сравнению с пациентами, получавшими плацебо (5,8%), а относительное уменьшение риска наступления данной конечной точки составило 17%. Основной вклад в снижение частоты развития первичной точки внесло значимое (на 27%) уменьшение риска развития госпитализаций по поводу сердечной недостаточности, при этом различий в частоте сердечно-сосудистой смерти в группах сравнения выявлено не было [12].
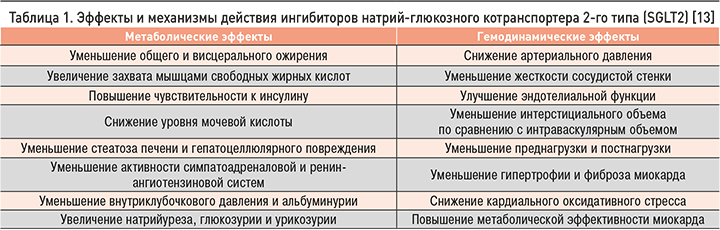
Подобное влияние на развитие сердечно-сосудистых осложнений не может быть обусловлено действием ингибиторов SGLT2 на снижение уровня глюкозы в крови, поскольку аналогичные эффекты не наблюдаются у других антидиабетических препаратов, которые обладают более сильным антигипергликемическим действием. В качестве объяснения уникальных свойств глифлозинов предложено несколько механизмов, основные из которых представлены в таблице 1. Эффекты глифлозинов принято делить на метаболические и гемодинамические [13].
Подтверждение положительного влияния ингибиторов SGLT2 на процессы обратного ремоделирования сердца было получено в исследовании SUGAR-DM-HF, в котором выявлено достоверное уменьшение объемов ЛЖ и снижение уровня натрийуретического пептида у пациентов с СНнФВ и СД 2-го типа или предиабетом при назначении эмпаглифлозина [14].
Таким образом, ингибиторы SGLT2 могут оказывать разностороннее действие на различные патогенетические механизмы развития и прогрессирования сердечной недостаточности, что позволило предположить их эффективность для профилактики сердечно-сосудистых осложнений, развития и ухудшения течения ХСН у пациентов и без СД [15].
Результаты многоцентрового рандомизированного исследования DAPA-HF, изучавшего влияние дапаглифлозина на течение сердечной недостаточности у пациентов с и сохраняющимися симптомами заболевания, несмотря на оптимальное лечение, продемонстрировали снижение относительного и абсолютного риска сердечно-сосудистой смерти или ухудшения течения сердечной недостаточности при приеме этого препарата по сравнению с группой плацебо независимо от наличия СД [16]. Это позволило экспертам рекомендовать назначение дапаглифлозина в данной клинической ситуации [3].
Гипотеза о том, что ингибиторы SGLT2 оказывают кардиопротективное действие независимо от причины поражения сердца и наличия или отсутствия СД 2-го типа, убедительно подтвердилась в исследовании EMPEROR-Reduced, результаты которого были представлены 29 августа 2020 г. на виртуальном конгрессе ESC. В исследование были рандомизированы 3730 пациентов с ХСН II–IV ФК по NYHA и ФВ ЛЖ ≤40%, получавших эмпаглифлозин (по 10 мг 1 раз/сут) или плацебо в дополнение к рекомендованной терапии [17]. Добавление эмпаглифлозина к базовой терапии СНнФВ позволило на 25% снизить относительный риск по первичной комбинированной конечной точке (сердечно-сосудистая смерть и госпитализации по поводу сердечной недостаточности). В частности, общая частота госпитализаций по поводу ХСН в группе эмпаглифлозина была значимо меньше, чем в группе плацебо (относительный риск (ОР) 0,70; 95% доверительный интервал (ДИ) 0,58–0,85; p <0,001), а количество первичных госпитализаций по поводу ХСН оказалось ниже на 31% [18]. Благоприятное влияние на исходы проявлялось рано, достигая статистической значимости уже через 12 дней после начала терапии, и сохранялось на протяжении всего дальнейшего периода наблюдения [19].
Дополнительный анализ результатов исследования позволил получить ответы на многие возникшие вопросы. Так, оказалось, что выявленные преимущества эмпаглифлозина наблюдались у всех пациентов независимо от наличия СД [20], предшествующей терапии ХСН, исходного статуса здоровья (оцениваемому по опроснику KCCQ-CSS) [21] и состояния функции почек на момент начала терапии, включая подгруппу пациентов со скоростью клубочковой фильтрации (СКФ) 20 мл/ мин/1,73 м2. Более того, эмпаглифлозин уменьшал частоту почечных событий (терминальной хронической болезни почек, стойкого снижения скорости клубочковой фильтрации), замедляя прогрессирование хронической болезни почек (ХБП) разной степени выраженности [22]. Следует отметить, что частота возникновения нежелательных явлений, включая гиперкалиемию, и острой почечной недостаточности была сходной для эмпаглифлозина и плацебо у пациентов с ХБП (53% больных в исследовании) и без таковой по всему спектру функции почек, включая подгруппу пациентов с СКФ 20 мл/мин/1,73 м2.
С безопасностью и переносимостью эмпаглифлозина ассоциирован вопрос возможности его комбинации с другими препаратами, назначаемыми для лечения ХСН. Отмечено отсутствие у него клинически значимых взаимодействий с АМКР и АРНИ. Так, больные, исходно принимавшие АМКР, после рандомизации на 22% реже прекращали лечение ими в группе эмпаглифлозина, чем в группе плацебо (ОР 0,78; 95% ДИ 0,64–0,96). Во многом это было связано с тем, что в группе эмпаглифлозина реже развивалась тяжелая гиперкалиемия [23]. Эффект препарата в виде снижения риска сердечно-сосудистой смерти и госпитализации по причине ухудшения сердечной недостаточности не зависел от сопутствующего приема сакубитрила/валсартана. Частота нежелательных явлений, таких как гипер- или гипокалиемия, артериальная гипотензия, была аналогичной у пациентов, получавших плацебо или эмпаглифлозин, и не зависела от фоновой терапии АРНИ. Таким образом, комбинация этих классов препаратов может приносить существенные дополнительные преимущества без увеличения частоты побочных эффектов [24].
Отдельный субанализ позволил оценить эффективность эмпаглифлозина в зависимости от наличия или отсутствия объемной перегрузки (задержки жидкости). Пациенты с признаками задержки жидкости в течение 12 мес, предшествующих рандомизации, с большей вероятностью были госпитализированы по поводу сердечной недостаточности и получали диуретик внутривенно в амбулаторных условиях, а также имели ухудшение заболевания после рандомизации даже в случае лечения высокими дозами петлевого диуретика в амбулаторных условиях (p <0,001). По сравнению с плацебо эмпаглифлозин снижал угрозу сердечно-сосудистой смерти или госпитализации по поводу сердечной недостаточности, снижал общее количество госпитализаций по поводу заболевания, улучшал состояние здоровья и ФК ХСН. Тем не менее, несмотря на предрасположенность пациентов с недавней перегрузкой объемом к задержке жидкости, данные преимущества (даже после 1 мес лечения) не превышали аналогичные показатели для пациентов без перегрузки (p >0,05). Изменения массы тела, гематокрита и уровня натрийуретического пептида (каждый из этих показателей потенциально свидетельствует о диуретическом действии ингибиторов SGLT2) не коррелировали между собой ни в зависимости от времени, ни у отдельных пациентов. В совокупности результаты этого субанализа не подтверждают доминирующую роль диуреза в опосредовании физиологических изменений или клинических преимуществ ингибиторов SGLT2 на течение СНнФВ [25].
Метаанализ исследований EMPEROR-Reduced и DAPA-HF показал, что результаты лечения ингибиторами SGLT2 не зависели от возраста, пола, наличия СД 2-го типа, приема АРНИ, расчетной СКФ и индекса массы тела, однако отличались у больных с разными ФК сердечной недостаточности и разной расовой принадлежностью. Несмотря на эти наблюдаемые различия между подгруппами, ни один из анализов не показал гетерогенности результатов лечения дапаглифлозином и эмпаглифлозином в рамках указанных категорий больных [26].
В опубликованном в 2021 г. обновленном Консенсусе по назначению и оптимизации терапии ХСН экспертов Американской коллегии кардиологов (ACC) были учтены результаты исследований EMPEROR-Reduced и DAPA-HF [27]. Согласно этому документу, ингибиторы SGLT2 дополняют терапию больных СНнФВ (ФВ ≤40%) II–IV ФК по NYHA с СД 2-го типа или без него, которые уже получают бета-блокаторы, ИАПФ/БРА/АРНИ и АМКР, при отсутствии противопоказаний (СД 1-го типа, известная непереносимость, период лактации и потребность в диализе).
С учетом имеющихся данных фармакотерапию СНнФВ целесообразно рассматривать в виде четырехкомпонентной схемы терапии, включающей группы препаратов, улучшающих прогноз за счет снижения риска сердечно-сосудистой смерти и госпитализаций по поводу сердечной недостаточности – АРНИ/ИАПФ/БРА, бета-блокаторы, АМКР и ингибиторы SGLT2. Однако традиционный подход основан на исторически обусловленной последовательности назначения перечисленных групп препаратов, которая не имеет убедительной доказательной базы. На практике для реализации этой схемы требуется срок до 6 мес, что зачастую приводит к безуспешности лечения вследствие недостаточно быстрого развития ожидаемого клинического эффекта, низкой приверженности больного и, как следствие, к повторным госпитализациям и летальным исходам.
В недавно опубликованной обзорной работе ведущих экспертов в области лечения ХСН была предложена стратегия ускоренной реализации базовой терапии СНнФВ, основанная на четырех принципах [28] (табл. 2). Предлагаемая стратегия ускоренной реализации базовой терапии СНнФВ – это обоснованная попытка оптимизировать реализацию известных лечебных подходов, снижающих смертность в данной когорте больных.

Следует отметить отчетливую тенденцию к более высокой приверженности врачей специализированных кардиологических стационаров и в меньшей степени терапевтов и кардиологов первичного звена к назначению ингибиторов SGLT2 в последние пару лет. Однако решение о назначении представителей этого класса лекарственных средств больным СНнФВ, страдающим СД, требует учета характера принимаемой гипогликемической терапии, степени контролируемости уровня глюкозы крови и других диабет-ассоциированных факторов, что означает необходимость его обсуждения с эндокринологом.
ЗАКЛЮЧЕНИЕ
В настоящее время в европейских и российских клинических рекомендациях больным СД 2-го типа и СНнФВ с сохраняющимися симптомами, несмотря на терапию ИАПФ/БРА/АРНИ, бета-адреноблокаторами и АМКР, предлагается дополнительное назначение препаратов класса ингибиторов SGLT2 – эмпаглифлозина, дапаглифлозина и канаглифлозина. Целью этого является снижение риска сердечно-сосудистой смерти и госпитализаций по поводу ухудшения ХСН. Результаты исследования EMPEROR-Reduced служат основанием для добавления в рекомендации и стандарты по лечению ХСН эмпаглифлозина после получения регистрационного удостоверения по новому показанию.



