Пандемия COVID-19 стала тяжелым экономическим и социальным бременем для всего мира. Клинический спектр инфекции SARS-CoV-2 может варьировать от бессимптомного течения до поражения респираторного тракта, развития полиорганной недостаточности и летального исхода [1]. В настоящее время эпидемиологические и клинические проявления, патогенез и осложнения у пациентов с COVID-19 во время острой фазы четко описаны, однако долгосрочные последствия заболевания остаются в значительной степени неясными [2].
Пост-COVID-19-синдром был впервые описан весной 2020 г., когда у пациентов через несколько недель после перенесенной острой инфекции сохранялись различные ее симптомы [3]. Пост-COVID-19-синдром, по-видимому, является мультисистемным заболеванием, возникающим даже после относительно легкого острого течения заболевания [3, 4]. Частота пост-COVID-19-последствий оценивается от 35% и выше [5, 6]. У тех, кто не был госпитализирован, симптомы могут сохраняться более четырех недель, а у госпитализированных пациентов в течение восьми или более недель после выписки [6]. У больных с COVID- 19 может развиться постинфекционная астения, которая проявляется длительным рецидивом истощения, когнитивной дисфункцией, депрессией и другими симптомами после минимальной физической и умственной активности, нарушением сна [7]. Астения – наиболее распространенный синдром, частота которого у госпитализированных пациентов с COVID-19 колеблется от 17,5% до значительно более высоких показателей (72%) [8–15]. О его наличии пациенты сообщали в течение семи месяцев после начала COVID- 19, что приводило к значительной инвалидности, при этом ряд больных продолжает испытывать астению и после семи месяцев наблюдения [16].
В связи с вышесказанным крайне важным представляется не только ранняя диагностика постинфекционной астении, но и ее медикаментозная коррекция.
Цель исследования – изучить эффективность и безопасность оксиэтиламмония метилфеноксиацетата (Трекрезана) у пациентов c постинфекционной астенией, перенесших COVID-19 на амбулаторном этапе.
МАТЕРИАЛ И МЕТОДЫ
В исследование были включены 80 человек. Критериями включения в исследование были возраст старше 18 лет, перенесенный в течение одного месяца СOVID-19, не требовавший госпитализации в стационар. Критериями исключения служили дыхательная и сердечная недостаточность, значимые сердечно-сосудистые заболевания (миокардит, тромбоэмболия легочной артерии, ишемическая болезнь сердца), аритмии, выраженные поведенческие и эмоциональные расстройства, применение психоактивных веществ, антидепрессантов.
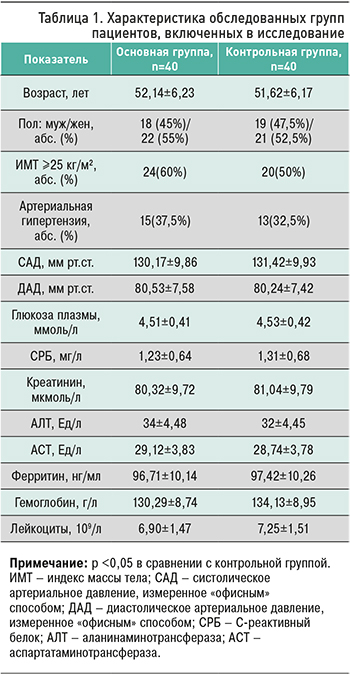
Пациенты, включенные в исследование, были рандомизированы на две группы – основную (n=40, средний возраст 52,14±6,23 лет) и контрольную (n=40, средний возраст 51,62±6,17 лет). Группы были сопоставимы по полу, возрасту, длительности течения и тяжести проявлений COVID-19.
Пациенты основной группы получали оксиэтиламмония метилфеноксиацетат (Трекрезан) по следующей схеме: в первый день – 3 таблетки (600 мг), в следующие 7 дней – по 1 таблетке (200 мг) в день. Длительность терапии составила 8 дней (суммарная доза препарата – 2000 мг). Пациенты контрольной группы терапию оксиэтиламмонием метилфеноксиацетатом (Трекрезаном) не получали.
Отметим, что препарат Трекрезан обладает высокой биодоступностью, быстро метаболизируется в печени, выделяясь почками преимущественно в виде глюкуронидов, и не кумулирует в организме при длительном применении [17].
Все пациенты проходили клиническое обследование с оценкой антропометрических показателей. При включении в исследование также проводились клинический анализ крови, биохимический анализ крови с определением уровня креатинина, глюкозы, аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), С-реактивного белка (СРБ), ферритина.
Исходно и после исследования в основной и контрольной группах выполнялось тестирование с помощью шкалы астенического состояния. Данная шкала Л.Д. Малковой была адаптирована Т.Г. Чертовой на основе Миннесотского многоаспектного личностного опросника (ММРI – Minnesota Multiphasic Personality Inventory) [18]. Методика предназначена для экспресс-диагностики астенического состояния. Шкала состоит из 30 пунктов, отражающих характеристики астенического состояния. Каждый выбранный ответ имеет балльную характеристику. Если пациент набирает от 30 до 50 баллов, это соответствует «отсутствию астении», от 51 до 75 – «слабой астении», от 76 до 100 – «умеренной астении», от 101 до 120 – «выраженной астении».
Уровень тревоги и депрессии измерялся с использованием госпитальной шкалы тревоги и депрессии (HADS – The Hospital Anxiety and Depression Scale). Также выполнялась балльная оценка субъективных характеристик сна [19].
Результаты обследования обрабатывались с помощью компьютерной программы Statistica 6.0. Для сравнения выборок, удовлетворяющих критериям нормального распределения, применялся t-критерий Стьюдента для независимых или зависимых выборок и дисперсионный анализ (ANOVA). Показатели представлены в виде среднего арифметического и стандартного отклонения (M±SD). При систематизации и статистической обработке данных различия считались достоверными при уровне значимости p <0,05.
РЕЗУЛЬТАТЫ
Пациенты основной и контрольной групп достоверно не различались по полу, возрасту, уровню артериального давления (табл. 1). Из сопутствующих заболеваний частыми были артериальная гипертензия и ожирение. Также не наблюдалось достоверных различий в обеих группах по уровням креатинина, СРБ, ферритина.
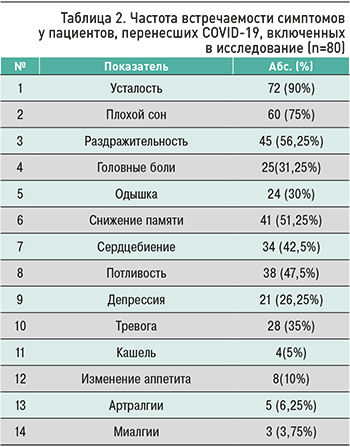
Большинство пациентов, перенесших COVID- 19, предъявляли в среднем 7,04±1,06 жалоб. Чаще всего отмечались такие симптомы, как усталость 72 (90 %), плохой сон 60 (75%), раздражительность 45 (56,25%). Почти у 1/3 пациентов имело место наличие тревоги и депрессии (табл. 2).
Согласно результатам тестирования по Шкале астенического состояния, в основной и контрольной группах пациентов, перенесших COVID-19, преобладали пациенты с умеренной астенией – 57 (71,25%). У 15 человек (18,75%), включенных в исследование, наблюдались проявления выраженной астении, и у 8 (10%) – легкой (табл. 3).
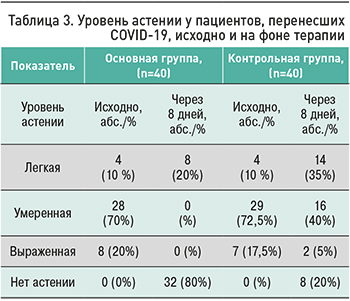
В основной группе пациентов на фоне терапии препаратом Трекрезан наблюдалась отчетливая положительная динамика: уменьшение количества пациентов с выраженной астенией с 8 (20%) до 0 (0%), с умеренной астенией – с 28 (70%) до 0 (0%). При этом в контрольной группе таких результатов не отмечалось: через 8 дней наблюдения у 2 (5%) пациентов из 40 оставались признаки выраженной астении, у 16 (40%) из 40 – проявления умеренной астении.
Через 8 дней после начала терапии Трекрезаном в основной группе пациентов было зарегистрировано уменьшение уровня тревоги (9,48±0,46 и 7,29±0,28 баллов, р <0,05; 9,42±0,43 и 8,91±0,36 баллов соответственно, р >0,05), улучшение параметров сна (19,42±0,64 и 21,39±0,75 баллов, р <0,05; 19,15±0,58 и 19,53±0,67 баллов соответственно, р >0,05) по сравнению с контрольной группой. Уровень депрессии в группах исследования достоверно не изменился (6,64±0,23 и 5,72±0,21 баллов р >0,05; 6,72±0,27 и 6,58±0,22 баллов соответственно, р >0,05).
Все пациенты закончили исследование. Препарат Трекрезан хорошо переносился, побочных эффектов отмечено не было.
ОБСУЖДЕНИЕ
Несмотря на то что большинство пациентов выздоравливает после COVID-19, некоторые долгосрочные эффекты заболевания могут иметь значительные клинические последствия в краткосрочной и среднесрочной перспективе наблюдения [4, 6]. Ряд авторов сообщает о наличии астении у 40% больных через 2 мес после перенесенного COVID-19 [14, 20, 21]. Однако нам не встретилось ни одного исследования, в котором бы констатировалось наличие постинфекционной астении после перенесенного COVID-19 и была оценена выраженность этого синдрома. В нашем исследовании среди пациентов, перенесших COVID-19, подавляющее большинство страдало умеренной астенией (71,25%). Еще у 15 (18,75%) больных были проявления выраженной астении.
Таким образом, 90% пациентов имели значимые проявления постинфекционной астении. Надо отметить, что это не были лица пожилого возраста, так как средний возраст выборки составил порядка 50 лет. Также среди включенных в исследование больных не было тех, кто был бы госпитализирован в связи с тяжелым течением COVID-19. И несмотря на это, доля пациентов с умеренной астений была высока.
Полученные нами результаты совпадают с данными ряда авторов, которые продемонстрировали, что даже самому легкому течению COVID-19 сопутствуют среднесрочные симптомы, требующие последующего наблюдения. Иными словами, пандемия COVID-19 сопряжена с бременем по уходу за больными еще в течение долгого времени после окончания заболевания [14]. Некоторые исследователи отмечают, что развитие постинфекционной астении может быть ассоциировано с более высоким индексом массы тела, артериальной гипертензией, женским полом [9, 22–25]. В нашем исследовании мы не получили подобных данных, возможно, из-за небольшого количества участников.
Выбор нами лекарственного средства для лечения пациентов с постинфекционной астенией, перенесших COVID-19, был не случаен. Трекрезан является высокоэффективным фармакологическим препаратом с адаптогенным и иммуностимулирующим действиями, которые были доказаны в многочисленных исследованиях. Известно, что Трекрезан стимулирует клеточный иммунитет за счет угнетения колониеобразующей активности полипотентных стволовых кроветворных клеток, повышает количество ядросодержащих клеток, стимулирует пролиферацию мононуклеарных клеток, действуя на разных этапах образования лимфоцитов, активирует гуморальный иммунитет [26–29]. Кроме того, препарат активно стимулирует интерфероногенез [30], а также обладает противовоспалительным эффектом [31, 32].
При постинфекционной астении происходит нарушение использования энергоресурсов, развитие гипоксии, ацидоза, а вследствие этого дестабилизация процесса образования и использования энергии на уровне клеток. В результате накопления продуктов окисления снижается способность тканей усваивать кислород. Дисбаланс окислительно‑восстановительных процессов в митохондриях вызывает образование свободных радикалов, которые способствуют нарушению микроциркуляции, эндотелиальной дисфункции и ведут к прогрессированию апоптоза [33]. В ряде работ показано, что Трекрезан создает условия для улучшения энергетического статуса организма за счет оптимизации процессов энергообразования и снижения энергозатрат, обладает антиастеническим действием [34, 35].
В нашем исследовании получены данные, свидетельствующие о высокой эффективности и безопасности терапии Трекрезаном в течение 8 дней (суммарная доза препарата 2000 мг) у пациентов, перенесших COVID-19. У 80% пациентов основной группы отсутствовали проявления постинфекционной астении после проведенного курса терапии.
Наряду с прочим Трекрезан обладает адаптогенным эффектом. В выполненных ранее исследованиях получены результаты, указывающие на способность этого препарата оказывать стресс-протективное действие на моделях иммобилизационного и болевого гиподинамического стресса, защищать внутренние органы от повреждающего действия токсинов и инфекционного влияния [36]. Возможно, именно с адаптогенным действием Трекрезана связано улучшение эмоционального фона и качества сна у пациентов, включенных в наше исследование.
ЗАКЛЮЧЕНИЕ
1. У пациентов, перенесших COVID-19 на амбулаторном этапе, преобладает умеренная астения.
2. На фоне терапии препаратом Трекрезан у 80% пациентов, перенесших COVID-19, отсутствовали проявления астении, тогда как в контрольной группе у половины больных сохранялась умеренная астения.
3. В ходе исследования на фоне терапии Трекрезаном отмечалось улучшение эмоционального фона и качества сна по сравнению с контрольной группой.
4. В проведенном исследовании Трекрезан хорошо переносился, побочных эффектов, связанных с его приемом, зарегистрировано не было. Препарат может быть рекомендован для лечения постинфекционной астении у пациентов, перенесших COVID-19.
5. Необходимо продолжить изучение последствий COVID-19 и прогноза выздоровевших пациентов с целью разработки рекомендаций по их ведению.



