




Комментарии
1
• К относительно здоровым лицам относятся все, не имеющие подтвержденного атеросклеротического сердечно-сосудистого заболевания (АССЗ), сахарного диабета 2-го типа или тяжелой сопутствующей патологии [1].
• Общая градация групп пациентов в зависимости от риска развития АССЗ отражена в таблице 1.


2
• У относительно здоровых лиц <70 лет без установленного АССЗ, сахарного диабета (СД), хронической болезни почек (ХБП), генетических/редких нарушений липидного обмена или артериальной гипертензии (АГ) показана оценка 10-летнего риска фатальных или нефатальных ССЗ по шкале SCORE2: класс рекомендаций/уровень доказательности в соответствии с рекомендациями Европейского общества кардиологов (ЕОК) – I/B [1].
• Систематическая или случайная оценка сердечно-сосудистого риска в общей популяции может быть рассмотрена у мужчин >40 лет и женщин >50 лет или в постменопаузе без известных факторов риска АССЗ: IIb/C [1].
• В России в целях оценки 10-летнего риска первого фатального атеросклеротического события используются шкалы SCORE 2-ОР для популяции очень высокого риска (рис.) [1].
3
• У относительно здоровых лиц ≥70 лет без установленного АССЗ, СД, ХБП, генетических/редких нарушений липидного обмена или АГ показана оценка 10-летнего риска фатальных или нефатальных ССЗ по шкале SCORE2-OP: I/B [1].
4
У относительно здоровых лиц после оценки 10-летнего риска фатальных и нефатальных ССЗ должны учитываться пожизненный риск и польза от лечения, модификаторы риска, старческая астения, полипрагмазия и предпочтения пациента: IIa/С [1].
5
• Лечение факторов риска АССЗ рекомендовано всем условно здоровым лицам без СД, ХБП, генетических/редких нарушений липидного обмена или гипертонической болезни при наличии очень высокого риска ССЗ (SCORE2 ≥7,5% для лиц до 50 лет; SCORE2 ≥10% для лиц 50–69 лет; SCORE2-OP ≥15% для лиц ≥70 лет): I/C [1].
• Следует рассмотреть лечение факторов АССЗ у относительно здоровых лиц без СД, ХБП, СД, генетических/редких нарушений липидного обмена или гипертонической болезни при наличии высокого риска ССЗ (SCORE2 от 2,5 до <7,5% для лиц до 50 лет; SCORE2 от 5 до <10% для лиц 50–69 лет; SCORE2-OP от 7,5 до <15% для лиц ≥70 лет) с учетом модификаторов ССР, пожизненного риска пользы и преимуществ лечения и предпочтений пациента: IIa/C [1].
• Поэтапная интенсификация терапии, направленная на интенсивное лечение факторов риска, рекомендуется для относительно здоровых лиц с высоким или очень высоким сердечно-сосудистым риском с учетом преимуществ лечения факторов риска, модификаторов риска, сопутствующих заболеваний и предпочтений пациента: I/B [1].
6
Подробнее о коррекции/контроле повышенного артериального давления (артериальной гипертензии) и липидного профиля крови как ведущих факторов кардиоваскулярного риска – см. схемы на стр. 56, 57 и комментарии к ним, а также тему сборника «Нарушения липидного обмена» (стр. 88–110).

7
• Пациенты с установленным АССЗ и/или СД и/или умеренным или тяжелым заболеванием почек и/или генетическим/редким нарушением липидного обмена или редкими формами гипертонической болезни относятся к категории высокого или очень высокого сердечно-сосудистого риска: I/A [1].
• Систематическая глобальная оценка сердечно-сосудистого риска рекомендуется лицам с любым большим кардиоваскулярным фактором риска, например с семейным анамнезом ранних ССЗ, семейной гиперхолестеринемией, а также с такими факторами риска ССЗ, как курение, артериальная гипертензия (АГ), сахарный диабет, повышение уровня липидов, ожирение или сопутствующая патология, повышающая кардиоваскулярный риск: ESC – I/C [1].
• Для пациентов ≥70 лет высокий 10-летний риск может быть связан с более низкой абсолютной пожизненной пользой от лечения из-за ограниченной продолжительности жизни.
8
Для пациентов с недавно перенесенным ОКС достижение целей на первом шаге сердечно-сосудистой профилактики являются частью участия в кардиореабилитации [1].
9
Поэтапная интенсификация терапии, направленная на интенсивное лечение факторов риска, рекомендуется для пациентов с установленным АССЗ и/или СД, с учетом сердечно-сосудистого риска преимуществ лечения ФР, модификаторов риска, сопутствующих заболеваний и предпочтений пациента: I/B [1].
10
• Пожизненный риск – это оценка возраста, в котором существует 50% вероятность того, что человек либо перенесет сердечно-сосудистое событие, либо умрет. Пожизненный сердечно-сосудистый риск может быть приблизительно определен клиническим опытом с критериями, такими как возраст, изменение уровней факторов риска, модификаторами риска и т.д., или оценен у практически здоровых людей, пациентов с установленным АССЗ и лиц с СД 2-го типа с помощью специальных шкал кардиоваскулярного риска [1].
• Профилактика ССЗ путем лечения факторов риска обычно проводится на протяжении всей жизни. Среднее преимущество такой профилактики в течение жизни легко интерпретировать. Его применение может облегчить обсуждение потенциальных преимуществ терапии c пациентами в рамках процесса совместного принятия решений. Это, в свою очередь, может увеличить вовлеченность пациентов, их самоэффективность, мотивацию к изменению образа жизни и приверженность к лечению [1].
• Пожизненная польза профилактики – это числовая разница между прогнозируемым возрастом, в котором существует 50% вероятность того, что человек либо перенесет сердечно-сосудистое событие, либо умрет с предложенным лечением и без него.
В настоящее время не существует официальных пороговых значений средней пользы на протяжении всей жизни. Кроме того, предполагаемую индивидуальную пожизненную пользу следует рассматривать в свете предполагаемой продолжительности лечения. В целом пожизненная польза коррекции факторов риска может рассчитываться путем комбинирования моделей пожизненного риска с относительным риском, полученными из рандомизированных контролируемых исследований (РКИ), метаанализов РКИ или исследований c менделевской рандомизацией, которые оценивают эффекты более длительного лечения факторов риска. Онлайн-калькуляторы (например, приложение ESC CVD Risk) можно использовать для средней оценки пользы отказа от курения, снижения липидов и АД на индивидуальный уровень риска пациента, выраженный в дополнительных годах жизни без ССЗ [1].
• Продолжительность пожизненного лечения, как правило, больше у молодых лиц по сравнению с пожилыми [1].
11
• Артериальная гипертензия (АГ) является ведущим фактором риска, во многом определяющим развитие множества заболеваний по всему миру. Повышенное АД – фактор риска ишемической болезни (ИБС), сердечной недостаточности, цереброваскулярных заболеваний, заболеваний периферических артерий, ХБП и фибрилляции предсердий (ФП). САД – обязательный компонент шкалы SCORE 2-ОР [1].
• Наибольшую доказательную базу для диагностики АГ и оценки эффективности антигипертензивной терапии (АГТ) имеет клиническое измерение АД [1, 3]. Градация результатов клинического (офисного) измерения АД приведена в таблице 2.
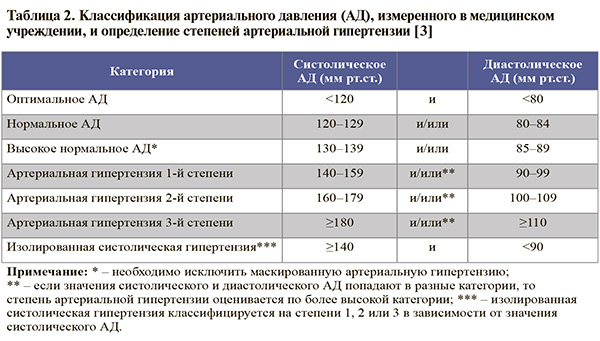
• Дополнительным состоянием, усугубляющим сердечно-сосудистый риск, является сахарный диабет (глюкоза плазмы натощак ≥7,0 ммоль/л при двух последовательных измерениях, и/или HbA1c ≥6,5%, и/или глюкоза плазмы после нагрузки или при случайном определении ≥11,1 ммоль/л) [3].
• Стадийная классификация гипертонической болезни, в зависимости от наличия факторов риска, поражения органов-мишеней, ассоциированных клинических состояний, хронической болезни почек (ХБП) и сахарного диабета, приведена в таблице 2.
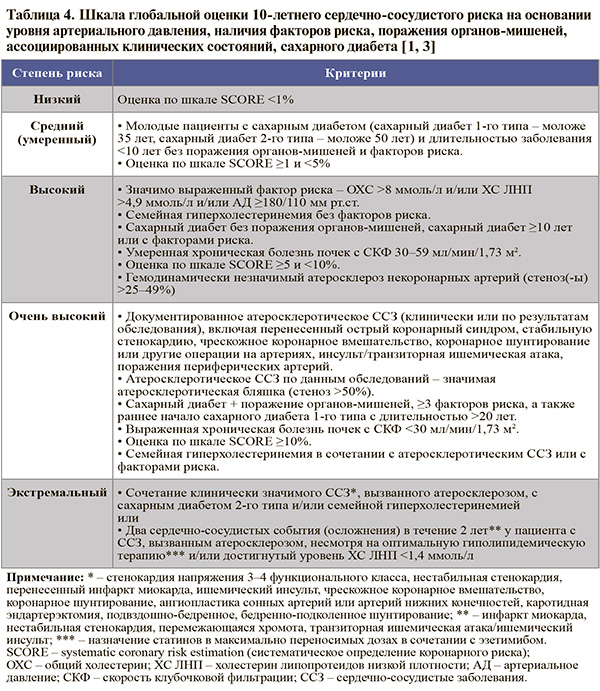
Стадия АГ не зависит от уровня АД [1]. В свою очередь, 5 категорий риска сердечнососудистых осложнений на основании уровня АД, наличия факторов риска, поражения органов-мишеней, ассоциированных клинических состояний, сахарного диабета приведены в таблице 4. Наиболее значимо определение категории кардиоваскулярного риска у пациентов с гипертонической болезнью I и II стадий [3].

• Нижняя граница безопасности целевых уровней АД при АГ установлена на основании результатов исследований, проведенных преимущественно в группах пациентов высокого и очень высокого риска (пожилые с коморбидностью, установленными сердечно-сосудистыми заболеваниями, в том числе лица с ИБС, заболеванием периферических артерий). Таким образом, в общей популяции пациентов с артериальной гипертензией (АГ), вероятно, нет необходимости в коррекции лечения при уровне САД <120 мм рт.ст. и диастолического ДАД <70 мм рт.ст. в случае его хорошей переносимости [3].
• Пациентам ≥65 лет, получающим антигипертензивную терапию (АГТ), при каждом визите к врачу рекомендуется проводить оценку возможных нежелательных явлений [3].
• Всем пациентам с АГ, получающим лечение, независимо от возраста и степени риска, рекомендуется в качестве первого целевого уровня снижать АД до значений <140/90 мм рт.ст., а при условии хорошей переносимости – до целевого уровня 130/80 мм рт.ст. или ниже в связи с доказанными преимуществами в плане снижения риска сердечно-сосудистых осложнений: уровни достоверности доказательств согласно рекомендациям Европейского общества кардиологов / Европейского общества артериальной гипертонии (ЕОК/ЕОАГ) – IA (уровень убедительности рекомендаций согласно действующим российским клиническим рекомендациям (УУР) – A, уровень достоверности доказательств согласно действующим российским клиническим рекомендациям (УДД) – 1) [3].
• Пациентам моложе 65 лет и без ХБП, получающих АГТ, рекомендуется снижать САД до значений 120–130 мм рт.ст. в связи с доказанным влиянием вмешательства на кардиоваскулярный риск: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Всем пациентам с АГ вне зависимости от возраста, уровня риска и наличия сопутствующих заболеваний рекомендуется снижать ДАД до целевых значений 70–79 мм рт.ст.: ЕОК/ЕОАГ – IIaB (УУР – B, УДД – 2) [3].
• Пациентам 65 лет и старше без старческой астении, получающим АГТ, вне зависимости от уровня сердечно-сосудистого риска и наличия ССЗ рекомендуется снижать САД до целевых значений 130–139 мм рт.ст., при условии хорошей переносимости: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Принципы и периодичность контроля АД при разных его уровнях в рамках сердечно-сосудистой профилактики отражены в таблице 5.

12
• Всем пациентам с АГ 1-й степени рекомендуется проводить мероприятия по изменению (оздоровлению) образа жизни с целью нормализации АД и коррекции факторов риска: ЕОК/ЕОАГ – IIaB (УУР – A, УДД – 1) [3]. Немедикаментозные методы лечения АГ способствуют снижению АД, уменьшают потребность в антигипертензивных препаратах и повышают их эффективность, позволяют осуществлять коррекцию факторов риска [3].
• Меры по изменению образа жизни рекомендованы не только всем пациентам с АГ, но и людям с высоким нормальным АД (130–139/85–89 мм рт.ст.) и/или факторов риска для первичной профилактики АГ [3].
• Всем пациентам с АГ для улучшения контроля заболевания рекомендуется ограничение употребления соли до <5 г/сут: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Всем пациентам с АГ для улучшения контроля заболевания рекомендуется ограничить употребления алкоголя (<14 единиц в неделю для мужчин и <8 единиц в неделю для женщин, где 1 единица соответствует 125 мл вина или 250 мл пива) и избегать хронического злоупотребления спиртным: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Всем пациентам с АГ для улучшения метаболических показателей рекомендуется увеличить употребление овощей, свежих фруктов, рыбы, орехов и ненасыщенных жирных кислот (оливковое масло), молочных продуктов низкой жирности, уменьшить употребление мяса: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Всем пациентам с АГ с целью снижения АД и сердечно-сосудистого риска рекомендуется контроль массы тела для предупреждения развития ожирения, достижение/поддержание индекса массы тела (ИМТ) в пределах 20–25 кг/м2, окружности талии <94 см у мужчин и <80 см у женщин: ЕОК/ЕОАГ – IA (УУР – A, УДД – 1) [3].
• Всем пациентам с АГ в связи с доказанным положительным эффектом на уровень сердечно-сосудистой смертности рекомендуются регулярные аэробные физические упражнения (≥30 мин динамических упражнений умеренной интенсивности 5–7 дней в неделю): ЕОК/ЕОАГ – IA (УУР – A, УДД – 2) [3].
• Всем пациентам с АГ в связи с доказанным негативным эффектом курения на уровень смертности рекомендуются прекращение курения, психологическая поддержка и выполнение программ по отказу от этой вредной привычки: ЕОК/ЕОАГ – IB (УУР – A, УДД – 2) [3].
13
Вопрос о начале медикаментозной АГТ решается на основании уровня АД и суммарного сердечно-сосудистого риска. Возможность применения фармакотерапии может быть рассмотрена и при высоком нормальном АД у пациентов высокого риска с ССЗ, особенно с ИБС [3].
14
• Пациентам с АГ 2-й или 3-й степени при любом уровне кардиоваскулярного риска рекомендуется незамедлительное начало медикаментозной АГТ для снижения риска развития сердечно-сосудистых осложнений, сердечно-сосудистой смерти одновременно с рекомендациями по изменению образа жизни: ЕОК/ЕОАГ – IА (УУР – A, УДД – 1) [3].
• Пациентам с АГ 1-й степени, относящимся к категории кардиоваскулярного высокого риска (по шкале SCORE), или при наличии поражения органов-мишеней (ПОМ) рекомендуется незамедлительное начало медикаментозной АГТ одновременно с рекомендациями по изменению образа жизни: ЕОК/ЕОАГ – IА (УУР – A, УДД – 1) [3].
15
• Пациентам с АГ 1-й степени, относящимся к категориям низкого/умеренного риска без признаков ПОМ (по шкале SCORE) рекомендуется начинать медикаментозную АГТ в том случае, если у них сохраняется повышенное АД несмотря на мероприятия по изменению образа жизни в течение 3 мес: ЕОК/ЕОАГ – IА (УУР – A, УДД – 1) [3].
• Пожилым пациентам с АГ (даже в возрасте >80 лет), находящимся в удовлетворительном физическом состоянии, рекомендуется изменение образа жизни и АГТ при уровне САД ≥160 мм рт.ст. Пожилым пациентам (>65 лет, но не >80 лет), находящимся в удовлетворительном физическом состоянии (без синдрома старческой астении), если их САД соответствует показателям АГ 1-й степени (140–159 мм рт.ст.), рекомендуются изменение образа жизни и АГТ при хорошей переносимости: ЕОК/ЕОАГ – IА (УУР – A, УДД – 1) [3].
• Рекомендуется рассмотреть возможность назначения АГТ пожилым пациентам с синдромом старческой астении при удовлетворительной переносимости: ЕОК/ЕОАГ – IIbB (УУР – A, УДД – 1) [3].
• У пациентов старше 80 лет не рекомендуется отменять медикаментозную АГТ при условии, что эта терапия хорошо переносится, не сопровождается ортостатической гипотонией, развитием/усугублением гериатрических синдромов и снижением функционального статуса в связи с доказанными преимуществами в отношении сердечнососудистой смертности: ЕОК/ЕОАГ – IIIА (УУР – A, УДД – 1) [3].
• Пациентам с высоким нормальным АД (130–139/85–89 мм рт.ст.) рекомендуется начало АГТ при очень высоком уровне сердечно-сосудистого риска вследствие наличия ССЗ (особенно ИБС): ЕОК/ЕОАГ – IIbA (УУР – A, УДД – 1) [3].
16
Большинству пациентов с АГ в качестве стартовой терапии рекомендована комбинация антигипертензивных препаратов, предпочтительно фиксированная, для улучшения приверженности к терапии. Исключение составляют пациенты низкого риска с АД <150/90 мм рт.ст., пациенты ≥80 лет, пациенты с синдромом старческой астении. Предпочтительные комбинации должны включать ингибитор АПФ или блокатор рецепторов ангиотензина II (БРА) и дигидропиридиновый антагонист кальция или диуретик: ЕОК/ЕОАГ – IА (УУР – A, УДД – 1) [3].
17
• К ингибиторам АПФ, зарегистрированным в России, относятся зофеноприл, каптоприл, лизиноприл, периндоприл, рамиприл, спираприл, трандолаприл, фозиноприл, хинаприл, цилазаприл, эналаприл. Блокаторы рецепторов ангиотензина II (БРА, сартаны), представленные в России, – азилсартана медоксомил, валсартан, ирбесартан, кандесартан, лозартан, олмесартана медоксомил, телмисартан, эпросартан [7].
• Ингибиторы АПФ и БРА эффективно предотвращают или приводят к обратному развитию ПОМ (гипертрофии левого желудочка, ремоделирования мелких артерий) на фоне соответствующего снижения АД. Обе группы препаратов снижают риск пароксизмов фибрилляции предсердий (ФП), что может быть обусловлено улучшением функции левого желудочка (ЛЖ) и более эффективным регрессом его структурных изменений [3].
• Ингибиторы АПФ и БРА обладают сходной эффективностью в отношении сердечнососудистых осложнений и смертности по сравнению как друг с другом, так и с другими классами антигипертензивных препаратов [3]. БРА по сравнению с другими классами характеризуются более низкой частотой отмены из-за побочных эффектов, сопоставимой с плацебо [3].
• Ингибиторы АПФ и БРА снижают альбуминурию в большей степени, чем другие антигипертензивные препараты, и эффективно замедляют прогрессирование диабетической и недиабетической ХБП [3]. По данным метаанализов, ингибиторы АПФ и БРА – единственные из всех антигипертензивных препаратов, доказанно снижающие риск терминальной ХБП [3].
• Прием ингибиторов АПФ ассоциирован с умеренным повышением риска ангионевротического отека, особенно у представителей негроидной расы. У таких пациентов следует отдавать предпочтение БРА [3].
• Ингибиторы АПФ и БРА абсолютно противопоказаны при высокой гиперкалиемии (≥5,5 ммоль/л), двухстороннем стенозе почечных артерий, стенозе почечной артерии единственной почки, беременным и кормящим женщинам, а также пациентам с ангионевротическим отеком в анамнезе [3].
• Длительно действующие антагонисты кальция (АК), зарегистрированные в России для лечения АГ [7]:
– дигидропиридиновые – амлодипин, лацидипин, левамлодипин, лерканидипин, нитрендипин, нифедипин (пролонгированные формы), фелодипин;
– недигидропиридиновые – прологированные формы верапамила и дилтиазема
• Все АК метаболически нейтральны и не оказывают отрицательного действия на углеводный, липидный и пуриновый обмен. Помимо антигипертензивного, они оказывают антиангинальное и органопротективное действие, тормозят агрегацию тромбоцитов. В целом их влияние на сердечно-сосудистый риск схоже с другими классами антигипертензивных препаратов [3].
• АК обладают бóльшим эффектом в отношении профилактики инсультов, чем этого можно было ожидать только от антигипертензивного эффекта, однако менее эффективны в плане профилактики хронической сердечной недостаточности (ХСН) с низкой фракцией выброса (ФВ) [3].
• Не рекомендуется (абсолютное противопоказание) назначение недигидропиридиновых АК при атриовентрикулярной блокаде 2–3-й степени, ХСН с низкой ФВ ЛЖ. Для дигидропиридиновых АК абсолютных противопоказаний нет [3].
• К тиазидным диуретикам, зарегистрированным в России, относится гидрохлоротиазид, к тиазидоподобным – индапамид и хлорталидон [7]. Они обладают выраженным антигипертензивным эффектом и остаются краеугольным камнем АГТ. Их эффективность в предотвращении всех вариантов сердечно-сосудистых осложнений и смертности подтверждена в рандомизированных контролируемых исследованиях (РКИ) и метаанализах [1, 8].
• В масштабном метаанализе 2019 г. (4,9 млн пациентов с АГ) большинство оценок не выявило различий в эффективности между ингибиторами АПФ, БРА, АК и тиазидными/тиазидоподобными диуретиками. Вместе с тем тиазидные/тиазидоподобные диуретики при первичном лечении АГ в большей степени, чем ингибиторы АПФ, первичную снижали риск развития острого инфаркта миокарда (отношение рисков (ОР) 0,84; 95% доверительный интервал (ДИ): 0,75–0,95), инсультов (ОР 0,83; 95% ДИ: 0,74–0,95), госпитализаций по поводу сердечной недостаточности (ОР 0,83; 95% ДИ: 0,74–0,95) [9].
• В исследовании NESTOR (n=570) было установлено благоприятное влияние индапамида на углеводный обмен: этот тиазидоподобный диуретик продемонстрировал равную эффективность с ингибитором АПФ эналаприлом в терапии коморбидных больных с АГ, сахарным диабетом (СД) 2-го типа и микроальбуминурией [10].
• Для тиазидных/тиазидоподобных диуретиков характерно снижение антигипертензивной эффективности при СКФ <45 мл/мин/1,73 м2, а при СКФ <30 мл/мин/1,73 м2 они становятся неэффективными. В этом случае в качестве альтернативы можно использовать петлевые диуретики (торасемид, фуросемид) [3].
• В исследовании PATS (5665 пациентов) прием индапамида в дозе 2,5 мг у больных АГ с острым нарушением мозгового кровообращения в анамнезе в сравнении с плацебо на 29% снижал частоту инсульта (ОР 0,71; 95% ДИ: 0,58–0,88) и на 23% – общего количества сердечно-сосудистых событий (ОР 0,77; 95% ДИ: 0,63–0,93) [11].
• У пациентов пожилого возраста с изолированной систолической АГ в отсутствие особых показаний для назначения других классов препаратов предпочтение отдается АК и тиазидоподобным диуретикам. Начинать терапию рекомендуется с половины традиционной стартовой дозы и медленно титровать дозировку препарата, не торопясь переходить на комбинированную терапию. С этой целью удобно использовать лекарственные препараты с возможностью титрования доз. Например, лекарственная форма индапамида в виде делимой таблетки позволяет использовать четыре разные дозы этого лекарственного средства (0,625, 1,25, 1,875 и 2,5 мг/сут) и тем самым тщательно подбирать дозировку с оптимальным соотношением переносимость/эффективность, а также управлять уменьшением интенсивности АГТ при необходимости [12].
• У пациентов, не достигших целевого АД при использовании монотерапии или комбинированной АГТ, не включавшей диуретики, рекомендуется назначение низких доз тиазидных/тиазидоподобных диуретиков в составе комбинированной терапии с БРА, ингибиторами АПФ и АК для усиления антигипертензивного эффекта и достижения целевого АД [3].
• В исследовании HYVET (3845 пациентов) [10] применение индапамида у пожилых пациентов с АГ в течение 2 лет в дозе 1,5 мг (при необходимости в комбинации с периндоприлом для достижения целевого АД <150/80 мм рт.ст.) снижало вероятность инсульта (ОР 0,70; 95% ДИ: 0,49–1,01; p=0,06), сердечно-сосудистых событий (ОР 0,66; 95% ДИ: 0,53–0,82; p <0,001), сердечной недостаточности (ОР 0,36; 95% ДИ: 0,22–0,58; p <0,001), сердечно-сосудистой смертности (ОР 0,77; 95% ДИ: 0,60–1,01; p=0,06), смертности от инсульта (ОР 0,61; 95% ДИ: 0,38–0,99; p <0,05) и смертности от всех причин (ОР 0,79; 95% ДИ: 0,65–0,95; p=0,02) по сравнению с плацебо [13].
• Абсолютными противопоказаниями для гидрохлортиазида и хлорталидона и относительным для индапамида служат подагра и бессимптомная гиперурикемия [3].
• Для лечения АГ показаны бета-блокаторы (ББ) с вазодилатирующими свойствами (карведилол, небиволол) и высокоселективные ББ (бисопролол, метопролол замедленного высвобождения) [3].
• ББ рекомендованы в качестве АГТ в особых клинических ситуациях. Их назначение предпочтительно при симптомной стенокардии напряжения, перенесенном инфаркте миокарда (ИМ), ХСН с низкой ФВ, ФП, аневризме аорты, контроле частоты сердечных сокращений, а также для лечения АГ у женщин детородного возраста, особенно планирующих беременность [3].
• В отдельных исследованиях продемонстрированы неодинаковые эффекты классических и вазодилатирующих ББ в отношении центрального АД, артериальной ригидности, риска развития СД, исходов при ХСН. Однако РКИ по сопоставлению эффективности ББ с разными свойствами у пациентов с АГ не проводились. У физически активных пациентов и при наличии метаболического синдрома, нарушенной толерантности к глюкозе (НТГ) рекомендованы ББ с вазодилатирующим эффектом (карведилол, небиволол), не оказывающие отрицательного влияния на инсулинорезистетность [3].
• Абсолютные противопоказания для назначения ББ – синоатриальная, атриовентрикулярная блокада 2–3-й степени, синдром слабости синусового узла и бронхиальная астма [3].
18
Предпочтительные варианты начальной АГТ при наличии у пациента с АГ ряда распространенных сопутствующих заболеваний представлена в таблице 6.
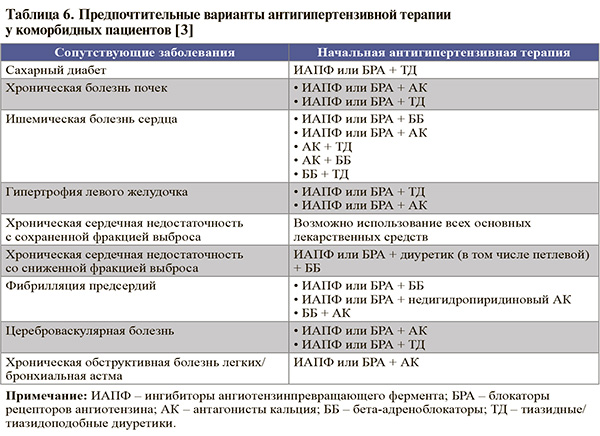
19
• Многочисленными РКИ показано, что монотерапия эффективно снижает АД лишь у ограниченного числа пациентов с АГ, и большинству больных для удовлетворительного контроля АД требуется комбинация как минимум из двух препаратов. Метаанализ более 40 исследований продемонстрировал, что рациональные комбинация двух препаратов из любых двух классов антигипертензивных средств усиливает степень снижения АД намного сильнее, чем повышение дозы одного препарата [3].
• В реальной практике на первом шаге комбинированной АГТ необходимо назначать препараты в оптимальных терапевтических дозах, которые могут обеспечить достижение целевого АД в первые 3 мес. В этом случае при недостижении целевого АД рациональным будет переход на следующий шаг – к тройной терапии [3].
20
Пациентам, не достигшим целевого АД на фоне двойной комбинированной терапии, рекомендуется тройная комбинация, как правило, включающая ингибитор АПФ или БРА с АК и тиазидным/тиазидоподобным диуретиком, предпочтительно в форме фиксированной комбинации: ЕОК/ЕОАГ – IА (УУР – В, УДД – 1) [3].
• Совершение «шага» в рамках АГТ при недостаточной эффективности используемой комбинации предполагает либо использование более высоких дозировок в комбинации, либо сразу переход на 3-компонентную схему лечения. Оба подхода допустимы на этапе применения двойной комбинации антигипертензивных средств, но при этом они должны обеспечить достижение целевого АД в течение 3 мес с шагом титрации дозы приблизительно 4 нед [3].
• При оценке необходимости расширения АГТ необходимо помнить, что целевые уровни АД являются рекомендованными для достижения в каждой подгруппе пациентов, но важнейшим принципом их достижения служит соблюдение безопасности и сохранения качества жизни пациента. Поэтому скорость достижения целевых значений и степень снижения АД может быть скорректирована у конкретного пациента в зависимости от конкретной клинической ситуации. При этом плохая переносимость снижения АД может быть основанием для более медленной титрации доз и числа назначаемых препаратов; равно как при хорошей переносимости АГТ, АД может быть снижено до более низких значений, чем рекомендовано в среднем [3].
• Недостижение целевого АД за 3 мес не считается неудачей АГТ, если это продиктовано клинической необходимостью. Если врач считает, что препятствием к достижению целевого АД выступает плохая приверженность пациента, это должно находить отражение в медицинской документации и должны быть предприняты и зафиксированы меры по повышению комплаенса. В этих случаях недостижение целевого уровня не должно считаться дефектом оказания помощи [3].
• К рекомендуемым комбинациям трех антигипертензивных препаратов относятся ингибитор АПФ + АК + диуретик и БРА + АК + тиазидный/тиазидоподобный диуретик. По показаниям, при наличии особых условий можно использовать и другие комбинации: ингибитор АПФ + дигидропиридиновый АК + ББ; БРА + дигидропиридиновый АК + ББ; ингибитор АПФ + тиазидный/тиазидоподобный диуретик + ББ; БРА + диуретик + ББ; дигидропиридиновый АК + тиазидный/тиазидоподобный диуретик + ББ [3].
• В России зарегистрировано несколько рациональных фиксированных тройных комбинаций антигипертензивных средств (БК + ингибитор АПФ/БРА + тиазидный/ тиазидоподобный диуретик) [7]. При их недоступности возможно использование двойной фиксированной комбинации + третьего компонента в виде монопрепарата или сочетание трех монопрепаратов [3].
21
• Резистентная АГ устанавливается на основании следующих критериев [2]:
– соблюдение мероприятий по изменению образа жизни и лечение с использованием оптимальных (или максимальных переносимых) доз трех и более лекарственных препаратов, включая ингибиторы АПФ или БРА, АК и диуретик, не приводят к снижению САД и ДАД до значений <140 и/или <90 мм рт.ст. соответственно;
– неадекватность контроля АД подтверждена с помощью суточного мониторирования АД (СМАД) и/или мониторирования АД в домашних условиях (ДМАД);
– подтверждена приверженность пациента к лечению;
– исключены причины псевдорезистентности и причины вторичной АГ.
• Прежде чем диагностировать резистентную АГ, необходимо исключить причины псевдорезистентности [3]:
– низкую приверженность к назначенной терапии, которая выявляется у ≤50% пациентов и прямо зависит от количества назначенных таблеток;
– феномен «белого халата» (при котором АД, измеренное в медицинском учреждении, повышено, но по данным СМАД или ДМАД уровень АД контролируется);
– нарушение правил измерения АД в медицинском учреждении, включая использование манжеты меньшего размера, может привести к ложному выявлению повышенного АД;
– выраженный кальциноз плечевой артерии, особенно у пожилых пациентов;
– клиническую инертность, приводящую к назначению нерациональных комбинаций и неадекватных доз антигипертензивных препаратов.
22
• У 15–20% пациентов контроль АД может быть не достигнут при использовании трех препаратов. В этом случае используется комбинация из ≥4 антигипертензивных препаратов (предпочтительно в двух таблетках). Однако в случаях резистентной АГ при добавлении каждого нового препарата необходимо контролировать их эффективность, и неэффективные антигипертензивные средства следует отменять, а не сохранять в рамках постепенного усиления многокомпонентной АГТ [3].
• Пациентам с АГ, не достигшим целевого АД на фоне тройной комбинированной терапии, рекомендуется добавление спиронолактона, который оказывает положительный эффект при сердечной недостаточности и резистентной АГ: ЕОК/ЕОАГ – IB (УУР – В, УДД – 1) [3].
• При непереносимости спиронолактона в качестве 4-го компонента терапии АГ возможно использование других диуретиков (эплеренона, петлевых диуретиков, в том числе в более высоких дозах), ББ, альфа-адреноблокаторов или препаратов центрального действия [3].
23
• Уровень липидов сыворотки – один из важнейших факторов сердечно-сосудистого риска. Первичная цель профилактики кардиоваскулярных осложнений в этом аспекте – достижение целевого уровня ХС ЛНП (его повышенный уровень – причина атеросклероза) в зависимости от категории риска (см. подробнее тему «Нарушения липидного обмена» – стр. 88–110) [1]. Вместе с тем, поскольку прямое измерение ХС ЛНП имеет свои ограничения, особенно при метаболическом синдроме, СД, гипертриглицеридемии (ГТГ), в этих случаях целесообразно ориентироваться на показатели холестерина, не связанного с липопротеидами высокой плотности (ХС неЛВП), который рассчитывается по формуле: ОХС – ХС ЛВП, где ОХС – общий холестерин, ХС ЛВП – холестерин липопротеидов высокой плотности. У пациентов с метаболическим синдромом, СД, ожирением показатель ХС неЛВП имеет более высокий уровень прогностической значимости по сравнению с ХС ЛНП [1, 2].
• Как альтернативу концентрациям ХС ЛНП для оценки сердечно-сосудистого риска, особенно у лиц с ГТГ, СД, ожирением, также можно использовать (при доступности измерения) уровни аполипопротеина В (апоВ). Соотношение ХС-неЛВП и уровня апо(В) для используемых целевых значений ХС-ЛНП приведено в таблице 7.

• Важными причинами сохраняющегося сердечно-сосудистого риска являются высокий уровень ТГ и низкий уровень ХС ЛВП в плазме крови. Даже при достижении целевого уровня ХС ЛНП у пациентов сохраняется риск сердечно-сосудистых осложнений. Так, в метаанализе 17 проспективных популяционных исследований было показано, что повышение ТГ сыворотки крови на 1 ммоль/л ассоциируется с увеличением новых случаев ИБС на 32% у мужчин и на 76% у женщин [14]. По данным крупнейшего эпидемиологического исследования (Framingham Study), уровень ТГ <1,7 ммоль/л (<150 мг/дл) указывает на более низкий риск сердечно-сосудистого риска, более высокие уровни указывают на необходимость поиска причин повышения уровня ТГ. Повышенные уровни ТГ и низкий уровень ХС ЛВП синергично увеличивают риск кардиоваскулярных осложнений у пациентов с уже достигнутыми целевыми уровнями ХС ЛНП [2, 15, 16].
• Пациентам любой категории сердечно-сосудистого риска рекомендован целевой уровень ТГ <1,7 ммоль/л: ЕОК/ЕОА – IIaC (УУР – B, УДД – 2) [2].
24
Немедикаментозные методы коррекции повышенного уровня ТГ включают исключение алкоголя (самый высокий уровень эффективности среди нелекарственных мер), повышение уровня регулярной физической активности, снижение общего количества углеводов, поступающих с пищей, прием пищевых добавок с омега-3 полиненасыщенных жирных кислот (ПНЖК), уменьшение потребления монои дисахаридов (средний уровень эффективности), замену насыщенных жиров монои полиненасыщенными, снижение избыточной массы тела (неоднозначная эффективность) [2].
25
В исследовании REDUCE-IT (8179 пациентов) было продемонстрировано снижение относительного риска неблагоприятных сердечно-сосудистых событий на 25% в группе пациентов, принимавших омега-3 полиненасыщенные жирные кислоты в дозе 4 г/сут, в сравнении с плацебо [17].
26
Пациентам высокого и очень высокого риска, достигшим на терапии статином уровня ТГ 1,7–2,3 ммоль/л, рекомендовано добавить препарат омега-3 ПНЖК в дозе до 2 г 2 раза/сут: ЕОК/ЕОА – IIaВ (УУР – В, УДД – 2) [2].
27
В исследовании УСПЕХ с участием 139 пациентов, страдающих неалкогольной жировой болезнью печени (НАЖБП), при приеме урсодезоксихолевой кислоты (УДХК) в дозе 15 мг/сут на протяжении 24 нед к концу наблюдения наблюдалось достоверное (p <0,001) снижение повышенного уровня ТГ относительно исходных показателей – с 3,50 до 2,20 ммоль/л [18].
28
• Пациентам с уровнем ТГ> 2,3 ммоль/л на терапии статином, рекомендовано добавить фенофибрат (предпочтительно в одной таблетке – розувастатин + фенофибрат) или препарат омега-3 ПНЖК в дозе до 2 г 2 раза в день: ЕОК/ЕОА – IIaВ (УУР – С, УДД – 5) [2]. Фенофибрат увеличивает синтез апоА1, апоА2, активность липопротеидлипазы и снижает синтез апоСIII, апоВ100 и концентрацию малых плотных частиц ЛНП на 50%. Это ведет к увеличению уровня ХС ЛВП на 10–30%, ускорению превращения хиломикронов в их ремнанты, снижению уровня ХС ЛНП на 25%, уменьшению синтеза ТГ и холестерина липопротеидов очень низкой плотности (ХС ЛОНП). Уровень ТГ может снижаться до 50%. Помимо влияния на обмен липидов, фенофибрат снижает уровень мочевой кислоты в среднем на 25%, фибриногена на 21%, С-реактивного белка на 34% [2].
• В исследовании ECLIPSE-REAL через 12 нед терапии комбинацией фенофибрата и статина наблюдалось значительное снижение уровней общего холестерина, ТГ, ХС ЛНП, ХС ЛОНП, но более значимым и статистически значимым снижение было в группе, получавшей комбинацию розувастатина и фенофибрата [2, 19–21].
29
Пациентам с уровнем ТГ >5,0 ммоль/л рекомендовано назначить фенофибрат и препарат омега-3 ПНЖК в дозе до 2 г 2 раза/сут: ЕОК/ЕОА – IIaВ (УУР – В, УДД – 2) [2].
30
При тяжелой ГТГ следует рассмотреть вопрос использования плазмафереза, плазмосорбции. Они проводятся только в специализированных отделениях больниц и клиник [2].
31
• Неалкогольная жировая болезнь печени (НАЖБП), представляющая собой накопление эктопического жира, связана с повышенным риском инфаркта миокарда и инсульта [1]. Пациенты с НАЖБП часто имеют избыточный вес или ожирение и нередко ненормальные уровни АД, глюкозы и липидов [1]. Метаанализ, включивший более 12 000 000 пациентов, позволил установить, что наличие НАЖБП повышает риск как общей, так и кардиоваскулярной смертности [22]. НАЖБП служит фактором риска развития ССЗ и определяет их исход даже в большей степени, чем исход заболевания печени [4]. Частота НАЖБП у пациентов с СД 2-го типа и ожирением, по данным различных исследований, варьирует от 70 до 100%, при этом СД 2-го типа или нарушение толерантности к глюкозе выявляют у 10–75%, ожирение – у 30 – 100%, гипертриглицеридемию – у 20–92% больных. НАЖБП повышает риск смертности от сердечно-сосудистых заболеваний в 2 раза [4].
• В связи с этим пациентам с НАЖБП следует рассчитывать сердечно-сосудистый риск, проводить скрининг на СД [4], проводить контроль липидного контроля [19]. При этом имеет смысл учитывать такой показатель, как ХС-неЛВП, включающий как общий холестерин, связанный с атерогенным ароВ, так и богатые ТГ частицы и их ремнанты, которые содержатся в ЛОНП [23].
• У всех пациентов с НАЖБП рекомендуется оценивать предикторы высокого риска ССЗ: УУР – С, УДД – 4 [4]. К предикторам высокого риска ССЗ у пациентов НАЖБП относятся [4]:
– высокие значения индекса стеатоза печени FLI. При значении FLI 30–60 кардиоваскулярный риск считается высоким;
– увеличение толщины эпикардиального жира, изменение показателей ремоделирования миокарда (увеличение толщины задней стенки левого желудочка, межжелудочковой перегородки, массы миокарда левого желудочка);
– увеличение толщины комплекса интима-медиа;
– удлинение комплекса QT;
– повышение уровней аланинаминотрансферазы (АЛТ), гамма-глютамилтранспептидазы (ГГТП), фактора некроза опухоли-альфа, интерлейкинов 1 и 6, С-реактивного белка, снижение уровня адипонектина.
32
• Доказано, что у пациентов с НАЖБП комплексные меры по изменению образа жизни, приводящие к разрешению заболевания, способствуют снижению риска смерти от сердечно-сосудистых осложнений на 40%, что сопоставимо с эффективностью медикаментозной коррекции [4].
• Пациентам с НАЖБП рекомендованы диетотерапия с постепенным снижением веса и увеличение физической нагрузки, которые являются ведущими факторами в лечении НАЖБП. Потеря веса при использовании гипокалорийной диеты или ее сочетание с повышенной физической активностью способствует уменьшению проявлений стеатоза: УУР – А, УДД – 1 [4]. Диетотерапия должна быть направлена на постепенное снижение массы тела при ее исходно повышенных показателях. При нормальной массе тела должна проводится коррекция состава рациона. Диетические рекомендации включают ограничение энергии и исключение компонентов, способствующих развитию НАЖБП (простых углеводов, напитков с высоким содержанием фруктозы, фастфуда). Показано что средиземноморская диета, по сравнению с диетой с ограничением жиров, лучше способствуют разрешению стеатоза. Установлено, что для уменьшения выраженности стеатоза при НАЖБП требуется снижение веса тела не менее чем на 3–5%, а для устранения некротических и воспалительных изменений в печени при стеатогепатите необходимо снижение веса не менее чем на 10% [4].
• Подбор диеты и выбор типа и объема физической нагрузки при НАЖБП рекомендовано адаптировать к индивидуальным предпочтениям пациента: УУР – В, УДД – 1 [4]. Не существует унифицированного немедикаментозного подхода в лечении НАЖБП, целесообразным является приспособление диеты, снижение веса и увеличение физической нагрузки к индивидуальным потребностям пациента, поскольку важным является сохранение достигнутого изменения в образе жизни на длительный период [4].
• Пациентам с НАЖБП противопоказано злоупотребление алкоголем, на стадии цирроза печени рекомендовано воздерживаться от приема алкоголя и табакокурения: УУР – С, УДД – 5 [4]. В настоящее время нет единой точки зрения на роль умеренных количеств потребления алкоголя и характера алкогольных напитков при НАЖБП (например, упоминавшаяся выше средиземноморская диета включает обязательные до 50 мл красного вина в день). Однозначно негативным фактором признается злоупотребление алкоголем. Показано, что прием алкоголя и табакокурение повышают риск развития гепатоцеллюлярной карциномы, поэтому требуется исключить их потребление пациентами с НАЖБП на стадии цирроза [4].
33
• Для лечения сопутствующего нарушения толерантности к углеводам и профилактики развития СД 2-го типа пациентам с НАЖБП рекомендуется метформин в дозе из расчета 20 мг/кг/сут курсами не менее года: УУР – С, УДД – 5 [4]. В клинических исследованиях по изучению эффективности метформина показано снижение резистентности к инсулину, уменьшение активности трансаминаз и выраженное снижение веса (более 10 кг) у 19% пациентов с НАЖБП. Однако улучшение гистологической картины печени было незначительным: уменьшения выраженности стеатоза удается достигнуть только у 30% пациентов. Общая суточная доза метформина у пациентов с НАЖБП и нарушениями толерантности к углеводам составляет 1000–2000 мг; дозу при этом следует наращивать постепенно, начиная с 500–850 мг/сут [4].
• Метформин НЕ рекомендуется в качестве специфического средства для лечения НАЖБП с синдромом инсулинорезистентности, поскольку не оказывает существенного влияния на гистологическую структуру печени: УУР – С, УДД – 3 [4]. Данные метаанализа показали, что прием метформина в течение 6–12 мес на фоне изменения образа жизни не снижает выраженности цитолиза, но улучшает гистологическую структуру печени аналогично контрольной группе, не принимавшей препарат, но изменявшей образ жизни [4].
34
Рекомендовано добавление урсодезоксихолевой кислоты (УДХК) в схемы гипогликемической терапии пациентам с НАЖБП и гипергликемией с целью дополнительного влияния на гомеостаз глюкозы: УУР – А, УДД – 1 [5]. В систематическом обзоре и метаанализе клинических исследований, опубликованном в 2018 г., было показано влияние УДХК, применяемой в различных дозах продолжительностью от 6 нед до 2 лет, на гликемические параметры. Метаанализ семи исследований с применением восьми групп лечения УДХК продемонстрировал значительное снижение уровня глюкозы натощак после такой терапии (-3,30 ммоль/л; 95% ДИ: от -6,36 до -0,24; р=0,034; I2=28,95%). Метаанализ двух групп лечения установил значительное снижение концентрации гликозилированного гемоглобина (-0,41%; 95% ДИ: от -0,81 до -0,01; р=0,042; I2 = 0%). В дополнение к этому метаанализ четырех групп лечения также выявил значительное снижение уровня инсулина в плазме (WMD: -1,50 мг/дл; 95% ДИ: от -2,81 до -0,19; р=0,025; I2=67,90%), но не продемонстрировал существенного влияния на HOMA-IR (WMD: -0,20 мг/дл; 95% ДИ: от -0,42 до 0,01; р=0,057; I2=85,34%). Результаты данного метаанализа указывают на способность УДХК значительно снижать концентрацию глюкозы в плазме натощак, гликозилированного гемоглобина и инсулина, что свидетельствует о ее положительном влиянии на гомеостаз глюкозы [5, 24].
35
• У пациентов с НАЖБП статины (ингибиторы ГМК-КоА редуктазы) рекомендованы для коррекции дислипидемии, но с учетом повышенного гепатотоксического риска их применения. При этом для специфического лечения неалкогольного стеатогепатита применять статины не рекомендуется: УУР – А, УДД – 1 [4].
• На фоне лечения статинами в течение первых месяцев терапии рекомендуется активный мониторинг каждые 3–4 нед печеночных тестов (общий билирубин в крови, определение активности АСТ, АЛТ, ГГТП, щелочной фосфатазы в крови), показателей углеводного и липидного обменов (уровни глюкозы, ТГ, общего холестерина, ХС ЛНП, ХС ЛВП, инсулина в крови): УУР – С, УДД – 5 [4].
36
• На фоне приема статинов в целях предупреждения развития цитолиза и повышения эффективности снижения повышенного уровня трансаминаз рекомендован прием урсодезоксихолевой кислоты (УДХК). Применение УДХК в дозе 10–15 мг/кг/сут на фоне статинотерапии сопровождается более выраженным снижением уровня ХС ЛПНП и рекомендуется для применения в реальной клинической практике: УУР – С, УДД – 5 [4].
• Снижение риска развития цитолиза и уменьшение повышенного уровня трансаминаз на фоне комбинированного применения статинов и УДХК подтверждены в наблюдательном исследовании РАКУРС длительностью 6 мес среди 262 пациентов в возрасте 60,1±8,9 лет. В этом же исследовании было установлено, что добавление УДХК к статинам приводило к достоверному снижению общего холестерина и ХС ЛНП в сравнении с монотерапией статинами [25, 26].
• Значимое снижение уровня печеночных ферментов, атерогенных липидов, толщины комплекса интима-медиа и 10-летнего расчетного риска сердечно-сосудистых осложнений установлено при применении УДХК (15 мг/кг/сут) в течение 6 мес в рамках международного многоцентрового исследования УСПЕХ, проведенного в реальной клинической практике [26, 27].
37
• При всех формах НАЖБП рекомендован прием УДХК в дозе 10–15 мг/кг/сут в 2 приема в течение не менее года, иногда до 2 лет и более: УУР – А, УДД – 1 [5]. УДХК обладает плейотропными эффектами: оказывает цитопротективное, антиоксидантное и антифибротическое действие, модулирует процесс апоптоза, проявляет антиканцерогенный эффект, который дополняется уменьшением агрессивного влияния токсичных желчных кислот на клетки печени и органов желудочно-кишечного тракта.
УДХК благоприятно влияет на стеатоз печени. УДХК – единственная молекула, обладающая доказанным диетоподобным эффектом в отношении регуляции аутофагии и уменьшения содержания жирных кислот в гепатоцитах [5].
• В метаанализе 12 исследований, в которых УДХК использовалась в рамках монотерапии или в комбинации с другими препаратами в дозе 10–35 мг/кг, она уменьшала уровень АЛТ и выраженность стеатоза [28]. Результаты отечественного многоцентрового исследования УСПЕХ показали, что УДХК улучшает показатели липидного обмена и обладает потенциальными антиатерогенными свойствами. У женщин также достоверно снизился показатель толщины интима-медиа каротидных артерий и 10-летний риск сердечно-сосудистых осложнений по калькулятору ASCVD 2013 [18].
В систематическом обзоре и метаанализе 2018 г. при приеме УДХК от 6 нед до 2 лет был установлен ее эффект в отношении еще одного фактора риска ССЗ – гипергликемии (значимое снижение глюкозы натощак и HbA1c) [29].
38
• У пациентов с НАЖБП, не имеющих СД, в качестве антиоксиданта при лечении доказанного неалкогольного стеатогепатита и прогрессирующего фиброза рекомендован альфа-токоферола ацетат (витамин E) в суточной дозе 800 МЕ, улучшающий гистологическую картину печени (F2 и более): УУР – С, УДД – 1 [4].
• В исследовании PIVENS применение альфа-токоферола ацетата (800 МЕ/сут) позволило снизить выраженность стеатоза, воспаления и баллонной дистрофии и стимулировать регресс неалкогольного стеатогепатита у 36% пациентов (против 21% в группе плацебо) [28]. В долгосрочном исследовании (средний период наблюдения 5,6 лет) прием витамина Е в дозе 800 ME/сут и более у пациентов с продвинутыми стадиями НАЖБП в течение ≥2 лет снижал риск смерти или потребность в трансплантации и печеночной декомпенсации без влияния на развитие гепатоцеллюлярной карциномы и сердечно-сосудистых событий. 10-летняя кумулятивная вероятность гепатоцеллюлярной карциномы, сосудистых событий и непеченочного рака не различалась [31].
• Важно помнить, что высокие дозы альфа-токоферола ацетата (более 800 мг/сут) при длительном приеме могут оказывать проканцерогенный эффект в отношении рака предстательной железы и увеличивают риск смерти от всех причин [30], поэтому вопрос об их использовании должен решаться в качестве персонализированного решения [4].
• Назначение альфа-токоферола ацетата НЕ рекомендовано при сочетании НАЖБП и СД, при НАЖБП без неалкогольного стеатоза и фиброза, при подозрении на неалкогольный стеатоз, но без гистологического подтверждения, а также при исходе НАЖБП в цирроз печени: УУР – С, УДД – 4 [4].
• Эссенциальные фосфолипиды (ЭФЛ) рекомендуются для лечения пациентов с признаками стеатоза печени вне зависимости от стадии заболевания «НАЖБП/неалкогольный стеатогепатит»: УУР – В, УДД – 2 [4]. В зависимости от соотношения количеств линолевой и линоленовой кислот у препаратов ЭФЛ могут отмечаться дополнительные гиполипидемические свойства. Анализ результатов исследования MANPOWER продемонстрировал дополнительные гиполипидемические возможности при назначении ЭФЛ на 12 и 24 нед пациентам с НАЖБП [32].
• Адеметионин рекомендован для лечения пациентов с НАЖБП, в том числе при наличии повышенной утомляемости (так называемый циркадный синдром), а также при сочетании НАЖБП и алкогольного поражения печени: УУР – С, УДД – 5 [4]. Мультицентровое наблюдательное исследование 250 пациентов с НАЖБП и проявлениями внутрипеченого холестаза продемонстрировало, что 6-недельный прием адеметионина сопровождался значимым снижением симптомов внутрипеченочного холестаза (желтухи, зуда кожи, лабораторных маркеров холестаза), а также снижением количества дней нетрудоспособности и посещений врачей [33].
• Метаанализ, включающий 25 контролируемых исследований, свидетельствует, что эффективность S-адеметионина как антидепрессанта существенно превышает плацебо и сопоставима с трициклическими антидепрессантами [34]. Этот момент может быть важен в контексте того, что депрессия, как и все психические расстройства, ассоциированы с развитием ССЗ [1].
• К другим гепатопротекторам, рекомендованным для лечения НАЖБП, относятся: глицирризиновая кислота + ЭФЛ (УУР – В, УДД – 2), экстракт плодов расторопши пятнистой (УУР – С, УДД – 2), таурин (УУР – С, УДД – 2), инозин + меглумин + метионин + никотинамид + янтарная кислота (УУР – С, УДД – 3), гидролизат плаценты человека (УУР – С, УДД – 4), морфолиний-метил-триазолил-тиоацетат (УУР – С, УДД – 4), экстракт листьев артишока (УУР – С, УДД – 4), орнитин (УУР – С, УДД – 5) [4].



