Диагностика
1
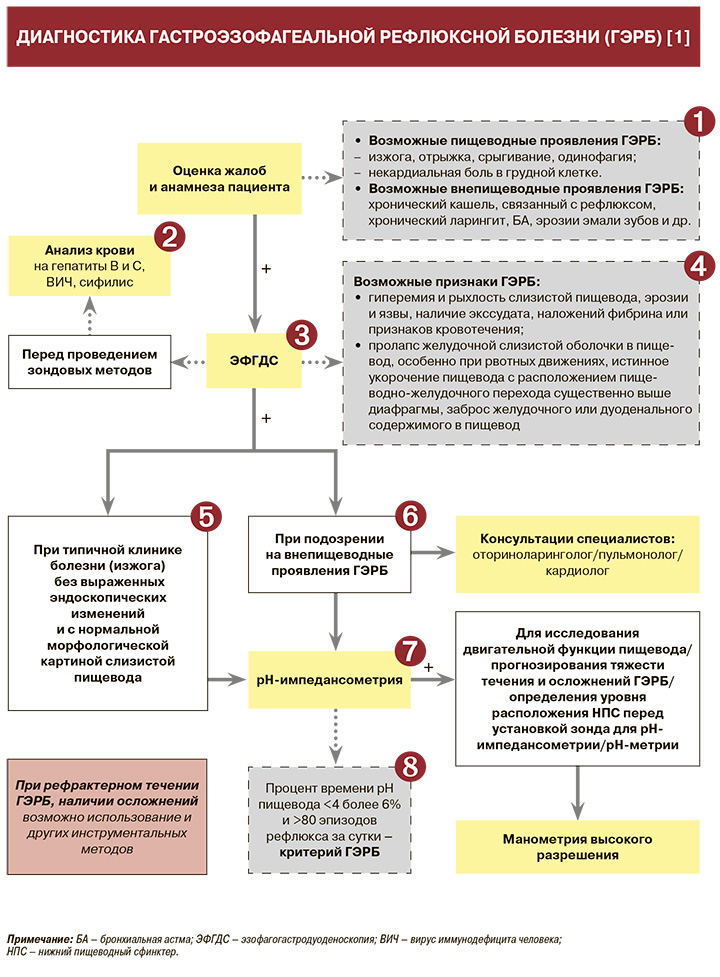
• Изжога, отрыжка, срыгивание, одинофагия составляют типичный симптомокомплекс рефлюкса при гастроэзофагеальной рефлюксной болезни (ГЭРБ).
В наибольшей степени они снижают качество жизни больных при возникновении в ночное время [1].
• Изжога – наиболее характерный пищеводный симптом ГЭРБ, встречающийся у 83% больных. Для этого симптома характерно усиление при погрешностях в диете, приеме алкоголя, газированных напитков, физическом напряжении, наклонах и в горизонтальном положении [1].
• Отрыжка как один из ведущих симптомов ГЭРБ обнаруживается у 52% больных. Она, как правило, усиливается после еды, приема газированных напитков. Срыгивание, наблюдаемое у некоторых больных ГЭРБ, усиливается при физическом напряжении и положении тела, способствующем регургитации [1].
• Дисфагия и одинофагия отмечаются у 19% пациентов с ГЭРБ. Появление стойкой дисфагии и одновременное уменьшение изжоги может свидетельствовать о формировании стеноза пищевода как доброкачественного, так и злокачественного характера.
• Некардиальные боли в грудной клетке по ходу пищевода (за грудиной) похожи на коронарную боль. Они купируются нитратами, но в отличие от стенокардии (ИБС) не связаны с физической нагрузкой, а появляются вследствие гипермоторной дискинезии пищевода, причиной которой может быть дефект системы ингибирующего трансмиттера – оксида азота. Пусковым моментом для возникновения эзофагоспазма и соответственно боли служит патологический желудочно-пищеводный рефлюкс [1].
• Ассоциация хронического кашля, обусловленного рефлюксом, хронического ларингита, бронхиальной астмы и эрозии эмали зубов с ГЭРБ основана на достаточно убедительных клинических доказательствах. Что касается таких внепищеводных проявлений, как фарингит, синусит, легочный фиброз, средний отит, то их связь с ГЭРБ лишь предполагается [1].
• Факторы риска ГЭРБ, которые следует учитывать при изучении анамнеза пациента, включают избыточную массу тела, высокое содержание жиров в пище, злоупотребление газированными напитками, возраст старше 50 лет, курение [2, 3]. Среди факторов риска развития осложнений ГЭРБ наибольшее значение имеют частота возникновения и длительность существования симптомов, в частности изжоги, выраженность эрозивного эзофагита, частота его рецидивов, наличие грыжи пищеводного отверстия диафрагмы (ГПОД), ожирение, наличие ночных рефлюксов [1].
• Отдельного внимания необходимо обратить на препараты, которые больной принимает на постоянной основе. К лекарственным средствам, способным вносить вклад в развитие симптомов верхних отделов желудочно-кишечного тракта (как связанных с ГЭРБ, так и с другими заболеваниями), относятся нестероидные противовоспалительные препараты (НПВП), включая ацетилсалициловую кислоту, препараты железа, калия, тетрациклин, бисфосфонаты; зидовудин, антихолинергические средств, альфа-адреноблокаторы, барбитураты; агонисты бета2адренергических рецепторов, блокаторы кальциевых канальцев, бензодиазепины, допамин; эстрогены, наркотические анальгетики, нитраты, прогестерон, простагландины, теофиллин; трициклические антидепрессанты, химиотерапия [2, 3].
• Наличие «тревожных» признаков (анемия, прогрессирующая потеря веса, лимфаденопатия, рецидивирующие бронхиальные симптомы, аспирационная пневмония, дисфония, болезненное глотание, рецидивирующий или постоянный кашель, желудочно-кишечное кровотечение, частая тошнота и/или рвота, персистирующая боль, образования в эпигастральной области и др.) не характерно для ГЭРБ; в большинстве стран такие признаки связаны с раком желудка, осложненной язвенной болезнью или другим серьезным заболеванием [2].
• Специфических физикальных признаков ГЭРБ не существует. При осмотре пациента целесообразно измерить объем талии, вес и ИМТ (чем они больше, тем выше риск ГЭРБ). Также при опросе/осмотре по возможности необходимо исключить такие заболевания/ состояния, как астма, заболевания сердца, анемия, потеря веса, изъязвления, кандидоз, повреждения, образования, дентальные эрозии, ротоглотки, кариес, узлы, образования в области шеи, одышка, хрипы, потеря слуха, выпот в среднем ухе, напряженность живота, признаки (локальные или системные) злокачественных новообразований [2].
2
Всем пациентам ГЭРБ перед проведением зондовых методов (эзофагогастродуоденоскопия, рН-метрия/рН-импедансометрия) необходимо исследовать анализы крови на гепатиты В и С (антитела к HCV, HBsAg), ВИЧ, сифилис: уровень убедительности рекомендаций (УУР) – С, уровень достоверности доказательств (УДД) – 5 [1].
3
Пациентам с подозрением на ГЭРБ при отсутствии противопоказаний с целью подтверждения диагноза и проведения дифференциальной диагностики рекомендована эзофагогастродуоденоскопия (ЭФГДС): УУР – С, УДД – 5 [1].
4
• В зависимости от площади поражения слизистой пищевода выделяют 4 степени тяжести (A–D) эрозивного эзофагита (табл. 1). Такие возможные осложнения ГЭРБ, как стриктуры, язвы, пищевод Баррета, рассматриваются отдельно и могут наблюдаться при любой степени рефлюкс-эзофагита [1].
• Оценить замыкательную функцию кардии при ЭФГДС сложно, так как кардия может быть приоткрыта рефлекторно в ответ на введение эндоскопа и инсуффляцию воздуха [1].

5
• Пациентам с типичными клиническими проявлениями ГЭРБ (изжога) без выраженных эндоскопических изменений и c нормальной морфологической картиной слизистой оболочки пищевода может быть рекомендовано проведение рН-импедансометрии: УУР – А, УДД – 1 [1]. Этот метод представляет собой сочетание рН-метрии пищевода (оценка воздействия кислоты на слизистую оболочку пищевода и взаимосвязи симптомов с кислым рефлюксом) и импендансометрии (регистрация жидких и газовых рефлюксов, основанный на измерении сопротивления, которое оказывает электрическому току содержимое, попадающее в просвет пищевода) [1].
• При диагностике гастроэзофагеального рефлюкса результаты рН-метрии оценивают по общему времени, в течение которого рН пищевода имеет значение <4 единиц, общему числу рефлюксов за сутки, количеству рефлюксов продолжительностью более 5 мин, длительности наиболее продолжительного рефлюкса [1]:
– процент времени рН <4 более 6% и >80 эпизодов рефлюкса – свидетельство в пользу диагноза ГЭРБ;
– процент времени рН <4 менее 4% и число рефлюксов <40 за период суточного мониторирования – вариант физиологической нормы;
– промежуточные значения указанных показателей не служат достаточным критерием для постановки диагноза.
• Импедансометрия позволяет диагностировать эпизоды рефлюкса в пищевод независимо от рН рефлюктата, его физического состояния (газ, жидкость), а также определения клиренса болюса, попавшего в пищевод во время рефлюкса. Кислотность рефлюктата (кислый, слабокислый, слабощелочной) определяется рН-датчиками. У пациентов с типичными проявлениями, характерными для ГЭРБ, рН-импедансометрия пищевода дает возможность провести дифференциальный диагноз между неэрозивной рефлюксной болезнью (НЭРБ), функциональной изжогой, гиперсенситивным рефлюксным синдромом (или гиперсенситивным пищеводом), а в случае с подтвержденной ранее ГЭРБ исключить их сочетание [1].
6
• Пациентам с подозрением на внепищеводные проявления ГЭРБ (боль в грудной клетке, не связанная с заболеваниями сердечно-сосудистой системы, хронический кашель, бронхиальная астма, хронический фарингит, ларингит, выраженная отрыжка) также рекомендовано проведение рН-импедансометрии: УУР – А, УДД – 1 [1]. Этот метод, в частности, верифицирует связь сухого кашля, першение в горле, осиплость с забросом желудочного содержимого в гортань: индекс симптома для этих проявлений превышает 50%, что свидетельствует об их достоверной ассоциации с гастроэзофагеальным рефлюксом [1].
• Следует иметь в виду, что супрагастральная отрыжка (отрыжка, при которой воздух, проходя в пищевод, не достигает желудка, а моментально выходит обратно в глотку) может выступать как проявлением ГЭРБ, так и самостоятельным функциональным заболеванием (синдромом чрезмерной отрыжки). Среди пациентов с диагностированной супрагастральной отрыжкой до 95% предъявляют жалобы на изжогу, а повышение процента времени рН <4 при проведении рН-импедансометрии выявляется у 41% больных [1].
• Также пациентам с атипичными формами и внепищеводными проявлениями ГЭРБ рекомендуется проведение консультации специалистов – кардиолога, оториноларинголога, пульмонолога: УУР – С, УДД – 5 [1]. Это, в частности, необходимо для дифференциальной диагностики ГЭРБ с ишемической болезнью сердца и заболеваниями перикарда (при боли в грудной клетке), патологией ЛОР-органов (при фарингите, ларингите), хроническим бронхитом (при кашле) и астмой [4].
7
• Другие показания для проведения рН-импедансометрии/рН-метрии включают [1]:
– рефрактерное течение ГЭРБ (отсутствие убедительной клинической и эндоскопической ремиссии в течение 4–8 нед проведения терапии стандартной дозой ингибиторов протонной помпы), а также наличие осложнений заболевания – стриктур, пищевода Баррета (УУР – С, УДД – 5);
– перед планируемым хирургическим лечением, в том числе у пациентов с характерными симптомами ГЭРБ, купируемыми приемом ИПП (УУР – А, УДД – 1);
– подбор минимально эффективной дозы лекарственных средств и контроль эффективности проводимого консервативного лечения у больных ГЭРБ (УУР – В, УДД – 3);
– после антирефлюксных операций для оценки эффективности хирургического лечения при сохраняющихся симптомах ГЭРБ (УУР – А, УДД – 1).
• Добавим, что пациентам с сохраняющимися типичными симптомами с доказанной ранее ГЭРБ рекомендуется рН-импедансометрия на фоне терапии ингибиторами протонной помпы, поскольку это позволяет установить эффективность действия антисекреторного препарата, оценить связь симптома с наличием кислого, слабокислого или слабощелочного рефлюкса (УУР – А, УДД – 1) [1]. Количественный анализ данных рН-импедансометрии позволяет исключить сочетание ГЭРБ с функциональной изжогой и гиперсенситивным рефлюксным синдромом [1]. Если же у пациента ранее не было доказано наличие ГЭРБ или данные были неубедительны, то суточный мониторинг проводится с отменой препарата для определения патологического воздействия кислоты на слизистую оболочку пищевода (процент времени рН <4), числа гастроэзофагеальных рефлюксов, их химических и физических характеристик, высоты распространения и связи симптомов с забросом желудочного содержимого в пищевод (УУР – А, УДД – 1) [1].
При анализе данных pH-импедансометрии целесообразно рассчитывать дополнительные новые параметры: средний ночной базальный импеданс (СНБИ) и индекс пострефлюксной глоток-индуцированной перистальтической волны (ПГПВ), позволяющие оценить клиренс пищевода, особенности поражения его слизистой оболочки (снижение ее резистентности) и эффективность перистальтики. Новые параметры служат дополнительными критериями, повышающими диагностическую ценность pH-импедансометрии в постановке диагноза и определении формы ГЭРБ. Снижение уровня данных показателей у пациентов отражает вероятность более тяжелого течения заболевания [1].
8
• Манометрия высокого разрешения может быть рекомендована пациентам с ГЭРБ [1]:
– для исследования двигательной функции пищевода (УУР – А, УДД – 1);
– для прогнозирования тяжести течения и осложнений ГЭРБ путем диагностики эффективности перистальтической активности грудного отдела пищевода (УУР – C, УДД – 5);
– для определения уровня расположения нижнего пищеводного сфинктера перед установкой зонда для рН-метрии/рН-импедансометрии (УУР – А, УДД – 1);
– для определения наличия показаний к хирургическому лечению, установления патогенеза развития симптомов ГЭРБ путем изучения морфологии пищеводножелудочного перехода (УУР – C, УДД – 5).
• При анализе результатов, полученных методом манометрии высокого разрешения, следует пользоваться Чикагской классификацией нарушений моторики пищевода (табл. 2).

• Совместное применение с pH-импедансометрией расширяет диагностические возможности манометрии. Комбинированная импеданс-манометрия позволяет визуализировать транзит болюса по пищеводу и эффективность перистальтики, выявлять тип отрыжки (гастральная, супрагастральная), определять, служит ли она проявлением основного заболевания или самостоятельным синдромом, что дает возможность назначать патогенетическую терапию [1].
9
Другие возможные методы инструментальной диагностики ГЭРБ [1].
• ЭФГДС с биопсией пищевода и гистологическим исследованием биоптатов. Может быть проведена у пациентов с рефрактерным течением заболевания, наличием осложнений ГЭРБ (стриктуры, пищевод Баррета), для исключения эозинофильного эзофагита, а также пищевода Баррета и аденокарциномы (УУР – В, УДД – 3);
• рентгенологическое исследование пищевода и желудка, комплексное ультразвуковое исследование (УЗИ) органов брюшной полости, регистрации электрокардиограммы. Могут выполняться при рефрактерном течении ГЭРБ, а наличии осложнений заболевания (УУР – С, УДД – 5). Подчеркнем, что рентгенологическое исследование пищевода не применяется с целью непосредственной диагностики ГЭРБ, но позволяет обнаружить грыжи пищеводного отверстия диафрагмы, диффузный эзофагоспазм, стриктуры пищевода и подозрение на короткий пищевод у тех пациентов, которым предполагается хирургическое лечение;
• импедансная планиметрия. Используется для выявления признаков ахалазии кардии;
• эндоскопическое УЗИ пищевода (эндосонография). Основной методикой, позволяющей выявлять эндофитно растущие опухоли и признаки ахалазии (УУР – С, УДД – 5).
Лечение
1
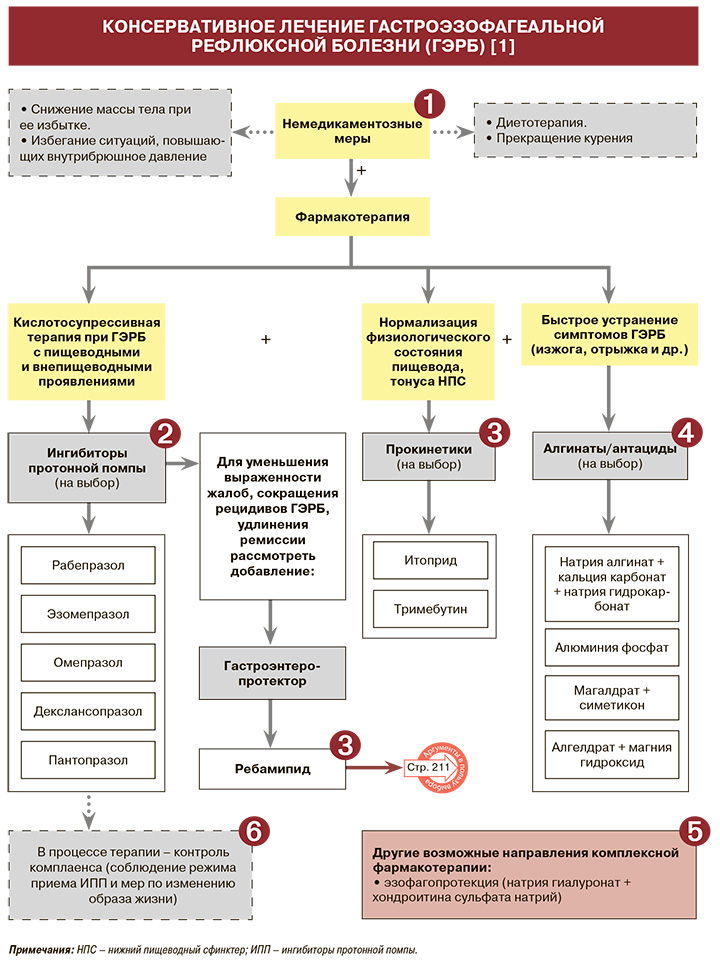
• Всем пациентам с ГЭРБ рекомендуется изменение образа жизни (снижение массы тела при ее избытке, прекращение курения, избегание ситуаций, повышающих внутрибрюшное давление) и диетотерапия: УУР – С, УДД – 5 [1].
• Изменение образа жизни следует считать обязательной предпосылкой эффективного антирефлюксного лечения пациентов с ГЭРБ. В первую очередь необходимо снизить массу тела, если она избыточна, и прекратить курение. Пациентам следует избегать переедания; они должны прекращать прием пищи за 2 ч до сна. В то же время не следует увеличивать число приемов пищи: необходимо соблюдать 3-, 4-разовое питание и тщательно избегать так называемых перекусов. Рекомендации по частому дробному питанию не обоснованы [1].
• Важно максимально избегать ситуаций, повышающих внутрибрюшное давление (ношения тугих поясов, корсетов и бандажей, подъема тяжестей более 8–10 кг на обе руки, работ, сопряженных с наклоном туловища вперед, физических упражнений, связанных с перенапряжением мышц брюшного пресса). Пациентам, которых беспокоит изжога или регургитация в лежачем положении, необходимо поднятие изголовья кровати [1].
• Диетические рекомендации должны быть строго индивидуальны с учетом тщательного анализа анамнеза пациента. Целесообразно избегать употребления томатов в любом виде, кислых фруктовых соков, продуктов, усиливающих газообразование, а также жирной пищи, шоколада, кофе. Необходимо максимально ограничить употребление алкоголя, очень горячей или холодной еды и газированных напитков [1].
• Больных нужно предупредить о побочном действии препаратов, которые снижают тонус нижнего пищеводного сфинктера (нитраты, антагонисты кальция группы нифедипина, теофиллин, прогестерон, антидепрессанты), а также могут сами стать причиной воспаления (НПВП, доксициклин) [1].
2
• Снижение кислотной продукции считается основным фактором, способствующим заживлению эрозивно-язвенных поражений при ГЭРБ; в клинических исследованиях ингибиторы протонной помпы (ИПП) постоянно демонстрируют наибольшую эффективность в лечении эрозивного эзофагита и купировании ГЭРБ-ассоциированных пищеводных и внепищеводных симптомов: УУР – А, УДД – 1 [1]. ИПП эффективно контролируют уровень рН в нижней трети пищевода, поэтому выраженность симптомов быстро уменьшается, и они исчезают у пациентов как с эрозивным эзофагитом, так и НЭРБ (табл. 3).
• Пациентам с типичным симптомокомплексом рефлюкса, у которых нет адекватного ответа на терапию ИПП в стандартной дозе 1 раз в день, может быть рекомендован прием ИПП дважды в день. При этом следует учитывать, что данная дозировка не утверждена в инструкциях по применению данных препаратов [1].
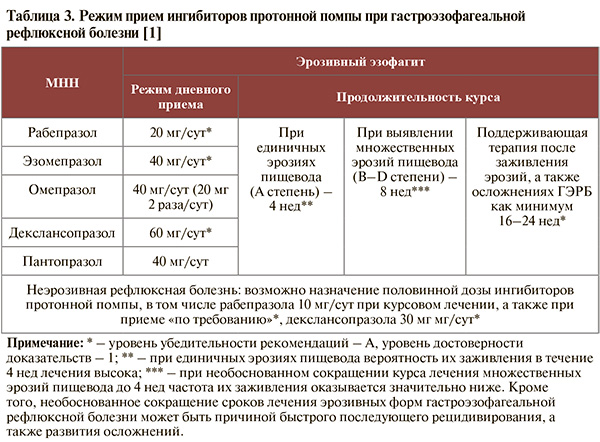
• Рекомендуется применять индивидуальный подход к назначению антисекреторной терапии и выбору препарата при лечении больных ГЭРБ, основанный на тщательном анализе клинической картины и данных ЭФГДС. В первую очередь анализируются жалобы больного, в частности изжога (кроме нее, могут приниматься во внимание и другие доказанные симптомы ГЭРБ). Критериями оценки жалоб служат частота их возникновения: редко (1–2 раза/нед) или часто (>2 раза/нед), а также длительность существования: небольшая (<6 мес) или значительная (>6 мес). При оценке статуса пациента и анамнеза учитываются мужской пол и возраст старше 50 лет как факторы риска развития рецидива, указания на наличие эрозивного эзофагита при проведении ЭФГДС в прошлом, причем существенное значение имеет степень существовавшего ранее эрозивного эзофагита. При оценке статуса больного также следует обратить внимание на наличие избыточной массы тела (индекс массы тела >25) и ожирения (индекс массы тела >30) и грыжи пищеводного отверстия диафрагмы. Необходимо исключить наличие симптомов тревоги: дисфагии, похудания, анемии [1].
• Благодаря высокой константе диссоциации рКа, рабепразол способен быстро аккумулироваться в большом числе париетальных клеток и приводить к быстрому и выраженному торможению секреции кислоты, ингибируя протонную помпу, что обеспечивает высокую скорость действия и позволяет достичь стойкого антисекреторного эффекта уже после первых суток приема препарата [1, 7, 8]. Фармакокинетические особенности рабепразола обусловливают эффективное купирование дневной и контроль ночной изжоги с первого дня терапии, высокую частоту заживления эрозий пищевода и поддержания длительной ремиссии ГЭРБ, в том числе при приеме «по требованию»: УУР – A, УДД – 1 [1, 9–11].
• Cекреция муцинов в слизи при ГЭРБ снижается в зависимости от тяжести эзофагита, что является дополнительным фактором, предрасполагающим к развитию эрозивного эзофагита в условиях продолжающегося гастроэзофагеального рефлюкса [1]. Двойной механизм действия рабепразола (кислотосупрессия наряду со стимуляцией секреции муцинов и повышением их концентрации в слизи пищевода) обеспечивает его дополнительные терапевтические преимущества: УУР – C, УДД – 4 [1, 12].
• Эзомепразол, благодаря стереоселективным особенностям взаимодействия с цитохромом P450, обладает большой биодоступностью и предсказуемым контролем секреции соляной кислоты, длительно поддерживая уровень рН >4; это обеспечивает эффективность терапии НЭРБ и эрозивного эзофагита [1, 13–15]. Лекарственная форма таблетки эзомепразола MUPS (мультипартикулярная система доставки), покрытой кислотоустойчивой оболочкой, обеспечивает быстрое и предсказуемое всасывание независимо от приема еды. Возможность растворения в воде таблетки MUPS может быть удобна пациентам с дисфагией и при использовании через назгогастральный зонд [1, 16].
• Декслансопразол – единственный ИПП с модифицированным высвобождением активного вещества. Его капсула включает два типа гранул, высвобождающих активное вещество в зависимости от pH в разных областях тонкой кишки через 1–2 ч и через 4–5 ч после приема препарата [1, 17, 18]. Двойное отсроченное высвобождение активного вещества позволяет пролонгировать его действие и способствует снижению секреции соляной кислоты в течение продолжительного времени. Пролонгированный эффект декслансопразола способствует эффективному контролю ночных симптомов ГЭРБ: УУР – A, УДД – 1 [1, 19].
• В целом ИПП демонстрируют невысокую частоту побочных эффектов (<2%), среди которых могут наблюдаться диарея, головная боль, тошнота [1]. При назначении ИПП в больших дозах на длительный срок следует также учитывать возможность развития таких побочных эффектов, как остеопороз (хотя прием ИПП не должен рассматриваться как самостоятельный и независимый фактор риска развития этой болезни), избыточный бактериальный рост, инфекция Clostridium difficile и пневмония среди пациентов из групп риска, в первую очередь старше 65 лет [1]. При длительном лечении ИПП возможно их назначение «по требованию» и прерывистыми курсами [1]. Решение о длительности поддерживающей терапии ГЭРБ и об ее отмене должно приниматься индивидуально с учетом стадии эзофагита, имеющихся осложнений, возраста пациента, прогноза заболевания, а также стоимости и безопасности лечения ИПП. Рабепразол демонстрирует высокий уровень безопасности в отношении частоты побочных эффектов и переносимости, а его метаболизм минимально зависит от системы цитохрома 450 [1], что позволяет рекомендовать его в качестве препарата выбора у полиморбидных пациентов, минимизируя риск межлекарственного взаимодействия; это важно при необходимости длительных курсов (УУР – А, УДД – 1) [1, 20].
• Нет необходимости выявления инфекции H. pylori и тем более ее эрадикации при ГЭРБ [1]. Эпидемиологические исследования показывают отрицательную связь между распространенностью этой инфекции и частотой/тяжестью ГЭРБ.
У большинства пациентов с этим заболеванием статус H. pylori не оказывает влияния на тяжесть симптомов и их рецидивирование. Эрадикация H. pylori не вызывает обострения ранее существовавшей ГЭРБ и не влияет эффективность терапии [2].
Вместе тем следует определить наличие H. pylori и провести ее эрадикацию при назначении терапии ИПП на длительный срок [1].
• Симптоматическое улучшение при терапии ИПП может наблюдаться и при других заболеваниях, в том числе злокачественном новообразовании желудка, поэтому необходимо исключить такие заболевания.
3
• Известно, что способность слизистой оболочки пищевода противостоять повреждающему действию рефлюктата обусловлена равновесием между факторами агрессии и защиты [1]. Нарушение этого равновесия у большой части пациентов сопровождается существенным замедлением восстановления рН дистальной части пищевода после каждого эпизода рефлюкса. Основным цитопротективным фактором защиты служит многослойный плоский неороговевающий эпителий пищевода, покрытый слоем слизи, содержащей муцин и бикарбонаты слюны.
Установлено, что секреция муцинов в слизи при ГЭРБ снижается в зависимости от тяжести эзофагита, что выступает дополнительным фактором, предрасполагающим к развитию эрозивного эзофагита в условиях продолжающихся рефлюксов. Также в цитопротекции немаловажное значение имеют эпителиальные клетки и плотные межклеточные контакты, заполненные гликопротеинами [1]. Избыточная секреция провоспалительных цитокинов (в частности, интерлейкина 8), образование свободных радикалов кислорода, нарушение баланса в образовании простагландинов (в частности, PgE2), повышенная эпителиальная проницаемость также приводят к прогрессированию воспаления в слизистой оболочке пищевода и нарушению его целостности [21, 22]. Действие ребамипида нацелено на указанные звенья патогенеза кислотозависимых заболеваний [1, 23, 24]:
– препарат регулирует синтез простагландинов через ЦОГ-2-опосредованные механизмы, повышает экспрессию белков плотных межклеточных контактов в эпителиальных клетках слизистых оболочек, снижает уровень интерлейкина 8, свободных радикалов кислорода, тем самым повышая защитный потенциал слизистой оболочки ЖКТ и стимулируя восстановление ее естественных барьерных свойств;
– ребамипид обладает способностью снижать повышенную эпителиальную проницаемость на трех структурных уровнях и на всем протяжении ЖКТ, в том числе в пищеводе и НПС.
Согласно данным ряда клинических исследований, добавление к ИПП ребамипида способствует большему регрессу жалоб у пациентов с ГЭРБ и меньшей частоте рецидивов заболевания в сравнении с монотерапией ИПП. Так, в исследовании 501 пациента с ГЭРБ комбинация ребамипида (300 мг/сут) и эзомепразола (40 мг/сут) через 4 нед на 21% снижала выраженность симптомов рефлюкса и на 16,5% выраженность всех симптомов заболевания относительно монотерапии ИПП (различия достоверны, p=0,009) [25]. В свою очередь, в исследовании 40 пациентов, получавших либо только ИПП (лансопразол 15 мг/сут), либо сочетание ИПП + ребамипид (300 мг/сут), на фоне комбинированного лечения в течение 12 мес наблюдения частота рецидивов ГЭРБ оказалась на 32,4% ниже, чем при монотерапии ИПП (различия достоверны, p <0,05) [26].
• Отметим, что в инструкциях к препаратам, содержащим ребамипид, среди официальных показаний к применению ГЭРБ отсутствует [27]. Вместе с тем в настоящее время проводится активное изучение и выработка рекомендаций по методике применения этого лекарственного средства у пациентов с ГЭРБ.
Это оправдано ввиду наличия у ребамипида механизма действия, нацеленного на устранение основных этапов патогенеза заболевания, что в конечном счете существенно снижает выраженность симптомов и способствует достижению главной цели терапии – сокращению частоты рецидивов ГЭРБ [1, 23, 24, 25].
4
• Прокинетики могут применяться в составе комплексной терапии ГЭРБ вместе с ИПП: УУР – А, УДД – 1 [1]. Они способствуют восстановлению нормального физиологического состояния пищевода, уменьшая количество преходящих расслаблений нижнего пищеводного сфинктера, улучшая пищеводный клиренс за счет стимуляции двигательной функции нижележащих отделов пищеварительного тракта. Наибольший эффект прокинетики оказывают при сочетании ГЭРБ и функциональной диспепсии [1].
• Метаанализ 12 рандомизированных контролируемых исследований, посвященных применению прокинетиков у пациентов с ГЭРБ (n=2403), показал, что добавление прокинетиков к ИПП способствовало более существенному уменьшению выраженности клинических симптомов и числа эпизодов рефлюкса [1, 28].
• Итоприд (50 мг 3 раза/сут) нормализует двигательную функцию верхних отделов пищеварительного тракта, уменьшает количество преходящих расслаблений нижнего пищеводного сфинктера [1, 29]. При использовании итоприда в составе комбинированной терапии с ИПП при ГЭРБ обнаружено, что он достоверно усиливает сократительную активность нижнего пищеводного сфинктера и моторику желудка, ускоряет желудочную эвакуацию, восстанавливает гастродуоденальную координацию и оказывает достоверное влияние на купирование изжоги [1, 30, 31]. В комбинации с рабепразолом препарат доказано улучшает клиническое течение хронического кашля, обусловленного ГЭРБ [1, 32].
• Тримебутин (100–200 мг 3 раза/сут) применяется для купирования изжоги и отрыжки при лечении НЭРБ. Он нормализует скорость опорожнения желудка у пациентов с его замедленным опорожнением: время от момента поступления пищи в желудок до начала эвакуации пищи из него существенно уменьшается [1, 33]. Тримебутин способствует более выраженному купированию эзофагита и симптоматики ГЭРБ в сочетании с ИПП, чем при монотерапии ИПП. При такой комбинации полное купирование симптоматики наблюдается достоверно чаще [1, 34]. Также отмечено более выраженное действие комбинации тримебутина и ИПП по сравнению с монотерапией ИПП в отношении нормализации показателей качества жизни и суточного мониторирования рН в пищеводе [1, 35].
5
• Алгинаты и антациды могут применяться как в качестве монотерапии редкой изжоги, не сопровождающейся развитием эзофагита, так и в схемах комплексной терапии ГЭРБ, поскольку оказываются эффективны в быстром устранении симптомов: УУР – А, УДД – 1 [1]. Алгинаты, представлены в России препаратами, содержащими натрия алгинат + кальция карбонат + натрия гидрокарбонат, натрия алгинат + калия гидрокарбонат [36].
• Алгинаты, наряду с быстрым купированием изжоги и кислой отрыжки, способны уменьшать количество как гастроэзофагеальных, так и дуоденогастроэзофагеальных рефлюксов [1, 37]. Доказана фармакологическая совместимость этих средств с антисекреторными препаратами для лечения ГЭРБ: УУР – А, УДД – 1 [1, 37–39].
• Антацидные средства (алюминия фосфат, магалдрат + симетикон, алюминия гидроксид + магния гидроксид) применяют в лечении умеренно выраженных и нечасто возникающих симптомов, особенно тех, которые связаны с несоблюдением рекомендованного образа жизни [1, 40].
• Комбинированный препарат, содержащий магалдрат + симетикон, способен быстро нейтрализовать соляную кислоту и длительно поддерживать стабильный уровень pH, активно связывать соли желчных кислот [1, 41]. При его применении наблюдается исчезновение симптомов у большинства пациентов с ГЭРБ: УУР – А, УДД – 1 [1, 42].
• Антациды и алгинаты следует принимать в зависимости от выраженности симптомов обычно после еды и на ночь до стойкого купирования симптомов заболевания, затем по требованию. Данных, свидетельствующих о возможности их постоянного применения, недостаточно: УУР – В, УДД – 2 [1].
6
• Эзофагопротекторы – новая фармакологическая группа, представителем которой является биоадгезивная формула на основе гиалуроновой кислоты и хондроитина сульфата для защиты слизистой оболочки (зарегистрирована в России как изделие медицинского назначения). Комбинация натрия гиалуроната и хондроитина сульфата натрия способствует защите слизистой оболочки желудка и пищевода от агрессивного воздействия соляной кислоты желудка (в том числе благодаря адгезии за счет поверхностно-активного компонента полоксамера 407), оказывает ингибирующее действие на протеолитическую активность пепсина. Также она способствует заживлению эрозий пищевода, в том числе в сочетании с ИПП. При такой комбинации полное купирование симптоматики наблюдается достоверно чаще, чем при монотерапии ИПП [1, 43, 44].
• Эзофагопротектор на основе гиалуроновой кислоты и хондроитина сульфата следует принимать по 10 мл после еды и на ночь. В клинических исследованиях доказана его эффективность при применении в течение 4–5 нед: УУР – А, УДД – 1 [1, 43, 44].
7
• Несоблюдение пациентами рекомендаций по изменению образа жизни и правил приема ИПП – наиболее распространенная причина уменьшения эффекта от проводимой терапии ГЭРБ. На соблюдение (или несоблюдение) предписанных врачом рекомендаций влияет прежде всего наличие симптомов и их тяжесть, знание основ патогенеза заболевания, сопутствующая терапия, побочные эффекты, возраст, социально-экономический статус, мотивация больного. Безусловно, выполнение рекомендаций врача, в том числе по режиму питания, нормализации массы тела, следует считать фундаментом успешного лечения. Неэффективность терапии нередко наблюдается также при неправильном назначении и несоблюдении дозировки ИПП и сроков терапии [1].
• Фактором развития рефрактерной (устойчивой к терапии) ГЭРБ также может выступать генетический полиморфизм CYP2C19. Пациенты из группы «быстрых метаболизаторов» CYP2C19 имеют повышенный риск развития рефрактерности к терапии ИПП по сравнению с «медленными метаболизаторами». В настоящее время выделен еще один тип метаболизаторов по изоферменту CYP2C19, названный «ультрабыстрым», который может встречаться в европейской популяции. В отдельных случаях такие больные нуждаются в применении высоких доз антисекреторных препаратов, что должно быть верифицировано с помощью 24-часовой рН-метрии [1].
• Еще одна потенциальная причина неэффективности ингибиторов секреции соляной кислоты – наличие слабокислого рефлюкса, а также преобладание в рефлюктате содержимого двенадцатиперстной кишки с преимущественно щелочной средой, когда изжога и другие симптомы ГЭРБ возникают в результате действия на слизистую оболочку пищевода компонентов желчи и панкреатических ферментов. Рефлюктат имеет преимущественно кислый характер у 50% больных ГЭРБ, кислый с желчным компонентом имеет место в 39,7% случаев, и 10,3% больных имеют желчный рефлюкс [1]. Компоненты дуоденального содержимого, повреждающие слизистую оболочку пищевода, представлены желчными кислотами, лизолецитином и трипсином. Из них наиболее хорошо изучена роль желчных кислот, которым, по-видимому, принадлежит основная роль в патогенезе повреждения пищевода при дуоденогастроэзофагеальном рефлюксе. При смешанном рефлюксе (кислый с желчным компонентом) ИПП оказывают клинический эффект не только вследствие подавления собственно кислотопродукции, но и за счет уменьшения общего объема желудочного секрета, что ведет к уменьшению объема рефлюктата. Однако повышение доз ИПП с целью купирования симптоматики в таком случае не показано. В случае дуоденогастроэзофагеального рефлюкса могут быть назначены в различных комбинациях (в сочетании с ИПП) следующие препараты: антациды, эзофагопротекторы, прокинетики, урсодезоксихолевая кислота, ребамипид: УУР – С, УДД – 4 [1].
• При неэффективности лечения пациентов с ГЭРБ в течение 4 нед следует провести подтверждение гастроэзофагеального рефлюкса с помощью объективного метода исследования 24-часовой рН-импедансометрии [1]. Пациенты с сохраняющимися симптомами, у которых при проведении рН-импедансометрии не обнаруживаются патологические рефлюксы и отсутствует корреляция рефлюксов с возникновением симптомов, скорее всего, страдают не ГЭРБ, а так называемой функциональной изжогой [1].



