Диагностика

1
Помимо собственно когнитивных нарушений, клиническая картина на любой стадии когнитивного расстройства (КР) может быть представлена их сочетанием с некогнитивными нервно-психическими расстройствами. При сосудистых КР таковыми могут быть двигательные, личностные или эмоциональные нарушения, расстройства мочеиспускания и др. Зачастую именно некогнитивные нервно-психические расстройства становятся причиной дистресса как для самого пациента, так и окружающих его (осуществляющих за ним уход) лиц [1].
2
• Рекомендуется проводить сбор жалоб и анамнестических сведений не только у самих пациентов с КР, но и у информантов с целью объективизации получаемой информации: уровень убедительности рекомендаций (УУР) – В, уровень достоверности доказательств (УДД) – 1 [1]. Также у всех пациентов с КР рекомендуется уточнять влияние когнитивных нарушений на их повседневную (базовую и инструментальную) деятельность: УУР – А, УДД – 3 [1]. Классификация степени КР, которая может быть выявлена на основе тщательного опроса, отражена в таблице 1. Выделение пациентов с возможной деменцией имеет кардинальное значение для последующего выбора медикаментозных и немедикаментозных методов лечения при, а также для определения потребности больного в посторонней помощи и уходе [1].

• При опросе пациента с подозрением на сосудистые КР (в том числе сосудистую деменцию) отдельное внимание уделяется характеристикам динамики когнитивного снижения. Эти характеристики могут существенно разниться в зависимости от патогенеза и типа сосудистой КР:
– для «подкорковых» сосудистых КР (в рамках «болезни малых сосудов», хронической ишемии головного мозга), которые являются наиболее распространенным вариантом, характерно флюктуирующее течение с эпизодами ухудшения или улучшения состояния, при этом не исключено формирование плато различной продолжительности;
– для постинсультных КР, как правило, типично острое начало, в большинстве случаев связанное по времени с острым нарушением мозгового кровообращения (ОНМК), с последующим стационарным течением, хотя не исключена как положительная, так и отрицательная динамика [1].
3
• Одни из наиболее характерных и ранних когнитивных симптомов «подкорковых» сосудистых КР (в рамках хронической ишемии мозга) – нарушения концентрации внимания и трудности поддержания интеллектуальной активности в течение необходимого времени. Пациенты не могут правильно организовать свою деятельность, часто оставляют начатое дело, быстро устают, не могут одновременно работать с несколькими источниками информации или быстро переходить от одной задачи к другой. Трудности могут возникать при анализе информации, выделении главного и второстепенного, определении сходств и различий между понятиями, построении алгоритма деятельности. При этом сами пациенты жалуются на общую слабость и повышенную утомляемость, иногда «неясность и тяжесть в голове». Нарушения памяти в этом случае связаны с недостаточностью активного воспроизведения информации при сохранности ее запоминания и хранения. Первичные (корковые) нарушения праксиса, гнозиса и речи для «подкорковых» сосудистых КР не характерны [1].
• При «подкорковом» варианте сосудистой деменции практически всегда наблюдаются двигательные расстройства, представленные в первую очередь нарушениями походки. Пациенты при этом часто жалуются на «головокружение», называя этим словом неустойчивость при ходьбе, особенно при поворотах [1].
• Другие типичные некогнитивные «спутники» сосудистых КР, не связанных с ОНМК, – абулия, депрессия или недержание аффекта, раннее присоединение недержания мочи, императивных позывов на мочеиспускание в отсутствие урологических заболеваний [1].
• Для постинсультных сосудистых КР в целом крайне характерны такие некогнитивные нервно-психические расстройства, как апатия, депрессия, тревога, нарушения сна. Единичные инфаркты мозга могут сопровождаться выраженными нарушениями в виде апатико-абулического синдрома, агрессии, депрессии, бредовых проявлений, в ряде случаев имитируя картину делирия [1].
• При сборе анамнестических сведений пациентов с предполагаемыми сосудистыми КР рекомендуется уделить особое внимание сопутствующим признакам цереброваскулярных заболеваний (ЦВЗ), сосудистым факторам риска и информации, свидетельствующей о возможных эпизодах ОНМК: УУР – В, УДД – 2 [1]. К важнейшим факторам риска сосудистых КР, включая сосудистую деменцию, относятся сахарный диабет (СД), курение, артериальная гипертензия (АГ), фибрилляция предсердий, ожирение, гиподинамия, депрессия, высокий уровень холестерина, атеросклероз, ишемическая болезнь сердца, нарушения сердечного ритма, высокий уровень гомоцистеина. Соответствующая информация может быть получена как из медицинской документации, так и из беседы с пациентом и информантами [1].
• На возможные эпизоды ОНМК, даже в отсутствии диагностированных ранее инсультов, может указывать острое возникновение некогнитивных неврологических симптомов с возможным их последующим регрессом. Для постинсультных сосудистых КР характерно появление когнитивных нарушений не позднее 6 мес от развития ОНМК. Для оценки связи между усугублением КР после развития инсульта у пожилых пациентов возможно использование опросников, например IQCODE [1].
• У всех пациентов с КР и при необходимости у информантов рекомендуется уточнять сопутствующую медикаментозную терапию для выявления полипрагмазии и препаратов, потенциально негативно влияющих на выраженность когнитивных нарушений: УУР – В, УДД – 2 [1]. К лекарственным средствам, которые могут вызывать ухудшение когнитивных функций, относятся антихолинергические препараты, трициклические антидепрессанты, нейролептики, барбитураты, производные бензодиазепина, антигистаминные средства, некоторые бета-блокаторы, липофильные статины (ловастатин, симвастатин, питавастатин), сердечные гликозиды и др. [1]. При сопутствующем приеме таких препаратов пациентом с КР требуется оценить необходимость их использования и по возможности выполнить их отмену или же заменить средствами без негативного влияния на познавательную сферу [1].
• Полипрагмазия (прием ≥5 лекарств) даже без использования препаратов с негативным влиянием на когнитивную сферу сама по себе ассоциирована со значимым риском КР. Учитывая возможные нарушения памяти и внимания, для должной оценки медикаментозного анамнеза пациента следует просить предоставить список принимаемых лекарств в письменном виде с указанием их доз, частоты и длительности приема [1].
4
• Всем пациентам с КР рекомендуется полное физикальное обследование для исключения соматической патологии, потенциально способствующей усугублению состояния пациента или даже развитию когнитивных нарушений: УУР – С, УДД – 4 [1]. Оценку коморбидных заболеваний необходимо проводить как при первичной постановке диагноза, так и развитии эпизодов ухудшения когнитивных нарушений или появлении симптомов некогнитивных нервно-психических расстройств. Особенно часто коморбидные заболевания встречаются у лиц пожилого и старческого возраста; они могут быть причиной быстрого ухудшения когнитивного и функционального статуса пациента. В случае сосудистых КР частыми сопутствующими или провоцирующими патологиями и медицинскими состояниями выступают сердечно-сосудистые заболевания, СД, недержание мочи. Важный фактор риска КР в целом и деменции в частности – старческая астения, вследствие чего требуются ее прицельное выявление и оценка степени тяжести [1].
• Всем пациентам с КР рекомендуется тщательный неврологический осмотр с целью уточнения нозологической принадлежности таких расстройств: УУР – С, УДД – 4 [1].
У пациентов с предполагаемым сопутствующим ЦВЗ необходимо детальное исследование неврологического статуса, позволяющее выявить очаговую неврологическую симптоматику. При этом должное внимание нужно уделить пальпации и аускультации магистральных артерий головы [1].
• Большое значение при осмотре пациентов с КР имеют правильная оценка тонуса мышц, признаков пирамидных и экстрапирамидных нарушений, ходьбы и поддержания равновесия, тазовой дисфункции (недержание мочи, запоры) [1].
5
• Рекомендуется выполнять скрининг когнитивного статуса у пациентов с жалобами на забывчивость, рассеянность, трудности при подборе слов (или при наличии жалоб со стороны родственников/ухаживающих на снижение памяти и ограничения функционирования пациента): УУР – С, УДД – 2 [1].
• В рутинной практике врачей первичного звена, в частности терапевтов, при наличии у пациента признаков выраженного КР возможно использование шкалы Мини-Ког как одной из самых удобных и малозатратных по времени (табл. 2). Она помогает в предварительной (беглой) оценке степени несомненных когнитивных нарушений (умеренная КР/деменция).

• Следует учитывать, что шкала Мини-Ког нечувствительна к недементным КР. При необходимости скрининга у пациентов без выраженного когнитивного снижения в отсутствии значимых изменений функционального статуса возможно использовать шкалы MMSE или MoCA-тест [1].
6
При несомненных и выраженных когнитивных нарушениях у пациента шкала Мини-Ког способна помочь врачам первичного звена в маршрутизации пациентов (табл. 3) [1].
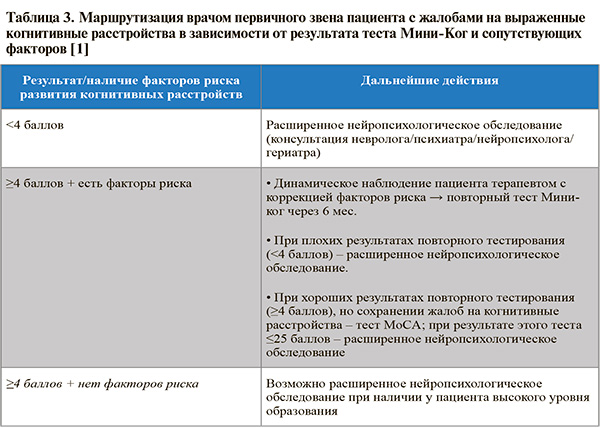
7
• Всем пациентам с КР для исключения сопутствующих состояний, усугубляющих тяжесть когнитивных нарушений, рекомендуется выполнение общих анализов мочи и крови, общетерапевтического биохимического анализа крови (с оценкой глюкозы, общего белка, общего билирубина, АЛТ, АСТ, креатинина, мочевины, уровней натрия, калия, кальция): УУР – В, УДД – 2 [1]. Рутинные анализы мочи и крови позволяют исключить ряд состояний, которые могут быть как самостоятельной причиной КР, так и способствовать их усугублению. Среди них анемия, гемобластозы, инфекционные заболевания, почечная и печеночная недостаточность, электролитные нарушения, в том числе связанные с приемом лекарственных средств, в частности гипонатриемия [1].
• У всех пациентов с КР рекомендуется исследование гликированного гемоглобина (Hb1Ac) для выявления ранних форм нарушения сахарного обмена: УУР – С, УДД – 4 [1]. Распространенность когнитивных нарушений при СД 2 составляет 20% у мужчин и 18% у женщин 60 лет [3], при этом СД 2 связан с 50% увеличением риска развития деменции [4]. Консенсусное мнение ведущих мировых экспертов сводится к необходимости оценки уровня глюкозы крови натощак у всех пациентов с КР. При этом все больше данных когортных исследований свидетельствуют о целесообразности диагностики нарушений углеводного обмена на более ранних стадиях, когда уровень глюкозы натощак может оставаться нормальным. Таким образом, у пациентов с КР целесообразно исследовать не только уровень глюкозы, но и Hb1Ac [1].
• Для исключения потенциально курабельных состояний у всех пациентов с КР рекомендуется определение тиреоидного профиля с исследованием уровней свободного тироксина и тиреотропного гормона в сыворотке крови, а также уровней витамина В12 и фолиевой кислоты: УУР – В, УДД – 2 [1]. Как гипо-, так и гипертиреоз ассоциированы с нарушением когнитивных функций, поэтому у всех пациентов с КР, особенно при клинических проявлениях тиреоидной дисфункции, требуется исследование гормонов щитовидной железы. Снижение концентрации витамина В12 менее 250 пмоль/л ассоциировано с риском развития выраженных КР, включая сосудистую деменцию. Концентрации менее 150 пмоль/л непосредственно связаны с развитием когнитивных нарушений. Поскольку дефицит витамина В12 и фолиевой кислоты часто обнаруживается у лиц старшего возраста, исследование концентрации этих витаминов в крови следует выполнять у всех пациентов с КР пожилого и старческого возраста [1].
• Всем пациентам с КР рекомендуется определение концентрации гомоцистеина в крови для исключения гипергомоцистеинемии: УУР – В, УДД – 3 [1]. Скрининг концентрации гомоцистеина оправдан в связи с важной ролью этого маркера в формировании КР, низкой стоимостью метода, а также простоты терапии гипергомоцистеинемии [1].
• Пациентам с ЦВЗ и предполагаемым сосудистым КР для выявления дислипидемии рекомендуется биохимический анализ крови по оценке нарушений липидного обмена (исследование общего холестерина, триглицеридов, ЛПНП, ЛПВП, коэффициента атерогенности): УУР – В, УДД – 3 [1]. Метаанализ исследований не показал определенной взаимосвязи между величиной общего холестерина крови и его фракций в позднем периоде жизни и прогрессированием когнитивных нарушений и сосудистой деменции, однако гиперхолестеринемия выступает общеизвестным сосудистым фактором риска и напрямую связана с риском ЦВЗ [1, 5]. Таким образом, эта рекомендация носит условный характер и должна рассматриваться в клиническом контексте конкретного пациента [1].
• Пациентам с подозрением на сосудистые КР вследствие перенесенного ишемического инсульта рекомендуется рассмотреть необходимость ориентировочного исследования системы гемостаза для исключения возможной коагулопатии: УУР – С, УДД – 5 [1]. Наряду с прочим контроль показателей свертываемости крови может потребоваться части пациентов с сосудистыми КР, получающих варфарин (контроль МНО) [1].
8
• Всем пациентам с подозрением на сосудистые КР рекомендуется выполнение структурной нейровизуализации с использованием магнитно-резонансной томографии (МРТ) или компьютерной томографии (КТ) головного мозга для подтверждения наличия и уточнения тяжести патологических изменений головного мозга, а также соответствия их клинической картине: УУР– А, УДД – 1 [1]. При сосудистых КР нейровизуализационные методы играют во многом ключевую роль в постановке диагноза; отсутствие типичных для разных типов сосудистого КР очаговых изменений по данным МРТ или КТ головного мозга исключает диагноз.
• Изображения КТ и МРТ головного мозга при сосудистых КР во многих случаях характеризуются наличием множественных корковых и/или подкорковых ишемических очагов (мультиинфарктная деменция), при этом для развития функциональных расстройств имеет значение как общий объем поврежденного мозгового вещества, так и локализация повреждений. Однако чаще сосудистая деменция вызывается поражением малых сосудов, классическими радиологическими маркерами которого служат лакунарные инфаркты в подкорковом белом и сером веществе и гиперинтенсивный сигнал от белого вещества перивентрикулярных и субкортикальных областей («лейкоареоз»), считающийся клинически значимым при распространении не менее чем на 25% белого вещества [1].
• Необходимо помнить, что само по себе выявление «сосудистых» очагов на МРТ/КТ не позволяет исключить сопутствующего нейродегенеративного процесса. Таким образом, «чистые» сосудистые КР могут быть диагностированы, если очаговые нейровизуализационные изменения полностью объясняют имеющуюся у пациента клиническую симптоматику [1].
9
• Для скрининговой оценки нейропсихологического статуса пациентов с подозрением на сосудистое КР рекомендуется использовать МоСА-тест: УУР– А, УДД – 1 [1]. Для пациентов с сосудистым КР основным нейропсихологическим феноменом является преобладание нарушений управляющих функций и нейродинамические расстройства. Систематический обзор эффективности применения различных методик при сосудистой КР показал, что наибольшей информативностью для данной популяции пациентов обладает именно МоСА-тест [1, 6].
• При развитии КР у пациентов, перенесших инсульт, для оценки доинсультного состояния когнитивной сферы возможно применение опросника IQCODE: УУР– В, УДД – 1 [1]. Этот опросник относится к методикам, основанным на сведениях, получаемых от третьих лиц (информанта), и широко используется как для диагностики КР, так и исключения когнитивной дисфункции у здоровых лиц пожилого и старческого возраста. Применение данного опросника в диагностике постинсультных КР позволяет предположить «смешанный» характер когнитивных нарушений (сочетание последствий ОНМК с предсуществующим хроническим цереброваскулярным заболеванием, или нейродегенеративным процессом, или комбинацией этих состояний). Применение IQCODE ограничено потребностью в надежном информанте, затратностью по времени применения, низкой специфичностью (не позволяет достоверно оценить генез предсуществующего инсульту КР). Однако, несмотря на это, рекомендация по использованию IQCODE в клинической практике может быть оправдана потребностью в выявлении лиц, перенесших инсульт с развитием КР смешанного генеза, поскольку для них характерна большая тяжесть когнитивных и функциональных нарушений, более высокая частота некогнитивных нервно-психических расстройств, делирия, что требует более высоких медицинских и социальных ресурсов для их ведения [1].
10
• В 2014 г. рабочей группой Международного общества по сосудистым поведенческим и когнитивным расстройствам (VASCOG) были сформулированы новые диагностические критерии сосудистых КР. Согласно им, на первом этапе необходимо подтвердить у пациента наличие либо деменции, либо умеренного (недементного) КР (табл. 4). На втором этапе подтверждается именно сосудистая этиология выявленного КР (табл. 5).
• Критерии исключения сосудистых КР [1, 7]:
– раннее присоединение нарушений памяти и прогрессирующее нарастание дефекта со стороны памяти, а также таких когнитивных функций, как речь (транскортикальная сенсорная афазия), двигательных навыков (апраксия) и восприятия (агнозия), в отсутствии соответствующих очаговых нейровизуализационных изменений или типичного сосудистого анамнеза;
– раннее возникновение выраженного синдрома паркинсонизма, типичного для деменции с тельцами Леви;
– анамнез, крайне характерный для какого-либо другого первично неврологического заболевания (рассеянный склероз, энцефалит, токсическая или метаболическая энцефалопатия и т.д.), достаточного для объяснения наблюдаемых когнитивных нарушений;
– отсутствие очаговых изменений при КТ или МРТ головного мозга либо их минимальная выраженность;
– большое депрессивное расстройство с наличием временной взаимосвязи между появлением когнитивного дефекта и вероятного развития депрессии;
– токсические и метаболические нарушения, подтвержденные специфическим клинико-лабораторным обследованием.


Лечение
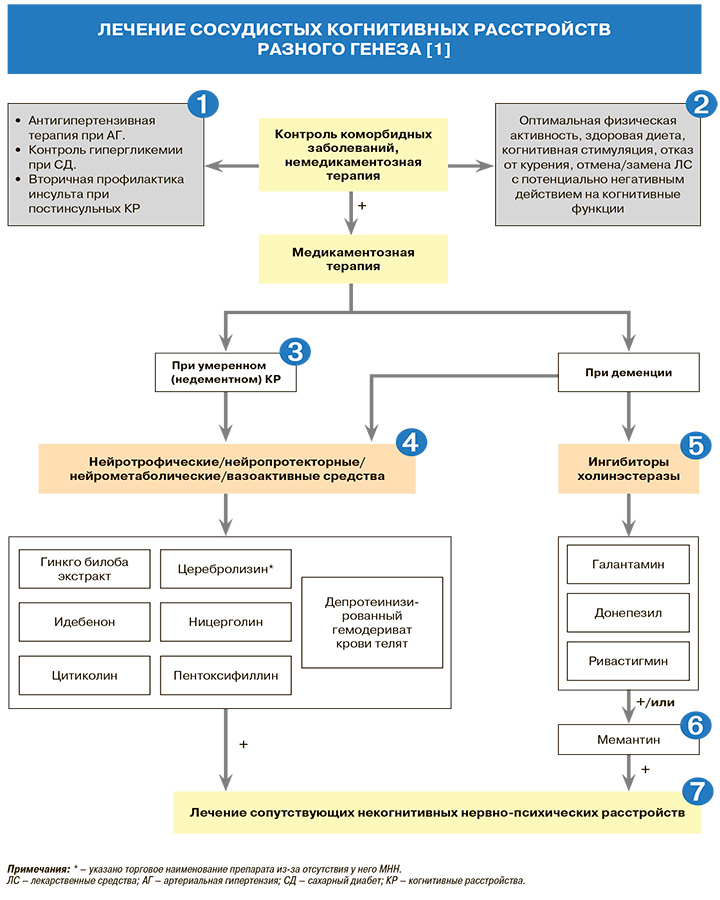
1
• Пациентам с сосудистым КР рекомендуется назначение антигипертензивной терапии с целью предупреждения дальнейшего прогрессирования когнитивного дефекта: УУР – С, УДД – 3 [1, 9, 10].
• АГ выступает важным фактором риска сосудистого КР. Несмотря на отсутствие прямых исследований антигипертензивной терапии у пациентов с недементными расстройствами, косвенный вывод о целесообразности ее применения может быть сделать на основе предварительных результатов рандомизированного контролируемого исследования (РКИ) SPRINT-MIND, в котором было показано преимущество более строгого контроля артериального давления (АД) с позиции прогрессирования когнитивных нарушений до умеренного уровня или даже деменции [1, 11]. У пациентов, перенесших инсульт, адекватная антигипертензивная терапия необходима для предотвращения повторных ОНМК и, таким образом, предотвращения усугубления имеющегося сосудистого КР и формирования сосудистой деменции [1].
• При деменции назначение антигипертензивных средств должно осуществляться исходя из общего состояния пациента, а также с учетом рисков, ассоциированных с такой терапией вообще и полипрагмазией в частности (ортостатическая гипотензия, делирий и т.д.) [1].
• При умеренном КР с сопутствующим СД рекомендуется должный контроль гипергликемии с целью предотвращения прогрессирования когнитивных нарушений: УУР – С, УДД – 5 [1, 12]. СД относится к важным факторам риска КР любой степени. Повышение HbA1c более 7% (начало субкомпенсации) сопряжено с 5-кратным повышением риска деменции [13]. Это свидетельствует о важности гликемического контроля у пациентов с КР различного генеза, включая сосудистые КР.
• У пациентов с постинсультными сосудистыми КР в целях предотвращения прогрессирования когнитивных нарушений рекомендуется проведение вторичной профилактики инсульта в соответствии с актуальной клинической практикой: УУР – В, УДД – 2 [1]. Объем вторичной медикаментозной профилактики ОНМК должен определяться его типом и профилем сопутствующих заболеваний [1].
2
• Всем пациентам с умеренным КР рекомендуется оптимальная физическая активность с целью улучшения общего состояния когнитивной сферы: УУР – А, УДД – 1 [1]. Результаты систематических обзоров свидетельствуют о том, что наибольшим преимуществом обладают мультимодальные тренировки, включающие аэробную и силовую нагрузку [1, 14].
• Всем пациентам с умеренным КР в целях улучшения повседневной активности рекомендуется выполнять упражнения для стимуляции когнитивных функций (когнитивный тренинг): УУР – А, УДД – 1 [1]. Когнитивная стимуляция у пациентов может осуществляться как путем активных упражнений (когнитивного тренинга), так и за счет поддержания высокого уровня бытовой, социальной и профессиональной активности. Предполагается, что у пациентов с умеренным КР когнитивная стимуляция позволяет более интенсивно задействовать когнитивный резерв. Согласно систематическим обзорам, желательные эффекты такого вмешательства существенно превышают возможные риски и, таким образом, могут быть рекомендованы всем пациентам с умеренным КР [1, 15].
• Проведение когнитивного тренинга рекомендуется и пациентам с деменцией легкой степени: УУР – А, УДД – 1 [1]. В то же время этот метод не рекомендован на стадии тяжелой деменции из-за низкой эффективности, так как он предполагает сохранную способность к восприятию информации и понимание инструкций, которые на поздних стадиях бывают уже утрачены [1].
• Всем пациентам с умеренным КР для предупреждения прогрессирования КР рекомендуется придерживаться здоровой («средиземноморской») диеты: УУР – В, УДД – 2 [1].
«Средиземноморский стол» подразумевает употребление большого количества свежих овощей и фруктов (за исключением крахмалистых), рыбы и морепродуктов, кисломолочных, цельнозерновых продуктов, орехов, растительных масел, содержащих полиненасыщенные жирные кислоты при одновременном ограничении свободных сахаров (<5–10% от общей суточной калорийности) и жиров (<30% от общей суточной калорийности). Однако превентивный эффект подобных вмешательств наблюдается только при строгом соблюдении принципов питания [1].
• С целью предотвращения нарастания когнитивного дефицита всем пациентам с недементными когнитивными нарушениями рекомендуется отказ от курения: УУР – С, УДД – 5 [1]. Существует значительное количество эпидемиологических исследований, включая метаанализы, указывающих на связь между курением (особенно у лиц, продолжающих курить на момент анализа) и риском деменции любой этиологии [1, 12].
• Всем пациентам с КР по мере возможности рекомендуется отмена препаратов с потенциально негативным действием на когнитивные функции: УУР – С, УДД – 5 [1]. Стоит учитывать, что КР могут быть прямым следствием приема препаратов с седативным и холинолитическим действием, что подчеркивает важность анализа и при возможности коррекции сопутствующей медикаментозной терапии [1]. Группы лекарственных средств с потенциальным негативным влиянием на когнитивную сферу указаны в пункте 3 раздела «Диагностика. Комментарии».
• Всем пациентам с деменцией легкой и умеренной степенью тяжести рекомендуется эрготерапия: УУР – В, УДД – 1 [1]. Она позволяет обучить пациента и ухаживающее лицо компенсации когнитивных нарушений и самообслуживанию, что, в свою очередь, упорядочивает поведение и продлевает автономию пациента, снижая нагрузку на опекуна [1]. В метаанализе исследований, посвященных изучению эффектов эрготерапии при деменциях различной нозологии, были показаны ее достоверное выраженное положительное влияние на качество жизни пациентов и ухаживающих за ними лиц, а также на функциональный статус пациентов по сравнению с рутинным уходом [1, 16].
3
Пациентам с недементными КР, в отличие от пациентов с деменцией, НЕ рекомендуется рутинное применение антихолинэстеразных средств (ингибиторов холинэстеразы): УУР – В, УДД – 2 [1]. В РКИ различных антихолинэстеразных препаратов (донепезила, ривастигмина, галантамина) не удалось показать их эффективность при умеренных КР с позиции сроков развития последующей деменции. Кроме того, в терапевтических группах была достоверно повышена частота нежелательных явлений со стороны желудочно-кишечного тракта и сердца [17–19]. В совокупности это не позволяет рекомендовать подобную терапию в рутинной практике при ведении пациентов с умеренными КР. Однако, поскольку граница между синдромом умеренных КР и легкой деменцией не всегда отчетлива, при решении вопроса о назначении антихолинэстеразных средств требуется тщательный анализ конкретной клинической ситуации [1].
4
• Для уменьшения выраженности субъективных симптомов и сопутствующих некогнитивных нарушений у пациентов с умеренными КР рекомендуется назначение экстракта листьев гинкго двулопастного: УУР – В, УДД – 2 [1, 20]. В нескольких небольших РКИ стандартизированного гинкго двулопастного листьев экстракта у пациентов с умеренными КР наблюдалось уменьшение мнестических нарушений, тревожности, улучшении концентрации внимания, а также был отмечен благоприятный профиль соотношения ожидаемой выгоды и неблагоприятных эффектов. В этих исследованиях препарат гинкго двулопастного листьев экстракт применялся в дозе 120 мг 2 раза/сут на протяжении до 24 нед. [1].
• Экстракт листьев гинкго двулопастного (240 мг/сут) рекомендован также для уменьшения выраженности когнитивной дисфункции и улучшения повседневной активности пациентам с сосудистой деменцией: УУР – В, УДД – 1 [1, 21]. Отдельных исследований терапии гинкго двулопастного листьев экстрактом при сосудистой деменции не проводилось, однако в ряде рандомизированных плацебо-контролируемых исследований этого лекарственного средства при легкой или умеренной деменции в изучаемую популяцию, помимо пациентов с болезнью Альцгеймера, входили и больные с сосудистой деменцией [1].
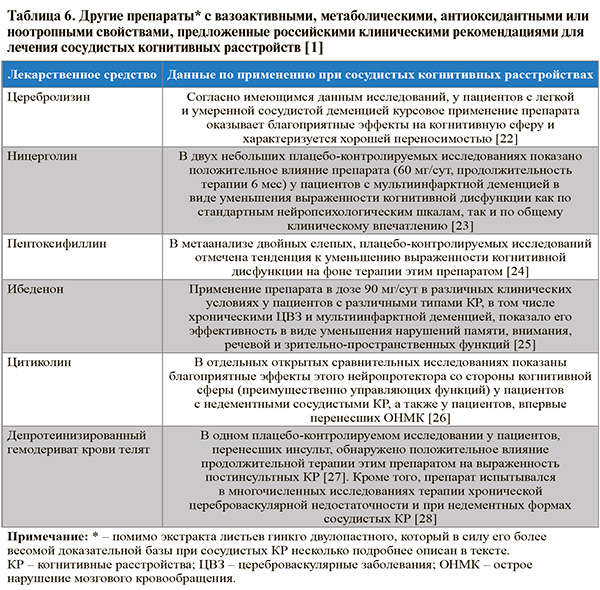
• Некоторые данные о других препаратах с вазоактивными, метаболическими, антиоксидантными или ноотропными свойствами, которые предложены российскими клиническими рекомендациями для лечения сосудистых КР, представлены в таблице 6.
5
Для коррекции когнитивного дефицита пациентам с сосудистой деменцией рекомендуется назначение антихолинэстеразных средств (ингибиторов холинэстеразы): УУР – B, УДД – 1 [1, 29]. Применение препаратов этой группы (донепезил, ривастигмин, галантамин) базируется на данных о наличии ацетилхолинергической недостаточности при сосудистой деменции и роли этого нейротрансмиттерного дефицита в формировании когнитивных нарушений. Причиной развития ацетилхолинергической недостаточности является характерное для церебральной микроангиопатии поражение перивентрикулярного белого вещества, в котором проходят основные ацетилхолинергические проводники в кору мозга из ядра Мейнерта [1].
6
• Для коррекции когнитивного дефицита и улучшения общего функционирования пациентам с сосудистой деменцией рекомендуется назначение мемантина: УУР – В, УДД – 1 [1, 29]. Целесообразность применения этого средства связана с повышением активности глутаматергической системы в условиях ишемии и гипоксии. Терапия мемантином способствует уменьшению выраженности типичных для сосудистых КР клинических проявлений, включая нарушение концентрации внимания и нейродинамические расстройства. В систематическом обзоре исследований с анализом различных патогенетических вариантов сосудистых КР было показано, что эффективность мемантина может быть выше при подкорковом типе сосудистой деменции. Препарат имеет лучшую переносимость по сравнению с ингибиторами холинэстеразы и может служить препаратом выбора у пациентов с сосудистыми КР, учитывая токсические эффекты антихолинэстеразных средств со стороны сердечно-сосудистой системы [1].
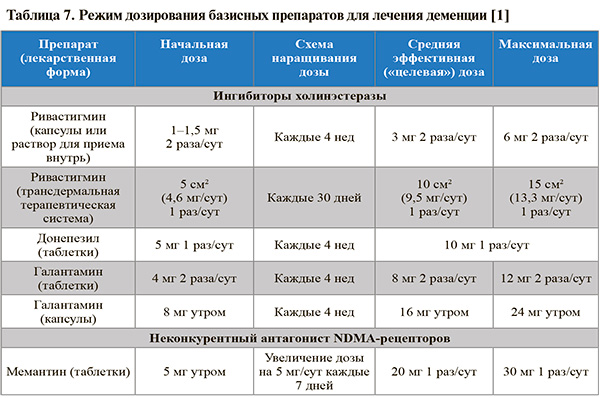
• Режимы дозирования ингибиторов холинэстеразы и мемантина при деменции отражены в таблице 7. Добавим, что, помимо монопрепаратов, в России также представлена фиксированная комбинация донепезила и мемантина (дозировки 10 мг + 5 мг, 10 мг + 10 мг, 10 мг + 15 мг и 10 мг + 20 мг) [30].
• При лечении КР различного генеза возможно использование и других ноотропных средств, применяемых при недементных КР [1].
7
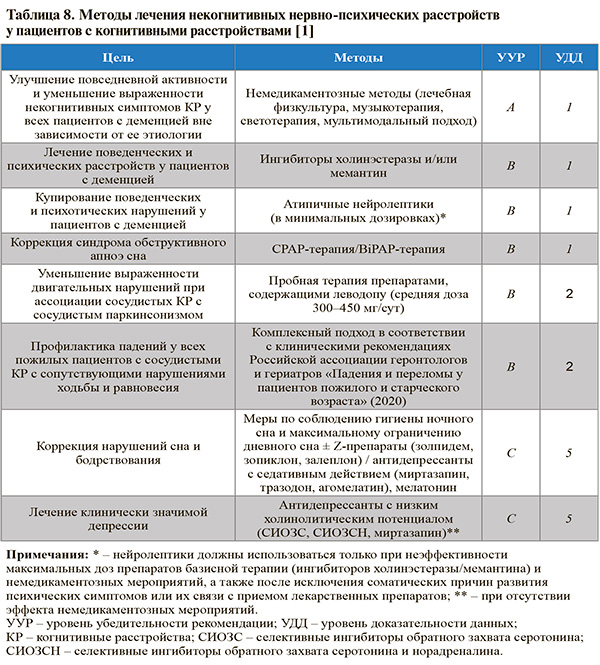
• Методы лечения некогнитивных нервно-психических расстройств у пациентов с КР обобщены в таблице 8. При появлении у пациентов с деменцией психотических расстройств (бредовых, галлюцинаторных, делирия), агрессивного поведения, возбуждения, необходимо проведение тщательного обследования для исключения внешних провокаторов (включая неадекватное ситуации поведение лиц, окружающих пациента), присоединившейся соматической патологии или декомпенсации имеющихся соматических заболеваний (патологии сердечно-сосудистой системы, СД, инфекции мочевыводящих или дыхательных путей и т.п.). Необходимо также проанализировать принимаемые пациентом препараты для исключения медикаментозной интоксикации и эффектов холинолитического спектра. Для коррекции поведенческих и психических нарушений в первую очередь должны применяться немедикаментозные методы [1].
8
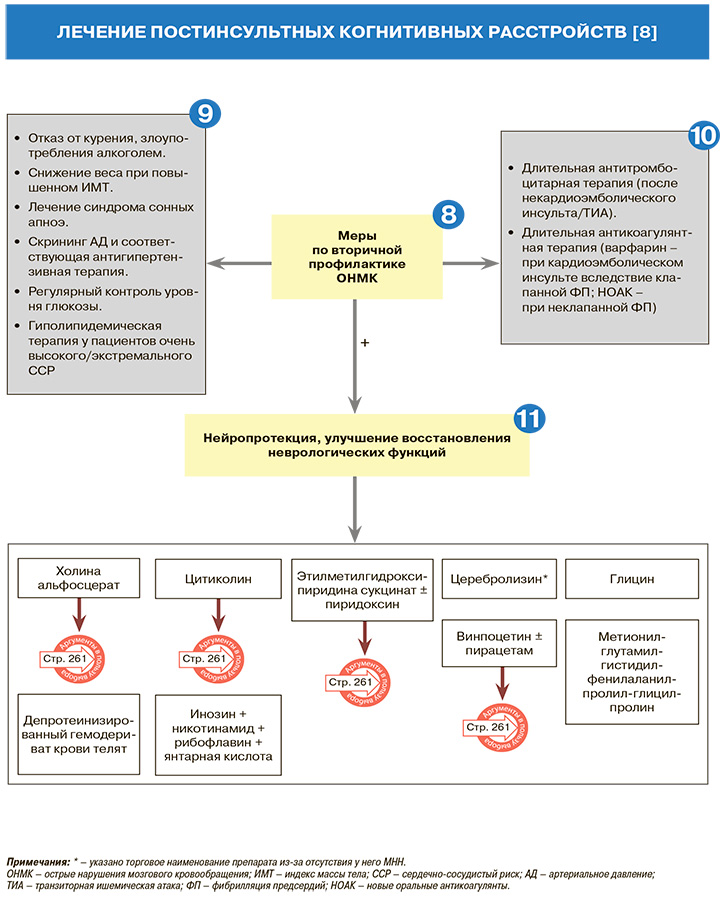
• Как уже отмечалось выше (см. пункт 1), при постинсультных сосудистых когнитивных расстройствах во избежание их нарастания необходимо проведение вторичной профилактики инсульта. При этом рекомендуется раннее (не позднее 48 ч после ОНМК) начало вторичной профилактики ишемического инсульта/транзиторной ишемической атаки (ТИА): УУР – С, УДД – 5 [8].
• У пациентов, перенесших ишемический инсульт или ТИА, риск развития повторных инсультов повышен почти в 10 раз и составляет около 25–30%. Риск повторного инсульта наиболее высок в первые несколько недель от его развития, повторной ТИА – в течение первых трех дней [8].
9
• В рамках нелекарственных мер вторичной профилактики ишемического инсульта рекомендованы отказ от курения (УУР – С, УДД – 5) и злоупотребления алкоголем (УУР – С, УДД – 5), диета для снижения веса у лиц с повышенным индексом массы тела (УУР – С, УДД – 5), лечение расстройств дыхания во сне (сонных апноэ) при помощи чрезмасочной аппаратной СРАР-терапии (УУР – С, УДД – 5) [8].
• Для снижения риска повторного ОНМК рекомендуются скрининг АД и соответствующая антигипертензивная терапия: УУР – С, УДД – 5 [8].
• В целях антигипертензивной терапии в данном случае могут быть использованы различные классы профильных лекарственных средств с учетом индивидуальных особенностей; при этом рекомендуется включение в терапию диуретиков, комбинации диуретика и ингибитора АПФ. Применение блокатора рецепторов ангиотензина II эпросартана более эффективно во вторичной профилактике ишемического инсульта и ТИА, чем блокатора кальциевых каналов нитрендипина. Для пациентов с АГ, СД или заболеванием почек рекомендуются целевые значения АД <130/80 мм рт.ст. [8].
• Рекомендуется регулярно контролировать уровень глюкозы с достижением уровня глюкозы, близкого к нормальному (5,6 ммоль/л). Коррекцию гликемии рекомендуется сочетать с гипоуглеводной диетой и повышением физической активности, назначением индивидуальной фармакотерапии: УУР – С, УДД – 2 [8].
• С целью уменьшения риска острых ишемических событий и прогрессирования атеросклеротического процесса рекомендуется назначение гиполипидемической терапии с терапевтическим режимом, при котором достигается снижение уровня холестерина липопротеидов низкой плотности (ХС ЛНП) ≥50% по сравнению с исходным уровнем, а уровень этого показателя не превышает ≤1,4 ммоль/л для пациентов, перенесших ОНМК и относящихся к категории очень высокого риска сердечно-сосудистых заболеваний. Для пациентов экстремального риска рекомендовано достижение целевого уровня ХС ЛНП как минимум <1,4 ммоль/л (при оптимальных значениях ≤1,0 ммоль/л): УУР – В, УДД – 1 [8].
• До начала гиполипидемической терапии важно уточнить причину дислипидемии. Гиполипидемические средства включают ингибиторы ГМГ-КoA-редуктазы (статины), ингибиторы всасывания холестерина в кишечнике, ингибиторы PCSK9 (пропротеиновой конвертазы субтилизин-кексинового типа 9), фибраты, препараты, содержащие омега-3 полиненасыщенные жирные кислоты. Схема лечения, при которой достигаются цели лечения у пациентов очень высокого сердечно-сосудистого риска (снижение уровня ХС ЛНП ≥50% по сравнению с исходным и целевые значения ХС ЛНП ≤1,4 ммоль/л), как правило, включает интенсивную монотерапию статинами. Суточная доза препаратов этой группы при интенсивной терапии для снижения ХС ЛНП ≥ 50% составляет 40 – 80 мг для аторвастатина и 20–40 мг для розувастатина. Терапия статинами должна быть назначена не позднее первых трех дней от эпизода ишемического инсульта. Ответ пациента на терапию статинами рекомендуется оценивать через 6–8 нед после начала приема/изменения дозы препарата. Если целевой уровень ХС ЛНП в соответствии с категорией риска при монотерапии статинами не достигнут, следует рассмотреть возможность комбинированной терапии [8]. Более подробное направление терапии дислипидемии в зависимости от уровня кардиоваскулярного риска, включая очень высокий и экстремальный риск, подробно рассмотрены в теме сборника «Нарушения липидного обмена» (стр. 88-110).
10
• Пациентам, перенесшим некардиоэмболический ишемический инсульт/ТИА, рекомендуется длительное проведение антитромбоцитарной терапии с целью вторичной профилактики ОНМК по ишемическому типу, а также других сосудистых событий: УУР – В, УДД – 1 [8].
• Выбор схемы антитромбоцитарной терапии индивидуален и зависит от профиля факторов риска пациента, особенностей клинической ситуации (наличие фоновых и сопутствующих заболеваний, включая сосудистую коморбидность), а также стоимости препаратов и приверженности пациента к лечению. При отсутствии специальных показаний у пациентов (например, ишемической болезни сердца/острого коронарного синдрома, операций коронарной реваскуляризации), требующих назначения двойной антитромботической терапии (ДАТТ), включающей ацетилсалициловую кислоту (АСК) в комбинации с различными ингибиторами P2Y12-рецепторов, обычно назначается:
– монотерапия АСК в дозе от 75 до 300 мг/сут или клопидогрелом в дозе 75 мг/сут;
– ДАТТ АСК в дозе 25 мг и дипиридамолом 200 мг с модифицированным высвобождением 2 раза/сут [8].
Небольшое преимущество клопидогрела над ацетилсалициловой кислотой наиболее значимо у пациентов с СД, мультифокальным атеросклерозом [8].
• Пациентам, перенесшим кардиоэмболический инсульт вследствие клапанной фибрилляции предсердий (механические клапаны сердца, митральный стеноз средней/тяжелой степени, биологические протезы в первые 6 мес после установки) с целью профилактики повторных ТИА/ишемических инсультов, рекомендуется назначение варфарина. Терапевтический диапазон международного нормализованного отношения (МНО) составляет 2,0–3,0. При этом назначение новых оральных антикоагулянтов (НОАК) таким пациентам не показано. Целевые значения МНО у пациентов с механическими протезами клапанов сердца могут быть выше в зависимости от вида протеза, его позиции и наличия дополнительных факторов риска тромбоэмболических осложнений: УУР – В, УДД – 1 [8].
• У пациентов с фибрилляцией предсердий и механическим протезом клапанов сердца в митральной позиции целевые значения МНО при назначении варфарина должны составлять 2,5–3,5. Для пациентов с фибрилляцией предсердий и ревматическим поражением митрального клапана и/или механическими клапанными протезами в настоящее время единственным методом лечения с доказанной безопасностью является терапия антагонистами витамина К (варфарином) [8].
• У пациентов с неклапанной фибрилляцией предсердий рекомендуется профилактика повторных ТИА/ишемических инсультов препаратами из группы НОАК (прямыми ингибиторами тромбина и прямыми ингибиторами фактора Xa), которые не уступают по эффективности варфарину, но имеют более низкую частоту внутричерепных кровотечений. Применение НОАК, в отличие от варфарина, не требует регулярного контроля МНО: УУР – В, УДД – 1 [8]:
• Режимы применения НОАК для профилактики ОНМК [8]:
– дабигатрана этексилат – по 150 или 110 мг/сут (при клиренсе креатинина 30–50 мл/мин) 2 раза/сут;
– ривароксабан – по 20 или 15 мг (при клиренсе креатинина 30–50 мл/мин) 1 раз/сут;
– апиксабан – по 5 или 2,5 мг (при наличии ≥2 из нижеперечисленных критериев: возраст ≥80 лет, вес ≤60 кг, уровень креатинина ≥133 ммоль/л) 2 раза/сут.
• Если пациенту не показана антикоагулянтная терапия, вторичную профилактику ОНМК необходимо проводить ингибиторами агрегации тромбоцитов [8].
11
В схеме приведены нейротропные лекарственные средства, включенные в клинические рекомендации Минздрава России по лечению ишемического инсульта/ТИА и имеющие среди показаний острый/восстановительный период инсульта, когнитивные нарушения сосудистого генеза [8, 30].
12
• Рекомендуется назначение этилметилгидроксипиридина сукцината пациентам среднего, пожилого и старческого (до 80 лет) возраста, перенесшим ишемический инсульт в каротидной системе, с наличием легкого, умеренного и тяжелого неврологического дефицита (NIHSS 5–20 баллов) с целью улучшения восстановления неврологических функций: УУР – А, УДД – 2 [8]. Препарат является ингибитором свободно-радикальных процессов и мембранопротектором, оказывает позитивное влияние на реологические показатели крови, уменьшает эндотелиальную дисфункцию и улучшает параметры липидного спектра, подавляет перекисное окисление липидов, увеличивает активность супероксиддисмутазы, повышает соотношение «липид–белок», уменьшает вязкость мембраны, увеличивает ее текучесть. Модулирует активность мембраносвязанных ферментов (Ca2+-независимой фосфодиэстеразы, аденилатциклазы, ацетилхолинэстеразы), рецепторных комплексов (бензодиазепинового, ГАМК, ацетилхолинового), что способствует их связыванию с лигандами, сохранению структурно-функциональной организации биомембран, транспорта нейромедиаторов и улучшению синаптической передачи [8].
• Этилметилгидроксипиридина сукцинат назначают по схеме: внутривенно капельно по 500 мг/сут в течение первых 10 сут от эпизода ишемического инсульта, далее – перорально по 125 мг 3 раза/сут в течение 8 нед [8].
• Помимо монопрепаратов этилметилгидроксипиридина сукцината, в России также представлена его фиксированная комбинация с пиридоксином (витамином B6), выпускаемая в форме таблеток. Пиридоксин, входящий в состав комбинированного препарата, участвует в поддержании нормального функционирования центральной и периферической нервной системы, обмене триптофана, метионина, цистеина, глутаминовой и других аминокислот, играет важную роль в обмене гистамина. Также он способствует нормализации липидного обмена [31], нарушения которого служат одним из факторов риска развития нарушения мозгового кровообращения и сопряженных с ним когнитивных расстройств [1, 8].
• Рекомендуется назначение холина альфосцерата пациентам различных возрастных групп с целью уменьшения неврологического дефицита и увеличения способности пациентов к самообслуживанию: УУР – С, УДД – 3 [8]. Препарат оказывает нейропротективное действие благодаря увеличению синтеза ацетилхолина и участию в синтезе фосфатидилхолина, что в итоге улучшает синаптическую, в том числе холинергическую нейротрансмиссию. В организме активный компонент препарата участвует в анаболических процессах, ответственных за мембранный и фосфолипидный синтез, оказывая положительное влияние на функциональное состояние мембранных структур путем улучшения цитоскелета нейронов. Важное преимущество препарата – прямое сохранение эндогенного пула ацетилхолина [8, 32].
• Холина альфосцерата может применяться инъекционно в дозе 1000 мг/сут или перорально по 400 мг 2–3 раза/сут. Длительность лечения определяется врачом в зависимости от клинической картины и особенностей течения заболевания, переносимости препарата [8, 33].
• Рекомендуется назначение цитиколина пациентам любых возрастных групп с целью улучшения функционального исхода к 3-му месяцу инсульта/ТИА: УУР – С, УДД – 5 [8]. Препарат стимулирует биосинтез фосфолипидов мембран нейронов, нормализует энергетические процессы в митохондриях, улучшает холинергическую трансмиссию. Препарат препятствует развитию эксайтотоксичности, блокируя вызванный ишемией выброс глутамата, ингибируя таким образом глутаматиндуцированный апоптоз. Цитиколин, с одной стороны, увеличивает обратный захват глутамата, снижая его синаптическую концентрацию при острой ишемии, с другой стороны, в фазе восстановления, наоборот, увеличивает его концентрацию, способствуя улучшению когнитивных функций у пациентов [8, 34]. В отдельных РКИ сообщалось о значимом улучшении функционального восстановления пациентов к 3-му месяцу ишемического инсульта [8].
• Цитиколин улучшает такие наблюдающиеся при гипоксии симптомы, как ухудшение памяти, эмоциональная лабильность, безынициативность, трудности при выполнении повседневных действий и самообслуживании. Эффективен при лечении когнитивных, чувствительных и двигательных неврологических нарушений как сосудистой, так и дегенеративной этиологии [35].
• Режим применения цитиколина при ишемическом инсульте: в острый период – по 1000 мг каждые 12 ч с первых суток постановки диагноза длительностью не менее 6 нед. В восстановительный период, в том числе для терапии когнитивных и двигательных нарушений сосудистого генеза, – 50–200 мг/сут (дозировка и продолжительность терапии определяются тяжестью симптомов). В острый период инсульта возможен ступенчатый режим применения препарата: сначала внутривенное или внутримышечное введение, с 3–5-го дня в отсутствие нарушений функции глотания – переход на пероральный прием. В восстановительный период возможно применение препарата внутрь [35].
• Рекомендуется применение депротеинизированного гемодеривата крови телят пациентам пожилого возраста (старше 60 лет) с острым супратенториальным инфарктом мозга, с различной степенью тяжести неврологического дефицита (NIHSS 3–18 баллов) и постинсультными когнитивными нарушениями (за исключением синдрома грубой и тотальной афазии) с целью улучшения восстановления когнитивных функций и снижения риска постинсультной деменции в восстановительном периоде ишемического инсульта: УУР – В, УДД – 2 [8].
• Клиническая эффективность депротеинизированного гемодеривата крови телят опосредована комплексным мультимодальным механизмом действия, включающим в себя антигипоксантный, нейропротективный эффекты и положительное воздействие на микроциркуляцию. Эти эффекты базируются на неспецифической стимуляции клеточного метаболизма, связанной с активацией окислительного фосфорилирования, синтеза углеводов и белков, увеличением концентрации аденозинтрифосфата, аденозиндифосфата, фосфокреатина, глутамата, аспартата, гамма-аминомасляной кислоты. По данным РКИ безопасность препарата удовлетворительная [8, 36].
• Лечение депротеинизированным гемодериватом крови телят следует начинать в течение первых 7 дней после эпизода ОНМК с внутривенных инфузий (1 раз/сут). Препарат вводят в дозе 2000 мг/250 мл в форме раствора для инъекций (0,9% раствор натрия хлорида 250 мл/200 мг) до 20 инфузий, с последующим переходом на пероральный прием препарата в дозе 1200 мг/сут в течение 6 мес [8].
• Рекомендуется назначение препарата, содержащего инозин + никотинамид + рибофлавин + янтарную кислоту, пациентам среднего, пожилого и старческого (до 85 лет) возраста вне зависимости от локализации сосудистого поражения мозга с целью более полного восстановления нарушенных неврологических функций: УУР – В, УДД – 2 [8]. Фармакологические эффекты этого препарата связаны с улучшением процессов дыхания в клетках, повышением активности факторов антиоксидантной защиты, активацией процессов метаболизма глюкозы и кислорода, синтеза белка внутри клеток и гаммааминомасляной кислоты в нейронах [8].
• Лечение препаратом, содержащим инозин + никотинамид + рибофлавин + янтарную кислоту, следует начинать в первые 10 сут с использованием парентеральной формы препарата 20 мл (в 400 мл 0,9% раствора натрия хлорида) 2 раза/сут с переходом в 11–35-е сутки на пероральную форму (850 мг 2 раза/сут) [8].
• Рекомендуется применение церебролизина пациентам различных возрастных групп вне зависимости от локализации сосудистого поражения мозга с целью улучшения функционального исхода заболевания к 3-му месяцу заболевания: УУР – С, УДД – 2 [8].
• Церебролизин оптимизирует энергетический метаболизм мозга и гомеостаз кальция, стимулирует внутриклеточный синтез белка, замедляет процессы глутамат-кальциевого каскада и перекисного окисления липидов и соответственно оказывает нейропротективное, нейротрофическое и нейрорегенеративное действие на ткань мозга. В доклинических исследованиях показано, что препарат уменьшает размер инфаркта мозга и способствует восстановлению нарушенных неврологических функций [8].
• Церебролизин следует назначать в течение первых 12 ч от эпизода ишемического инсульта по схеме 30 мл 1 раз/сут в течение 10 сут (внутривенно капельно) [8].
• Пациентам, перенесшим ишемический инсульт в системе внутренней сонной артерии, вне острого периода заболевания рекомендуется применение винпоцетина в составе комплексной медикаментозной терапии с целью улучшения процессов церебральной микрогемоциркуляции и функционального исхода заболевания: УУР – С, УДД – 4 [8].
• Механизм действия винпоцетина основан на комплексном нормализующем влиянии препарата на церебральный кровоток и метаболические процессы в ткани мозга: обладает неселективным вазодилататорным эффектом, уменьшает агрегацию тромбоцитов, влияет на деформируемость и эластичность эритроцитов, окислительно-восстановительные процессы, способствует утилизации глюкозы, стимулирует метаболизм норадреналина и серотонина в тканях мозга, уменьшает процессы нейровоспаления, опосредованные цитокинами и матриксной протеазой в кровеносных сосудах головного мозга [8]. Назначение винпоцетина требует особой осторожности у пациентов со стенооклюзирующим поражением экстраи интракраниальных сосудов головного мозга вследствие возможного формирования синдрома обкрадывания в каротидной или в вертебробазилярной системе. В пожилом и старческом возрасте чувствительность мозговых сосудов к вазодилататорному действию винпоцетина возрастает, что обусловлено сенсибилизацией системы аденилатциклазы-цАМФ при старении. В большинстве случаев у винпоцетина не наблюдается лекарственного взаимодействия, однако следует помнить о невозможности его одновременного применения (парентерально) с гепарином натрия. При применении винпоцетина на фоне гепаринотерапии повышается риск развития геморрагических осложнений [8].
• Вне острого периода инсульта винпоцетин назначается в виде капельной инфузии (скорость введения не должна превышать 80 капель/мин) 1 раз/сут из расчета 1 мг/кг массы тела на 500 мл изотонического раствора натрия хлорида длительностью курса 14 дней [8].
• Для лечения когнитивных расстройств, в том числе постинсультных, показана также фиксированная комбинация винпоцетина и пирацетама [37]. Пирацетам, входящий в состав препарата наряду с винпоцетином, оказывает положительное влияние на обменные процессы и кровообращение мозга, повышает утилизацию глюкозы, улучшает течение метаболических процессов, микроциркуляцию в ишемизированных зонах, угнетает агрегацию активированных тромбоцитов, проявляет защитное действие при повреждениях головного мозга, вызываемых гипоксией, улучшает интегративную деятельность мозга, ингибирует повышенную агрегацию активированных тромбоцитов и в случае патологической ригидности эритроцитов улучшает их деформируемость и способность к фильтрации [38].
• Режим приема фиксированной комбинации винпоцетин + пирацетам – по 1 таблетке 2–3 раза/сут курсом от 2–3 нед до 2–6 мес [36].
• Рекомендуется назначение глицина в дозе 1–2 г/сут в течение первых 5 сут от момента эпизода ишемического инсульта (начиная с шестого часа после развития первых симптомов ишемического инсульта) пациентам c ОНМК по ишемическому типу в каротидной системе, находящимся в общем удовлетворительном состоянии, состоянии средней тяжести или тяжелом состоянии. Препарат назначается с целью улучшения противоишемической защиты мозга, улучшения восстановления нарушенных неврологических функций и снижения риска 30-дневной летальности: УУР – В, УДД – 2 [8]. Глицин выпускается в форме таблеток для сублингвального применения [39].
• Рекомендуется назначение метионил-глутамил-гистидил-фенилаланил-пролил-глицил-пролина в течение первых 5 суток от момента эпизода полушарного ишемического инсульта пациентам любых возрастных групп с легким, умеренным и тяжелым неврологическим дефицитом (NIHSS менее 18 баллов) c целью улучшения восстановления неврологических функций: УУР – С, УДД – 3 [8].
• Метионил-глутамил-гистидил-фенилаланил-пролил-глицил-пролин является синтетическим аналогом фрагмента адренокортикотропного гормона, лишенным гормональной активности. Фармакологический эффект его связан с устранением дисбаланса цитокинов вследствие достоверного уменьшения уровня индукторов воспаления и повышения содержания противовоспалительных и нейротрофических факторов, что приводит к угнетению локальной воспалительной реакции и улучшению трофического обеспечения мозга в остром периоде инсульта [8]. Препарат применяется интраназально в дозе 12 и 18 мг/сут 1% раствора [8].
• Рекомендуется назначение полипептидов коры головного мозга скота пациентам среднего и пожилого возраста с ишемическим инсультом в каротидной системе (тяжесть неврологического дефицита менее 20 баллов NIHSS) с целью более полного восстановления нарушенных неврологических функций. Лечение следует проводить по схеме: 2 курса внутримышечных инъекций препарата 20 мг (10 + 10) в течение 10 сут с перерывом в 10 сут: УУР – С, УДД – 2 [8]. Соответствующий препарат способен оказывать тканеспецифичное воздействие на кору головного мозга, нормализовывать соотношение возбуждающих и тормозящих аминокислот в головном мозге, регулировать содержание дофамина и серотонина [8].



