Для комплексной диагностики морфологических и функциональных изменений сердца в кардиологии все чаще применяют различные методы малоинвазивной и неинвазивной лучевой диагностики [1, 2]. Еще одна методика, которая может занять существенное место в диагностике сердечно-сосудистых заболеваний, — магнитно-резонансная спектроскопия (МРС).
МРС по фосфору дает информацию о состоянии энергетического метаболизма миокарда, а также о его нарушении при различной патологии [2]. МР-спектроскопия лишена лучевой нагрузки и не требует введения контрастных или радиофармацевтических препаратов.
В предыдущих исследованиях показано что методом МРС по фосфору возможно определить не только наличие дефицита макроэргических фосфатов в миокарде левого желудочка (ЛЖ), но и отразить степень развития патологии, так как показатели МРС коррелируют с результатами функциональных исследований сердца [3].
Гипертрофированный миокард ассоциируют с нарушением его энергетического метаболизма — уменьшением концентрации креатина и снижением активности креатинкиназы [4]. Гипертрофия миокарда левого желудочка (ГЛЖ) является независимым прогностическим фактором развития сердечно-сосудистых осложнений. Благодаря этому значительная часть научных исследований МРС посвящена изучению гипертрофированного миокарда [5].
Гипертрофическая кардиомиопатия (ГКМП) — наследственное заболевание, передающееся по аутосомно-доминант-ному типу наследования [2, 3], при котором отмечается значительная гипертрофия миокарда (более 15 мм), преимущественно за счет утолщения межжелудочковой перегородки (МЖП).
Одной из основных причин смертности у больных ГКМП является нарушение ритма, а общая смертность пациентов с таким заболеванием составляет от 1 до 6% [4].
 Кроме того, в группу заболеваний, осложняющихся гипертрофией миокарда, входит артериальная гипертония – АГ [5].
Кроме того, в группу заболеваний, осложняющихся гипертрофией миокарда, входит артериальная гипертония – АГ [5].
Выявление поражения органов-мишеней, таких как сердце, головной мозг и почки является важным прогностическим признаком. ГЛЖ как осложнение АГ значительно ухудшает прогноз и может служить причиной развития злокачественной тахикардии, инфаркта миокарда и внезапной сердечной смерти [6].
Значительный прогресс в развитии методов лучевой диагностики привел к расширению понимания патогенеза гипертрофии миокарда. У больных ГЛЖ методами лучевой диагностики мы преимущественно получаем данные о морфологических или функциональных нарушениях в миокарде.
Этим изменениям предшествуют более глубокие нарушения на молекулярном уровне, связанные с перестройкой энергетического обмена в мышечной ткани. А состояние энергетического метаболизма миокарда может быть одним из факторов, индуцирующих последующее развитие сердечно-сосудистых осложнений. МРС сердца — это достаточно сложное исследование как в техническом исполнении, так и в интерпретации результатов [7].
В связи с постоянным техническим развитием, появлением в клинической практике высокопольных магнитно-резонансных томографов с напряженностью магнитного поля 3Т и более, а также новых последовательностей для сбора спектроскопических данных МРС может занять клинически значимое место в диагностике сердечно-сосудистых заболеваний. Сочетанное использование магнитно-резонансной томографии (МРТ) и МРС сердца может позволить создать универсальный метод диагностики, отвечающий на вопросы о строении, функции сердца и причинах их нарушения на молекулярном уровне.
Целью данной работы было выявление возможностей фосфорной спектроскопии в оценке нарушений метаболизма миокарда у больных ГЛЖ различной природы и их сопоставление с морфологическими и функциональными результатами МРТ сердца.
Материал и методы
В исследование были включены 94 человека, распределенных в 3 группы — здоровые добровольцы (1-я группа, n=35), больные АГ с ГЛЖ (2-я группа, n=30) и больные ГКМП (3-я группа, n=29).
В группу здоровых добровольцев вошли 22 мужчины и 13 женщин в возрасте 54±7,1 года. Для группы больных АГ с ГЛЖ были отобраны 19 мужчин и 11 женщин в возрасте 52±6,3 года, в группу больных ГКМП вошли 18 женщин и 11 мужчин, средний возраст составил 52±6,7 года.
Во всех группах достоверного различия по возрасту выявлено не было. Диагноз ГКМП устанавливали в соответствии с рекомендациями Всемирной организации здравоохранения на основании клинических, анамнестических и инструментальных данных. Больных включали в группу при толщине миокарда МЖП не менее 15 мм.
Всем пациентам и здоровым лицам проводили гибридное исследование сердца, включавшее МРТ с целью оценки морфологии и функции ЛЖ, а также МРС миокарда ЛЖ по фосфору с целью определения концентраций высокоэнергетических фосфатов. Оба исследования приводили в комплексе за один раз.
Для выполнения исследования использовали высокопольный МР-томограф, напряженность магнитного поля 3Т.
МРТ сердца выполняли по стандартному протоколу с использованием 12-канальной приемно-передающей катушки, последовательность сбора данных синхронизировали с дыханием и электрокардиограммой (ЭКГ). В результате исследования и обработки полученных данных были оценены анатомические особенности сердца, определена толщина миокарда, рассчитана фракция выброса (ФВ) ЛЖ.
В стандартный протокол МРТ вошли статичные срезы через все сердце (от дуги аорты до купола диафрагмы) в аксиальной плоскости для оценки общей анатомии и особенностей положения, а также кино-последовательности в стандартных плоскостях: длинная двух- и четырехкамерная ось, короткая ось через желудочки. Использовали импульс-ную последовательность со «светлой» кровью (турбо-спин-эхо).
Толщина аксиальных срезов составляла 10 мм, а кино-изображений — 8 мм.
Полученные при МРТ сердца данные были обработаны с использованием специализированного программного пакета оценки кардиологических исследований (Philips).
Для проведения МРС был разработан и применен специализированный протокол исследования, включавший особенности укладки пациента, расположения датчиков синхронизации с ЭКГ, локализации приемно-передающей катушки и настройки импульсной последовательности.
МРС по фосфору проводили с использованием фосфорной приемно-передающей катушки P-140 и встроенной в туннель МР-томографа кубатурной катушки, располагавшейся на передней поверхности грудной клетки в проекции сердечного толчка. Обследуемый находился в положение на спине, электроды синхронизации с ЭКГ помещены на заднюю стенку грудной клетки для исключения их воздействия на получаемый сигнал. Сбор данных происходил в момент конечной диастолы (см. таблицу).
Зона сбора данных располагалась в проекции верхушки ЛЖ с захватом среднего и дистального сегментов МЖП.
Для исследований была выбрана одновоксельная спектроскопия, позволяющая захватить больший объем ткани по сравнению с мультивоксельным исследованием, для увеличения значения сигнал/шум.
Обработка полученных спектроскопических данных производилась на базе программного пакета Spectrowiev (Philips).
После обработки спектра путем расчета площадей под пиками макроэргических фосфатов были рассчитаны два энергетических индекса: основной – отношение концентрации фосфокреатина к аденозинтрифосфату (ФК/АТФ) и альтернативный (НФ – неорганический фосфат×100/ФК), а также pH.
Статистический анализ полученных результатов был проведен с использованием программного продукта SPSS версии 16.
Для определения различия между результатами, полученными в 2 группах, использовали U-критерий Манна—Уитни. Был определен коэффициент корреляции Спирмена.
Результаты
По результатам МРТ сердца во всех группах были определены следующие значения: толщина миокарда МЖП в 1-й группе составила 7,7±1,4 мм, во 2-й группе (АГ с ГЛЖ) — 16±1,1 мм, в 3-й группе (ГКМП) — 17,6±2,1 мм (для всех сравнений p<0,05).
При расчете массы миокарда было определено ее значительное увеличение во 2-й и 3-й группах (212,04±37 и 273,21±36,28 г соответственно; p<0,05) по сравнению с 1-й группой (154,31±31,84 г), все результаты достоверно различались (p<0,05).
 ФВ ЛЖ в группе нормы и у больных ГКМП оставалась в зоне нормальных значений и достоверно не различалась (64,21±2,31 и 67±3,16% соответственно; p>0,05).
ФВ ЛЖ в группе нормы и у больных ГКМП оставалась в зоне нормальных значений и достоверно не различалась (64,21±2,31 и 67±3,16% соответственно; p>0,05).
Во 2-й группе было выявлено снижение сократительной функции ЛЖ, ФВ составила 56,23±7,13%, что достоверно отличалось от результатов в 1-й и 2-й группах (p<0,05).
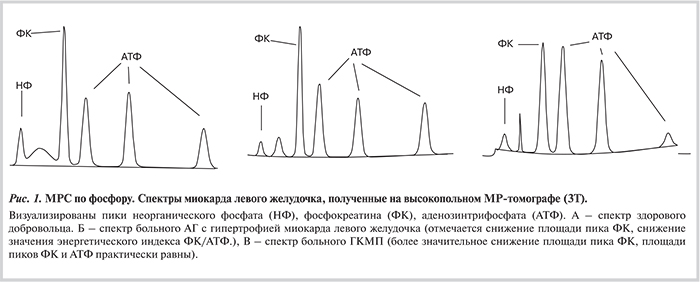
В результате проведения МРС по фосфору были получены спектры, примеры которых представлены на рис.1.
При обработке данных МРС были получены значения относительных концентраций высокоэнергетических фосфатов в миокарде здоровых лиц и больных ГЛЖ различной природы.
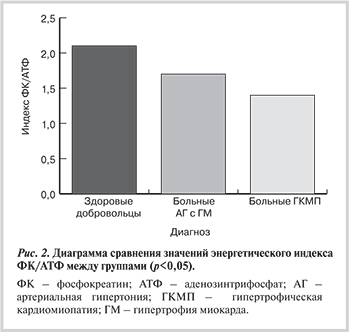
Нормальные значения индекса ФК/АТФ, полученные в группе здоровых добровольцев, составили 2,11±0,29.
При расчете данных фосфорной МРС у больных АГ с ГЛЖ было выявлено достоверное снижение основного энергетического индекса миокарда до 1,65±0,12 по сравнению с группой нормы (p<0,05; рис. 2). Достоверное и более значительное снижение значений энергетического индекса было выявлено в группе больных ГКМП — 1,32±0,16 (p<0,05).
При статистическом сравнении результатов МРТ и МРС сердца были выявлены слабые корреляции. Так, в группе больных АГ с ГЛЖ была выявлена прямая слабая корреляция между значениями индекса ФК/АТФ и ФВ ЛЖ (r=0,29; p<0,05). Кроме того, в группе больных ГКМП определена слабая обратная корреляция между значениями ФК/АТФ и величиной массы миокарда 0,31 (p<0,05).
Обсуждение
До последнего времени абсолютное большинство МРС-исследований сердца проводили на высокопольных МР-томографах с напряженностью магнитного поля до 1,5 Т [8]. Для решения одной из основных проблем фосфорной спектроскопии — слабого сигнала от ядер фосфора ввиду их низкой концентрации — данная работа выполнялась с использованием МР-томографа с напряженностью магнитного поля 3Т, что позволило в значительной степени увеличить качество получаемого спектра.
Состояние энергетического метаболизма миокарда оценивали с помощью расчета относительных концентраций макроэргических фосфатов — определения значения индекса ФК/АТФ.
При оценке результатов предыдущих исследований, посвященных определению значений энергетических индексов миокарда у здоровых лиц, прослеживается значительная вариабельность полученных результатов — от 1,1 до 2,5 [2].
Причиной столь значительных различий может быть отсутствие стандартизации МРС-исследования — применение различных МР-томографов и настроек МРС-последовательностей. Однако полученные нами результаты (ФК/АТФ=2,08±0,35) в группе здоровых добровольцев согласуется с частью представленных ранее исследований [9].
Группы лиц, включенные в наше исследование, достоверно не различались по возрасту. Такое условие было введено, так как в предшествовавшей работе М. Schocke и соавт. [13] продемонстрировали гендерную зависимость значений энергетических индексов — обратную корреляцию между возрастом и ФК/АТФ при обследовании добровольцев (возраст от 20 до 67 лет). У молодых лиц ФК/АТФ составил 2,16±0,36, а в группе более взрослых лиц — 1,83±0,37 (p<0,05).
В здоровом миокарде расход энергии покрывается ее адекватным производством, и эти механизмы тесно связаны. Значение энергетических индексов является постоянным и не может значительно изменяться даже при высокой нагрузке [10]. S. Schaefer и соавт. предполагают что на фоне ГЛЖ развивается гипертрофия стенки коронарной артерии, что может вести к снижению коронарного кровотока.
У 80% таких пациентов отмечается клинически значимое уменьшение просвета сосуда, а их дилатационный резерв значительно снижен [14].
Несколько предыдущих исследований были посвящены изучению гипертрофированного миокарда различной природы [12—15]. Степень описываемых нарушений достаточно вариабельна. В нашей работе МРС была проведена пациентам двух групп с различной природой гипертрофии миокарда для сравнения возможных различий. В обеих группах энергетический индекс демонстрировал снижение. Так, снижение индекса ФК/АТФ у больных АГ встречается в работе J.P. Heyne [16], в которой результаты МРС сравниваются с результатами эхокардиографии. В работе представлено значительное снижение энергетического индекса у больных с нарушением систолической функции ЛЖ (1,43±0,21) по сравнению с группой больных, у которых была нарушена диастолическая функция (1,65±0,25; p<0,05). В нашей работе больным проводилось гибридное исследование, включавшее МРТ и МРС сердца, что позволило выявить зависимость значений энергетического индекса и значений ФВ ЛЖ у больных АГ и ГЛЖ.
В группе больных ГКМП были выявлены наиболее статистически значимые изменения энергетического метаболизма; кроме того, изменение индекса ФК/АТФ в данной группе зависело от массы гипертрофированного миокарда.
P.W. Hochachka [17] и соавт. выделяют 3 причины нарушения энергетического метаболизма миокарда — запуск анаэробного типа производства АТФ по причине гипоксии миоцита, сверхнагрузка давлением, смена субстрата метаболизма. В результате снижаются активность креатинкиназы и концентрация креатина, что проявляется в снижении энергетических индексов. По мнению S. Betocchi [18] и соавт., увеличенная мышечная масса и особенности сократимости миокарда ЛЖ (увеличенное систолическое утолщение и нарушение диастолической функции) должны рассматриваться как основные причины описанных метаболических изменений [18].
Изучение возможностей фосфорной МРС продолжается уже более 20 лет, за это время были обследованы лишь немногим более 700 здоровых лиц и 1000 пациентов, получены данные о наличии нарушений метаболизма миокарда ЛЖ при различных сердечно-сосудистых заболеваниях. Однако невысокие значения пространственного и временнóго разрешения фосфорной спектроскопии значительно сужают круг заболеваний, которые можно эффективно исследовать. Основной фокус все больше исследователей направляют на гипертрофированный миокард, так как он, вероятно, дает более высокий сигнал при МРС по фосфору. Те же ограничения делают одовоксельный вид фосфорной МРС более перспективным, так как при нем в зону интереса попадает больший объем ткани [19].
Значительное время исследования препятствует применению метода у больных в остром или тяжелом состоянии. Отсутствие стандартизованного протокола проведения исследования, включающего рекомендации по укладке исследуемого, последовательностям сбора данных, а также алгоритмов последующей обработки данных значительно препятствуют возможности проведения крупных популяционных исследований.
Данные факторы являются существенными для ускорения прогресса и создания новой МР-техники для увеличения возможностей МРС. Благодаря решению этих вопросов МРС может стать не только более мощным исследовательским инструментом, но и занять существенное место в кардиологической практике. Сочетанное (гибридное) использование данного метода совместно с МРТ сердца позволит получить комплекс данных о состоянии сердца как с морфологической и функциональной сторон, так и на молекулярном уровне.
Выводы
Таким образом, в нашей работе были получены данные о нарушении состояния энергетического метаболизма в гипертрофированном миокарде. Кроме того, установлено достоверное различие между степенью снижения концентраций макроэргических фосфатов и природой гипертрофии. Впервые проведено гибридное исследование, позволившее получить комплекс морфологических, функциональных и спектроскопических данных и сравнить их между собой.
Работа выполнена в рамках реализации Гранта Президента РФ по поддержке Ведущей научной школы НШ-5035.2014.7 «Гибридные технологии лучевой медицины в сердечно-сосудистой хирургии и кардиологии».



