История развития магнитно-резонансной спектроскопии (МРС) началась в 1945 г., когда было открыто
явление ядерно-магнитного резонанса. Четырьмя годами позже было описано еще одно важное физическое явление — химический сдвиг резонансной частоты. Эти два физических явления стали основой МРС. Первое упоминание о МРС по фосфору в научной литературе датируется 1976—1977 гг. [1, 2], а первые результаты фосфорной МРС в исследовании сердца были опубликованы в 1985 г. [3]. В течение своего развития методика МРС применялась для исследований как различных биоптатов,
так и для тканей животных и человека.
Принято считать, что в однородном магнитном поле частота вращения ядер одного и того же вещества одинакова, однако это касается лишь идеальных условий. При реальных исследованиях с помощью магнитно-резонансной томографии (МРТ) магнитное поле в области исследуемого объекта не совсем однородное, что связано с образованием локальных магнитных полей. Электронные связи крупных молекул создают собственные «маленькие» магнитные поля, которые воздействуют
на окружающие их протоны, что приводит к некоторому изменению резонансной частоты этих протонов. Вследствие этого в различных средах или вне их воздействия резонансные частоты одних и тех же ядер различаются. Данное смещение частоты и называется химическим сдвигом резонансной частоты. Изменяя частоту радиочастотного излучения, мы можем возбуждать, а затем получать сигнал от ядер, находящихся в определенных веществах. Например, можно получить сигнал от ядер
фосфора (31Р), находящихся в молекуле аденозинтрифосфата (АТФ).
При проведении методики получается спектральная картина, которая отражает пики различных веществ, содержащие ядра одного типа, но с разной резонансной частотой. Резонансная частота веществ заранее известна, следовательно, известно, к какому веществу относится каждый пик. Площадь под каждым пиком пропорциональна концентрации данного вещества.
Наибольшее распространение в исследованиях сердца приобрела МРС по ядрам фосфора, продемонстрировавшая большие возможности в изучении состояния энергетического метаболизма миокарда как у здоровых лиц, так и у лиц, страдающих различными сердечно-сосудистыми заболеваниями. МРС по ядрам фосфора уникальна тем, что позволяет неинвазивно получать
данные о концентрациях высокоэнергетических фосфатов в живом миокарде. К таким веществам, в первую очередь, относятся фосфокреатин (ФК) и аденозинтрифосфат (АТФ). Оба эти вещества являются важнейшими элементами энергетического метаболизма клетки. АТФ — универсальная энергетическая единица клетки,
а ФК — энергоаккумулирующая молекула, участвующая в восстановлении аденозиндифосфата до аденозинтрифосфата. Снижение уровня АТФ свидетельствует о нарушении его транспорта или утилизации и приводит к уменьшению сократительной функции миоцитов [4]. Однако уровень ФК начинает снижаться раньше, поскольку расходуется на поддержание концентрации АТФ [5, 6]. Следовательно, отношение площадей пиков ФК и АТФ отражает раннее снижение концентраций
ФК и является признаком нарушения энергетического метаболизма миокарда при дисбалансе потребности в энергии и возможностях ее покрытия.
Преимущество МРС перед альтернативными методами изучения нарушений метаболизма (однофотонная эмиссионная компьютерная и позитронно-эмиссионная томографии) обусловлено отсутствием необходимости введения радиофармпрепаратов. Сравнивая МРС с биопсией, стоит подчеркнуть ее неинвазивность, отсутствие осложнений, а также возможность получения результата
от живого, сокращающегося миокарда. Важным преимуществом МРС является то, что она выполняется
на том же оборудовании, что и магнитно-резонансная томография сердца, исключение составляет использование специализированных приемно-передающих катушек. Несложное объединение этих методик может позволить за одно исследование получать данные не только об анатомии, размерах и функции сердца, но и о состоянии энергетического метаболизма миокарда.
Изучение возможностей фосфорной МРС продолжается уже более 20 лет [3], за это время были обследованы немногим более 700 здоровых лиц и 1000 пациентов. Наш обзор посвящен результатам этих немногочисленных, но очень важных исследований.
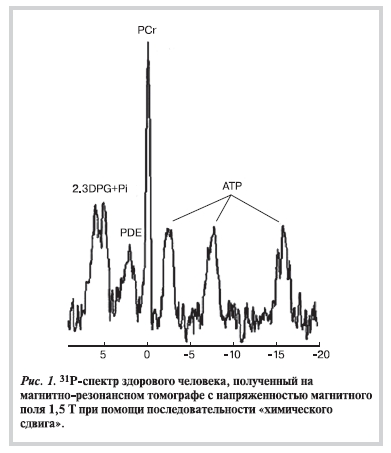
31P дает возможность неинвазивного исследования высокоэнергетических фосфатов, участвующих в энергетическом метаболизме миокарда. Типичный спектр сердца содержит следующие пики (рис. 1): фосфокреатина (PCr), триплет аденозинтрифосфата (ATP), неорганического фосфата (Pi), 2,3-дифосфоглицерата (2.3DPG), фосфодиэфиров (PDE) [7].
Несколько групп ученых [8—10] показали, что у здоровых добровольцев нет снижения отношения ФК к АТФ в ответ на аэробные нагрузочные пробы, потому что дефицит энергии покрывается за счет увеличения потребления кислорода без участия ФК. Таким образом, было показано, что АТФ не является основным регулятором повышения энергетического метаболизма во время нагрузки. Однако H.J. Lamb и соавт. [11] показали снижение энергетического индекса на 14% у здоровых добровольцев в ответ на атропин-добутаминовый нагрузочный тест. Противоречие результатов может быть объяснено более значительным действием атропин-добутаминового теста, чем тестов, использованных в других работах.
Несколько работ посвящено изучению гипертрофии миокарда у спортсменов, при «атлетическом сердце». B.M. Pluim и соавт. показали, что гипертрофия левого желудочка (ЛЖ) у спортсменов является физиологической адаптацией, а не патологией [12]. В недавнем исследовании также был сделан вывод о том, что гипертрофия левого и правого желудочков ассоциируется с нормальными показателями энергетического метаболизма по данным МРС [13].
Основным объектом изучения миокарда с помощью 31Р-МРС во многих работах был индекс ФК/АТФ. Однако значение этого индекса при исследовании миокарда здоровых добровольцев варьирует от 0,83 до 2,46, что является слишком широким диапазоном. Такая разница результатов может быть объяснена многими факторами: различное насыщение ядер фосфокреатином и АТФ, возможное изменение пиков АТФ за счет подмешивания сигнала от крови, эффекты от использования методов
усиления, таких как ядерный эффект Оверхаузера [14, 15]. Отсутствие среднего значения энергетического индекса миокарда, стандартизованного протокола проведения исследования, включающего рекомендации по укладке исследуемого, последовательностям сбора данных,
а также алгоритмов последующей обработки данных значительно препятствует возможности проведения крупных популяционных исследований.
Внимание ученых было уделено изучению возрастных различий значений энергетического индекса миокарда. M.F. Schocke и соавт. продемонстрировали снижение индекса ФК/АТФ у здоровых лиц пожилого возраста по сравнению с таковым у молодых добровольцев [16]. Половые различия по энергетическому индексу не выявлены [17, 18].
Многие авторы высказывают мнение, что фосфорная МРС имеет огромные перспективы в изучении ишемической болезни сердца (ИБС) включая диагностику ишемии с использованием фармацевтических нагрузочных тестов, оценку жизнеспособности миокарда после инфаркта миокарда (ИМ), оценку результатов хирургического лечения. Объединение данного метода с МРТ сердца может помочь в решении большинства вопросов диагностики ИБС. P.A. Bottomley предположил, что МРС может использоваться для дифференциации здорового миокарда от ишемизированного, гибернированного
и рубцово-измененного миокарда. Отмечается тенденция к снижению концентраций высокоэнергетических фосфатов в зоне хронической ишемии, в гибернированном миокарде отмечается их достоверное снижение, а в рубцовой ткани концентрации метаболитов стремятся
к нулю. Однако в зоне рубцовых изменений сохраняется спектр неорганического фосфата [15].
Опубликовано небольшое количество работ, посвященных изучению энергетического метаболизма у больных в острой стадии ИМ. Их результаты соответствуют данным экспериментальных исследований на животных. Показан подъем пика неорганического фосфата в течение 4 дней со дня начала необратимой ишемии [19]. Группа P.A. Bottomley и соавт. в 1987 г. провела одно из первых в мире исследований с помощью фосфорной МРС, целью которого была оценка нарушения энергетического метаболизма у больных с острым ИМ. В результате получены снижение отношения фосфокреатина (ФК)
к неорганическому фосфату и увеличение отношения неорганического фосфата к АТФ, однако достоверного снижения энергетического индекса ФК/АТФ зафиксировано не было [20].
Многие исследования были посвящены изучению ИМ в хронической стадии. Наиболее часто анализируемым показателем было соотношение ФК и АТФ. К примеру, были обследованы 12 пациентов, перенесших ИМ за 2 мес до проведения исследования, у которых не было зафиксировано достоверного снижения индекса ФК/АТФ. Однако после нормализации площадей пиков ФК и АТФ с использованием референсного пика было показано значительное снижение их площадей [21]. S.Neubauer и соавт. не нашли достоверных различий между отношениями ФК к АТФ и фосфодиэфира к АТФ у больных
с гемодинамически значимым стенозом передней нисходящей артерии по сравнению с таковыми у здоровых добровольцев. Кроме того, не было обнаружено достоверных различий этих показателей у больных с ИМ и у здоровых добровольцев. Авторами был сделан вывод, что в состоянии покоя у данных больных показатели энергетического метаболизма миокарда остаются в пределах нормы [22].
Тем не менее в последующих исследованиях описано значительное снижение индекса ФК/АТФ у пациентов с ИМ [23—26].
При исследовании постишемического метаболизма миокарда с помощью МРС группа R. Kalil-Filho и соавт. продемонстрировала нормальные значения показателей энергетического метаболизма в гибернированном миокарде после реперфузии. Данные значения оставались неизменными в течение всего периода наблюдения [21]. Был сделан вывод, что в оглушенном или гибернированном миокарде отсутствует значительное нарушение энергетического метаболизма. Описан опыт экспериментальных работ на собаках, разделенных на две группы: первая — с зоной гибернированного миокарда, вторая — без нарушения сократимости. Индуцирование ишемии сопровождалось быстрым снижением сократительной способности миокарда и значительным снижением индекса ФК/АТФ. Однако было выявлено превышение контрольного значения индекса ФК/АТФ в группе животных с «оглушенным» миокардом сразу же после реперфузии; данные изменения сохранялись в течение следующих
60 мин. Кроме того, описаны снижение общей активности креатинкиназы в зоне гибернированного миокарда, а также обратная связь между удельной активностью креатинкиназы и отношением ФК/АТФ. Авторы сделали вывод, что увеличение индекса ФК/АТФ вызвано ухудшением передачи энергии к сократительному аппарату миоцитов, приводящим к сократительной дисфункции при ИБС [28].
При обследовании пациентов с ИМ без зубца Q методом ОЭКТ в зоне гипокинезии, совпадающей с зоной сниженного поглощения радиофармпрепарата Тс-МИБИ 99м, также обнаружено снижение индекса ФК/АТФ. Из этого был сделан вывод, что в данном случае происходит не только морфологическое ремоделирование миокарда, нарушающее его функцию, но и нарушение
энергетического метаболизма в зоне этих изменений [23]. В другом исследовании у пациентов с подострым ИМ и локальными зонами нарушения сократимости после реваскуляризации выявлено значительное снижение энергетического индекса по сравнению с больными, у которых сократительная функция была восстановлена. Кроме того, снижение индекса было определено и в
прилежащих к зоне нарушения сократимости отделах миокарда. Таким образом, нарушения энергетического метаболизма выявляются не только в зоне инфаркта, где нарушена сократительная функция, но и частично в прилежащих к ней участках нормально сокращающегося миокарда [25].
Сигнал от АТФ является биохимическим маркером ремоделирования миокарда и его гипертрофии, происходящих в непораженных сегментах у больных ИМ и, следовательно, коррелирует с жизнеспособным миокардом [29, 30]. Экспериментальные исследования показали, что рубцовая ткань при ИМ содержит незначительное количество АТФ, в то время как в зоне гибернированного миокарда уровень ФК остается в норме. М. Beer и соавт. показали значительное снижение уровня сигнал/шум
от зоны акинетичного миокарда через 6 мес после реваскуляризации по сравнению с таковым у здоровых лиц. В данных зонах сигнал от ФК не был обнаружен, а авторы сделали вывод, что значение сигнал/шум от АТФ может быть прогностическим признаком возможного восстановления функции после реваскуляризции [24]. Исследования показали, что уровень ФК падает как при необратимых, так и при обратимых нарушениях функции миокарда, однако в первом случае нормальное значение так и не восстанавливается [31].
По мнению P.A. Bottomley, нормальные значения энергетического индекса у больных ИМ, найденные в некоторых исследованиях, не означают отсутствия нарушения энергетического метаболизма. Вероятно, это может быть объяснено ограничениями размеров зоны интереса (воксела), который может покрывать не только зону рубца, но и прилегающие ткани, обусловливая получение общего сигнала от всей зоны и ошибочного результата [15]. Данная проблема может быть решена путем использования у таких пациентов мультивоксельной спектроскопии, позволяющей позиционировать несколько вокселей на различные зоны миокарда, однако данный метод нуждается в дальнейшем совершенствовании МРС с целью уменьшения минимального объема вокселя.
Гипертрофия миокарда ЛЖ может быть определена у спортсменов как проявление атлетического сердца — физиологической адаптации к постоянной высокой физической нагрузке [12]. У больных различными сердечно-сосудистыми заболеваниями (стеноз аортального клапана, артериальная гипертония — АГ, гипертрофическая кардиомиопатия — ГКМП) гипертрофия миокарда является патологической реакцией различного генеза [32—34].
M.A. Conway и соавт. показали, что по данным фосфорной МРС отмечалось значительное снижение энергетического индекса миокарда ЛЖ у больных с гипертрофией миокарда и сердечной недостаточностью (СН), вызванных стенозом аортального клапана, по сравнению с таковым у больных без СН (рис. 2). Авторы сделали вывод, что фосфорная МРС может быть использована с целью определения оптимальных сроков проведения хирургического лечения у больных стенозом аортального клапана [32].
S. Neubauer и соавт. провели обследование 13 пациентов с аортальным стенозом и 9 пациентов с недостаточностью аортального клапана. В обеих группах пациентов отмечено значительное снижение индекса ФК/АТФ (1,64±0,09 против 2,02±0,11 у здоровых добровольцев). При отдельном рассмотрении значительное снижение было продемонстрировано только в группе с аортальным
стенозом (1,55±0,12), а при недостаточности аортального клапана энергетический индекс лишь стремился к снижению (1,77±0,12; p=0,148). При последующем анализе было отмечено, что значительное снижение (до 1,51±0,09; р=0,001) имелось лишь у больных с СН III функционального класса (по классификации NYHA), а у больных с СН I—II функционального класса снижение было менее
значительным (1,86±0,18). Кроме того, в данной работе было показано, что гипертрофия, вызванная перегрузкой объемом, не ведет к нарушению энергетического метаболизма, а решающую роль в нарушении метаболизма несет перегрузка давлением. В данном исследовании была также продемонстрирована корреляция между степенью СН и степенью нарушения энергетического мета-
болизма миокарда [35].
В недавних исследованиях показано влияние хирургического лечения (протезирование аортального клапана) на восстановление энергетического метаболизма миокарда. М. Beer и соавт. в группе из 10 пациентов с аортальным стенозом продемонстрировали, что показатели энергетического метаболизма начали возвращаться к норме, кроме того было отмечено снижение массы миокарда ЛЖ [36]. H.P. Beyerbacht и соавт. отметили более значительную стабилизацию энергетического метаболизма
у больных с аортальным стенозом, а именно, полное восстановление отношения ФК/АТФ через 40±12 нед после замены аортального клапана.
Снижение энергетического индекса у больных с гипертрофией миокарда, индуцированной стенозом аортального клапана, в состоянии покоя может быть объяснено хронической ишемией миокарда, возникающей из-за дисбаланса между потребностью перегруженного миокарда и возможностью доставки энергии. Соответственно, нормализация данных показателей связана с уменьшением давления и нагрузки на миокард после хирургического лечения таких больных. Таким образом, отношение ФК/АТФ может быть критерием оценки степени тяжести поражения миокарда, вызванного хронической перегрузкой давлением [37]. Данные, получаемые с помощью МРС по фосфору, могут быть прогностически важными, поскольку у больных с аортальным стенозом со стенокардией или синкопальными состояниями прогноз значительно хуже, чем у больных без признаков ишемии [38].
Рисунок 2. 31Р-спектры, полученные на томографе с напряженностью магнитного поля 1,9 Т.
У 22 пациентов с недостаточностью митрального клапана показано значительное снижение отношения ФК к АТФ при тяжелой степени регургитации, в отличие от такового в контрольной группе. У больных с тяжелой степенью недостаточности митрального клапана соотношение ФК к АТФ было равно 1,29, при умеренной степени — 1,49, при легкой степени — 1,73. Результаты МРС коррелировали с такими показателями ЭхоКГ, как конечный систолический размер, толщина миокарда левого
желудочка, размеры, фракция выброса и масса миокарда ЛЖ [39].
Авторы, обследовавшие больных АГ, описали снижение индекса ФК/АТФ по сравнению с таковым в группе контроля. Кроме того, у больных с нарушением систолической функции было отмечено более значительное снижение индекса, чем у больных с нарушением диастолической функции. В группе с систолической дисфункцией отношение фосфодиэфира к гамма-АТФ было значительно ниже (0,56±0,36), чем в контрольной группе (1,14±0,42), что свидетельствует о нарушении метаболизма фосфолипидов в данной группе [40]. H.J. Lamb и соавт. проводили исследование с фармакологическим нагрузочным тестом у больных АГ. У данной группы наблюдалось снижение энергетического индекса во время нагрузочного теста до 0,95±0,25 против 1,16±0,18 (р<0,05) в покое. В данном исследовании было подтверждено также снижение энергетического индекса у больных АГ с нарушением диастолической функции ЛЖ [41].
Рассматривая многочисленные работы различных авторов, посвященные ГКМП и дилатационной кардиомиопатии (ДКМП), можно констатировать, что получены сходные результаты [33, 34, 42—51]. У больных ДКМП обнаруживались незначительные изменения энергетического индекса миокарда, в отличие от контрольных групп. В одном исследовании описано значительное снижение показателей фосфорной МРС у пациентов с ишемической, а не идиопатической ДКМП, что подтверждает
наличие различных механизмов развития данного заболевания [42].
Единичный случай значительного снижения пика ФК был зафиксирован Y. Masuda и соавт. у одного больного с бессимптомной ДКМП, что можно трактовать как скрытое нарушение метаболизма на раннем этапе формирования кардиомиопатии [43]. Кроме того, у 6 больных ДКМП был продемонстрирован рост показателей энергетического метаболизма в ответ на лекарственную терапию, что означает теоретическую возможность применения МРС в оценке действия лекарственных препаратов. Было показано, что небольшая физическая нагрузка у больных ДКМП не дает значительного снижения энергетического индекса, свидетельствуя о возможности
некоторой компенсации у данных больных [45].
Ряд работ, посвященных ГКМП, отражает значительное снижение индекса ФК/АТФ по сравнению с таковым у здоровых добровольцев. Кроме того, исследования показали, что изменения данных МРС не всегда коррелируют с нарушением перфузии миокарда при проведении сцинтиграфии с таллием. Авторы предполагают, что разобщение перфузии и энергетического метаболизма является уникальной чертой ГКМП [34]. В одной из публикаций описаны нарушения энергетического метаболизма у больных с бессимптомной ГКМП, что может свидетельствовать о первичности нарушений энергетического метаболизма и вторичности клинических проявлений [33]. При обследовании 31 одного пациента с ГКМП, обусловленной генными мутациями (тяжелая цепь бета-миозина, сердечного тропонина-Т, С-миозинсвязывающего белка), обнаружено нарушение энергетического метаболизма, независимо от группы мутаций. Схожие изменения найдены и у больных с генетическими мутациями без гипертрофии миокарда [51].
Существуют данные, подтверждающие возможность оценки тяжести СН у больных ДКМП, поскольку изменения энергетического индекса миокарда коррелируют с уровнем в плазме натрийуретического пептида В-типа, а значит и с тяжестью СН [52]. S. Neubauer и соавт., обследовавших 39 пациентов с ДКМП, показали, что отношение ФК/АТФ является очень чувствительным предиктором общей и сердечно-сосудистой смертности у данной группы больных. Авторы выявили, что среди трех прогностических признаков — функциональный класс по классификации Нью-Йоркской кардиологической ассоциации, фракция выброса ЛЖ и индекс ФК/АТФ — последний имел наибольшую статистическую значимость, а для фракции выброса ЛЖ выявлена только тенденция к прогнозированию сердечно-сосудистой смертности [53] (рис. 3).
Рисунок 3. 31Р-спектры, полученные на томографе с напряженностью магнитного поля 1,5 Т.
Заключение
МРС по фосфору имеет уникальные преимущества, в первую очередь, возможность неинвазивного определения концентраций высокоэнергетических фосфатов, играющих одну из основных ролей в энергетическом метаболизме миокарда [14]; альтернативным методом является лишь биопсия [15]. Теоретически возможное объединение магнитно-резонансной спектроскопии с магнитно-резонансной томографией сердца позволяет обсуждать вопрос о методе комплексной диагностики заболеваний сердца, с оценкой анатомии, размеров, функции, наличия дефектов перфузии или структурных изменений миокарда, а также состояния его энергетического метаболизма [54]. Данный комплексный метод не будет нуждаться в ионизирующем излучении или введении радиофармпрепаратов [55]. Однако магнитно-резонансная спектроскопия по фосфору имеет ряд ограничений, препятствующих ее внедрению в клиническую практику [14]. В первую очередь, это неспецифичность изменений при различных сердечно-сосудистых заболеваниях.



