ВВЕДЕНИЕ
Системные васкулиты, ассоциированные с антинейтрофильными цитоплазматическими антителами (АНЦА-СВ), относятся к числу редких тяжелых ревматологических заболеваний с полиорганным поражением, в связи с чем требуют внимания врачей широкого круга специальностей.
Группа АНЦА-СВ характеризуется некротизирующим васкулитом с отсутствием иммунных депозитов и преимущественным вовлечением мелких сосудов (капилляров, венул, артериол и мелких артерий), что ассоциируется с гиперпродукцией АНЦА, проявляющих специфичность к миелопероксидазе (МПО) или протеиназе-3 (ПР-3) [1]. АНЦА-СВ включают три нозологические формы – гранулематоз с полиангиитом (ГПА), микроскопический полиангиит (МПА) и эозинофильный гранулематоз с полиангиитом (ЭГПА), общепринятые определения которых приведены в таблице 1.
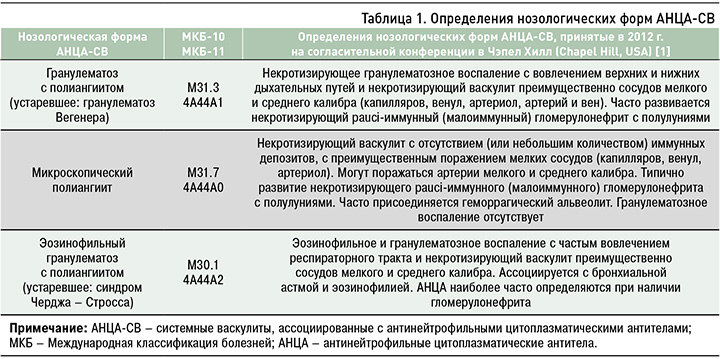
Для АНЦА-СВ характерна клиническая триада, включающая поражение верхних дыхательных путей, легких и почек, но возможна и локальная патология ЛОР-органов или развитие изолированного АНЦА-ассоциированного гломерулонефрита (ГН). Типичной триаде могут сопутствовать поражение различных других органов и систем, неспецифические симптомы.
Патология респираторных органов при АНЦА-СВ может сопровождаться весьма скудной клинической симптоматикой, поэтому при подозрении на эту патологию необходимо планомерное обследование пациента с использованием методов визуализации, прежде всего компьютерной томографии (КТ), для выявления возможных локализаций поражения.
В основе патологии почек при всех формах АНЦА-СВ лежит pauci-иммунный (малоиммунный) ГН с полулуниями, при котором в ткани этого органа отсутствуют иммунные отложения, и наблюдается наличие клеточных или фиброзных полулуний в клубочках. Такой ГН характеризуется быстро прогрессирующим снижением фильтрационной функции почки – более чем на 50% за период менее 3 мес. [2]. В большинстве случаев pauci-иммунный быстропрогрессирующий ГН (БПГН) с полулуниями выступает проявлением АНЦА-СВ и может рассматриваться как его синоним [3].
Особо редкий случай – сочетание гиперпродукции АНЦА и антител к базальной мембране клубочков; в такой ситуации заболевание характеризуется крайне тяжелым течением с развитием БПГН и диффузного альвеолярного кровотечения.
Следует учитывать, что АНЦА-ассоциированный ГН способен осложнять течение инфекционного эндокардита.
Большую роль в подтверждении диагноза АНЦА-СВ играет выявление АНЦА со специфичностью к ПР-3 или МПО, а также данные биопсии (почки, слизистой верхних дыхательных путей, легких, при ЭГПА – кожи). Для ГПА типична гистологическая картина некротизирующего гранулематозного воспаления с полиморфным клеточным инфильтратом, содержащим многоядерные гигантские клетки, и/или некротизирующего васкулита мелких сосудов. При МПА выявляют только признаки некротизирующего васкулита в отсутствие гранулематозной воспалительной реакции. Для ЭГПА, в свою очередь, характерно присутствие эозинофилов в периваскулярном инфильтрате, могут обнаруживаться явления гранулематозного воспаления. Несмотря на большое значение гистологического исследования для подтверждения диагноза АНЦА-СВ, результаты биопсии не всегда информативны. Биопсия кожи имеет значение прежде всего при диагностике ЭГПА для подтверждения тканевой эозинофилии. Наибольшую диагностическую ценность демонстрируют биопсия почки и трансторакальная биопсия легких, сложные инвазивные вмешательства.
Определение в сыворотке крови AНЦA прежде всего имеет значение в качестве диагностического маркера в дебюте АНЦА-СВ, в отсутствие клинической активности чувствительность АНЦА снижается до 60–70%. АНЦА с цитоплазматическим типом иммунофлуоресцентного свечения (цАНЦА), обусловленные присутствием антител к ПР-3, высокочувствительны и специфичны (более 90%) для ГПА. АНЦА с перинуклеарным типом свечения (пАНЦА), наличие которых при АНЦА-СВ связано с антителами к МПО, обнаруживают у 35–70% больных ЭГПА. При МПА в европейской популяции примерно с одинаковой частотой выявляют антитела к ПР-3/цАНЦА и к МПО/пАНЦА. В Китае и Японии у пациентов с МПА преимущественно присутствуют антитела к МПО, при этом ГПА диагностируют крайне редко.
В зависимости от нозологической принадлежности и специфичности АНЦА при этом заболевании наблюдаются различия в спектре клинических проявлений, прогнозе и ответе на патогенетическую терапию ритуксимабом (РТМ), циклофосфаном (ЦФ) и мофетила микофенолатом (ММФ) [4].
Необходимо отметить, что АНЦА могут отсутствовать в сыворотке крови пациентов при рauci-иммунном ГН с полулуниями: доля таких случаев варьирует от 6 до 20% (так называемый АНЦА-негативный АНЦА-ГН) [9–11]. АНЦА-негативные варианты составляют примерно половину случаев ЭГПА. При локальной форме ГПА, ограниченной патологией респираторного тракта или глаз, также могут встречаться АНЦА-негативные случаи (17–46%) [5], требующие проведения подробного дифференциально-диагностического поиска, в том числе с исключением IgG4-связанного заболевания, злокачественных новообразований.
АНЦА имеют невысокую ценность для мониторирования активности заболевания, поскольку могут присутствовать в сыворотке крови даже во время полной клинической ремиссии заболевания. С другой стороны, возможно быстрое исчезновение АНЦА после начала лечения, включая изолированное применение глюкокортикоидов, несмотря на разгар клинических симптомов. Это может становиться препятствием для диагностики АНЦА-СВ, когда в неясных случаях применяют глюкокортикоиды для уменьшения воспалительных проявлений заболевания.
Активная стадия АНЦА-СВ сопровождается увеличением скорости оседания эритроцитов (СОЭ), концентрации С-реактивного белка (СРБ), нормохромной нормоцитарной анемией, нейтрофильным лейкоцитозом, тромбоцитозом, склонностью к гиперкоагуляции, гиперфибриногенемии. Для ЭГПА типична периферическая эозинофилия. Отмечается корреляция между уровнем СРБ и активностью заболевания. В некоторых случаях в сыворотке крови обнаруживают ревматоидный фактор, что у пациентов с артритом и/или артралгиями может быть причиной ошибочной диагностики раннего ревматоидного артрита.
Классификационные критерии ГПА, МПА и ЭГПА [6–8], предложенные в 2022 г. Американской коллегией ревматологов (American College of Rheumatology, ACR) и Европейским альянсом ревматологических ассоциаций (European Alliance of Associations for Rheumatology, EULAR), представлены в таблице 2. Подчеркнем, что эти критерии разработаны для создания однородных групп пациентов в научных исследованиях и не предназначены для широкого применения в клинической практике. Они могут иметь ограничения при диагностике АНЦА-СВ на ранней стадии заболевания или при заинтересованности одного органа (например, почек). Тем не менее в клинической практике критерии ACR – EULAR 2022 г. могут быть полезным ориентиром при установлении диагноза АНЦА-СВ.
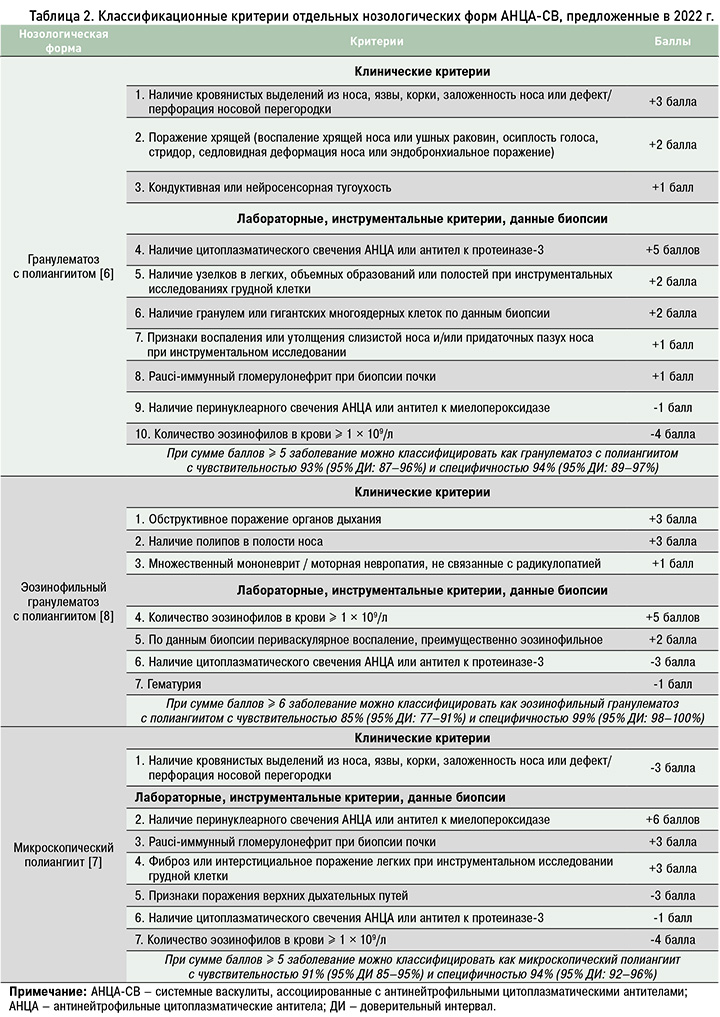
Критерии ACR – EULAR 2022 г. [6–8] имеют ограничения при АНЦА-негативных вариантах АНЦА-СВ, моноорганном поражении (органа зрения, гортани, почек и др.), в случаях невозможности выполнения морфологического исследования (например, в связи с тяжестью состояния пациента или риском опасных осложнений манипуляции), а также на ранней стадии заболевания, когда различия между отдельными нозологическими формами АНЦА-СВ могут быть не очевидны. Так, появление клинических эквивалентов гранулематозного воспаления в респираторных органах (деструктивного синусита, перфорации носовой перегородки, формирование подскладочной гранулемы гортани) при ГПА может быть значительно отсрочено [9], а в редких случаях ЭГПА эозинофилия в циркулирующей крови иногда не определяется, несмотря на выраженную тканевую эозинофилию. В этих обстоятельствах при установлении диагноза возможно использование общего термина АНЦА-СВ [1], который включен в Международную классификацию болезней 11-го пересмотра под кодом 4А44А.
Основываясь на собственном анализе клинических проявлений первого месяца заболевания у 210 пациентов с различными формами АНЦА-СВ (123 ГПА, 71 МПА, 16 ЭГПА), можно отметить, что спектр манифестных признаков патологии прежде всего представлен симптомами поражения ЛОР-органов (30–81%), легких и/или бронхов (27–69%) в сочетании с лихорадкой (52–63%) и поражением суставов (18–44%), при ЭГПА и МПА – чаще артритом, чем артралгиями. Наиболее агрессивно дебютирует МПА: в первый месяц болезни нередко присутствуют симптомы ГН (27%), а поражение легких у каждого второго осложняется кровохарканьем. Период от начала заболевания до фазы максимально выраженных клинических проявлений в среднем составляет при ГПА 3 (мах–мin 1–156) мес., при МПА 1 (1–102) мес., при ЭГПА 1 (1–6) мес. Быстрому прогрессированию АНЦА-СВ с генерализацией васкулита, развитием БПГН могут способствовать хирургические вмешательства на придаточных пазухах носа, экстракция зуба.
Проявления развернутой стадии АНЦА-СВ рассмотрены ниже.
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА ГРАНУЛЕМАТОЗА С ПОЛИАНГИИТОМ
Клиническое течение ГПА может значительно варьировать [9]: протекать как генерализованное заболевание с тяжелой полиорганной патологией, включая ГН (так называемая генерализованная форма), или ограничиваться локальным процессом с изолированным поражением органов верхних дыхательных путей и/или глаз (локальная форма), частота которой достигает 38%. Манифестируя как локальный процесс, ГПА в течение последующих месяцев может трансформироваться в генерализованную форму у 70% больных. В сравнении с другими АНЦА-СВ, ГПА отличает высокая склонность к рецидивам (65%), причем последние могут развиваться после многолетней полной ремиссии заболевания.
Развернутую клиническую картину ГПА определяет клиническая триада с вовлечением верхних дыхательных путей, легких и почек, которую сопровождают неспецифические симптомы: общая слабость, лихорадка (70–90%), артралгии (реже артрит) и миалгии (50%), снижение массы тела.
ЛОР-органы – самая типичная область поражения при ГПА (93–99%), его визитная карточка. В подавляющем большинстве случаев присутствует некротизирующее гранулематозное воспаление верхних дыхательных путей, способное приводить к деструкции хрящевой и костной тканей (с формированием перфорации носовой перегородки, деструкции костных стенок придаточных пазух, в том числе стенки орбиты с распространением гранулематозного воспаления в полость орбиты). Язвенно-некротический ринит характеризуется жалобами пациентов на заложенность носа, сукровичное отделяемое из носа, а также кровянистые корки, порой весьма массивные, из-за которых течение заболевания у трети больных осложняется рецидивирующими носовыми кровотечениями. Поскольку у части пациентов клинические симптомы со стороны ЛОР-органов могут быть мало выраженными или отсутствовать, особенно в дебюте заболевания, в процессе диагностики во всех случаях подозрения на АНЦА-СВ следует выполнять КТ придаточных пазух носа и сосцевидных отростков. По данным КТ, более чем в 60% случаев ГПА выявляются разнообразные изменения придаточных пазух – от изолированного гайморита, фронтита, этмоидита, мастоидита до тяжелого деструктивного пансинусита. Полости придаточных пазух могут быть тотально заполнены гранулематозной тканью, возможно воспаление хрящей носа. У 25% больных вследствие прогрессирования деструктивного ринита формируется седловидная деформация носа.
Помимо язвенно-некротического риносинусита, у пациентов наблюдается вовлечение в патологический процесс гортани и трахеи (гранулематозный трахеобронхит), сопровождающееся формированием подскладочной гранулемы (35%), стенозом гортани с необходимостью наложения трахеостомы. На этапе диагностики всем лицам с подозрением на АНЦА-СВ требуется проведение ларингоскопии.
Более чем у половины пациентов поражается орган слуха (средний отит, евстахеит, мастоидит), что влечет за собой снижение слуха или полную глухоту. При этом чаще отмечается смешанная, а не изолированная нейросенсорная или кондуктивная тугоухость. Возможно воспаление наружной ушной раковины (хондрит, кожный васкулит). Течение серозного среднего отита нередко осложняется гнойной инфекцией.
Легкие поражаются в 50–70% случаев: наблюдается некротизирующее гранулематозное воспаление паренхимы этого органа и/или слизистой бронхов. Зачастую патология легких сопровождается скудными симптомами, и даже при весьма крупных легочных гранулемах кашель, одышка, аускультативные признаки могут отсутствовать. При рентгенографическом исследовании в легких определяются, как правило, двусторонние, нередко субплеврально расположенные, узлы или инфильтраты, склонные к распаду и формированию полостей, что значительно повышает риск инфекционных осложнений. Несмотря на то что деструктивный процесс в легких у 35% сопровождается кровохарканьем, легочное кровотечение при ГПА развивается относительно редко, в сравнении с МПА. У 30% пациентов с ГПА выявляют гранулематозный эндобронхит. Значительно реже отмечаются плеврит, умеренное увеличение внутригрудных лимфатических узлов.
Почки вовлекаются в патологический процесс у 55–70% пациентов, что может проявляться разнообразно, от бессимптомной протеинурии и микрогематурии (редко макрогематурией) до БПГН. Описаны случаи обструктивной нефропатии вследствие васкулита с гранулематозным воспалением мочеточников, уретры или простаты. У больных ГПА быстропрогрессирующее течение ГН наблюдается значительно реже, чем при МПА. Не свойственны ГПА, как и другим формам АНЦА-СВ, нефротический синдром или злокачественная артериальная гипертензия.
Частота поражения сердца и сосудов на фоне ГПА не превышает 20%. Как и при всех других АНЦА-СВ, у больных ГПА отмечается возрастание риска сердечно-сосудистых заболеваний (ишемической болезни сердца, инсульта, периферической артериальной окклюзии), при этом высока вероятность развития острого инфаркта миокарда, но не стенокардии, особенно у лиц старше 50 лет, у мужчин, а также при применении высокой кумулятивной дозы ЦФ. В 60% случаев поражение сердца может протекать асимптомно. Возможны васкулит крупных сосудов, напоминающий артериит Такаясу, тромбофлебит различных локализаций, тромбоэмболия легочной артерии (ТЭЛА).
Орган зрения страдает в половине случаев ГПА, и у каждого пятого пациента это приводит к слепоте. Для этой формы АНЦА-СВ типичен псевдотумор орбиты вследствие формирования периорбитальной гранулемы (25%). Реже встречаются конъюнктивит, эписклерит, склерит, увеит. Склерит может осложняться перфорацией, рубцеванием. Возможна заинтересованность слезных желез, в том числе в рамках редкого сочетания ГПА с IgG4-связанным патологическим процессом. Вторичный дакриоцистит обусловлен гранулематозным воспалением с затруднением оттока жидкости по слезному каналу, при этом нередко происходит присоединение инфекции. Описаны неврит зрительного нерва, окклюзия центральной артерии сетчатки. Тяжелой патологии глаз сопутствует развитие вторичной глаукомы.
У 25–35% пациентов имеют место кожные изменения в виде геморрагических или язвенно-геморрагических высыпаний преимущественно на конечностях, также для ГПА характерны язвенно-геморрагические образования на разгибательной поверхности локтей. Реже наблюдаются уртикарные высыпания, подкожные узелки, livedo reticularis (пурпурный сетчатый сосудистый рисунок на коже, обусловленный расширением венул вследствие образования мелких тромбов в капиллярах). Описана симптоматика гангренозной пиодермии, панникулита, феномен Рейно.
Периферическая нервная система бывает поражена в первую очередь с развитием асимметричного сенсомоторного множественного мононеврита (20–30%), значительно реже встречается дистальная симметричная полинейропатия. Возможен одонтогенный неврит V, VII пары черепно-мозговых нервов, который диагностируют у каждого четвертого больного ГПА с патологией органа слуха. Нейропатия может сопровождаться весьма выраженными болями.
Центральная нервная система затрагивается заболеванием в единичных случаях (3%), при этом пациентов могут беспокоить головная боль, пахименингит, нарушение мозгового кровообращения, эписиндром, гипопитуитаризм. Вовлечение спинного мозга в патологический процесс не характерно.
Желудочно-кишечный тракт у больных ГПА заинтересован редко (5%), возможно развитие ишемических язв желудка, кишечника, осложняющихся кровотечением. Отмечаются патология слюнных желез, гингивит, глоссит, изъязвления слизистой полости рта.
В основу обновленных в 2022 г. критериев ГПА (см. табл. 2) [6] прежде всего положены его клинические признаки:
- патология верхних дыхательных путей с наличием кровянистых выделений из носа, изъязвлений, корок, заложенности носа или дефекта/перфорации носовой перегородки (+3 балла);
- поражение хрящевой ткани с воспалением хрящей носа или ушных раковин, осиплостью голоса или стридором, седловидной деформацией носа, эндобронхитом (+2 балла);
- поражение органа слуха с кондуктивной или нейросенсорной тугоухостью (+1 балл).
Лабораторные и инструментальные критерии ГПА включают:
- наличие цитоплазматического свечения АНЦА или антител к ПР3 (+5 баллов);
- по данным методов визуализации – узелки, объемные образования или полости в легких (+2 балла), признаки воспаления или утолщения слизистой носа и/или придаточных пазух носа (+1 балл);
- при гистологическом исследовании биоптата – наличие гранулем или гигантских многоядерных клеток (+2 балла), в почках – картина рauci-иммунного ГН (+1 балл).
К критериям с отрицательной коннотацией отнесен ряд лабораторных маркеров, такие как наличие перинуклеарного свечения АНЦА или антител к МПО (-1 балл) и выявление эозинофилии крови ≥ 1 × 109/л (-4 балла).
При сумме баллов ≥ 5 заболевание можно классифицировать как ГПА.
В качестве иллюстрации представляем клиническое наблюдение.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ ГРАНУЛЕМАТОЗА С ПОЛИАНГИИТОМ
Пациентка, 58 лет, через 3 мес. после ларинготрахеита отметила появление высыпаний на коже в области коленных и локтевых суставов. Вскоре к этим симптомам добавилась заложенность носа, при рентгенографии был выявлен левосторонний гайморит.
Лечение включало пункцию гайморовой пазухи и применение антибиотиков (цефиксима, левофлоксацина), без эффекта. Появились субфебрилитет и кашель. На КТ сохранялись явления левостороннего синусита, в легких были обнаружены двусторонние инфильтраты, присутствовала высокая лабораторная воспалительная активность (СРБ > 150 мг/л). Диагностирована полисегментарная бронхопневмония, пациентке были назначены антибиотики, противогрибковые препараты. На фоне терапии улучшения состояния не происходило, сохранялись заложенность и кровянистое отделяемое из носа, присоединились фебрильная лихорадка, двусторонний средний отит со снижением слуха до глухоты. По данным КТ, наблюдалась отрицательная динамика с увеличением размеров двусторонних очагов в легких.
Пациентку госпитализировали в ФГБУ «Центральная клиническая больница с поликлиникой» Управления делами Президента РФ. Был заподозрен ГПА, выполнена биопсия слизистой носа, сыворотка крови направлена в лабораторию для определения АНЦА. При гистологическом исследовании биоптата отмечалась картина умеренно выраженной лимфоплазмоцитарной инфильтрации с примесью эозинофилов и сегментоядерных лейкоцитов. Выявлена гиперпродукция аПР-3 более 10 норм, присутствовала высокая лабораторная воспалительная активность (СРБ > 200 мг/л, СОЭ 120 мм/ч, тромбоцитоз 543 × 109/л), нейтрофильный лейкоцитоз 15 × 109/л, анемия (гемоглобин – 95 г/л), эритроцитурия (все поля зрения), протеинурия 1,2 г/сут., быстро нарастал уровень креатинина до 239 мкмоль/л, что свидетельствовало о развитии БПГН.
Была неотложно индуцирована анти-В-клеточная терапия РТМ в сочетании с метилпреднизолоном (МП) 32 мг/сут., ММФ 1,5 г/сут. Наблюдался положительный эффект лечения с восстановлением слуха, исчезновением изменений в анализах мочи, нормализацией СРБ (1 мг/л) и гемоглобина (120 г/л), снижением креатинина через 6 мес. лечения до 98 мкмоль/л. Доза МП была уменьшена до 12 мг/сут.
Подводя итог, констатируем, что клиническое течение болезни в представленном наблюдении соответствовало критериям диагноза ГПА (суммарно 12 баллов): кровянистые выделения из носа, заложенность носа (+3); тугоухость (+1); аПР-3 (+5); по данным КТ – объемное образование в легких (+2) и синусит (+1). Вместе с тем в результате гистологического исследования биоптата слизистой придаточных пазух носа гранулематозное воспаление, наличие гигантских многоядерных клеток выявлены не были. Обратим внимание, что выполнение синусотомии в этом случае можно обсуждать в качестве фактора, спровоцировавшего прогрессирование заболевания с развитием БПГН. Быстрое, через 2 мес. от манифестации заболевания, назначение адекватной патогенетической терапии позволило добиться выраженного эффекта с обратным развитием всех симптомов, восстановлением функции почек.
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА МИКРОСКОПИЧЕСКОГО ПОЛИАНГИИТА
Визитной карточкой МПА можно назвать pauci-иммунный ГН с полулуниями. Часто имеет место геморрагический альвеолит, причем в респираторных органах всегда отсутствует гранулематозное воспаление [10]. На ранних стадиях заболевания отмечаются такие неспецифические симптомы, как общая слабость, лихорадка, боли в суставах, мышцах. Артралгии, реже стойкий неэрозивный артрит (преимущественно крупных суставов) выявляются более чем у половины пациентов и могут ошибочно расцениваться как проявления ревматоидного артрита, особенно при положительном результате определения ревматоидного фактора. После появления первых признаков МПА, как правило, быстро происходит генерализация васкулита. Развернутая фаза МПА характеризуется как тяжелое полиорганное заболевание.
ЛОР-органы могут быть заинтересованы в виде некротического или атрофического ринита (30–70%), синусита с невыраженным пристеночным утолщением слизистой придаточных пазух носа, но без деструкции костных стенок по данным КТ. Возможен средний отит (20–30%). Вовлечение ЛОР-органов при МПА подчас не сопровождается клиническими симптомами и обнаруживается только при прицельном обследовании (риноскопия, КТ). В отличие от ГПА, носовые кровотечения при данной форме АНЦА-СВ развиваются редко (10%), перфорация носовой перегородки встречается в единичных случаях.
Легкие поражаются в 35–70% случаев, что морфологически представлено некротизирующим альвеолитом. Для МПА свойственно тяжелое течение легочной патологии, у половины больных возникает легочное кровотечение, в 50% случаев – фатальное. На начальных этапах альвеолит нередко протекает асимптомно и обнаруживается только при выполнении КТ; диффузное легочное кровотечение при этом может развиться внезапно. На КТ в легочной паренхиме выявляют инфильтраты и/или участки «матового стекла», но зоны деструктивных изменений отсутствуют. У пациентов с МПА и АНЦА со специфичностью к МПО, в отличие от МПА с аПР-3, возможно формирование интерстициального фиброза с КТ-картиной «сотового легкого» или очагового фиброза.
Почки попадают под удар у подавляющего числа больных МПА (90–100%): характерен pauci-иммунный (малоиммунный) ГН с полулуниями, в трети случаев протекающий как БПГН. ГН может быть манифестным признаком или длительно оставаться единственным проявлением заболевания. Наблюдаются микрогематурия (реже макрогематурия), умеренная протеинурия. Развитие нефротического синдрома для МПА не характерно. Более чем у 60% больных снижается азотовыделительная функция почек, вплоть до терминальной стадии с потребностью в заместительной почечной терапии, что во многом определяет прогноз. Катастрофическое течение заболевание приобретает при сочетании АНЦА и антител к базальной мембране клубочков – наиболее тяжелом клинико-иммунологическом варианте АНЦА-СВ.
Сердце при МПА поражено в каждом пятом случае. Как и у всех больных АНЦА-СВ, при МПА возрастает риск кардиоваскулярных осложнений (ишемической болезни сердца, инсульта, окклюзий периферических артерий). В активную фазу заболевания могут формироваться тромбозы, включая ТЭЛА.
Орган зрения заинтересован у 30% пациентов, преимущественно в виде конъюнктивита, склерита и эписклерита. Васкулит сетчатки приводит к слепоте.
Кожа изменена в 70% случаев в виде геморрагических или язвенно-геморрагических высыпаний большей частью на коже конечностей. Реже встречаются уртикарные элементы, livedo reticularis, некрозы кожи и подлежащих тканей, возможен панникулит.
Периферическая нервная система страдает у 30% пациентов, что может сопровождаться асимметричным сенсорно-моторным множественным мононевритом, как правило, нижних конечностей.
Центральная нервная система вовлекается крайне редко, при этом отмечаются головная боль, нарушения мозгового кровообращения.
Желудочно-кишечный тракт поражен у 10% пациентов: могут присутствовать боли в животе, диарея, иногда происходит кровотечение как следствие ишемических язв желудка и кишечника. Описаны панкреатит, холецистит, гепатомегалия, синдром Бадда – Киари. Поражение слизистой полости рта проявляется язвенным стоматитом, глосситом.
Ключевые критерии МПА 2022 г. (см. табл. 2) [7] – лабораторные и инструментальные данные:
- наличие перинуклеарного свечения АНЦА или антител к МПО (+6 баллов);
- картина рauci-иммунного ГН при биопсии почки (+3 балла);
- фиброз или интерстициальное заболевание легких при инструментальном исследовании (+3 балла).
Единственному клиническому критерию МПА присвоено отрицательное значение: это наличие кровянистых выделений из носа, язвы, корки, заложенность носа или дефект/перфорация носовой перегородки (-3 балла). Такие признаки являются клиническими эквивалентами гранулематозного воспаления, типичного для ГПА, что исключает диагноз МПА, так же как и инструментальное подтверждение поражения верхних дыхательных путей (-3 балла).
Лабораторные критерии с отрицательной коннотацией включают наличие цитоплазматического свечения АНЦА или антител к ПР3 (-1 балл) и эозинофилию крови ≥ 1 × 109/л (-4 балла), что типично для ГПА и ЭГПА соответственно.
При сумме баллов ≥ 5 заболевание можно классифицировать как МПА.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ МИКРОСКОПИЧЕСКОГО ПОЛИАНГИИТА
У пациентки 51 года с ожирением (индекс массы тела 35,6 кг/м2) и артериальной гипертензией после перенесенного затяжного гайморита появились боли и отечность в мелких суставах кистей, позже – прогрессирующие боли в локтевых, плечевых суставах. По месту жительства был диагностирован серонегативный ревматоидный артрит, лечение гидроксихлорохином в течение 3 мес. не дало эффекта. К клинической картине присоединились миалгии, одышка, после чего пациентку госпитализировали в стационар по месту жительства.
При КТ с контрастированием была выявлена ТЭЛА, интерстициальные изменения в легких в виде симптома матового стекла. При ультразвуковом исследовании – признаки тромбоза левой подколенной вены. Больную беспокоили лихорадка 38 °С, кровянистые выделения из носа, носовые кровотечения, артралгии, возникло онемение кистей рук, в лабораторных анализах обнаружено повышение креатинина до 239 мкмоль/л. Был заподозрен АНЦА-СВ, при исследовании АНЦА получены положительные результаты аМПО.
Назначенное лечение включало ЦФ внутривенно суммарно 3 г, далее – прием микофеноловой кислоты 1440 мг/сут., а также МП внутрь 48 мг/сут. с положительным, но неполным эффектом. Лабораторные признаки воспалительной активности отсутствовали (СРБ 2 мг/л), но сохранялись эритроцитурия по Нечипоренко 7400, протеинурия 0,3 г/л, повышение креатинина 188 мкмоль/л, гиперпродукция аМПО 11 норм, анемия (гемоглобин – 101 г/л). По данным КТ, имелись фиброзные изменения в легких, по данным эхокардиографии – признаки перикардита. Прогрессировал медикаментозный синдром Иценко – Кушинга, развилась стероидная миопатия. Пациентке была выполнена биопсия почки, получена картина pauci-иммунного фокального склерозирующего ГН с 45% фиброзных полулуний в клубочках почки (4 из 11 склерозированы).
Через год от начала заболевания в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» пациентке была инициирована терапия РТМ в сочетании с ММФ 2 г/сут., что позволило достичь ремиссии МПА со снижением креатинина до 97 мкмоль/л, доза МП была уменьшена до 4 мг/сут.
Таким образом, клиническая картина заболевания в представленном наблюдении соответствовала критериям диагноза МПА (суммарно 6 баллов): аМПО (+6); pauci-иммунный ГН при биопсии почки (+3); интерстициальное поражение легких по данным КТ (+3); кровянистые выделения из носа (-3); признаки поражения верхних дыхательных путей при рентгенологическом исследовании (-3). В манифестный период заболевание было ошибочно расценено как серонегативный ревматоидный артрит. Однако внимательное изучение анамнеза и выявление связи начала заболевания с затяжным гайморитом должно было позволить обоснованно заподозрить дебют АНЦА-СВ.
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА ЭОЗИНОФИЛЬНОГО ГРАНУЛЕМАТОЗА С ПОЛИАНГИИТОМ
Для клинического течения ЭГПА характерны три последовательных фазы [11], которые разворачиваются на протяжении нескольких лет. Первая из них (длительностью до 30 лет) включает появление бронхиальной астмы, полипозного синусита, аллергического ринита, симптомов лекарственной непереносимости, при этом периферическая эозинофилия не всегда выражена. Для второй фазы типично присоединение эозинофильных инфильтратов в виде эозинофильной пневмонии или эозинофильного гастроэнтерита, что часто сочетается с периферической эозинофилией более 10%. Третья фаза непосредственно отражает формирование ЭГПА, характеризуется быстро прогрессирующим полиорганным поражением, обусловленным системным некротизирующим эозинофильным васкулитом с эозинофильным гранулематозным воспалением.
Генерализацию васкулита сопровождают неспецифические симптомы: общая слабость, лихорадка (80%), миалгии голеней (50%). Поражение суставов в виде неэрозивного полиартрита или артралгий наблюдается у 50% больных.
Центральное место в диагностике ЭГПА занимает правильная оценка бронхиальной астмы и эозинофилии, которая может встречаться при широком спектре заболеваний [12]. Необходимо исключить реактивную эозинофилию, в том числе крайне редкую семейную гиперэозинофилию, эозинофилии лекарственного и инфекционного генеза, вызванные прежде всего гельминтами (токсокароз, стронгилоидоз) и грибами (аспергиллез), эозинофилии при миелопролиферативных заболеваниях (хронический эозинофильный лейкоз, хронический миелолейкоз, системный мастоцитоз, миелодиспластические синдромы), паранеопластическую реакцию (при раке легкого, шейки матки и др.).
Ранним признаком болезни выступает бронхиальная астма, частота которой при ЭГПА достигает 80–100%. Для поражения верхних дыхательных путей при ЭГПА (80%) характерны аллергический полипозный ринит (55%) и синусит (45%), которые, наряду с бронхиальной астмой, относятся к манифестным симптомам заболевания. В отличие ГПА, образование кровянистых корок в носу, носовые кровотечения наблюдаются крайне редко.
Легкие заинтересованы у 70% пациентов с развитием мигрирующих легочных инфильтратов (эозинофильная пневмония) или узлов без полостей распада по данным КТ. Кровохарканье наблюдается у трети больных, но случаи легочного кровотечения крайне редки. Возможны поражение плевры (эозинофильный плеврит), умеренное увеличение внутригрудных лимфатических узлов.
Почки при ЭГПА страдают реже (20%), и ГН протекает менее злокачественно, чем при ГПА или МПА. При биопсии почки с иммунолюминесцентной микроскопией у небольшого числа пациентов с ЭГПА выявляют pauci-иммунный ГН с полулуниями.
Сердце при этой форме АНЦА-СВ, напротив, поражается значительно чаще (30–50%), чем при ГПА и МПА. У пациентов имеют место перикардит (гидроперикард, констриктивный перикардит), эндокардит, миокардит, острый коронарный синдром на фоне васкулита коронарных артерий, диффузная ишемическая кардиомиопатия, сердечная недостаточность, разнообразные нарушения ритма и проводимости. Могут развиваться венозные и артериальные тромбозы различных локализаций, ТЭЛА. При ЭГПА сердечная патология становится причиной летального исхода в 50% случаев и протекает тяжелее, чем при ГПА и МПА, что связано с эозинофилией и высвобождением кардиотоксичных эозинофильных протеинов. При этом патологию сердца реже выявляют при АНЦА-позитивном варианте ЭГПА, чем при АНЦА-негативном.
Орган зрения вовлечен в патологический процесс у 30% пациентов, у каждого пятого возникает окклюзия центральной артерии сетчатки или задняя ишемическая нейроретинопатия, что может осложняться преходящим нарушением зрения, слепотой. Возможно развитие эписклерита, склерита.
Кожа изменена в 65% случаев, что проявляется геморрагическими, язвенно-геморрагическими, реже уртикарными высыпаниями преимущественно на коже конечностей, подкожными узелками, livedo reticularis. При биопсии кожи обнаруживают картину некротизирующего васкулита с эозинофильной инфильтрацией.
Периферическая нервная система поражена у 65% пациентов в виде асимметричного сенсорно-моторного множественного мононеврита, что, как правило, сопровождается выраженной болью, медленно отвечающей на лечение. Возможен неврит черепно-мозговых нервов. Неврологические симптомы встречаются при ЭГПА чаще, чем при других вариантах АНЦА-СВ.
Центральная нервная система может быть заинтересована у 10% пациентов в виде нарушений мозгового кровообращения, очаговых изменений мозга по данным визуализационных методов исследований, эписиндрома, которые обычно сочетаются с множественным мононевритом.
Симптомы со стороны желудочно-кишечного тракта беспокоят 10% пациентов в виде болей в животе, диареи, иногда желудочно-кишечного кровотечения, что обусловлено эозинофильным гастроэнтеритом, васкулитом стенки кишечника. Возможно образование ишемических язв, перфорации стенки кишечника. Описаны панкреатит, холецистит, перитонит, асцит, гепатоспленомегалия, синдром Бадда – Киари.
Клинические критерии ЭГПА 2022 г. включают следующие пункты (см. табл. 2) [8]:
- обструктивное поражение органов дыхания (+3 балла);
- наличие полипов в полости носа (+3 балла);
- множественный мононеврит или моторную невропатию, не связанные с радикулопатией (+1 балл).
К лабораторным и инструментальным критериям отнесены:
- эозинофилия крови ≥ 1 × 109/л (+5 баллов);
- данные биопсии с гистологическими признаками преимущественно эозинофильного периваскулярного воспаления (+2 балла).
В качестве отрицательных критериев признаны наличие цитоплазматического свечения АНЦА или антител к ПР3 (-3 балла) и гематурия (-1 балл).
При сумме баллов ≥ 6 заболевание можно классифицировать как ЭГПА.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ ЭОЗИНОФИЛЬНОГО ГРАНУЛЕМАТОЗА С ПОЛИАНГИИТОМ
Пациентка, 23 года, с 18 лет страдающая тяжелым полипозным риносинуситом, по поводу которого выполняли повторные хирургические вмешательства, с 19 лет – эозинофильной бронхиальной астмой, в 22 года перенесла пневмонию. Через 3 мес. после начала лечения ингибитором IgE омализумабом отметила значительное ухудшение самочувствия с присоединением лихорадки 39 °С, артралгий, артрита левого голеностопного сустава, одышки. На КТ наблюдалась картина тотального снижения воздушности придаточных пазух носа, при рентгенографии легких инфильтрат в верхней доле 8 × 44 мм.
Пациентка была госпитализирована в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой». Отмечены обширные экхимозы на коже тыльной поверхности стоп, явления множественного мононеврита конечностей (в большей степени нижних). По результатам обследования были выявлены эозинофилия 40%, высокая лабораторная воспалительная активность (СРБ 95 мг/л), повышение IgE 3,8 нормы, гиперпродукция аМПО более 20 норм. Диагностирован АНЦА (аМПО) – ассоциированный ЭГПА.
После введения внутривенно ЦФ суммарно 2,2 г на фоне преднизолона 50 мг/сут. клинического эффекта не отмечалось, рецидивировала лихорадка, прогрессировало поражение кожи, периферической нервной системы с выраженными болями. Была индуцирована терапия РТМ с последующим достижением полной ремиссии, значительной положительной динамикой изменений придаточных пазух носа по данным КТ, восстановлением дыхания через нос, полным разрешением нейропатии, контролем бронхиальной астмы на фоне снижения дозы МП до 4 мг/сут.
Впоследствии у пациентки состоялись две беременности с благополучными родами в срок. Дальнейшая стойкая ремиссия заболевания поддерживается терапией ингибитором интерлейкина 5 меполизумабом.
Клиническая картина заболевания в представленном случае соответствовала критериям диагноза ЭГПА (суммарно 12 баллов): бронхиальная астма (+3); полипозный риносинусит (+3); множественный мононеврит (+1); эозинофилия ≥ 1 × 109/л (+5). Здесь можно проследить последовательное развитие трех фаз триады Лагнгхама в течение 5 лет: полипозный риносинусит и эозинофильная бронхиальная астма, далее – эпизод пневмонии, возможно, эозинофильной, через 9 мес. после которой разворачивается полиорганное поражение. Достаточно быстрое установление диагноза (через 1,5 мес. после манифестации генерализованной фазы заболевания) и своевременное назначение генно-инженерной биологической терапии (сначала РТМ, затем меполизумаб) позволили минимизировать последствия тяжелого поражения органов.
ЗАКЛЮЧЕНИЕ
Необходимо помнить, что диагноз любого варианта АНЦА-СВ должен быть обоснован выявлением типичных клинических проявлений, результатами визуализационных методов и данными лабораторных исследований. Положительные результаты биопсии играют существенную роль в подтверждении заболевания, но прижизненное патоморфологическое исследование в ряде случаев может оказаться невыполнимым или малоинформативным. Таким образом, важнейшее значение в диагностике АНЦА-СВ имеет детальное клиническое обследование пациента для раннего обнаружения патогномоничных признаков, в том числе протекающих без явных клинических симптомов.
Информированное согласие
От пациентов было получено письменное добровольное информированное согласие на публикацию результатов обследования и лечения в представленных клинических случаях.



