ВВЕДЕНИЕ
Интерес к острым респираторным вирусным инфекциям (ОРВИ), включая грипп и новую коронавирусную инфекцию (COVID-19), связан с высокой распространенностью этих заболеваний и огромным медико-социальным значением. Так, по данным Всемирной организации здравоохранения (ВОЗ), ОРВИ составляют 90–95% всей инфекционной заболеваемости [1]. В России число ежегодно болеющих пациентов превышает 30 млн человек, а ежегодный экономический ущерб оценивается в 60 млрд руб. (приблизительно 80% потерь от всех инфекционных заболеваний) [2, 3]. Медицинские и экономические последствия пандемии COVID- 19 еще предстоит оценить, но сейчас уже понятно, что эти потери будут колоcсальны [4].
Однако при всей значимости пандемии COVID- 19 следует помнить, что и предыдущие пандемии гриппа были глобальны и серьезны. Самая знаменитая инфекция новейшего времени – испанка, по разным данным, унесла жизни от 18 до 50 млн человек [5, 6]. Для сравнения: за год пандемии COVID-19 по всему миру зарегистрировано более 130 млн случаев инфицирования, за 16 мес эпидемии умерло более 4,2 млн человек [7]. Несомненно, важную роль в борьбе с новой коронавирусной инфекцией сыграли оперативное информирование, быстрое реагирование и методы профилактики распространения инфекции. Понятно, что 100 лет назад в разгар испанки не существовало подобных информационных и организационных технологий.
Среди осложнений ОРВИ наиболее часто встречается поражение дыхательной системы: гайморит, трахеит, острый бронхит, пневмония, обострение хронической обструктивной болезни легких (ХОБЛ). На фоне подавления вирусами иммунной системы часто происходит присоединение бактериальной инфекции. Высокий риск осложненного течения ОРВИ имеют пожилые пациенты, а также больные с хроническими заболеваниями [8, 9].
Необходимость комплексного воздействия на различные патогенетические механизмы развития респираторной патологии диктует необходимость поиска и применения средств с полимодальным эффектом [10–12]. К таковым обоснованно относят препараты растительного происхождения. При существенных различиях в составе, формах выпуска, механизмах действия производство таких препаратов должно обеспечиваться надлежащими и соответствующими современным требованиям видами контроля по сбору, хранению, переработки сырья и технологических методик. Безопасными признаются компоненты растений, выращенные в экологически чистых условиях, прошедшие специальную обработку при соблюдении современных технологий. Одним из таких лекарственных препаратов, предназначенных для терапии острых и хронических инфекционно-воспалительных заболеваний органов дыхательной системы, является Умкалор – лекарственное средство растительного происхождения, выпускаемое компанией Dr. Willmar Schwabe (Германия). Из корней южноафриканского растения Pelargonium sidoides производится запатентованный экстракт EPs® 7630, стандартизированный фармакопеями многих европейских странах (Германии, Швейцарии, Австрии, Румынии, Болгарии, России, Латвии, Литвы, Украины, Турции) [13]. Показания к применению препарата Умкалор включают острые и хронические инфекционно-воспалительные заболевания верхних дыхательных путей и ЛОР-органов (синусит, ринофарингит, тонзиллит, бронхит).
Компоненты, входящие в его состав (флавоноиды, танины, кумарины, фенольные соединения, галловая кислота, а также микроэлементы железо, цинк, марганец, медь, стронций), обеспечивают секретомоторное действие, противовирусный и антибактериальный эффект [14]. Противовирусное действие Умкалора проявляется в ингибировании репликации широкого спектра вирусов, вызывающих развитие инфекций респираторного тракта: вирусов гриппа H1N1, H3N2; РС-вируса, вируса парагриппа, вируса Коксаки, коронавируса. Это действие реализуется за счет подавления взаимодействия вирусных частиц с поверхностными белками слизистой, ингибирования гемагглютинации и снижения активности нейраминидазы [15, 16]. Выявлено цитопротективное действие препарата Умкалор, т.е. его способность защищать клетку от проникновения в нее вируса, тем самым снижая степень инвазии и тяжесть воспалительного процесса [16].
В исследовании Roth M. et al. [17] препарат EPs® 7630 в клетках эпителия бронхов человека снижал репликацию риновируса-16 за счет подавления экспрессии индуцируемого костимулятора (ICOS) и его лиганда (ICOSL), а также поверхностного кальретикулинового рецептора, в то время как уровни белков, поддерживающих защиту клетки-хозяина, на фоне его приема возросли. Обсуждается перспективность применения и терапевтический потенциал EPs® 7630 в раннем лечении новых вариантов тяжелой коронавирусной инфекции [18].
Наряду с прочим Умкалор проявляет свое противомикробное действие в отношении грамположительных (Staphilococcus aureus, Staphilococcus pneumonia, β-гемолитический Streptococcus) и грамотрицательных (E.Coli, Klebsiella pneumonia, Proteus mirabilis, Hemophilus influenzae и др.) бактерий [19–21].
Антибактериальное действие препарата обусловлено несколькими механизмами: прямым бактериостатическим эффектом (впрочем, меньшим, чем у антибиотиков); ингибированием адгезии бактерий к здоровым клеткам слизистой и подавлением инвазии бактерий в слизистую оболочку; увеличением адгезии бактерий к мертвым клеткам слизистой, активацией иммунного ответа – усилением фагоцитоза, оксидативного взрыва и внутриклеточного лизиса [22]. Наличие у препарата секретомоторного действия [22, 23] определяет целесообразность его применения при бронхитах и цилиарных дисфункциях. Показана и иммуномодулирующая активность экстракта Pelargonium sidoides [15, 24–26]. Так, препарат EPs® 7630 стимулировал высвобождение оксида азота (NO), интерферона I типа и различных цитокинов, принимающих участие в функционировании защитных механизмов клетки-хозяина [27, 28]. У спортсменов EPs® 7630 модулировал иммунный ответ во время физических упражнений за счет увеличения продукции иммуноглобулина A в слюне, снижения концентраций интерлейкина-15 (ИЛ-15) и ИЛ-6 в сыворотке крови и увеличения уровня ИЛ-15 в слизистой оболочке носа [29]. Совокупность антивирусного, иммуномодулирующего, антибактериального и секретомоторного действия обусловливает многофункциональность препарата Умкалор, которая способствует подавлению и элиминации вирусов из органа-мишени и организма в целом, сдерживанию бактериального процесса [14, 19–21].
Экстракт EPs® 7630 хорошо изучен во многих клинических и экспериментальных исследованиях с середины 70-х гг. XX в. Проведено более 30 клинических исследований по всему миру с участием около 10 000 пациентов (примерно 2/3 – взрослые и 1/3 – дети до 12 лет), использовано 180 млн доз экстракта EPs® 7630 [14]. Исследования показали эффективность и безопасность данного препарата при лечении острых респираторных инфекций, бронхитов, нестрептококковых тонзиллитов, катаральных синуситов у взрослых и детей (табл.).
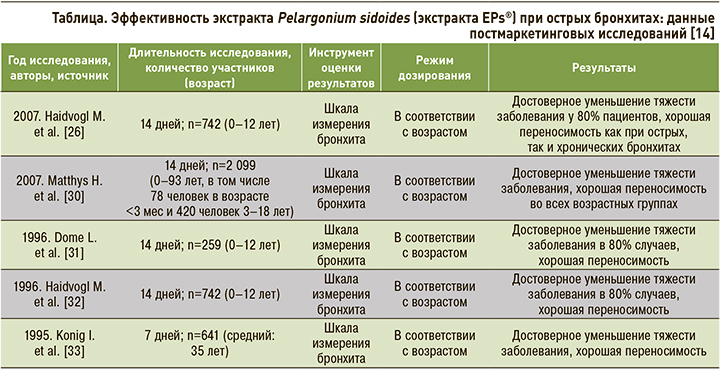
Целый ряд клинических исследований показал, что Умкалор высокоэффективен и безопасен при лечении инфекций дыхательных путей, особенно при остром бронхите, тонзиллофарингите и синусите как у взрослых, так и у детей [12, 13, 15, 25, 34]. Эти и более поздние двойные слепые плацебо-контролируемые РКИ стали предметом систематических обзоров и метаанализов, подтвердивших перспективность применения экстракта EPs® 7630 в лечении респираторной патологии [35–40].
Эффективность экстракта Pelargonium sidoides (EPs® 7630) при остром бронхите у детей проанализирована в систематическом обзоре (5 наблюдательных клинических исследований, n=723), который продемонстрировал достоверное преимущество жидкой формы препарата перед плацебо (рис. 1) [41].
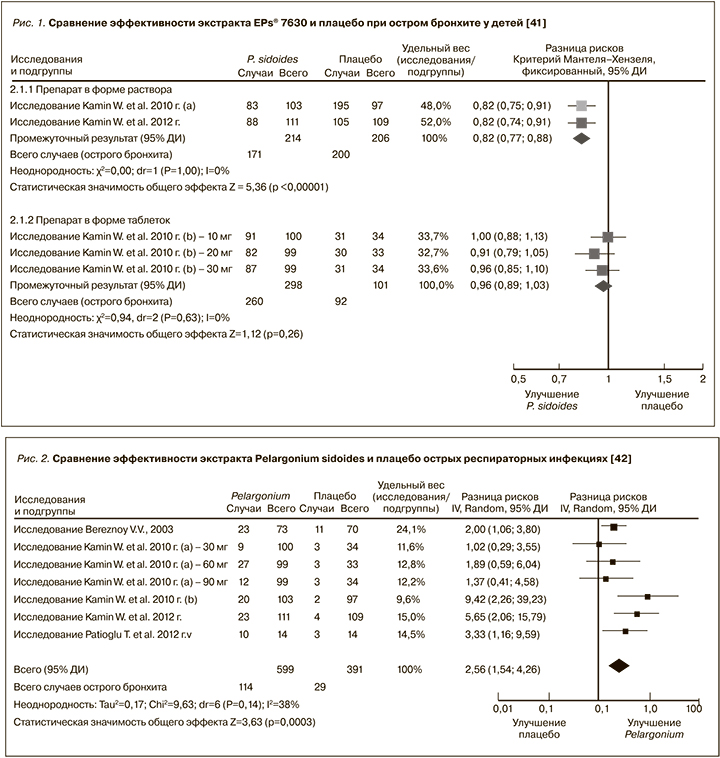
Превосходство экстракта Pelargonium sidoides (EPs® 7630) над плацебо при инфекциях дыхательных путей у детей было также показано в систематическом обзоре 7 наблюдательных клинических исследований, включавших 990 пациентов (рис. 2) [42]. Эти результаты подтверждены и более современными публикациями [43].
Интересным следует признать недавний метаанализ 6 плацебо-контролируемых двойных слепых исследований с участием 523 детей в возрасте от 6 до 10 лет c острым нестрептококковым тонзиллофарингитом или острым бронхитом. В нем было показано, что применение EPs® 7630 позволило значительно снизить среднюю кумулятивную дозу парацетамола, применявшегося у детей в качестве симптоматической терапии. Исследуемый препарат приводил к значительно более быстрому выздоровлению по сравнению с плацебо: через 6–7 дней приема EPs® 7630 доля детей, возобновивших посещение школы, составила 69,8 %, тогда как в группе плацебо аналогичный показатель был равен только 25,6% [44].
ЗАКЛЮЧЕНИЕ
Препарат Умкалор, содержащий высокоактивный и должным образом стандартизированный экстракт Pelargonium sidoides, имеет убедительную доказательную базу при различных заболеваниях дыхательных путей у взрослых и детей. Умкалор рекомендовано назначать на любой стадии острого респираторного заболевания, а также обострениях хронических состояний. В дебюте заболевания это способствует борьбе с инфекцией и облегчает симптомы. Вкупе с симптоматическими противопростудными средствами препарат может использоваться в качестве базовой терапии: в этом случае он минимизирует риски присоединения бактериальной инфекции, обеспечивает мягкое иммуномодулирующее действие и сокращает сроки выздоровления.
Комбинированное антибактериальное, антивирусное, иммуномодулирующее, противовоспалительное, муколитическое и секретомоторное действие препарата Умкалор делает оправданным его назначение для терапии проявлений острых респираторных инфекций и их осложнений (бронхитов, тонзиллитов и риносинуситов) как у детей, так и взрослых. Способность Умкалора подавлять бактериальный процесс создает условия для уменьшения частоты назначения антибактериальной терапии и снижения угрозы развития резистентности микроорганизмов.



