Синдром Кавасаки — острый системный васкулит детского возраста, последствия которого могут являться причиной острого коронарного синдрома у детей и молодых взрослых. Клинические симптомы острой стадии синдрома Кавасаки напоминают инфекционное заболевание (лихорадка, сыпь, инъекция сосудов конъюнктивы, хейлит, шейный лимфаденит). Высокий уровень лабораторных маркеров воспаления отражает выраженность васкулита, поражающего артерии среднего калибра, преимущественно коронарные. Даже без лечения острая стадия сменяется подострой и через 6—8 нед наступает выздоровление. Однако у 25% нелеченых больных васкулит может приводить к тяжелым структурным изменениям сосудистой стенки, включая разрушение внутренней эластической мембраны, истончение медии, что ведет к формированию аневризм коронарных артерий (КА). Назначение иммуноглобулина внутривенно в первые 7—10 дней болезни снижает риск развития аневризм в 5 раз [1, 2]. Несмотря на своевременное лечение, у 13—40% больных выявляется транзиторная эктазия КА, у 5—9% образуются аневризмы КА, в том числе у 1% — гигантские аневризмы диаметром 8 мм и более [3, 4]. Пациенты со средними и особенно гигантскими коронарными аневризмами находятся под угрозой развития тромбоза и стеноза КА, что может привести к ишемии, инфаркту миокарда (ИМ) и внезапной смерти. С течением времени частота развития сердечно-сосудистых осложнений возрастает [5], и через несколько лет или десятилетий больные, перенесшие в детстве синдром Кавасаки и нуждающиеся в пожизненном наблюдении, становятся пациентами терапевтов, кардиологов и кардиохирургов. Характер поражения КА, динамика патологического процесса у реконвалесцентов синдрома Кавасаки отличаются от таковых у больных с атеросклерозом. Исходы и прогноз поражения КА при синдроме Кавасаки во многом зависят от осведомленности врачей и тактики динамического наблюдения пациентов [6—8]. Кроме того, через несколько лет в терапевтическую сеть впервые в нашей стране войдут пациенты, которые в детском возрасте перенесли аортокоронарное шунтирование (АКШ) и эндоваскулярные вмешательства на КА.
К группе максимального риска развития кардиальных осложнений относятся пациенты с гигантскими аневризмами КА [4, 5, 8—12]. Собственные многолетние наблюдения таких пациентов и обобщение международного опыта легли в основу настоящей публикации.
Цель исследования — изучение клинико-демографических особенностей группы больных с гигантскими аневризмами КА, а также динамики патологических изменений КА и исходы синдрома Кавасаки у больных этой группы.
Материал и методы
Обследованы 262 ребенка с диагнозом синдром Кавасаки, обратившиеся в Университетскую детскую клиническую больницу Первого МГМУ им. И.М. Сеченова в 2003—2015 гг. Диагноз устанавливали в соответствии с диагностическими критериями, рекомендованными Американской ассоциацией сердца [4]. У 86% пациентов был «полный», у 14% — «неполный» синдром Кавасаки. Возраст пациентов на момент заболевания составил от 1 мес до 12,7 года (медиана 1,6 года), преобладали лица мужского пола (62,2%). Длительность наблюдения составила от 0,5 до 13 лет.
Динамическое наблюдение пациентов с аневризмами КА включало врачебный осмотр, электрокардиографию, эхокардиографию (ЭхоКГ) каждые 3—12 мес в зависимости от тяжести поражения КА. Стресс-электрокардиографию проводили пациентам старше 4—5 лет со средними и гигантскими аневризмами каждые 1—2 года. Рентгеновская инвазивная коронарография выполнена 12 пациентам, мультиспиральная компьютерная томография (МСКТ) КА — 29. МСКТ выполняли на 320-спиральном томографе. Исследование проводили со следующими параметрами: толщина среза 0,5 мм, режим сканирования объемный, без перемещения стола (питч 0), зона томографии по оси Z 8—10 см, параметры трубки: 80—100 кВ, 150—250 мA. Сначала выполняли исследование в нативную фазу для подсчета коронарного кальция, затем — исследование на фоне введения контрастного препарата (в количестве не более 1,5 мл/кг массы тела в катетер в локтевой вене со скоростью 2,5—3,5 мл/с). Доза облучения составила 1—2 мЗв.

ЭхоКГ выполняли всем детям на приборах Vivid-5 и Vivid-9 с применением датчиков с частотой от 1,7 до 8 МГц. Помимо стандартного исследования использовали дополнительные позиции, для визуализации ствола левой КА (ЛКА), передней нисходящей и огибающей артерий, проксимального, среднего и дистального сегментов правой КА (ПКА), задней нисходящей артерии [13, 14]. Оценивали абсолютный и относительный диаметр КА с учетом площади поверхности тела пациента. Для этого вычисляли Z-баллы — количество стандартных отклонений от среднего диаметра соответствующего сегмента КА здоровых детей с соответствующей площадью поверхности тела [15].
Локальное расширение сосуда считали аневризмой, если его диаметр ≥2,5 Z-баллов или в ≥1,5 раза превышал диаметр соседнего неизмененного участка КА [4, 15]. Если диаметр КА был больше нормы без сегментарной аневризмы, сосуд считали расширенным (эктазия). Транзиторной эктазией считали расширение КА, которое исчезло (диаметр КА нормализовался) через 8 нед после начала синдрома Кавасаки. Мелкими считали аневризмы диаметром менее 5 мм, средними — от 5 до 8 мм, гигантскими — 8 мм и более [4].
Статистическую обработку полученных данных проводили с помощью пакета программ IBM SPSS Statistics v22 и Microsoft Excel 2010. Количественные и порядковые показатели представляли как среднее значение ± стандартное отклонение или медиана и диапазон значений. Качественные показатели представляли в виде абсолютного числа наблюдений и доли (в процентах) от общего числа больных по выборке в целом или в соответствующей группе. Достоверность различий сравниваемых величин определяли с помощью дисперсионного анализа, критерия t Стьюдента для интервальных переменных, метода χ2 для номинальных переменных, критерия Фишера, критерия Манна—Уитни и Крускала—Уоллиса для порядковых переменных. Отношение шансов рассчитывали методом бинарной логистической регрессии. Различия считали статистически значимыми при р<0,05.
 Результаты
Результаты
Аневризмы КА были обнаружены у 84 (32,1%) из 262 пациентов, транзиторная эктазия — у 34 (13%). Большая часть аневризм были мелкими, гигантские аневризмы найдены у 15 больных (5,7% от общей группы, 17,9% среди больных с коронарными аневризмами).
Основные сведения о пациентах с гигантскими аневризмами КА представлены в таблице.
Факторы риска образования гигантских аневризм. Значение факторов, ассоциированных с образованием гигантских аневризм КА, было изучено с помощью многофакторного регрессионного анализа. Изучали следующие независимые переменные: пол, возраст, число клинических диагностических критериев синдрома Кавасаки, длительность заболевания до установления диагноза, длительность лихорадки, дозу иммуноглобулина, резистентность к иммуноглобулину, некоторые лабораторные показатели. По нашим данным, риск образования гигантских аневризм значительно выше при позднем назначении лечения (отношение шансов — ОШ 2,6; р=0,044), длительной лихорадке (ОШ 2,2; р=0,001), высоком уровне АЛТ (ОШ 1,5; р=0,026) и АСТ (ОШ 2; р=0,003).
Локализация гигантских аневризм. Гигантские аневризмы в правой и ЛКА обнаруживались с одинаковой частотой (см. таблицу): 24 гигантских аневризмы локализовались в проксимальных сегментах, 7 — в средних, 2 — в дистальных сегментах КА. У всех пациентов, кроме одного, помимо гигантских были еще аневризмы меньшего диаметра в других сегментах КА. Все гигантские аневризмы были доступны визуализации при ЭхоКГ, их наличие подтверждено при МСКТ или коронарографии (рис. 1).
Динамику размеров гигантских аневризм оценивали у 13 больных, наблюдавшихся более 1 года. Диаметр одних аневризм не изменился, другие уменьшились (см. таблицу). Мы обнаружили зависимость уменьшения размера гигантских аневризм от возраста: у детей, заболевших на первом году жизни, аневризмы уменьшились более значительно, чем у старших детей: диаметр, выраженный в миллиметрах, уменьшился в 1,3 и 2,5 раза соответственно, в Z-баллах — в 2 и 5,9 раза соответственно.
Тромбоз КА. Интракоронарные тромбы обнаружены у 11 из 15 больных, интервал от начала синдрома Кавасаки до выявления тромба составил от 27 дней до 11 лет (медиана 60 дней), у абсолютного большинства (10 детей) тромбы образовались в течение первых 2 лет. У 9 пациентов тромбы в аневризмах были визуализированы при ЭхоКГ, у 2 больных плоские пристеночные тромбы толщиной 0,8 и 2 мм не были выявлены при ультразвуковом исследовании (УЗИ) и найдены при МСКТ.
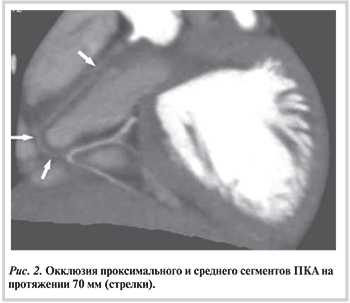
При динамическом наблюдении тромбы регрессировали в 5 аневризмах у 4 больных без тромболизиса на фоне применения стандартной антитромботической терапии: гепарин, низкомолекулярные гепарины, варфарин, ацетилсалициловая кислота (АСК). У 2 пациентов развилась окклюзия правой КА. У одного из них мы не выявили клинических и инструментальных признаков ишемии миокарда, при МСКТ дистальный сегмент правой КА и задняя нисходящая артерия заполнялись контрастным веществом из системы ЛКА по артерии Кюгеля, обнаруживались признаки реканализации (рис. 2).
У другого пациента окклюзия правой КА привела к развитию ИМ задненижних сегментов левого желудочка на 33-й день от начала синдрома Кавасаки. Через 3 мес этот больной перенес повторный ИМ, обусловленный критическим стенозом в среднем сегменте передней межжелудочковой артерии.
Стеноз КА более 75% был выявлен у 5 больных на «входе» или «выходе» гигантских аневризм, у 3 из них — субтотальный стеноз. Болевой синдром и изменения на электрокардиограмме (ЭКГ) имелись только у одного больного с ИМ. У 4 из 5 больных жалоб не было, отсутствовали признаки ишемии миокарда на ЭКГ покоя и при холтеровском мониторировании. Тредмил-тест, выполнявшийся у одного из пациентов (остальные не достигли 5-летнего возраста), не выявил скрытой ишемии миокарда. У 3 больных наличие гемодинамически значимого стеноза на «входе» в аневризму проксимального сегмента передней межжелудочковой ветви было предположено при ЭхоКГ (на основании локального мозаичного окрашивания потока в режиме цветового допплеровского картирования, увеличения скорости потока более 0,6 м/с [16]) и подтверждено при МСКТ и коронарографии. При УЗИ не был обнаружен стеноз у 3 больных на выходе из аневризм передней межжелудочковой ветви и у 1 больного — стеноз правой КА, выявленные в последующем при рентгеноконтрастных исследованиях.
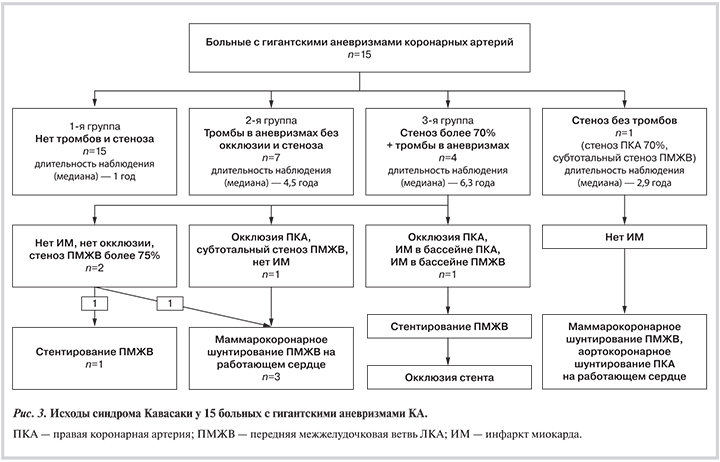
В связи с наличием гемодинамически значимого стеноза передней межжелудочковой артерии проведено хирургическое лечение 5 больным, один из них до операции перенес повторный ИМ (см. таблицу; рис. 3).
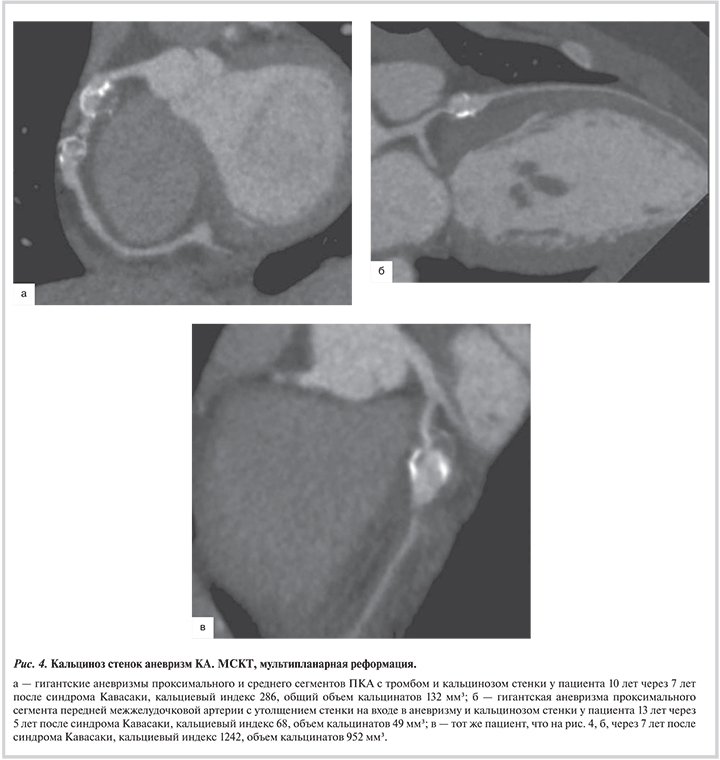
Кальциноз КА. Мы наблюдали появление кальцинатов у 7 больных как в организовавшихся коронарных тромбах, так и в стенке коронарных аневризм без тромбоза. Единичные кальцинаты выявлялись при ЭхоКГ через 2 года после развития синдрома Кавасаки, в последующем у 2 пациентов кальциноз быстро прогрессировал (рис. 4).
Исходы синдрома Кавасаки у наблюдаемых нами больных с гигантскими аневризмами представлены на рис. 3. Можно предположить, что пациенты из наиболее благоприятной 1-й группы с наименьшей длительностью наблюдения со временем пополнят группы с осложненным течением, а некоторые больные из 2-й группы перейдут в 3-ю. Таким образом, терапевты и кардиологи, курирующие взрослое население, увидят этих пациентов с еще более тяжелым поражением КА.
Обсуждение
Слизисто-кожный лимфонодулярный синдром (синдром Кавасаки) впервые описан доктором Т. Кавасаки в 1974 г. [17]. Автор считал заболевание не опасным, самоизлечивающимся. Однако через несколько лет появились доказательства поражения КА, и возможности внезапной смерти от тромбоза коронарных аневризм. В 1974 г. в Японии впервые произведено АКШ ребенку 4 лет с ИМ, окклюзией ПКА и передней нисходящей артерий в результате перенесенного синдрома Кавасаки. С тех пор накоплен немалый клинический опыт, особенно в Японии, где заболеваемость в 10—20 раз выше, чем в США и Европе, и достигла к 2012 г. 265 случаев на 100 000 детей младше 5 лет [2, 18], проведено большое количество научных исследований, отработана схема лечения в острой стадии с применением высоких доз иммунного глобулина, позволившая снизить частоту формирования коронарных аневризм. Тем не менее не решена проблема предотвращения сердечно-сосудистых осложнений, которые могут возникать как в раннем детском возрасте, так и впервые манифестировать у взрослых, длительно оставаясь бессимптомными. Риск развития тяжелых, угрожающих жизни последствий синдрома Кавасаки возрастает при позднем или неэффективном лечении в острой стадии заболевания [19—21] и в отсутствие адекватного многолетнего динамического наблюдения педиатром, терапевтом, кардиологом [6].
Неизвестная этиология заболевания, отсутствие патогномоничных клинических и лабораторных признаков затрудняют диагностику, особенно в случае неполного синдрома Кавасаки, что приводит к несвоевременному назначению лечения, прогрессированию васкулита, тяжелым структурным изменениям КА. По данным регрессионного анализа, продолжительность лихорадки и отсутствие своевременного лечения являются независимыми факторами риска формирования гигантских аневризм КА. В нашей группе больных гигантские аневризмы обнаружены только у пациентов, получивших лечение позднее 10-го дня болезни. Однако следует отметить, что у всех наших пациентов с гигантскими аневризмами был полный синдром Кавасаки, следовательно, трудности диагностики были обусловлены не столько объективными причинами, сколько отсутствием настороженности и недостаточной информированностью о синдроме Кавасаки врачей первичного звена.
Динамика репаративных и патологических процессов в КА после синдрома Кавасаки описана в литературе по данным патоморфологических [22, 23], гистологических и иммуногистохимических исследований [24], изучения стенки КА при интракоронарном УЗИ [25, 26]. Наиболее полная и современная информация получена при анализе методами световой и электронной микроскопии материала 32 аутопсий, 8 сердец, извлеченных при трансплантации, и одной иссеченной аневризмы [27]. В результате проведенных исследований авторы описывают 3 взаимосвязанных патологических процесса, происходящих в КА при синдроме Кавасаки: 1) острый некротизирующий артериит, который начинается в первые дни заболевания и, распространяясь от интимы кнаружи, может привести к воспалению и некрозу всех слоев КА; 2) подострый/хронический васкулит, начинающийся через несколько недель после дебюта синдрома Кавасаки и распространяющийся от адвентиции к внутренним слоям артерии. Признаки подострого/хронического васкулита обнаружены в КА через несколько месяцев или лет после СК; 3) люминальная миофибробластная пролиферация — процесс, приводящий к утолщению интимы КА, результат которого может быть как положительным для больного (уменьшение диаметра аневризм), так и потенциально опасным (развитие коронарного стеноза).
У 2 наших пациентов наблюдалось отчетливое сочетание значительного утолщения стенки, уменьшения размера аневризм и прогрессирования стеноза на «входе» в аневризму.
При интракоронарном УЗИ в Японии получены данные о том, что аневризмы диаметром менее 4 мм могут исчезать без утолщения стенки, а диаметр просвета более крупных аневризм уменьшается за счет утолщения интимы и организации пристеночных тромбов, причем степень утолщения стенки аневризмы коррелирует с ее первоначальным диаметром [25]. С течением времени просвет некоторых аневризм может уменьшиться вплоть до восстановления нормального диаметра. Согласно нашим данным и другим исследованиям, пациенты с уменьшившимися и исчезнувшими аневризмами остаются в группе высокого риска развития кардиальных осложнений [6, 8, 12], а прекращение регулярного наблюдения кардиологом приводило к развитию угрожающих жизни осложнений [6].
Вероятность регресса аневризм больше при их маленьком размере, веретенообразной форме, локализации в дистальных сегментах КА и у детей первого года жизни [4, 28]. Гигантские аневризмы, по мнению большинства авторов, не исчезают [10], хотя есть сообщения о регрессе 8—11% гигантских аневризм [5, 29]. Мы наблюдали значительное уменьшение размеров гигантских аневризм, однако их диаметр до настоящего времени более 2,5 Z-баллов, что не позволяет констатировать полное исчезновение. Не исключено, что в случае дальнейшего уменьшения аневризм и увеличения антропометрических данных пациентов мы сможем констатировать полное исчезновение некоторых гигантских аневризм.
Пациенты с гигантскими аневризмами находятся под угрозой развития тромбоза КА [2, 30]. Максимальный риск тромбоза и ИМ приходится на первые 45—60 дней от начала заболевания, остается высоким в первые 2 года и обусловлен снижением скорости и турбулентным характером кровотока в аневризмах, снижением антитромботических свойств эндотелия вследствие коронариита и гипертромбоцитоза, характерного для подострой стадии синдрома Кавасаки [2]. Хотя риск тромбоза и окклюзии КА с течением времени снижается, следует подчеркнуть, что сохраняющиеся гигантские аневризмы могут стать причиной коронарного тромбоза и ИМ спустя многие годы после синдрома Кавасаки [8].
Наши наблюдения о сроках образования, локализации и последствиях коронарных тромбов и окклюзии полностью согласуются с данными литературы. У всех пациентов, кроме одного, коронарные тромбы в гигантских аневризмах были обнаружены в первые 2 года после дебюта синдрома Кавасаки, более чем у 50% из них — в первые 60 дней.
Пристеночные коронарные тромбы могут не нарушать кровоток, однако существует риск их увеличения с развитием окклюзии. Окклюзия ПКА встречается чаще, чем ЛКА (58/12 ветвей ПКА и ЛКА соответственно по данным A. Suzuki и соавт. [31, 32]), что обусловлено особенностями гемодинамики в ПКА и ЛКА. Окклюзия ПКА только в 1/3 случаев приводит к ИМ, в 2/3 случаев протекает бессимптомно вследствие быстрой реканализации и включения коллатерального кровообращения [9, 32, 33].
Эффективная профилактика коронарного тромбоза может значительно улучшить прогноз. В настоящее время больным с мелкими и средними аневризмами КА назначают антиагреганты (обычно низкие дозы АСК) длительно, до исчезновения аневризм. В связи с недостаточной эффективностью этой схемы у больных со средними аневризмами появились рекомендации применения двух антиагрегантных препаратов [2]. При наличии гигантских аневризм КА принято сочетанное применение антиагрегантов и антикоагулянтов (наиболее распространенная схема — АСК + варфарин) [2, 4, 9]. Для оценки эффективности и безопасности этой схемы в Японии проведено несколько исследований, в том числе многоцентровое ретроспективное исследование, включившее 83 пациентов с гигантскими аневризмами [29, 34, 35]. Авторы отмечают, что включение варфарина в схему профилактики тромбоза снизило частоту развития ИМ у больных с гигантскими аневризмами с 33% до 5—6%, у 91% в течение 10 лет сердечно-сосудистые осложнения отсутствовали. Однако, несмотря на проведение сочетанной профилактики, отмечалось 8 эпизодов ИМ у 5 больных, один из них перенес ИМ четырехкратно через 1, 11, 12 и 14 мес после начала синдрома Кавасаки [34]. Отмечено 8 геморрагических эпизодов у 5 больных, включая эпидуральную гематому у ребенка 7 мес; 6 из 8 кровоизлияний и кровотечений были обусловлены травмой (падение, автомобильная авария). Авторы обращают внимание на невысокую частоту геморрагических осложнений и важность соблюдения охранительного режима у больных этой категории. В нашем наблюдении анализ эффективности профилактики тромбоза не проводился, поскольку у 5 больных уже при первичном УЗИ КА были обнаружены гигантские аневризмы с тромбами. Не всем больным с гигантскими аневризмами назначался варфарин, в некоторых случаях нерегулярно проводился контроль международного нормализованного отношения, не всегда достигались его целевые значения.
Сложной проблемой динамического наблюдения реконвалесцентов синдрома Кавасаки остается коронарный стеноз, частота развития которого возрастает по мере увеличения времени, прошедшего после острой стадии синдрома Кавасаки, и коррелирует с диаметром аневризм. По данным E. Tsuda и соавт., у пациентов с гигантскими аневризмами стеноз КА через 5, 10 и 15 лет после перенесенного синдрома Кавасаки был выявлен в 44, 62 и 74% случаев соответственно; у пациентов с аневризмами диаметром от 6 до 8 мм — в 6, 20 и 58% случаев; ни у одного из пациентов с аневризмами менее 6 мм стеноз КА обнаружен не был [5]. A. Suzuki и соавт. у всех пациентов с аневризмами диаметром более 9 мм при катамнестическом наблюдении через 7,8±3,6 года выявили обструктивные изменения КА (стеноз более 25%, окклюзию) [31]. По нашим наблюдениям, по мере увеличения периода от дебюта синдрома Кавасаки частота обструктивных изменений КА возрастает. Стеноз, в отличие от тромботической окклюзии, значительно чаще возникает в ЛКА и ее ветвях, чем в ПКА [9]. Методы профилактики коронарного стеноза у реконвалесцентов синдрома Кавасаки не разработаны. Появились сообщения о возможном применении с этой целью статинов, которые способны модулировать активность (ингибировать пролиферацию) миофибробластов [12].
Важной задачей динамического наблюдения пациентов является своевременное выявление гемодинамически значимого стеноза КА для проведения хирургического вмешательства с целью предотвращения ИМ. По данным литературы и полученным нами результатам, даже при тяжелом стенозе клинические и инструментальные признаки ишемии миокарда могут отсутствовать вплоть до развития ИМ или внезапной смерти [31, 32]. По наблюдениям J.B. Gordon и соавт., у большинства пациентов, перенесших синдром Кавасаки в детстве и хирургическое лечение по достижении взрослого возраста, на протяжении многих лет течение болезни оставалось бессимптомным, и первые жалобы появились при развитии острого ИМ и терминальной стадии сердечной недостаточности. Авторы отмечают, что для улучшения исходов синдрома Кавасаки необходимы постоянные динамическое наблюдение и обследование пациентов, преемственность между детскими и взрослыми кардиологами [6].
Опубликованы наблюдения, свидетельствующие о недостаточной чувствительности методов выявления ишемии миокарда [31], об отсутствии патологических изменений при электрокардиографии с физической нагрузкой у больного с 99% стенозом передней межжелудочковой артерии [11]. Применение более чувствительных методов — нагрузочной ЭхоКГ и радионуклидных исследований – в педиатрической практике ограничено. Эти наблюдения подчеркивают важность регулярного применения методов визуализации КА у больных с гигантскими аневризмами даже в отсутствие жалоб и указаний на ишемию миокарда. Трансторакальное УЗИ КА, являющееся наиболее доступным неинвазивным методом визуализации, обладает высокой чувствительностью и специфичностью при выявлении коронарных аневризм и играет ведущую роль в диагностике поражения КА в дебюте синдрома Кавасаки [36, 37]. При динамическом наблюдении пациентов диагностическая ценность УЗИ снижается в связи с недостаточной чувствительностью метода при выявлении коронарного стеноза и ухудшением визуализации КА при прогрессировании их кальцинации и увеличении антропометрических данных пациента [2]. Соответственно возрастает необходимость применения компьютерной томографии КА и инвазивной коронарографии.
Исходы синдрома Кавасаки у больных с гигантскими аневризмами изучены в Японии при длительном наблюдении 76 [11] и 245 [30] пациентов с гигантскими аневризмами. Выявлено, что 30-летняя выживаемость у этой группы больных с наиболее тяжелым поражением КА оказалась довольно высокой — 88—90%, что, по-видимому, сопряжено со своевременным успешным хирургическим лечением: 41 и 61% перенесли хирургические вмешательства. После АКШ 25-летняя выживаемость составила 92%, причем при проведении оперативного лечения у больных после ИМ — 72%, без ИМ — 100%. После АКШ необходимость в повторном хирургическом лечении была достоверно ниже, чем после чрескожного интервенционного лечения (баллонной ангиопластики, стентирования, ротационной абляции). ИМ перенесли 16 и 23% больных с гигантскими аневризмами. Двустороннее поражение КА и повторный ИМ значительно ухудшали прогноз.
В нашем наблюдении у 4 из 5 больных с тяжелым стенозом КА хирургическое лечение было выполнено до развития ИМ, что оказалось возможным благодаря регулярному динамическому наблюдению пациентов и сотрудничеству педиатров, кардиологов и кардиохирургов. Авторы полагают, что такая тактика позволит снизить риск развития необратимых изменений миокарда.
Японскими авторами опубликовано описание исходов синдрома Кавасаки у 60 больных, перенесших ИМ в возрасте от 3 мес до 33 лет (медиана 2 года) [38]. У 51 больного в дебюте синдрома Кавасаки были гигантские аневризмы, о состоянии КА остальных 9 пациентов данных нет; 30 (50%) больных перенесли ИМ в первые 6 мес от начала болезни, еще 16 — через 0,5—2 года; 13 пациентов перенесли повторный ИМ через 20 дней—12,3 года (медиана 4 мес) после первого. Через 10 лет и более после ИМ увеличивалась частота развития желудочковой тахикардии, которая в нескольких случаях была фатальной; 30-летняя выживаемость после ИМ составила всего 62,7%. Авторы предполагают, что высокая летальность обусловлена отчасти возрастом пациентов, которые не могут описать клинические симптомы, отсутствием опыта диагностики и лечения ИМ у педиатров и детских кардиологов, сложностью проведения реваскуляризации у детей раннего возраста.
Кальциноз стенок КА, выявляющийся у пациентов с коронарными аневризмами через несколько лет после перенесенного синдрома Кавасаки, может быть значительным и является неблагоприятным прогностическим признаком [39]. В наблюдении A. Kahn и соавт. у всех пациентов с кальцинозом интервал от острой стадии болезни до обследования составил не менее 10 лет [40], в нашей группе у некоторых больных уже через 5—7 лет после острой стадии синдрома Кавасаки сформировался значительный кальциноз. При возникновении выраженного циркулярного кальцинирования стенок КА ухудшались возможности детальной ультразвуковой визуализации просвета коронарного русла, оценки наличия и размеров коронарных тромбов, поскольку слой кальция экранирует ультразвуковые лучи. Возможность значительного кальциноза КА у больных, которые перенесли синдром Кавасаки, необходимо учитывать при выборе тактики хирургического лечения, поскольку при высоком кальциевом индексе попытки баллонной ангиопластики и стентирования могут оказаться неэффективными. В Японии и США больным, у которых при интракоронарном УЗИ или компьютерной томографии выявляется выраженный кальциноз КА, при необходимости хирургического лечения рекомендуют ротационную абляцию [41] или АКШ.
Заключение
Синдром Кавасаки может приводить к тяжелому повреждению коронарных артерий, осложнения которого могут проявиться как сразу, так и через несколько лет или десятилетий, и представлять угрозу для жизни пациента. Наш опыт подтверждает мнение других авторов о том, что для улучшения прогноза и исходов синдрома Кавасаки необходимо сотрудничество педиатров, кардиологов и кардиохирургов, которые имеют опыт ведения пациентов с ишемическим поражением сердца и информированы об особенностях патологии коронарных артерий при синдроме Кавасаки [1, 12, 38, 41]. Задача динамического наблюдения — снижение риска развития угрожающих жизни осложнений путем профилактики коронарного тромбоза, своевременного выявления обструктивных изменений коронарных артерий, скрытой ишемии миокарда, нарушений ритма сердца, выбора оптимальных сроков и метода хирургического лечения.
Благодарность. Авторы выражают глубокую благодарность коллегам, которые внесли большой вклад в обследование и лечение включенных в исследование пациентов: Батыревой О.В., Баяндиной Г.Н., Галазыриной А.С., Головановой Н.Ю., Дегтяревой Е.А., Иванову А.С., Леонтьевой А.А., Мазанковой Л.Н., Петровой М.С., Родионовской С.Р., Тарасовой А.А., Тебеньковой Т.А., Трифоновой Л.В., Тюлькиной С.А., Школьниковой М.А., Шпитонковой О.В., а также коллегам, проделавшим большую работу по сбору материала и обработке медицинской документации: Ивиной А.А., Леонтьевой А.А.



