ВВЕДЕНИЕ
Острое повреждение почек (ОПП) – одно из наиболее опасных осложнений и частых причин смерти у пациентов с циррозом печени (ЦП). Распространенность ОПП у госпитализированных больных ЦП колеблется, по данным разных авторов, от 12,9 до 53% [1–3]. При этом доля ОПП составляет 53,6–61,4% в общей структуре летальности госпитализированных пациентов с ЦП [1, 4]. Опубликованы данные, свидетельствующие о том, что у выживших после перенесенного ОПП больных ЦП сохраняется высокий риск смерти в течение одного года наблюдения [3]. Несомненно, иммунная система, как одна из гомеостатических систем организма, вовлекается в патогенетическую цепочку развития ОПП при ЦП. Однако особенности функционирования иммунной системы у пациентов с ЦП, осложненных ОПП, изучены недостаточно.
Цель исследования – изучить особенности Т- и B-систем иммунитета у пациентов с ОПП, развившимся на фоне декомпенсированного ЦП.
МАТЕРИАЛ И МЕТОДЫ
В исследование была включена когорта больных (n = 25), госпитализированных по поводу острой декомпенсации ЦП, у которых ОПП было установлено на момент госпитализации или возникло в первые дни стационарного лечения. Критериями ОПП в соответствии с обновленными рекомендациями Международного клуба по изучению асцитов (International Ascitic Club, IAC) служило повышение содержания креатинина в сыворотке крови на 26,5 мкмоль/л менее чем за 48 ч или на 50% по сравнению с исходным уровнем менее чем за 7 дней. За исходный уровень креатинина принимали его значения в течение последних 3 мес. до госпитализации пациента [5]. В группу исследования отбирали больных старше 18 лет.
Критерии исключения: трансплантация донорской печени, наличие онкологических заболеваний, обнаружение ВИЧ-инфекции, выраженная дисфункция сердечно-сосудистой системы.
Протокол исследования был представлен в локальный этический комитет при ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова» Минобрнауки России, который одобрил данное исследование. Согласно протоколу, проводились общеклинические исследования, лабораторные (общеклинические, биохимические, коагулогические) анализы крови, общеклинические анализы мочи, протеинограмма крови и мочи, инструментальные исследования (одномерная эластография сдвиговой волной – транзиентная эластография печени с применением фиброскана Echo-Sens, Франция), ультразвуковое исследование органов брюшной полости, почек с помощью аппарата Mindray DC-7 (Китай), определение скорости клубочковой фильтрации (СКФ) c помощью математической модели CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration), иммунологические исследования.
В рамках специальных (иммунологических) исследований оценивались показатели, характеризующие Т- и B-системы иммунитета: Т-лимфоциты (CD3+CD19-), Т-хелперы/индукторы (CD3+CD4+), цитотоксические Т-лимфоциты (CD3+CD8+), активированные Т-лимфоциты, экспрессирующие антиген гистосовместимости II класса HLA-DR (CD3+HLA-DR+CD45+) и рецептор интерлейкина 2 – CD25 (CD3+CD25+CD45+), В-лимфоциты (CD3-CD19+), уровни сывороточных иммуноглобулинов IgM, IgG, IgA, циркулирующих иммунных комплексов (ЦИК). Идентификация В-лимфоцитов и Т-лимфоцитов различных субпопуляций выполнялась методом иммунофенотипирования с использованием моноклональных антител, меченных флюоресцирующими красителями. Детекция результатов осуществлялась на проточном цитометре Beckman Coulter (США). Уровни иммуноглобулинов и ЦИК измерялись иммунотурбидиметрическим методом при помощи реагентов и биохимического анализатора фирмы Beckman Coulter (США) и реагентов ООО «Хема» (Москва) на биохимическом анализаторе ILab 650 (Япония, Италия) соответственно. При выполнении иммунологических исследований мы руководствовались стандартными методиками лабораторного иммунологического анализа, описанными ранее [6]. Дополнительно к общепринятым показателям гуморального звена иммунного ответа проводилось определение ревматоидного фактора (аутоантител, принадлежащих к классу IgM) иммунотурбидиметрическим методом (реагенты Beckman Coulter, США) и антител к тиреопероксидазе (анти-ТПО) посредством иммуноферментного анализа (реагенты «ДС-ИФА-Тироид-анти-ТПО», НПО «Диагностические системы», Нижний Новгород) с целью получения информации о содержании аутоантител в крови исследуемых больных. Данные исследования выполнялись в соответствии с методиками производителей лабораторных тест-систем.
Статистическая обработка полученных результатов осуществлялась с помощью стандартного пакета программ STATISTICA 10 (США). Статистический анализ включал проверку характера распределения частных показателей в выборке. В случае отличия распределения от нормального использовались непараметрические методы статистики, при нормальном распределении – параметрические методы. В качестве группы сравнения выступала когорта пациентов с декомпенсированным ЦП с отсутствием почечной дисфункции (n = 30), контрольной группы – практически здоровые лица (n = 30), не имевшие хронической патологии, а также острых заболеваний в течение последних 2 мес. перед обследованием.
РЕЗУЛЬТАТЫ
В таблице 1 приведены основные клинические и демографические показатели 25 участников основной группы исследования, в которой преобладали лица мужского пола. Показатели среднего возраста больных ЦП этиологически различающихся групп колебались от 49 ± 8 до 60 ± 11 лет. Пациенты с ЦП смешанной этиологии (гепатит С + алкогольная болезнь печени) были в целом моложе, чем больные других групп. Лица с ЦП вирусной этиологии были старше остальных. Общий стаж ЦП в когорте обследованных составлял 8,9 ± 1,4 года.
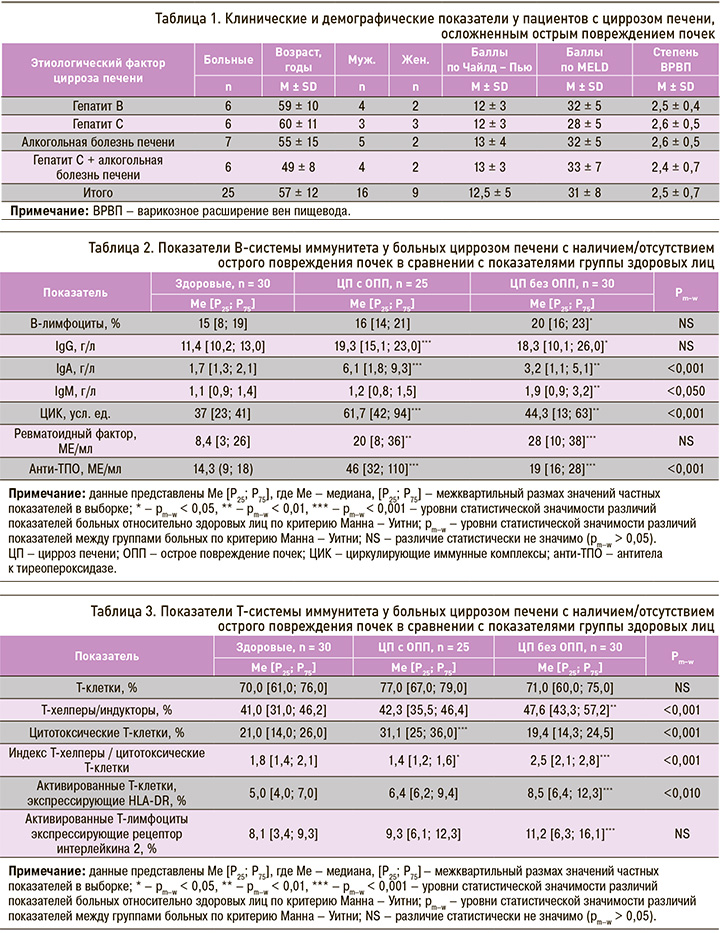
Асцит был выявлен у 23 (92%) больных, кровотечения из варикозно расширенных вен пищевода/желудка – у 3 (6%), печеночная энцефалопатия I–III стадий – у 17 (68%), признаки спонтанного бактериального перитонита – у 2 (8%). Степень фиброза по шкале Метавир соответствовала F4 (39,1 ± 3,2 кПа). Рассчитанные по шкалам Чайлд – Пью, MELD баллы свидетельствовали о тяжелом течении ЦП и высоком риске летального исхода. У 20 (80%) пациентов был установлен класс С по шкале Чайлд – Пью, у остальных – класс В. Во всех группах больных преобладали 2–3-я степени варикозного расширения вен пищевода. Включенные в группы сравнения и контроля участники были сопоставимы по демографическим показателям с пациентами, вошедшими в состав основной группы исследования.
Результаты исследования B-системы иммунитета показали, что у больных ЦП, осложненным ОПП, были повышены уровни двух классов иммуноглобулинов – IgG и IgА, а также ЦИК по сравнению с группой здоровых лиц (табл. 2).
Более выраженные изменения обнаруживались у больных ЦП сравниваемой группы с отсутствием ОПП. У них были повышены уровни всех трех основных классов иммуноглобулинов и ЦИК, увеличено число В-клеток. Сравнение показателей B-системы иммунитета у больных рассматриваемых групп между собой позволило выявить различия по уровням IgА и IgМ: в группе пациентов с ОПП был значительно выше уровень IgА на фоне сниженного уровня IgМ. В обеих группах больных обнаруживалось повышение относительно группы здоровых содержания в сыворотке крови аутоантител – ревматоидного фактора, анти-ТПО, при этом уровень последних оказался значительно выше у больных ЦП, осложненным ОПП.
Больше различий выявлено между показателями исследуемых групп больных по Т-системе иммунитета (табл. 3). Так, если в группе больных с отсутствием ОПП были повышены относительно группы здоровых показатели содержания Т-хелперных клеток, активированных клеток, экспрессирующих антиген гистосовместимости II класса – HLA-DR и рецептор интерлейкина 2, иммунорегуляторного индекса, то в группе пациентов с ЦП, осложненным ОПП, был повышен лишь один показатель – содержание цитотоксических Т-лимфоцитов на фоне уменьшения иммунорегуляторного индекса.
ОБСУЖДЕНИЕ
Из представленных данных следует, что в группе больных с отсутствием ОПП происходит активация как клеточного звена (Т-системы) иммунитета, так и гуморального (В-системы), в то время как возможности активации этих систем иммунитета у пациентов с ОПП ограниченны. У последних, в отличие от сравниваемой группы больных, не повышено содержание активированных и Т-хелперных клеток, иммунорегуляторный индекс снижен, однако увеличено число цитотоксических Т-клеток. Что касается гуморального звена иммунитета, то при ОПП не повышены показатели содержания В-клеток и IgМ. При этом ОПП ассоциировалось со значительно увеличенным уровнем IgА, ЦИК и анти-ТПО, что, по всей видимости, указывает на выраженность аутоиммунного процесса (возрастание уровней аутоантител к ТПО, ЦИК), более глубокие изменения на уровне слизистой оболочки кишечника (повышение уровня IgА). ОПП за счет увеличенного содержания цитотоксических Т-клеток может способствовать прогрессированию ЦП. Основанием для такого предположения служат ранее опубликованные данные, полученные в экспериментах на лабораторных животных и свидетельствующие о том, что цитотоксические Т-клетки активируют звездчатые клетки печени и процессы фиброгенеза [7].
Снижение иммунорегуляторного индекса у пациентов с ОПП может быть обусловлено угнетением потенциала иммунного ответа. Обнаруженная неспособность гуморального механизма адаптивного иммунитета обеспечивать усиление продукции IgМ, связанного, как известно, с активностью Т-хелперных клеток 2-го типа, может свидетельствовать об угнетении антибактериальной защиты, так как протективный иммунитет в отношении бактерий осуществляется преимущественно иммуноглобулинами (антителами). Как было показано Albillos A. et al. [8], в условиях угнетения адаптивного иммунитета нарастает бактериальная антигенемия, в результате чего активируются клетки врожденного иммунитета и продукция провоспалительных цитокинов, растет гиперцитокинемия. Последняя приводит к развитию системной воспалительной реакции, а затем, когда создаются условия для персистирующей транслокации бактерий в брюшную полость (вследствие гиподинамии кишечника, повышенной проницаемости стенок кишечника и выраженной стойкой антигенемии), происходит «истощение» врожденного иммунитета, снижается способность воспроизводства провоспалительных цитокинов, нейтрофилов, моноцитов/макрофагов и лимфоцитов, повышается продукция противовоспалительных цитокинов. При этом протективный иммунитет, связанный с адаптивными механизмами иммунного ответа, блокируется, развиваются синдром компенсаторного противовоспалительного ответа и связанная с ним иммуносупрессия.
ЗАКЛЮЧЕНИЕ
1. В отличие от группы больных ЦП без ОПП, у пациентов с наличием этого осложнения обнаружено снижение иммунорегуляторного индекса на фоне увеличения цитотоксических Т-клеток и отсутствия возрастания числа активированных Т-клеток.
2. Отличия в гуморальном звене иммунного ответа у пациентов с ОПП проявлялись в отсутствии увеличения числа В-клеток и повышения уровня IgМ при значительном возрастании уровней IgА, ЦИК и анти-ТПО.



