При гипертрофии левого желудочка (ГЛЖ) в результате артериальной гипертензии (АГ) может нарушаться функция левого предсердия (ЛП) [1].
Как известно, механическую функцию ЛП можно разделить на 3 фазы: наполнения, протекания и сокращения. Первая фаза происходит во время систолы левого желудочка (ЛЖ) и его изоволюмического расслабления и заключается в накоплении крови, поступающей из легочных вен.
Во второй фазе происходит перенос крови в ЛЖ — протекание во время ранней диастолы после открытия митрального клапана за счет градиента давления между полостями. Третья фаза отражает собственно сокращение ЛП. Снижение податливости миокарда ЛЖ ведет к затруднению кровотока из ЛП в ЛЖ. Для увеличения объема ЛЖ в диастолу требуется большее давление заполнения. Это является одной из причин увеличения ЛП у пациентов с умеренной и тяжелой АГ [2]. В настоящее время для оценки изменений в ЛП чаще всего применяются объемы ЛП. Индекс максимального объема ЛП (отношение объема к площади поверхности тела, BSA) является маркером тяжести диастолической дисфункции и предиктором сердечно-сосудистых заболеваний [3, 4]. У пациентов с АГ I степени и незначительной ГЛЖ могут наблюдаться изменения объемов ЛП [4]. Однако расширение ЛП (увеличение индекса максимального объема ЛП) наблюдалось только у 22% пациентов с АГ.
С развитием методов оценки деформации миокарда, таких как тканевый допплер (ТД) и не-допплеровский режим двухмерной серошкальной деформации (ДСД), появилась возможность анализа деформации миокарда ЛП. Как известно, у ТД есть недостатки, которые не позволили применять этот метод в повседневной практике. Речь идет о зависимости от угла сканирования, необходимости регистрации данных с высокой частотой кадров, достаточно «трудоемкой» обработке материала. ДСД лишен недостатков ТД. Метод ДСД позволяет быстро определить региональную деформацию миокарда [5, 6], не зависит от угла сканирования и от общего движения сердца, а полученные с его помощью результаты характеризуются высокой воспроизводимостью. В предыдущих
работах были определены показатели деформации и скорости деформации миокарда ЛП у здоровых лиц [7, 8]. Результаты свидетельствовали об отсутствии корреляции с показателями объемов ЛП. В связи с этим встает вопрос о возможности использования ДСД для изучения функции предсердий у пациентов с АГ и небольшой ГЛЖ.
Целью работы явилась оценка региональной продольной деформации и скорости деформации миокарда предсердий методом ДСД у пациентов с АГ и небольшой ГЛЖ.
Материал и методы
Всего в исследование были включены 40 обследованных: 30 пациентов с АГ I степени и небольшой ГЛЖ, а также контрольная группа из 10 здоровых лиц.
Пациенты с АГ. Обследованы 30 пациентов с АГ длительностью от 1 года до 15 лет (17 женщин, 13 мужчин, средний возраст 57±8 лет). Критериями включения в исследование были: а) возраст 40—65 лет; б) документированное повышенное артериальное давление (АД) >140/90 мм рт.ст., но <160/100 мм рт.ст.; в) нерегулярный прием лекарственных препаратов; г) отрицательный тест велоэргометрии на ишемию; д) индекс массы миокарда ЛЖ (ИММ ЛЖ) менее 108 г/м² у жен- щин и менее 131 г/м² у мужчин, что соответствовало небольшой гипертрофии миокарда ЛЖ (в соответствии с рекомендациями Американского и Европейского эхокардиографических обществ) [9]; е) синусовый ритм на электрокардиограмме (ЭКГ).
Контрольная группа здоровых лиц. В контрольную группу были включены 10 здоровых взрослых лиц
(средний возраст 53±4 года, 7 женщин и 3 мужчин). Они не предъявляли жалоб, у всех отмечено нормальное АД, отсутствовали кардиологический анамнез, хронические и системные заболевания, никто из них не употреблял лекарственные препараты, не курил. На ЭКГ у всех был зарегистрирован синусовый ритм, патологические изменения отсутствовали. В крови определялись нормальные биохимические показатели (глюкоза, липидный состав). У всех обследованных рассчитывали площадь поверхности тела (ППТ) по формуле: ППТ=(вес0,425) × (рост 0,725) × 0,007184 [10]. Все обследованные подписали письменное соглашение на участие в исследовании.
Эхокардиография. Всем включенным в исследование была выполнена стандартная трансторакальная
эхокардиография (ЭхоКГ) с последующим анализом методом ДСД. Все эхокардиографические исследования были выполнены на ультразвуковом сканере GE Vivid7 Dimension (GE Medical Systems, Horten, Norway) с использованием матричного датчика M4S (1,5—4,3 МГц). Для обработки данных в памяти сохраняли в виде кинопетли 3 последовательных сердечных цикла.
В парастернальной позиции длинной оси ЛЖ с использованием М-режима были получены линейные размеры ЛЖ: конечный диастолический (КДР) и конечный систолический размеры (КСР), фрак-
ция выброса (ФВ), толщина межжелудочковой перегородки в систолу и диастолу (ТМЖПс и ТМЖПд),
толщина задней стенки в систолу и диастолу (ТЗСс и ТЗСд), диаметр аорты и диаметр ЛП. Расчет массы
миокарда ЛЖ (ММЛЖ) выполняли по формуле: ММЛЖ = 0,8 × {1,04[(КДР +ТМЖПд +ТЗСд)³–КДР)³]}+0,6 [9]. Рассчитывали ИММЛЖ по формуле: ММЛЖ/ППТ.
Для вычисления объемов предсердий использовали 4- и 2-камерные апикальные позиции. Биплановым
методом площадь—длина измеряли: а) максимальный объем ЛП непосредственно перед открытием митрального клапана — (Vmax ЛП); б) минимальный объем ЛП в момент закрытия митрального клапана — (Vmin ЛП); в) объем ЛП в момент начала зубца Р на ЭКГ — (Vp ЛП); г) в 4-камерной апикальной позиции измеряли максимальный объем правого предсердия (ПП) — перед открытием трикуспидального клапана (Vmax ПП) и минимальный объем ПП — в момент закрытия трикуспидального клапана (Vmin ПП).
Вычисляли следующие показатели функции предсердий: а) индекс Vmax ЛП как отношение Vmax ЛП/ППТ; б) индекс Vmin ЛП как отношение Vmin ЛП/ППТ; в) индекс Vр ЛП как отношение Vр ЛП/ППТ; г) фракцию пассивного опорожнения (ФПО) ЛП по формуле: ФПО =Vmax ЛП — Vp ЛП/ Vmax ЛП × 100%; д) фракцию активного опорожнения (ФАО) ЛП по формуле: ФАО ЛП = Vp ЛП —Vmin ЛП / Vp ЛП × 100%; е) индекс растяжения (ИР) ЛП по формуле: ИР ЛП = Vmax ЛП – Vmin ЛП/ Vmin ЛП × 100%; ж) ФВ ПП по формуле: ФВ ПП = Vmax ПП – Vmin ПП / Vmax ПП × 100%.
Каждый из вычисляемых показателей функции предсердий характеризует определенную фазу в их деятельности. ФПО ЛП характеризует фазу протекания (фп) ЛП, ФАО ЛП — фазу сокращения (фс) ЛП, а ИР ЛП — фазу накопления (фн) ЛП.
В импульсноволновом режиме из верхушечной 4-камерной позиции регистрировали трансмитральный кровоток, легочный кровоток (в верхней правой легочной вене) и транстрикуспидальный кровоток.
Измеряли следующие показатели трансмитрального кровотока: максимальную скорость раннего диастолического наполнения ЛЖ (Е, см/с); максимальную скорость систолы предсердий (пик А, см/с) и ее продолжительность (Adur, мс); время замедления кровотока раннего диастолического наполнения (DT, мс); д) время изоволюмического расслабления ЛЖ (IVRT, мс). Рассчитывали отношение Е/А.
По допплерограмме кровотока из легочной вены измеряли максимальную скорость систолического (пик S, см/с), диастолического компонента (пик D, см/с) потока легочных вен и максимальную скорость ретроградного потока из предсердия (V max AR, см/с). Рассчитывали отношение максимальных скоростей легочного кровотока в систолу и диастолу (S/D). По трехстворчатому кровотоку измеряли максимальную скорость раннего диастолического наполнения правого желудочка (ПЖ) (Етк, см/с).
В импульсноволновом режиме ТД из верхушечной 4-камерной позиции измеряли скорости движения фиброзных колец атриовентрикулярных клапанов: среднее значение максимальной скорости движения латерального и септального отделов фиброзного кольца митрального клапана (МК) в раннюю диастолу (E′ ср. МК); максимальную скорость движения латерального отдела фиброзного кольца трикуспидального клапана (ТК) в раннюю диастолу (E′ ТК). Рассчитывали отношение E/E′ср. МК, отношение Eтк/E′ ТК.
Метод двухмерной серошкальной деформации предсердий. Не-допплеровский метод ДСД — это новый
способ получения данных о деформации (stain, S, ε) и скорости деформации миокарда (strain rate, SR). В его основе лежит анализ движения «следовых пятнышек» — tracking speckles — естественного акустического маркера в двухмерном ультразвуковом изображении. Эти маркеры равномерно рассредоточены в миокарде. Их размер составляет от 20 до 40 пикселей. От кадра к кадру происходит смещение пятнышек. При этом рассчитывается скорость их смещения. Для адекватной обработки изоб-
ражения необходима частота кадров 30—90 Гц.
Для анализа продольной функции миокарда предсердий в «пост-процессинге» использовалось программное обеспечение рабочей станции (EchoPac PC Dimension 06, version 6.x.x., GE Healthcare, Norway), в памяти которой были записаны двухмерные серошкальные изображения в виде кинопетли с обязательной регистрацией ЭКГ на мониторе (c хорошей визуализацией зубцов Р и R), с частотой кадров от 40 до 80 Гц, в 4-, 2-, 3-камерных позициях, с одинаковыми интервалами RR на ЭКГ в указанных позициях.
Рисунок 1. График продольной деформации (Д) средних сегментов нижней (голубая кривая) и передней (синяя кривая) стенок ЛП в 2 камерной проекции.
Рисунок 2. График продольной скорости деформации (СД) среднего сегмента задней (голубая кривая) стенки ЛП в 3 камерной проекции.
Затем, выбирая необходимую проекцию, специалист обозначает границу эндокарда в предсердиях (циркулярно) в конце систолы предсердий, в момент максимального утолщения миокарда. Вторая граница появляется автоматически около эпикарда, тем самым обозначая толщину миокарда. Программа делит исследуемую зону на 6 стандартных сегментов и оценивает по 3-балльной системе (от 1 до 3) стабильность регионального смещения пятнышек. Оценка < 2,5 является допустимой для
анализа. В результате анализа программа выстраивает графики продольной деформации и продольной скорости деформации выбранных оператором сегментов предсердия. На рис. 1 и 2 приведены примеры графиков кривых деформации и скорости деформации миокарда ЛП. На полученных графиках проводились измерения деформации и скорости деформации в разные фазы
сердечного цикла. Максимальная продольная деформация была измерена в фазу сокращения (МДфс, %), соответствующую систоле предсердий, от начала зубца Р на ЭКГ до закрытия МК (MVC) и в фазу накопления (МДфн, %), соответствующую систоле желудочков, от закрытия МК до закрытия аортального клапана (AVC). В фазу протекания измерение максимальной деформации не проводилось. Это связано с полученными результатами предыдущей работы, в которой были обследованы здоровые лица [8]. В этом исследовании было продемонстрировано, что в фазу протекания у 50% обследованных здоровых лиц показатели максимальной деформации были равны 0 независимо от сегмента, позиции и качества визуализации. Это связано с отсутствием пика деформации миокарда в указанный период. Деформация в эту фазу переходит из одного пика (максимального удлинения) в другой пик (максимального укорочения) в фазу сокращения. Как известно, в фазу протекания предсердие является пассивным проводником для переноса крови и миокард практически не смещается. Максимальная скорость деформации была измерена в фазу сокращения (МСДфс, 1/s), в фазу накопления (МСДфн, 1/s) и в фазу протекания предсердий (МСДфп, 1/s), соответствующую периоду раннего наполнения ЛЖ с момента открытия МК (MVO) до зубца Р на ЭКГ. МСД и МД рассчитывали для следующих сегментов ЛП: а) в 4-камерной верхушечной позиции для средних сегментов боковой стенки ЛП и ПП, перегородки предсердий; б) в 3-камерной верхушечной позиции для средних сегментов задней стенки ЛП; в) в 2-камерной верхушечной позиции для средних сегментов нижней стенки ЛП и передней стенки ЛП.
Кроме того, оценивалось среднее (глобальное) значение максимальной деформации миокарда ЛП по всем 15 сегментам: 6 сегментов 4-камерной позиции, 6 сегментов 2-камерной позиции, 3 сегмента 3-камерной позиции в фазы накопления (ГМДфн, %) и сокращения ЛП (ГМДфс, %).
Временные интервалы в фазу систолы предсердий были вычислены следующим образом. При анализе
одной из верхушечной позиций (графические кривые деформации и скорости деформации) отмечали 2 точки на ЭКГ в момент начала зубца Р (1-й пункт) и пик зубца R (2-й пункт). Вычисляли разницу между этими пунктами (мс), которая служила постоянной величиной для всех трех позиций (интервал P—R). Затем измеряли разницу времени между 1-м пунктом и пиком волны сокращения ЛП или ПП на графических кривых деформации и скорости деформации (см. рис. 2).
Результаты
В табл. 1 представлены результаты сравнения анализируемых показателей между 2 группами. В группе
больных с АГ отмечены ожидаемо больший ИММ ЛЖ, достоверно меньшая ФВ ЛЖ. Большая площадь поверхности тела в группе у больных АГ была обусловлена большей средней массой тела пациентов. Наблюдались изменения ряда показателей, характеризующих диастолическую функцию ЛЖ: достоверное снижение Е′среднего МК (р<0,001) и отношения Е/Е′ (р=0,003), увеличение максимальной скорости пика А МК (р=0,02) в группе больных АГ.
Таблица 1. Эхокардиографические показатели обследованных групп здоровых лиц и больных АГ.
Объемы ЛП и ПП. У всех обследованных линейный размер ЛП, максимальный объем и индекс максимального объема ЛП были в пределах нормы. Наряду с этим в группе больных АГ регистрировалось достоверное увеличение всех объемов и их индексов. ФПО ЛП, ИР ЛП и ФВ ПП были достоверно меньше у пациентов с АГ. ФАО ЛП и максимальный объем ПП достоверно не различались в обследованных группах (табл. 2).
Таблица 2. Структурно функциональные показатели предсердий у здоровых лиц и больных АГ.
Деформация и скорость деформации миокарда в сегментах ЛП и ПП. Фаза сокращения. В фазу сокращения максимальная продольная деформация и скорость деформации миокарда предсердий между двумя группами достоверно не различались. Время от начала зубца Р на ЭКГ до МСДфс достоверно не различалось для всех сегментов как ЛП, так и ПП.
Интервал от начала зубца Р на ЭКГ до МДфс был длиннее в группе больных АГ во всех сегментах ЛП,
однако достоверные различия наблюдались только для задней стенки ЛП (р=0,05) (табл. 3).
Таблица 3. Время наступления максимальной деформации стенок предсердий в фазу систолы (МДфс), %.
Фаза накопления. У больных АГ максимальная продольная деформация и скорость деформации в фазу
накопления были меньше, чем в контрольной группе, для всех стенок предсердий (табл. 4, 5). Достоверно меньшие значения максимальной продольной деформации в фазу накопления зарегистрированы для боковой, септальной, задней и нижней стенок ЛП (см. табл. 4). Достоверные различия максимальной скорости деформации в фазу накопления между группами наблюдались для боковой, септальной и задней стенок ЛП и боковой стенки ПП (см. табл. 5).
Таблица 4. Значения максимальной деформации миокарда предсердий в фазу накопления (МДфн), %.
Таблица 5. Значения максимальной скорости деформации миокарда предсердий в фазу накопления (МСДфн), 1/с.
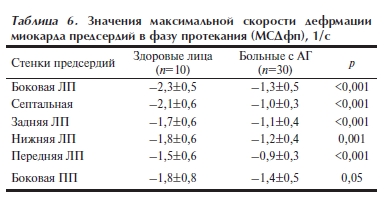
Таблица 6. Значения максимальной скорости дефрмации миокарда предсердий в фазу протекания (МСДфп), 1/с.
Фаза протекания. Для фазы протекания мы анализировали только максимальную скорость деформации. При этом во всех без исключения стенках предсердий наблюдалось достоверное снижение МСДфп
в группе больных АГ, которое было в большей степени выражено для стенок ЛП (табл. 6).
Глобальная максимальная деформация миокарда ЛП. В фазу сокращения глобальная максимальная
деформация миокарда (ГМДфс) ЛП в группе больных АГ достоверно не различалась по сравнению
с контрольной группой.
В фазу накопления глобальная максимальная деформация миокарда (ГМДфн) ЛП в группе больных АГ оказалась достоверно меньше, чем в контрольной группе (10,1±2,1% против 16,2±3,8%; р<0,001).
В табл. 7 представлены результаты корреляции глобальной максимальной деформации с возрастом
и показателями ЭхоКГ. ГМДфн демонстрирует достоверную отрицательную корреляцию с ИММ ЛЖ,
возрастом, индексами объемов ЛП и индексом минимального объема ПП. Достоверная положительная
корреляция наблюдается с ФАО и ФПО ЛП, ИР ЛП, ФВ ПП, средним Е′ МК.

Таблица 7. Коэффициенты корреляции глобальной максимальной деформации миокарда ЛП в фазу накопления и сокращения с возрастом и эхокардиографическими показателями.
В фазу сокращения обращает внимание достоверная положительная корреляция ГМДфс с индексом
минимального объема ЛП и индексом объема ЛП в момент начала зубца Р на ЭКГ. Кроме того, наблюда-
лась достоверная отрицательная корреляция ГМДфс с ФАО ЛП и ИР ЛП.
Обсуждение
В нашем исследовании изучалась механическая функция предсердий при небольшой ГЛЖ у пациентов с АГ I степени. Обследованные нами группы были сопоставимы по возрасту. Достоверно большее значение ППТ в группе больных АГ представляется вполне закономерным. Больные АГ нередко
имеют избыточную массу тела, чем и обусловлена большая площадь его поверхности в этой группе
по сравнению с контрольной [11].
В группе больных АГ достоверно больше были ИММ ЛЖ, КСР ЛЖ и достоверное меньше — ФВ ЛЖ. Такие результаты в первую очередь связаны с влиянием постоянно повышенного, не корригируемого лекарственными препаратами, АД.
Допплер-эхокардиографические показатели диастолической функции ЛЖ отражают нарушение релаксации миокарда ЛЖ в группе больных АГ: достоверное увеличение скорости пика А трансмитрального кровотока, увеличение времени замедления потока раннего диастолического наполнения, удлинение времени изоволюметрического расслабления, снижение E′ ср. MК, увеличение E/E′ср. МК. Следует отметить отсутствие достоверных изменений венозного легочного спектра.
Структурно-функциональные показатели предсердий. Увеличение объемов предсердий представляет собой кумулятивный показатель, так как это происходит с течением времени под воздействием определенных факторов. В данной ситуации это повышенное АД и небольшая гипертрофия миокарда ЛЖ.
В нашем исследовании все статические объемы ЛП и ПП и индексы объемов в группе больных АГ были
больше, чем в контрольной группе. ФПО ЛП, ИР ЛП и ФВ ПП были достоверно меньше у пациентов с АГ.
При этом не наблюдалось увеличения ФАО ЛП в группе больных АГ в ответ на уменьшение ФПО ЛП.
Математически это объясняется достоверно возросшими объемами как Vp ЛП, так и Vmin ЛП в группе
больных АГ. Однако следует отметить, что в предыдущих исследованиях у пациентов с АГ и ГЛЖ было
выявлено усиление контрактильной функции ЛП в систолу [4, 18]. Это объясняется законом Франка—
Старлинга: на увеличение объема ЛП, увеличивалась контрактильность миокарда ЛП. Достоверные изменения (увеличение) объемов ЛП касались Vmax ЛП и Vp ЛП, тогда как Vmin ЛП не изменялся. Кроме того, у 22% больных АГ наблюдалось расширение ЛП [4], тогда как в нашем исследовании максимальный объем и индекс ЛП оставались в пределах нормы у всех пациентов с АГ. Возможно, это не послужило достаточным «пусковым» моментом для реализации компенсаторного механизма и увеличения ФАО ЛП.
Деформация и скорость деформации миокарда в сегментах ЛП и ПП. Фаза сокращения. Максимальная скорость деформации и максимальная деформация не имели достоверных различий между группой больных АГ и контрольной группой. ГМД также не продемонстрировала значимых изменений. Подобные результаты были получены при использовании ТД [15].
Время до максимальной деформации в фазу сокращения достоверно не различалось между группой больных АГ и контрольной группой.
Обобщая результаты, связанные с фазой сокращения, можно сделать вывод, что увеличение объемов ЛП и ПП, которое наблюдалось в обследованной нами группе, не вызвало компенсаторную реакцию в виде усиления деформации и скорости деформации миокарда ЛП и ПП.
В исследовании A.N. Borg и соавт. [19] была изучена продольная деформация миокарда ЛП методом ТД
при хронической умеренной митральной регургитации (в результате пролапса МК). Результаты продемонстрировали достоверное увеличение максимальной скорости деформации во всех фазах и увеличение максимальной деформации в фазу накопления по сравнению с таковыми у здоровых лиц, т.е. в ответ на перегрузку объемом миокарда ЛП наблюдалось увеличение его деформации.
При АГ степень увеличения объема ЛП перед началом фазы сокращения, вероятно, не столь значительна по сравнению с увеличением объема ЛП при митральной регургитации. Возможно, реакция миокарда ЛП в этом случае будет отличаться, так как в первую очередь происходит повышение давления в ЛП.
Фаза накопления. В фазу накопления значения максимальной деформации и скорости деформации для всех стенок ЛП и ПП были меньше в группе больных АГ по сравнению с контрольной группой, т.е. миокард ЛП и ПП не расслабляется (не растягивается) полностью после систолы предсердий, тем самым не выполняя полноценно функцию присасывания крови из легочных вен. Это подтверждает и выраженное достоверное снижение ГМД в данную фазу. Возможно, миокард предсердий реагировал так же, как и миокард ЛЖ, а именно, нарушением расслабления.
При использовании ТД были получены неоднозначные результаты. S. Eshoo и соавт. [15] продемонстрировали отсутствие достоверного снижения максимальной скорости деформации и деформации миокарда ЛП в фазу накопления. Однако N. Kokubu и соавт. [16] выявили достоверное снижение максимальной скорости деформации в сегментах миокарда ЛП в фазу накопления у больных АГ с расширенным ЛП, но без ГЛЖ и у больных АГ с ГЛЖ, но без расширения ЛП по сравнению с аналогичными показателями у здоровых лиц. Достоверное снижение максимальной деформации миокарда ЛП у больных АГ с ГЛЖ было выявлено и методом двухмерной серошкальной деформации [17].
Фаза протекания. Наиболее достоверные результаты были получены в фазу протекания: значительное
уменьшение максимальной скорости деформации в средних сегментах ЛП и ПП. Похожие результаты были получены при использовании ТД для оценки максимальной скорости деформации ЛП [15]. Эти результаты дополняют и подтверждают наличие нарушения наполнения ЛЖ в данную фазу, которая
фактически определяет количество крови, поступающее в ЛЖ в диастолу.
Таким образом, структурно-функциональные показатели ЛП и ПП как показатели оценки функции
предсердий в настоящее время наиболее хорошо изучены. Доказана и прогностическая значимость этих показателей [3, 14, 20]. Появление новых методов, таких как ТД и ДСД, дает возможность анализировать другие аспекты функции предсердий. В литературе описаны только единичные исследования, посвященные изучению деформации миокарда предсердий методом ДСД. Полученные нами результаты подтверждают уменьшение деформации миокарда ЛП и ее скорости в фазе накопления (во время систолы желудочков) и в фазе протекания (во время раннего наполнения ЛЖ).
Однако в обследованной нами группе больных АГ с небольшой ГЛЖ не наблюдалось достоверных изменений показателей деформации миокарда предсердий в фазу их сокращения. Требуются дальнейшие исследования для понимания изменений деформации, происходящих в миокарде предсердий.
Выводы
С помощью метода двухмерной серошкальной деформации у больных артериальной гипертензией удается выявить изменения состояния миокарда предсердий даже при небольшой гипертрофии левого желудочка.
Изменения показателей деформации миокарда левого предсердия наблюдаются в фазе накопления (во время систолы желудочков) и в фазе протекания (во время раннего наполнения левого желудочка) и отсутствуют в фазе сокращения предсердий.
Изменения состояния миокарда левого предсердия проявляются уменьшением его деформации и скорости деформации.



