ВВЕДЕНИЕ
Наиболее частая внелегочная патология, влияющая и формирующая ситуации взаимного отягощения с бронхиальной астмой (БА), – поражения верхних отделов желудочно-кишечного тракта (ЖКТ), которые встречаются в 40–90% случаев у пациентов с БА. Изменения аллергического происхождения, имеющие воспалительный характер, характерны для астмы и атопических заболеваний, но вместе с тем могут выявляться и в различных отделах органов пищеварения [1, 2]. С точки зрения гигиенической гипотезы существует связь инфекции H. pylori с БА и другими аллергическими заболеваниями. Более того, согласно этой гипотезе, некоторые бактериальные возбудители оказывают влияние на формирование аутоиммунных и аллергических заболеваний [3]. При этом некоторые авторы считают H. pylori лишь маркером неблагоприятных санитарно-гигиенических условий в каждой индивидуальной популяции, а не значимым фактором в развитии указанной группы заболеваний [4, 5].
Неконтролируемая БА с тяжелым персистирующим течением сложна для диагностики (в том числе дифференциальной) и фармакотерапии. Важным патогенетическим механизмом формирования астмы и фактором отсутствия контроля над заболеванием зарубежные авторы считают сенсибилизацию [5, 6]. В последние годы у коморбидных больных БА увеличилась частота встречаемости поливалентной сенсибилизации к пищевым, бактериальным, грибковым аллергенам, которая приводит к тяжелому неконтролируемому течению болезни и снижению эффективности базисной фармакотерапии у данной группы пациентов [7–9].
Мнения о роли пищевой сенсибилизации в развитии БА различные. Так, ряд авторов отмечает, что пищевая аллергия при БА – основной компонент поливалентной сенсибилизации и один из многих патогенетических факторов развития астмы. Другие исследователи считают, что прочие формы ингаляционной аллергии присоединяются к уже имеющейся пищевой аллергии. У многих пациентов пищевая сенсибилизация выступает единственной причиной приступов удушья при БА и намного чаще встречается в общей врачебной практике, нежели выявляется пульмонологами и аллергологами-иммунологами [10–12]. В настоящее время имеется очень мало работ по изучению частоты и характера этого нарушения при изолированной БА и БА в сочетании с H. pylori-ассоциированным хроническим гастритом (Hp-АХГ).
Цель исследования – определить характер и частоту пищевой сенсибилизации у пациентов с изолированной БА и БА в сочетании с Hp-АХГ.
МАТЕРИАЛ И МЕТОДЫ
Обследовано 85 пациентов с БА: 1-я группа (основная) – больные БА в сочетании с Hp-АХГ (n = 50); 2-я группа – лица с изолированной БА (n = 35). На долю мужчин пришлось 40,6%, на долю женщин – 59,4% исследуемых. Средний возраст участников составил 52,4 ± 4,2 года.
Диагностика и лечение БА проводились на основании федеральных клинических рекомендаций по ведению взрослых пациентов с БА 2021 г. [13]. Пациентам выполнялись клиническое, лабораторное (общий и биохимические анализы крови), инструментальное (рентгенография легких, эзофагогастродуоденоскопия, спирография, пикфлоуметрия), аллергологическое (изучение аллергологического анамнеза, оценка общего IgE и специфических иммуноглобулинов IgЕ и IgG к различным пищевым аллергенам – молоку коровы, свинине, говядине, курице, треске, пшенице, гречке, овсянке) обследования. Содержание Ig определяли в диапазонах от 0 до 4 в КЕд./л: 0-й уровень – от 0 до 0,35; 1-й – от 0,35 до 1,0; 2-й – от 1,0 до 3,5; 3-й – от 3,5 до 17,5 и 4-й – от 17,5 до 50.
РЕЗУЛЬТАТЫ
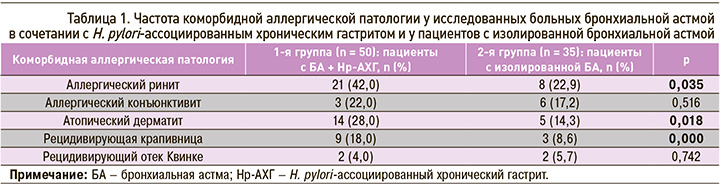
В обеих группах исследуемых больных БА отмечался неблагоприятный аллергологический анамнез (непереносимость ряда лекарственных препаратов) и наследственная отягощенность по атопическим заболеваниям. У пациентов с БА в сочетании с Hp-АХГ по сравнению с больными, имеющими изолированное течение БА, достоверно чаще выявлялись коморбидные атопические заболевания: рецидивирующая крапивница (18,0 и 8,6%; р = 0,000), аллергический ринит (42,0 и 22,9%; р= 0,035), атопический дерматит (28,0 и 14,3%; р = 0,018). Аллергический конъюнктивит в 1-й группе наблюдался чаще, чем во 2-й, но это различие было статистически недостоверным (р = 0,516). В то же время у больных изолированной БА чаще регистрировался рецидивирующий отек Квинке, однако и эта разница в сравнении с 1-й группой оказалась статистически недостоверной (р = 0,742; табл. 1).
Отечественные и зарубежные исследователи отмечают большое значение пищевой сенсибилизации в развитии БА [7, 8]. Пищевая аллергия в нашем исследовании была установлена как сопутствующая форма сенсибилизации у большинства обследуемых пациентов с астмой (90,6%). Роль пищевой сенсибилизации была подтверждена высоким / очень высоким уровнем антител (АТ) IgE к свинине – у 69 (81,2%), говядине – у 73 (84,7%), курице – у 65 (76,5%), молоку коровы – у 71 (83,1%), треске – у 80 (94,4%), овсянке – у 58 (68,2%), пшенице – у 57 (67,1%), гречке – у 62 (72,9%) больных БА.
В свою очередь, высокие / очень высокие уровни АТ IgG к свинине определялись у 66 (79%), говядине – у 75 (88,2%), курице – у 77 (90,5%), молоку коровы – у 48 (56,5%), треске – у 82 (96,5%), овсянке – у 82 (96,5%), пшенице – у 79 (92,9%), гречке – у 76 (89,4%) пациентов с БА.
У больных БА в сочетании с Hp-АХГ частота пищевой сенсибилизации по IgЕ к молоку коровы достоверно превышала таковую в группе пациентов с изолированной БА в 2 раза, к свинине – в 1,3, к говядине – в 2,4, к треске – в 2,8, к овсянке – в 2,2, к пшенице – в 4,3 раза (табл. 2).
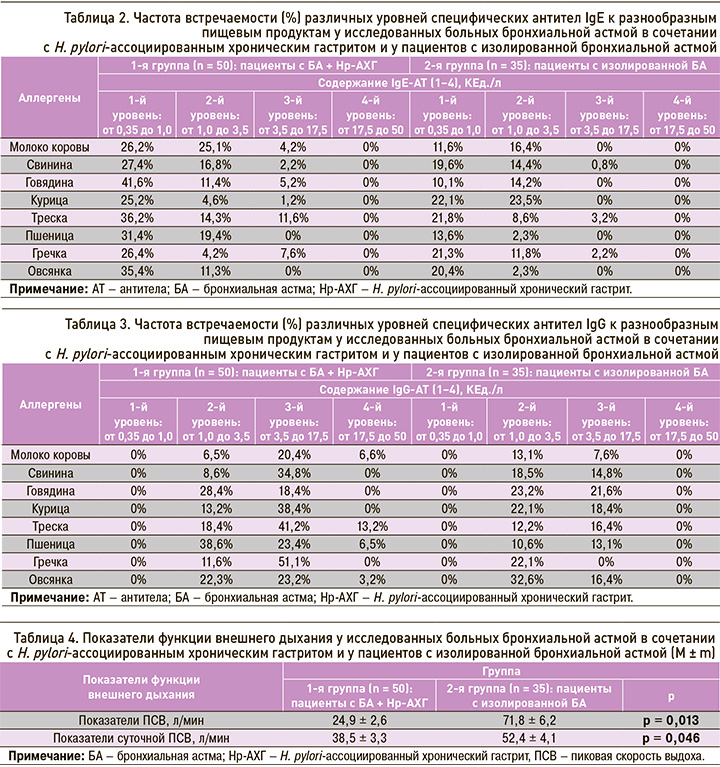
У больных 1-й (основной) группы частота пищевой сенсибилизации к молоку коровы по IgG достоверно превышала аналогичный показатель во 2-й группе в 1,6 раза, к треске – в 2,6, к свинине – в 1,4, к пшенице – в 2,4, к гречке – в 2,8 раза (табл. 3).
У 36 (42,6%) обследуемых больных БА аллергия к указанным пищевым продуктам не была указана в диагнозе. Ранее диагностика на наличие пищевой сенсибилизации к пищевым продуктам у этой категории пациентов не проводилась. Не выявленная пищевая аллергия у пациентов с изолированной БА и в сочетании с Hp-АХГ способствовала прогрессированию заболевания, развитию тяжелого неконтролируемого течения астмы и отсутствию эффекта от стандартной фармакотерапии.
Изучение функции внешнего дыхания (ФВД) у участников исследования продемонстрировало, что более выраженные изменения имели место у больных БА в сочетании с Hp-АХГ относительно пациентов с изолированной БА. Показатели пиковой скорости выдоха (ПСВ) и суточной ПСВ в 1-й (основной) группе были достоверно ниже в сравнении со 2-й группой (табл. 4).
У большинства больных БА в сочетании с Hp-АХГ (92,0%) фиксировалось снижение эффективности базисной фармакотерапии БА, тяжелое рецидивирующее течение и отсутствие контроля над заболеванием.
ЗАКЛЮЧЕНИЕ
Аллергия к различным пищевым продуктам часто встречается как у пациентов с изолированной БА, так и больных, у которых наряду с астмой имеется Hp-АХГ. Всем лицам БА с тяжелым персистирующим течением, частыми обострениями, отсутствием контроля над заболеванием необходимо определять уровень общего IgE и специфических пищевых IgE и IgG для изучения характера и частоты пищевой сенсибилизации и проведения рациональной фармакотерапии при изолированной астме и сосуществовании БА с Hp-АХГ. Дальнейшее изучение влияния пищевой аллергии на развитие и ухудшение течения БА в сочетании с Hp-АХГ позволит получить новые данные для совершенствования ведения больных с этой коморбидностью.



