Больные с пороками клапанов сердца (ПКС) составляют значительную долю среди лиц с заболеваниями сердечно-сосудистой системы [1]. В последние десятилетия достигнуто значительное улучшение результатов лечения пациентов этой категории, прежде всего, за счет широкого применения и совершенствования хирургической техники. Однако у многих больных ПКС, несмотря на восстановление внутрисердечной гемодинамики, после хирургического вмешательства сохраняется и продолжает прогрессировать сердечная недостаточность [2—5]. Это обусловлено исходным предоперационным ремоделированием миокарда c возникновением зон кардиосклероза и рубцовых изменений, дефицитом микроциркуляторного русла, а также гибернацией кардиомиоцитов вследствие хронической гипоперфузии [6—8].
Традиционные методы, используемые для оценки состояния миокарда (электрокардиография, эхокардиография, коронарография – КГ), недостаточно информативны, поскольку не позволяют охарактеризовать перфузию и метаболизм миокарда. Необходимость получения таких сведений привела к внедрению в клиническую практику однофотонной эмиссионной компьютерной томографии (ОФЭКТ), позитронной эмиссионной томографии в сочетании с компьютерной томографией (ПЭТ КТ), магнитно-резонансной томографии сердца [9—13].
Цель исследования — комплексная оценка состояния перфузии, метаболизма и регионарной сократимости миокарда у больных ПКС в отдаленные сроки после хирургической коррекции порока.
Материал и методы
Исследование выполнено у 30 больных ПКС через 1—8 лет после протезирования клапанов сердца. Среди них были 21 мужчина и 9 женщин, средний возраст пациентов — 57,1±12,5 года, средний функциональный класс сердечной недостаточности по классификации NYHA 1,5±0,6. У 13 пациентов имелся корригированный порок митрального клапана, у 17 — аортального клапана. Причинами пороков сердца были ревматическая болезнь сердца у 10 пациентов, дегенерация соединительной ткани — у 13, инфекционный эндокардит — у 7. По данным эхокардиографии, все протезы клапанов сердца имели удовлетворительную функцию, признаков парапротезных фистул и эндокардита не было. У всех больных, по данным КГ, не было выявлено гемодинамически значимых стенозов.
 Для перфузионной ОФЭКТ, синхронизированной с электрокардиограммой, использовали радиофармпрепарат технетрил (ООО «Диамед») в дозе 740±50 Мбк на одного пациента. Оценка регионарной сократимости выполнена по полярным картам подвижности и систолического утолщения стенки левого желудочка (ЛЖ). Полярная карта подвижности может быть представлена сведениями об изменении положения эндокарда в период от конечной диастолы до конечной систолы в миллиметрах, а также в баллах от 0 (максимально подвижные сегменты) до 5 (акинезия).
Для перфузионной ОФЭКТ, синхронизированной с электрокардиограммой, использовали радиофармпрепарат технетрил (ООО «Диамед») в дозе 740±50 Мбк на одного пациента. Оценка регионарной сократимости выполнена по полярным картам подвижности и систолического утолщения стенки левого желудочка (ЛЖ). Полярная карта подвижности может быть представлена сведениями об изменении положения эндокарда в период от конечной диастолы до конечной систолы в миллиметрах, а также в баллах от 0 (максимально подвижные сегменты) до 5 (акинезия).
На полярной карте систолического утолщения отображается изменение толщины миокардиальной стенки в период от конечной диастолы до конечной систолы в процентах, а также в баллах — от 0 до 3 (акинезия).
Спустя 2—3 сут после оценки перфузии была выполнена метаболическая ОФЭКТ миокарда с радиофармпрепаратом йодофен. Доза препарата составила 230±50 МБк. Качественную и количественную оценку метаболизма жирных кислот в миокарде, как и перфузию, проводили по реконструируемым полярным диаграммам. Уровень накопления радиофармпрепарата оценивали по критериям J. Taki [14], выделяя нормальный (>70%), легко сниженный (от 69 до 56%), умеренно (от 55 до 45%), выраженно (от 44 до 30%) и резко сниженный (<29%).
На основании полученных данных проводили анализ комплексного состояния миокарда. Зоны снижения перфузии и метаболизма рассматривали как участки кардиосклероза. К гибернации миокарда относили участки, в которых снижение перфузии превалировало (разница более 10%) над снижением метаболизма, к станнингу миокарда относили участки, в которых снижение метаболизма превалировало (разница более 10%) над перфузией [15].
Результаты
Всего было рассмотрено 600 сегментов миокарда ЛЖ у 30 пациентов. Комплексная оценка состояния сегментов миокарда представлена на рис. 1. Кардиосклероз (К) отмечен в 160 (27%) участках, гибернация — в 15 (3%), станнинг — в 1, снижение перфузии при нормальном метаболизме — в 54 (9%), снижение метаболизма при нормальной перфузии — в 13 (2%), сегменты без перфузионно-метаболических нарушений — в 355 (59%). В большинстве сегментов перфузионно-метаболические нарушения отсутствовали. Наиболее распространенным видом изменений в миокарде был кардиосклероз.
В большинстве случаев у пациентов отмечалась легкая степень нарушения перфузии и метаболизма. Резких нарушений метаболизма в отличие от перфузии не отмечено. Для сегментов с нарушениями захвата перфузионной и метаболической меток (кардиосклероз) нарушения кинетики миокарда отмечены лишь в 55% случаев. Таким образом, отсутствие нарушений кинетики миокарда не всегда означает, что в данном участке миокарда отсутствуют перфузионно-метаболические нарушения.
При этом сегменты миокарда ЛЖ с нарушением кинетики без перфузионно-метаболических нарушений локализовались в 73% случаев в области межжелудочковой перегородки.
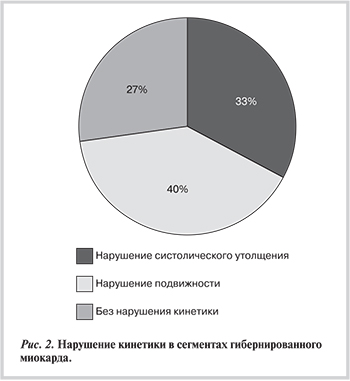
Для 73% сегментов в состоянии гибернации отмечены нарушения кинетики миокарда, что подтверждает обязательное для «спящего» миокарда ограничение сократимости в целях сохранения источников энергии, необходимой для выживания в условиях хронической ишемии (рис. 2).
Нарушение метаболизма жирных кислот даже при сохраненной перфузии сопровождалось нарушением сократимости миокарда. Сегменты с нормальным метаболизмом жирных кислот, как правило, не имели нарушений кинетики, несмотря на присутствие дефицита кровоснабжения.
 Базальные сегменты миокарда ЛЖ в обследованной группе больных являлись участками наиболее распространенных перфузионно-метаболических нарушений.
Базальные сегменты миокарда ЛЖ в обследованной группе больных являлись участками наиболее распространенных перфузионно-метаболических нарушений.
Наиболее выраженные перфузионно-метаболические нарушения регистрировались у пациентов, у которых причиной ПКС был инфекционный эндокардит. У них наблюдались разнообразные варианты нарушений состояния миокарда: кардиосклероз (48% сегментов), гибернация (21% сегментов), снижение перфузии при нормальном метаболизме (15% сегментов), снижение метаболизма при нормальной перфузии (16% сегментов).
У пациентов с корригированной митральной недостаточностью дегенеративной этиологии также часто отмечались разнообразные варианты перфузионно-метаболических нарушений миокарда: кардиосклероз (60% сегментов), гибернация (13% сегментов), снижение перфузии при нормальном метаболизме (12% сегментов), снижение метаболизма при нормальной перфузии (15% сегментов).
Обсуждение
Проведенные исследования показали, что у больных ПКС, перенесших хирургическую коррекцию порока, в миокарде доминируют склеротические изменения диффузного характера. Локализация этих изменений преимущественно затрагивает базальные сегменты. Объяснение этого явления может быть следующим. Для пациентов с ПКС характерна гипертрофия миокарда ЛЖ, в связи с этим отмечается относительное истончение базальных отделов, а также нижней стенки ЛЖ, которая выполняет опорную функцию, располагаясь на диафрагме. Кроме того, истончение базальных отделов ЛЖ может быть истинным. Перегрузка давлением или объемом влияет в первую очередь на базальные сегменты, увеличивая их истончение и снижая кровоток за счет компрессии эндокарда.
Миокард в состоянии гибернации встречается у больных ПКС значительно реже. Причиной гибернации с учетом того, что в проведенной группе больных, по данным КГ, не было гемодинамически значимых изменений, являются нарушения перфузии на уровне микрососудистого русла — «хроническая микрососудистая ишемия». Для гибернации характерно значительное снижение кинетики миокарда, поэтому такие больные отмечают прогрессирующее снижение толерантности к физическим нагрузкам.
У пациентов исследованной группы выявлены сегменты пограничного состояния, в которых нормальные показатели метаболизма сочетаются с легкими нарушениями перфузии без существенных нарушений кинетики. Можно предположить, что в дальнейшем данные сегменты могут изменить свое состояние как в сторону ухудшения, так и в сторону улучшения. Кроме того, отмечены сегменты с нормальной перфузией и легким снижением метаболизма. Нарушения кинетики в них встречаются значительно чаще, что обусловлено дефицитом энергетических субстратов. Возможно, что состояние данных сегментов в дальнейшем улучшится, так как нормальная перфузия является важнейшим фактором восстановления миокарда.
Необходимо отметить, что у пациентов с инфекционным поражением клапанов наблюдается картина сочетания различных нарушений перфузии и метаболизма миокарда во многих сегментах. Этот факт подтверждается данными морфологического исследования миокарда у пациентов с инфекционным эндокардитом [16]. Поражение эндокарда при инфекционном эндокардите сопровождается также нарушением кровообращения в миокарде на уровне микроциркуляторного русла вследствие повреждения эндотелия циркулирующими иммунными комплексами и образования микротромбов. Инфекционный миокардит сопровождает любые ПКС бактериального происхождения.
Распространенные нарушения перфузии и метаболизма характерны для пациентов с дегенеративными пороками (миксоматозная дегенерация). Изменение структуры соединительной ткани затрагивает не только клапанный аппарат сердца, но и фиброзный остов сердца, который образует тесную анатомическую и функциональную связь с кардиомиоцитами. Хирургическое вмешательство не останавливает процесс дегенерации соединительной ткани миокарда, поэтому нарушения его кровоснабжения и сократимости сохраняются и прогрессируют.
Выводы
У больных пороками клапанов сердца даже после успешной хирургической коррекции порока и нормализации внутрисердечной гемодинамики может сохраняться сердечная недостаточность, которая обусловлена перфузионно-метаболическими нарушениями миокарда.
Перфузионные нарушения в миокарде у больных пороками клапанов сердца могут наблюдаться при отсутствии нарушений кровотока в коронарных артериях.



