ВВЕДЕНИЕ
Убедительно доказано, что женщины, перенесшие артериальную гипертензию (АГ) во время беременности, в последующем имеют гораздо более высокий риск развития гипертонической болезни [1, 2]. Также они характеризуются более высоким риском развития сахарного диабета 2-го типа и нарушений липидного обмена [3].
Ренин-ангиотензин-альдостероновая система (РААС) представляет собой гормональную систему, регулирующую артериальное давление (АД), электролитный и жидкостный гомеостаз. На основе априорных знаний о биологических функциях с использованием подхода генов-кандидатов предлагалось проанализировать генетическую основу АГ и регуляции АД [4, 5]. Несмотря на то что во многих исследованиях показана ассоциация АГ с полиморфными вариантами генов ангиотензиногена AGT rs699 (M235T) и AGT rs4762 (T174M), рецептора 1-го типа ангиотензина II ATR1 rs5186 (A1166C), ангиотензинпревращающего фермента ACE rs4340 (I/D), данные об их ассоциации с ожирением, метаболическим синдромом (МС), некоторыми болезнями легких и нервной системы ограниченны [6–8]. Между тем изучение полиморфных вариантов генов и их связи с заболеваниями очень важно для оценки индивидуального риска развития последних. Следовательно, анализ ассоциации любого полиморфизма в разных популяциях специфичен для этих групп и может рассматриваться как маркер для определения вероятности возникновения патологии. Отдельный интерес представляет исследование полиморфных вариантов генов РААС у женщин в молодом и среднем возрасте в российской популяции до развития кардиометаболических заболеваний.
МАТЕРИАЛ И МЕТОДЫ
Тип исследования – «случай – контроль».
Исследуемая популяция – пациенты амбулаторного звена МАУЗ «Городская клиническая больница № 11» г. Челябинска, обратившиеся к терапевту или кардиологу по месту жительства в 2013–2016 гг. Протокол исследования был одобрен локальным Этическим комитетом ФГБОУ ВО «Южно-Уральский государственный медицинский университет» Минздрава России (протокол № 11 от 09.11.2013, с изменениями от 22.02.2019 – протокол № 7). Все участники дали письменное информированное согласие на участие в исследовании.
Критерии включения: возраст 18–45 лет, подписанное информированное согласие на участие в исследовании, наличие родов в анамнезе.
Критерии исключения: симптоматические АГ, различные клинические формы ишемической болезни сердца, инсульты и прочие сосудистые катастрофы в анамнезе, хроническая сердечная и дыхательная недостаточность, острая патология опорно-двигательного аппарата (острые артриты), аутоиммунные заболевания, онкологические заболевания в последние 5 лет, беременность и период лактации.
В общей сложности исследование вошли 66 женщин: группа 1 («случаи») – 33 участницы с анамнезом АГ в период беременности; группа 2 («контроли») – 33 участницы без АГ в период беременности в анамнезе.
В соответствии с действующими клиническими рекомендациями среди гипертензивных нарушений во время беременности выделяли следующие их формы: хроническая АГ, гестационная АГ, преэклампсия и преэклампсия, развившаяся на фоне хронической АГ [9, 10]. В структуре АГ на долю гестационной АГ приходилось 75,8% случаев, хронической АГ и преэклампсии – по 12,1% случаев.
Антропометрические измерения. Вес (кг) измеряли с помощью калиброванных весов с точностью до 0,1 кг. Рост (см) определяли посредством ростомера с точностью до 1 см. Измерения веса и роста использовались для расчета индекса массы тела (ИМТ в кг/м2). Окружность талии (ОТ) оценивалась в средней точке между нижним краем последнего прощупываемого ребра и верхней части гребня подвздошной кости.
Измерение АД. АД измерялось механическим тонометром по методу Короткова в амбулаторных условиях после отдыха участниц в течение не менее 5 мин.
Метаболические показатели. Анализируемые биохимические параметры включали общий холестерин, холестерин липопротеидов высокой плотности (ХС ЛПВП) и холестерин липопротеидов низкой плотности (ХС ЛПНП), триглицериды (ТГ), глюкозу в сыворотке крови.
Метаболический синдром (МС) устанавливался в соответствии с критериями Российского медицинского общества по артериальной гипертонии при наличии центрального (абдоминального) типа ожирения (ОТ > 80 см) и дополнительных критериев:
- уровень АД > 140/90 мм рт. ст. или лечение антигипертензивными препаратами;
- повышение уровня ТГ > 1,7 ммоль/л;
- снижение уровня ХС ЛПВП < 1,2 ммоль/л;
- повышение уровня ХС ЛПНП > 3,0 ммоль/л или лечение липидснижающими препаратами;
- нарушение гликемии натощак – повышенный уровень глюкозы плазмы натощак ≥ 6,1 и < 7,0 ммоль/л.
МС считается достоверным при наличии хотя бы трех указанных критериев – одного основного и двух дополнительных [11].
Молекулярно-генетическое тестирование выполнялось методом полимеразной цепной реакции (ПЦР) в лаборатории областной станции переливания крови г. Челябинска с применением набора реактивов («Литех», Москва) на ПЦР-анализаторе «Терцик» («ДНК-технология», Россия). Анализу подвергалась геномная ДНК, выделенная из лейкоцитов цельной крови, стабилизированной ЭДТА, с помощью реагента «ДНК-экспресс-кровь». Исследовались полиморфные варианты генов РААС: рецептора ангиотензина II типа 1 (rs5186), ангиотензиногена (rs699), ангиотензиногена (rs4762), ангиотензинпревращающего фермента (rs4340).
Статистический анализ. Данные, обрабатывавшиеся при помощи пакета статистических программ MedCalc (версия 22.014), представлены как медиана и межквартильный диапазон для непрерывных переменных с использованием U-критерия Манна – Уитни и как абсолютные и относительные частоты – для категориальных переменных с применением критериев χ2 Пирсона и Фишера. Для каждого исследования «случай – контроль» частоты генотипов или аллелей сравнивались между случаями и контролем в трех разных режимах, соответствие равновесию Харди – Вайнберга оценивалось посредством критерия χ2 Пирсона в онлайн-программе SNPStats (Каталонский институт онкологии, Барселона, Испания) [12]. В первом режиме (режим частот аллелей) частоты аллелей сравнивались между случаями и контролем с помощью таблицы сопряженности 2 × 2. Во втором (рецессивном) режиме частоты испытуемых, гомозиготных по аллелю 1, сопоставлялись с остальными при помощи таблицы сопряженности 2 × 2. В третьем (доминантном) режиме частоты испытуемых, которые имели аллель 1 (гомозиготы и гетерозиготы по аллелю 1), сравнивались с остальными также при помощи таблицы сопряженности 2 × 2. Отношение шансов (ОШ) и 95% доверительные интервалы (ДИ) рассчитывались путем логистического регрессионного анализа с поправкой на возраст, пол и ИМТ. За статистически достоверные принимались значения p < 0,05.
РЕЗУЛЬТАТЫ
Средний возраст исследованных женщин составил 41 [40–43] год в группе 1 и 38 [33–41] лет – в группе 2 (p = 0,006). Участницы в обеих группах имели как высшее, так и среднее специальное образование, все проживали в благоустроенных квартирах. Общая характеристика групп исследования приведена в таблице 1.
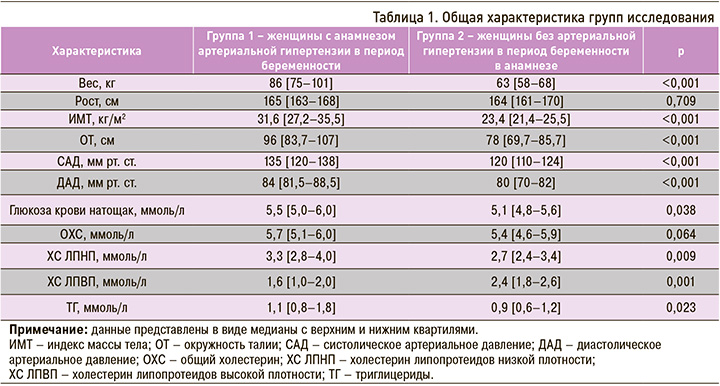
Женщины с анамнезом АГ в период беременности имели более высокие значения веса, ИМТ и ОТ, показатели САД и ДАД, концентрации глюкозы и атерогенных липидов по сравнению с группой 2. Следует отметить, что МС встречался у каждой третьей женщины в группе 1 и имел место лишь у одной женщины в группе 2 (p = 0,003). Три полиморфизма (rs699, rs4762, rs5186) соответствовали равновесию Харди – Вайнберга в контрольной группе (р > 0,05). Мы сравнили различия в распределении частот аллелей между случаями и контролем с помощью критерия χ2 Пирсона и обнаружили ряд аллелей, ассоциированных с МС (табл. 2).
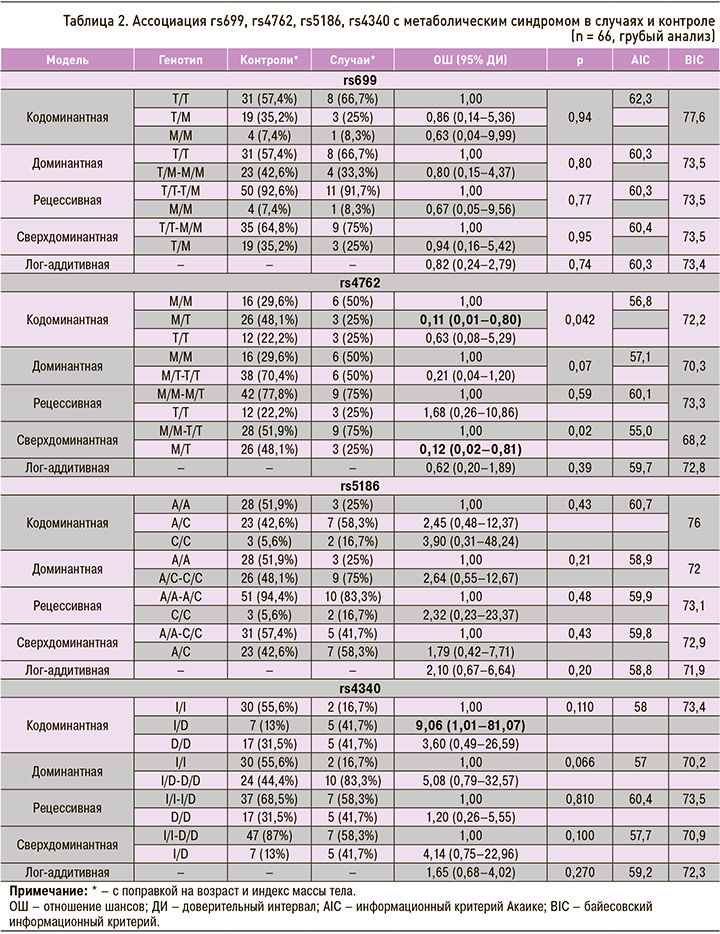
Для оценки ассоциации между изучаемыми полиморфными вариантами генов РААС и МС с использованием 5 генетических моделей (кодоминантной, доминантной, рецессивной, сверхдоминантной и логарифмически-аддитивной) применялся логистический регрессионный анализ. Как показано в таблице 2, грубый анализ выявил, что генотип M/T в rs4762 связан со сниженным риском МС в рамках кодоминантной модели (p = 0,042; ОШ 0,11; 95% ДИ: 0,01–0,80) и по логарифмически-аддитивной модели (p = 0,002; ОШ 0,12; 95% ДИ: 0,02–0,81). После корректировки на возраст и ИМТ мы обнаружили, что генотип M/T в rs4762 оставался связанным со сниженным риском МС (ОШ 0,09; 95% ДИ: 0,01–0,78; табл. 3).
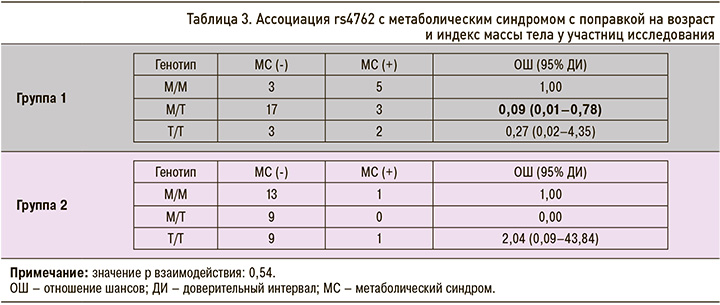
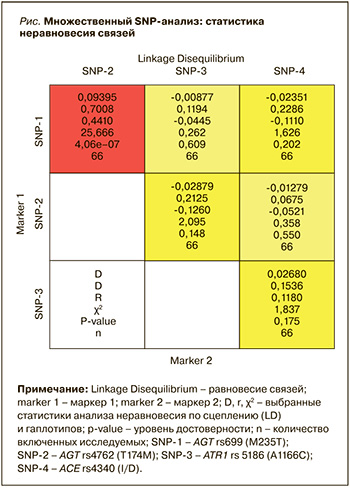
При выполнении анализа гаплотипов, которые включали 4 полиморфных варианта последовательностей генов (rs699, rs4762, rs5186, rs4340), была оценена ассоциация между предполагаемыми гаплотипами и риском МС. Блок гаплотипов, включавший 2 полиморфных варианта последовательностей (rs699, rs4762), показан на рисунке; при этом не было установлено, что эти гаплотипы взаимно связаны с риском развития МС.
ОБСУЖДЕНИЕ
В последние десятилетия было показано, что полиморфные варианты генов РААС ассоциированы с рядом сердечно-сосудистых заболеваний, включая АГ, инфаркт миокарда, инсульт, ишемическую болезнь сердца, сердечную недостаточность [13, 14]. Кроме того, ряд других болезней, таких как депрессия, ожирение, диабетическая нефропатия, преэклампсия и поражение печени, также могут быть связаны с названными генетическими факторами [15–17]. Полиморфный вариант rs4762 гена ангиотензиногена способен повышать активность РААС, приводя к вазоконстрикции. Ангиотензин II вызывает высвобождение большего количества альдостерона, что в конечном итоге приводит к увеличению объема плазмы и развитию АГ [18].
Различные исследования продемонстрировали положительную ассоциацию полиморфных вариантов rs4762 гена ангиотензиногена (ATG Thr174Met) с АГ [19–21] и c сахарным диабетом 2-го типа [22] и негативную связь – с ожирением [23]. В других работах наличие подобных ассоциаций доказано не было [24].
Ряд данных свидетельствует о причастности РААС не только к АГ, но и к развитию ожирения и инсулинорезистентности, что указывает на ее потенциальную причинно-следственную связь с МС. Экспериментальные исследования показали, что ангиотензин II подавляет адипогенную дифференцировку адипоцитов человека через рецептор AT1, что способствует увеличению секреции воспалительных цитокинов или диабетогенных адипокинов, ингибированию передачи сигналов инсулина и развитию резистентности к этому гормону [25]. Ангиотензиноген – важный регулятор АД, синтезируемый не только в печени, но и в жировой ткани и сам по себе являющийся фактором роста адипоцитов [26]. Полученную в нашем исследовании негативную ассоциацию генотипа M/T гена ангиотензиногена rs4762 (ATG Thr174Met) у женщин с АГ в анамнезе в период беременности мы связываем с более низкой концентрацией компонентов РАСС (в том числе ангиотензиногена) при данном полиморфном варианте гена, что потенциально может указывать на его «протективную» роль в отношении патофизиологических эффектов этих компонентов.
Ограничения исследования. Хотя и существует возможность идентифицировать генетические ассоциации с МС, полученные нами данные не позволяют прояснить причинно-следственные механизмы. В то же время, несмотря на ограничения небольшого размера выборки, нам удалось продемонстрировать ассоциацию полиморфного варианта гена rs4762 (ATG Thr174Met) с МС. Вероятно, больший размер выборки и большее количество локусов позволили бы получить дополнительные доказательства роли изучаемых последовательностей генов в развитии МС у женщин, имевших АГ во время беременности. Кроме того, трудно сделать четкие выводы насчет влияния конкретных генетических вариантов на регуляцию АД, что, вероятно, связано с плохо изученными в доступной литературе ген-генными взаимодействиями и/или механизмами «ген – окружающая среда», а также плохо определенными фенотипами при МС.
Тем не менее, согласно полученным в нашем исследовании результатам, M/T полиморфный вариант гена rs4762 (ATG Thr174Met) продемонстрировал отрицательную связь в отношении развития МС у женщин, имевших анамнез АГ в период беременности, с поправкой на возраст и ИМТ.
ЗАКЛЮЧЕНИЕ
Полученные данные могут помочь в разработке предиктивных моделей развития кардиометаболических заболеваний у женщин с анамнезом АГ в период беременности, а также стать важным шагом на пути к выявлению экспрессии генов-кандидатов, участвующих в развитии многофакторных заболеваний.



