ВВЕДЕНИЕ
Бронхиальная астма (БА) – наиболее распространенное хроническое заболевание, поражающее бронхолегочную систему, которое регистрируется повсеместно во всех половых и возрастных группах [1]. По разным данным, этой патологией страдают от 5 до 10% человечества [2]. С 1990 по 2019 г., несмотря на успехи в лечении и профилактике БА, число случаев ее регистрации возросло на 14,97%, что может быть связано с ростом численности населения Земли [3]. Показатель распространенности БА к 2025 г. может достичь 400 млн случаев [4].
Установлено, что при БА коморбидные состояния регистрируются чаще, чем при других хронических патологиях [5]. Наиболее часто вместе с ней развиваются ожирение, нарушения сна, гастроэзофагеальная рефлюксная болезнь, хроническая обструктивная болезнь легких (ХОБЛ) и психические заболевания [6]. Наличие сопутствующих хронических заболеваний у пациентов с БА обусловлено снижением ее контроля, повышением тяжести течения и риска обострений, а также ухудшением качества жизни (КЖ) [7]. Кроме того, возрастание числа коморбидных состояний при БА ассоциировано с увеличением риска смертности от всех причин [8].
Существует большое количество данных, указывающих на взаимное негативное влияние БА и ожирения [9, 10]. В то же время данные об особенностях мультиморбидного течения БА и остеоартрита (ОА) на сегодняшний день ограниченны. При этом широкая распространенность обеих патологий в популяции приводит к высокой вероятности их регистрации у одного пациента. Течение как БА, так и ОА сопровождается активацией воспалительных реакций и снижением физической активности (ФА) [11, 12]. По этим причинам представляется актуальным изучение мультиморбидного течения БА, ожирения и ОА.
Цель – изучить влияние ОА на течение БА в сочетании с ожирением, а также ФА и КЖ в данной группе пациентов.
МАТЕРИАЛ И МЕТОДЫ
В исследовании приняли участие 137 пациентов с БА. Доля участников женского пола составила 73,7% (n = 101), мужского – 26,3% (n = 36). Медиана возраста равнялась 54 [47; 60] годам. Основные характеристики включенных в исследование пациентов представлены в таблице 1.

Критерии включения: наличие согласия пациента на участие в исследовании, установленный диагноз БА, возраст от 18 до 75 лет. Верификация диагноза БА производилась на основании руководства «Бронхиальная астма: федеральные клинические рекомендации по диагностике и лечению» (Российское респираторное общество, Российская ассоциация аллергологов и клинических иммунологов, Союз педиатров России) [13].
Критерии невключения: хронические заболевания легких (за исключением самой БА), острые респираторные инфекции, злокачественные новообразования, беременность и лактация. Кроме того, в исследование не включались пациенты, имеющие психические расстройства и декомпенсированные соматические заболевания.
На первом этапе участники были разделены на две группы в соответствии с наличием или отсутствием установленного диагноза ОА (в исследовании учитывался ОА коленных и тазобедренных суставов). На втором этапе выполнялось обследование пациентов, которое включало клиническую оценку заболеваний, определение альгофункционального индекса Лекена, рентгенологическое исследование коленных и тазобедренных суставов, спирометрию на спироанализаторе «Диамант» (Россия), оценку ФА (опросник двигательной активности ОДА23+ и международный опросник для определения ФА International Questionnaire on Physical Activity – IPAQ), контроля БА (опросник контроля симптомов астмы Asthma Control Questionnaire-5 – ACQ-5) и КЖ (опросник качества жизни при астме Asthma Quality of Life Questionnaire – AQLQ-S).
В рамках лабораторного исследования проводилось определение концентрации интерлейкина 4 (ИЛ-4), ИЛ-6 и фактора некроза опухоли (ФНО-α), оксидантно-антиоксидантного статуса (при помощи набора реагентов ImAnOx и PerOx, Immundiagnostik, Германия) с использованием планшетного фотометра iMark (Biorad), а также уровня лептина крови.
Статистическая обработка данных осуществлялась с использованием программы Statgraphics Centurion 18 (Statgraphics Technologies Inc., США). Численные данные с нормальным распределением представлены в виде среднего ± стандартного отклонения. При распределении данных, отличном от нормального, полученные значения записывались в виде медианы и межквартильного размаха. Корреляционный анализ проводился с расчетом рангового коэффициента корреляции Спирмена (r) и уровня значимости (p). Определение критерия Хи-квадрат (χ2) Пирсона применялось для сравнения частотных показателей в формируемых таблицах сопряженности. Сравнение показателей в исследуемых группах выполнялось с помощью критерия Манна – Уитни. Статистически значимыми считались значения p < 0,05.
РЕЗУЛЬТАТЫ
У 46 пациентов исследуемой выборки ОА выявлено не было. Таким образом, 1-я группа состояла из 46 участников с БА без ОА – 13 (28,26%) мужчин и 33 (71,74%) женщин (средний возраст 51,57 ± 10,45 года). 2-я группа включала 91 больного с БА и ОА – 23 (25,27%) мужчины и 68 (74,73%) женщин (средний возраст 54,10 ± 9,17 года).
В соответствии с рентгенологическими критериями Келлгрена – Лоуренса I стадия ОА была зарегистрирована у 25 (27,5%) пациентов 2-й группы, II – у 60 (65,9%), III – у 6 (6,6%) человек.
На рисунке 1 показано распределение исследованных пациентов с учетом индекса массы тела (ИМТ) и наличия/отсутствия ОА. В группе больных БА в сочетании с ОА оказалось достоверно больше лиц с ожирением (χ2 = 132,612; p = 0,0000).
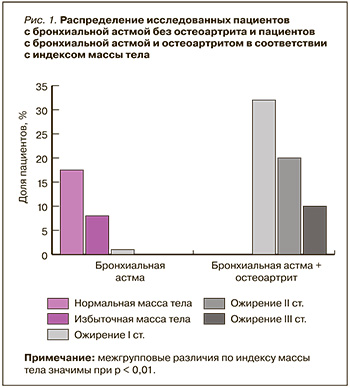
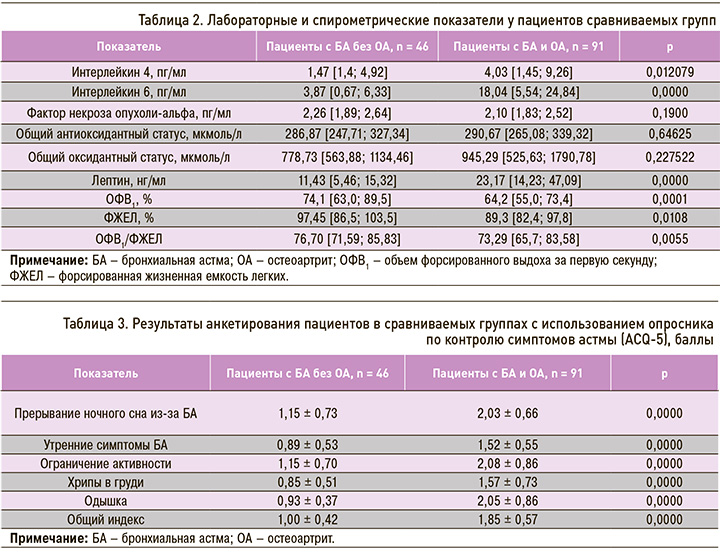
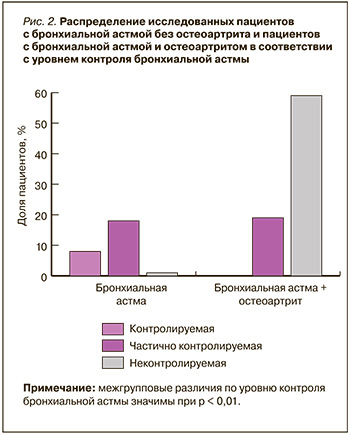
Сформированные группы не различались по полу (p = 0,71), возрасту (p = 0,16), длительности течения БА (p = 0,34), общему антиоксидантному статусу (p = 0,65), общему оксидативному статусу (p = 0,23) и концентрации ФНО-α (p= 0,19). В то же время были получены различия в отношении уровня контроля БА (p = 0,0000), индекса Лекена (p = 0,0000), ИМТ (p = 0,0000), уровня ИЛ-4 (p = 0,012079), ИЛ-6 (p = 0,0000) и лептина (p = 0,0000). Также группы различались по основным спирометрическим показателям и результатам анкетирования с использованием опросника ACQ-5 (табл. 2, 3). У пациентов с БА и ОА уровень контроля соответствовал частично контролируемой или неконтролируемой астме (1,85 ± 0,57 балла), в группе без ОА – контролируемой или частично контролируемой БА (1,00 ± 0,42 балла). Представленные группы статистически значимо различались по уровню контроля астмы (рис. 2). Среди пациентов с БА и ОА было достоверно больше больных с неконтролируемой БА (χ2 = 55,232; p = 0,0000).
Корреляционный анализ позволил выявить положительные связи между уровнем контроля БА и стадией ОА (r = 0,55; p = 0,0000), ИМТ (r = 0,63; p = 0,0000), концентрацией ИЛ-4 (r = 0,21; p = 0,0145), ИЛ-6 (r = 0,37; p = 0,0000) и лептина (r = 0,33; p = 0,0002). Наряду с этим присутствовала положительная корреляционная связь между стадией ОА, уровнем ИЛ-4 (r = 0,19; p = 0,0299), ИЛ-6 (r = 0,48; p = 0,0000), лептина (r = 0,50; p = 0,0000) и общим оксидативным статусом (r = 0,17; p = 0,0471), а также отрицательная – с объемом форсированного выдоха за 1 сек. (ОФВ1, r = -0,23; p = 0,0234) и форсированной жизненной емкостью легких (ФЖЕЛ, r = -0,24; p = 0,0157).
Показатели ИМТ имели положительную связь с концентрацией ИЛ-4 (r = 0,18; p = 0,0382), ИЛ-6 (r = 0,46; p = 0,0000), лептина (r = 0,62; p = 0,0000), общим оксидативным статусом (r = 0,15; p = 0,0865) и отрицательную – с ОФВ1 (r = -0,37; p = 0,0003) и ФЖЕЛ (r = -0,44; p = 0,0000).
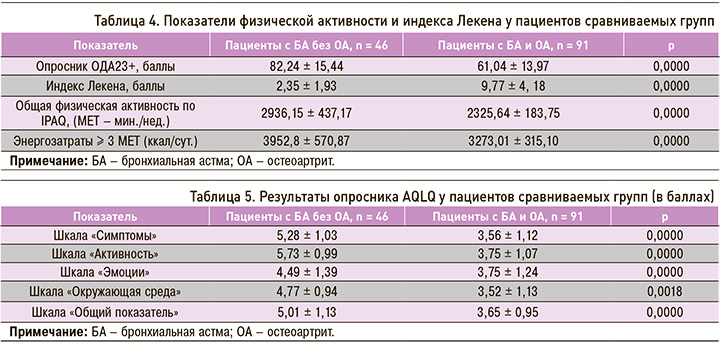
При сравнении групп по уровню ФА были установлены значимые различия по данным опросников ОДА23+ и IPAQ. Так, у пациентов с БА без ОА среднее значение этого параметра составило 82,24 ± 15,44 балла, что соответствовало ФА от умеренной до высокой, в то время как у пациентов с БА и ОА уровень ФА был умеренным или низким (средний балл 61,04 ± 13,97). При оценке энергозатрат повседневной активности «МЕТ-минуты в неделю» и метаболического эквивалента (МЕТ-минуты в неделю – отношение скорости метаболизма при работе к скорости метаболизма в состоянии покоя) по опроснику IPAQ более низкие показатели также были в группе участников с ОА (табл. 4). При сравнении результатов опросника AQLQ в группах исследования были найдены статистически значимые различия по всем его шкалам. В наибольшей степени группы различались по шкалам «активность» и «общий показатель» (табл. 5).
ОБСУЖДЕНИЕ
Совместное течение ОА и БА является малоизученным сочетанием патологий. В исследуемой выборке пациентов с БА была зафиксирована высокая частота встречаемости ОА, которая равнялась 66,42%. В работе Koo H.K. et al. было показано, что распространенность ОА выше у пациентов с БА (31,9% ± 2,8%), чем у больных ХОБЛ (17,8% ± 1,5%) [14]. Кроме того, авторы указали, что связь между БА и ОА оставалась значимой как у пациентов с ожирением, так и без него (отношение шансов 1,70; 95% доверительный интервал: 1,07–2,70). В нашем исследовании в структуре мультиморбидных заболеваний у пациентов с сочетанием БА и ОА была выявлена более высокая доля лиц с ожирением, чем среди пациентов с БА без ОА. Мы установили прямые корреляционные связи между уровнем контроля БА и стадией ОА (r = 0,55; p = 0,0000), а также ИМТ (r = 0,63; p = 0,0000). Наличие ожирения у пациентов с БА ассоциировано со снижением контроля БА и ответа на проводимую терапию. При этом связь указанных патологий двунаправленна: наличие БА увеличивает риск развития и прогрессирования ожирения, а у пациентов с ожирением возрастает вероятность развития БА [15].
В свою очередь, повышение осевой нагрузки на суставы и метаболические нарушения, возникающие при ожирении, способствуют формированию ОА [16]. Имеются работы, согласующиеся в плане полученных результатов с представленным исследованием, в которых определялась связь ОА и повышения лептина сыворотки крови [17]. Также в нашем исследовании наблюдалось значимое повышение концентрации провоспалительных цитокинов, в частности ИЛ-6, в группе пациентов с БА и ОА относительно больных БА без ОА. Астма в сочетании с ожирением приводит к возрастанию уровня адипокинов и провоспалительных цитокинов (лептина, резистина, ИЛ-6, ФНО-α), показателей оксидативного стресса (PerOx) и снижению противовоспалительных эффектов адипонектина в сравнении с пациентами, имеющими нормальную или избыточную массу тела [18]. Кроме того, развитие системного эндогенного воспаления при ожирении способствует прогрессированию дегенеративных процессов в хрящевой ткани [19].
Для повышения контроля БА в настоящее время уделяется большое внимание поиску индивидуальных внелегочных персонифицированных признаков, поддающихся лечению [20]. Bahmer T. et al. обнаружили, что более высокие уровни ФА позволяли добиться лучшего контроля БА и были ассоциированы с лучшими показателями спирометрии, меньшим количеством обострений и лучшим КЖ [21]. В проведенном нами исследовании выявлены более низкие значения ФА у пациентов с ОА и БА. С одной стороны, это может быть объяснено совокупным негативным влиянием болевого синдрома, нарушения локомоции, проприоцепции и мышечной слабости, а с другой – усилением одышки и кашля.
Наряду с этим полученные нами результаты свидетельствуют о негативном влиянии мультиморбидного течения указанных патологий на КЖ пациентов. Установлено, что показатель КЖ у больных БА связан с уровнем контроля заболевания и выраженностью его симптомов [22]. Наибольшие различия между сформированными в нашем исследовании группами по данным опросника AQLQ отмечались в отношении шкалы «Активность». Как было сказано ранее, ожирение и ОА выступают факторами, способствующими снижению уровня контроля БА, и их наличие необходимо учитывать при подборе персонализированной терапии пациентам с этим бронхолегочным заболеванием.
ЗАКЛЮЧЕНИЕ
Сочетание БА, ожирения и ОА является малоизученной мультиморбидностью, которая тем не менее широко распространена и негативно сказывается на контроле астмы, тяжести ОА и ожирения, равно как и на прогнозе этих патологий. Результаты представленного исследования свидетельствуют об отрицательном влиянии ОА на ФА и КЖ пациентов с БА.



