Системная склеродермия (ССД) — аутоиммунное заболевание соединительной ткани, основные проявления которого связаны с ишемией и фиброзом органов. Фиброз и нарушение микроциркуляции, приводящие к развитию ишемии и кардиосклероза, служат основной причиной развития одного
из ведущих висцеральных проявлений при ССД — поражения сердца. Кроме того, наличие ССД предполагает более раннее развитие атеросклероза [1], что также увеличивает риск развития сердечно-сосудистых заболеваний (ССЗ) у пациентов с ССД. Частота поражения сердца при ССД
по данным аутопсии достигает 50—90% [1—3]. По данным литературы, желудочковые аритмии обнаруживаются у 4—6% больных ССД при стандартной электрокардиографии, тогда
как при суточном мониторировании электрокардиограммы (ЭКГ) — у 67% [2, 3]. По данным различных источников, для больных ССД характерен высокий риск смерти от ССЗ, причем в 40—60% всех случаев она может быть внезапной [2].
В настоящее время доказана важная роль дисбаланса между процессами оксидации и антиоксидации в развитии и поддержании хронического ревматического воспаления [4, 5]. Антиоксидантная система (АОС) организма представлена целым рядом ферментов, призванных нивелировать патогенный эффект активных форм кислорода. При патологических состояниях нарушается равновесие между агрессивными и защитными факторами, что ведет к еще более глубокому повреждению тканей [4], активизации прооксидантных факторов способствует состояние хронической гипоксии, обусловленной синдромом Рейно [6]. Одними из важных звеньев системы антиоксидантной защиты являются суперок-
сиддисмутаза (СОД — EC 1.15.1.1), глутатионредуктаза (ГР — ЕС 1.6.4.2) и глутатионпероксидаза (ГП — EC 1.11.1.9).
Целью настоящего исследования явились изучение уровня антител (АТ) к ферментам АОС (СОД, ГП, ГР) с использованием иммобилизированной формы магнитоуправляемого сорбента у больных ССД с поражением сердца и определение возможной роли АТ к ферментам в развитии ССЗ при ССД.
Материал и методы
Под наблюдением находились 40 больных с диагнозом ССД, установленным на основании критериев АРА [7] и отечественной классификации болезни (Н. Гусева, 1975) [8] и 30 практически здоровых лиц — доноров станции переливания крови (17 женщин и 13 мужчин) в возрасте от 25 до 47 лет.
Больные ССД. Среди обследованных больных ССД было 38 (95%) женщин и 2 (5%) мужчин. Средний возраст больных составил 38±3,3 года, продолжительность заболевания — 14±2,6 года. Лимитированная форма ССД имелась у 27 (67,5%) из наблюдавшихся больных, диффузная — у 13 (32,5%). I степень активности определена у 16 (40%) больных, II — у 23 (57,5%), III — у одного (2,5%). Хроническое течение выявлено у 16 (40%) пациентов, подострое — у 23 (57,5%), острое — у одного (2,5%). Больные с подострым и острым течением заболевания, II и III степенью активности в дальнейшем будут рассматриваться в одной группе вследствие малого количества больных
с острым течением и III степени активности.
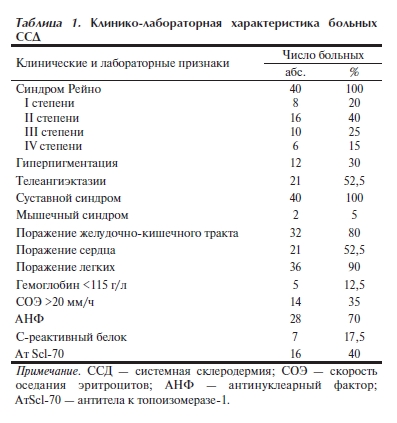
I стадия заболевания (начальная) диагностирована у 10 (25%) больных, II (генерализованная) — у 26 (65%), III (терминальная) — у 4 (10%). У 80% больных ССД отмечалась выраженная форма синдрома Рейно (II, III, IV степени). Характеристика больных представлена в табл. 1.
АТ к СОД, ГР определяли в сыворотке крови больных по разработанному нами варианту непрямого иммуноферментного анализа (И.П. Гонтарь, 2001) [9], с использованием иммобилизированных антигенных форм ферментов и иммунопероксидазного конъюгата производства НИИ ЭМ
им. Гамалеи, АТ к ГП по аналогичному методу с применением конъюгата на основе фосфатазы производства ЗАО «Биосан» (Новосибирск, Россия). Иммобилизацию проводили методом эмульсионной полимеризации в потоке газообразного азота с включением магнитного материала в структуру полиакриламидного геля. Положительными считали результаты, превышающие 2 стандартных отклонения показателей, полученных при обследовании здоровых лиц. Все исследования проводили при поступлении и при выписке больных из стационара после завершения лечения. В качестве антигена при определении АТ к СОД использовали коммерческий препарат СОД из эритроцитов человека производства НПО «Биопрепарат» с активностью 30 ед./мг, при определении АТ к ГП — препарат глутатионпероксидазы производства НПО РЕАХИМ, серия 186—68 с активностью
380 ед./мг, ГР — препарат производства НПК «Спутник» с активностью 340 ед./мг. Активность СОД определяли по методу С. Чевари и соавт. (1993) [10] , активность ГП — по методу Flohe и Gunzler (1984) [11], ГР — по методу Hosoda и Nakamura, описанному М.А. Шифриным (1977) [12].
Всем больным ССД проводили капилляроскопию сосудов ногтевого ложа.
Влияние АТ к СОД, ГП, ГР на их активность изучали в опытах in vitro с растворимой и иммобилизированной формами ферментов. Источником специфических иммуноглобулинов
служили сыворотки больных ССД с заранее высоким титром АТ (экстинкция 0,2—0,6 ед. опт. пл.). «Чистые» АТ к ферментам получали с помощью соответствующего антигенного иммуносорбента. После диализа против забуференного физиологического раствора и последующего концентрирования через полупроницаемую мембрану системы Sartorius до первоначального объема сыворотки АТ использовали
в эксперименте по изучению их взаимодействия с ферментом. Количество фермента в иммобилизированной и растворимой формах было сопоставимо. В качестве контроля использовали
физиологический раствор и сыворотки доноров.
У всех больных оценивали риск развития ССЗ (10-летний риск развития фатальных сердечно-сосудистых осложнений) по шкале SCORE [13].
Всем пациентам назначали лабораторные и инструментальные исследования, включающие электрокардиографию, суточное мониторирование ЭКГ, эхокардиографию (ЭхоКГ), ультразвуковое исследование органов брюшной полости, а также клиническое, иммунологическое и биохимическое
исследование крови при поступлении и при выписке из стационара после завершения лечения.
Статистическую обработку данных проводили с использованием программных пакетов Statistica 6.0. Применяли методы описательной статистики, критерий χ². Различия и связь признаков считали статистически значимыми при p<0,05.
Результаты и обсуждение
Здоровые лица. При исследовании сывороток здоровых лиц уровень АТ к СОД составил 0,07±0,004 МЕ, к ГП —0,065±0,003 МЕ, к ГР — 0,08±0,004 МЕ. Значения, превышающие их на 2 стандартных отклонения, были приняты за верхнюю границу нормы: для АТ к СОД — 0,114 МЕ, к ГП — 0,1 МЕ, к ГР — 0,124 МЕ. Общая активность СОД в группе здоровых лиц составила 38,2±1,2 ед./мг, амплитуда
колебаний 25,1—51,28 ед./мг. Общая активность ГП составила 0,153±0,007 ед./мг, амплитуда колебаний — 0,073—0,23 МЕ. Общая активность ГР — 114,3±3,7 ед./мг, амплитуда колебаний — 73,6—155,0 ед./мг.
Существенных различий уровня АТ к ферментам в зависимости от пола и возраста не выявлено.
Больные ССД. При поступлении на стационарное лечение у больных ССД наблюдалось достоверное снижение активности СОД (22,6±2,4 ед./мг; р<0,002), ГП (0,099±0,06 ед./мг; p<0,001) и ГР (76,2±3,8 ед./мг; p<0,001), причем отмечалась тенденция к более выраженному снижению активности
по мере нарастания активности процесса. В группе больных ССД АТ к СОД выявлены у 16 (40%), к ГП — у 14 (35%), к ГР — у 15 (37,5%).
При минимальной степени активности патологического процесса (16 пациентов) высокие уровни АТ к СОД выявлены у 6 (37,5%), к ГП — у 5 (35,7%), к ГР — у 4 (26,7%). При ССД со II и III степенью активности (24 больных) по сравнению со здоровыми выявлено снижение активности СОД, ГП,
ГР (р<0,001) и увеличение уровня АТ (р<0,001). Отмечено увеличение числа больных, у которых в сыворотке выявлены высокие уровни АТ: к СОД — у 10 (41,6%), к ГП — у 9 (37,5%), к ГР — у 11 (45,8%).
Всем больным ССД была проведена капилляроскопия ногтевого ложа, выявлены характерные изменения разной степени выраженности: у 22 (55%) — значительные (уменьшение количества капилляров, их деформация, наличие нескольких аваскулярных зон), у 10 (25%) — умеренные, у 8
(10%) — невыраженные.
Кроме того, у всех больных с высоким содержанием АТ к изучаемым ферментам обнаружена высокая степень синдрома Рейно (II—IV). Известно, что синдром Рейно приводит к ишемии и, следовательно, гипоксии тканей [6]. В результате усиливаются пероксидация мембранных структур, апоптоз
клеток, что при снижении антиоксидантной защиты, в том числе, вероятно, вследствие образования АТ к ферментам, наблюдающейся при диффузных заболеваниях соединительной ткани, способствует развитию различной висцеральной патологии [4].
В группе больных ССД у 21 (52,5%) отмечалось поражение сердца. Основные симптомы, отмечавшиеся в клинической картине этих пациентов, представлены в табл. 2.

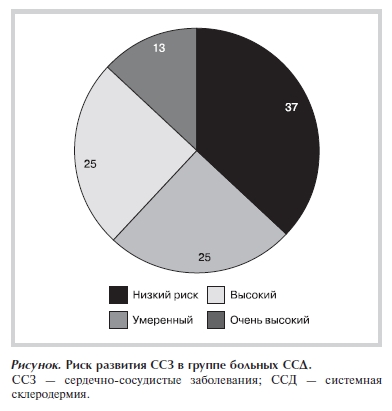
Результаты оценки риска развития ССЗ по шкале SCORE представлены на рисунке. Согласно полученным нами данным необходимо проведение более тщательного обследования всех больных ССД.
При регистрации ЭКГ у 13 (32,5%) больных ССД выявлены нарушения ритма и проводимости: желудочковые и предсердные экстрасистолы, нарушения атриовентрикулярной проводимости I, II степени, блокады ножек пучка Гиса, а также явления ишемии миокарда. В то же время при суточном
мониторировании ЭКГ подобные изменения обнаруживались у 21 (52,5%) больного. По данным ЭхоКГ у 18 (45%) пациентов выявлялась диастолическая дисфункция миокарда, у 12 (30%) — снижение фракции выброса левого желудочка.
При лабораторных исследованиях крови выявлены высокие уровни холестерина у 19 (47,5%) пациентов, а также повышение уровня мочевой кислоты у 16 (40%).
По данным литературы [14], выявлена положительная связь уровня мочевой кислоты с ССЗ, а возможными механизмами влияния мочевой кислоты на коронарный риск, являются увеличение адгезии и агрегации тромбоцитов, усиление процессов свободнорадикального окисления, образование свободных радикалов, что особенно актуально на фоне снижения активности антиоксидантных ферментов при ССД [4].
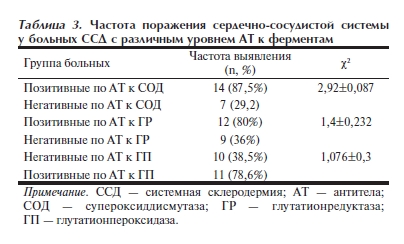
Нами были выделены группы больных с высоким уровнем АТ к изучаемым ферментам (СОД — у 16, ГР — у 15, ГП — у 14) и без таковых (СОД — 24, ГР — 25, ГП — 26), а затем проанализирована частота выявления ССЗ. В группах больных с высоким уровнем АТ к изучаемым ферментам получено
достоверно более частое поражение сердечно-сосудистой системы чем, у пациентов без таковых (табл. 3).
Кроме того, при анализе активности ферментов и уровня АТ к ним в группе больных с поражениями сердечно-сосудистой системы и без таковых нами выявлено снижение активности ферментов и увеличение количества АТ к ним (табл. 4).
Закономерности, выявленные нами в опытах in vitro, которые были проведены для определения патогенетической роли АТ к изучаемым ферментам, представлены в табл. 5. При исследовании активности иммобилизированных форм ферментов после взаимодействия с АТ in vitro обнаружено
снижение активности фермента на 60—70% по сравнению с исходной; кроме того, получены статистически значимые различия с контролем (физиологический раствор) и донорами (р<0,05).
Таблица 4. Показатели активности ферментов и уровни АТ к ним в зависимости от наличия ССЗ.
Таблица 5. Сравнительная характеристика активности иммобилизированной и растворимой форм ферментов после взаимодействия с АТ.
Эти изменения связаны, вероятно, с блокированием активного центра фермента, являющегося одновременно антигенной детерминантой. При исследовании взаимодействия растворимых форм ферментов нами обнаружено снижение его активности на 30—40%. Вероятно, это можно объяснить
конформационными изменениями структуры молекулы, приводящими к неполному совпадению активного центра фермента и его антигенной детерминанты. Таким образом, можно предположить, что выявляемые нами АТ к ферментам АОС служат одной из вероятных причин снижения их фер-
ментативной активности.
Заключение
В крови больных системной склеродермией выявляются антитела к супероксиддисмутазе, глутатионпероксидазе и глутатионредуктазе, продукция которых увеличивается с возрастанием активности процесса, наличием более тяжелых форм течения заболевания, в том числе поражением сердечно-сосудистой системы, и сопровождается снижением активности ферментов. Следовательно, одной из причин угнетения антиоксидантной активности могут являться аутоантитела к ферментам.



