Сталкиваясь с неоднозначным диагнозом, врачу следует помнить простое правило: редкие заболевания встречаются редко. В подавляющем большинстве случаев даже необычные сочетания симптомов оказываются проявлением распространенной патологии. Тем важнее продолжить освещение эффективного взаимодействия клинициста и морфолога в сложных клинических ситуациях, начатое на страницах журнала статьей многоуважаемых Аркадия Львовича Верткина и Натальи Олеговны Ховасовой («Клиницист и морфолог: эффективный симбиоз», журнал «Терапия» № 1, 2015). Название их статьи могло бы стать заглавием регулярного раздела. Необходимость обмена клиническим опытом подтверждается также растущим успехом ставших международными Гаазовских чтений. Что касается приведенного ниже случая, то нам не удалось найти ни одного сообщения о подобном – с метастатическим поражением сердца – течении рака вульвы. Описаны случай метастатического поражения сердца при цистаденокарциноме яичника [1] и несколько случаев такого же метастазирования при раке шейки матки, собранных в тематических обзорах [2, 3]. Для каждой пациентки заболевание закончилось фатально в самые ранние сроки (1–13 мес) после выявления кардиальных метастазов.
Больная П., 43 лет, в сентябре 2015 г. госпитализирована в многопрофильный стационар из инфекционного отделения другой больницы, куда была доставлена несколькими часами ранее бригадой скорой медицинской помощи с направительным диагнозом: ОРВИ средне-тяжелого течения. Гипертермия. Интоксикационный синдром. Инфекционистом диагноз ОРВИ был отвергнут.
 При поступлении предъявляла жалобы на малоинтенсивный непродуктивный кашель, повышение температуры тела до 38,5°С.
При поступлении предъявляла жалобы на малоинтенсивный непродуктивный кашель, повышение температуры тела до 38,5°С.
В анамнезе: трое родов, из которых последние в 2012 г., других беременностей не было; инвазивно растущий неороговевающий плоскоклеточный рак вульвы II ст. (по FIGO), Т2NхM0, комбинированное лечение (лучевая и химиотерапия с последующим хирургическим лечением в объеме резекции половой губы) в сентябре 2014 г.; пункционная биопсия лимфатического узла правой паховой области в июне 2015 г. в связи с его увеличением – опухолевые клетки не были обнаружены; хронический тонзиллит.
Вышеперечисленные жалобы появились за 3 нед до госпитализации на фоне явлений острого респираторного заболевания, в т.ч. фарингита. Амбулаторно лечилась амоксициллином в нерациональном режиме (500 мг 1 раз/сут перорально), наблюдалось временное улучшение в виде стихания лихорадки. Однако через 2 нед от начала заболевания фебрильная лихорадка вернулась, в связи с чем пациентка и обратилась в сентябре за медицинской помощью.
В приемном отделении была осмотрена гинекологом, констатировавшим наличие правосторонней паховой лимфаденопатии, и терапевтом, заподозрившим на основании лабораторного обследования (лейкоцитоз 16×109/л) и рентгенографии органов грудной клетки пневмонию. С этим диагнозом пациентка была госпитализирована в пульмонологическое отделение.
При объективном исследовании: ожирение I ст., отеков нет, цианоза нет, зоны локального ослабления дыхания и хрипы в легких отсутствуют, значительно расширены границы относительной и абсолютной тупости сердца, определяется акцент II тона над легочной артерией, вместо второго тона над верхушкой сердца выслушивается грубый систолический шум, проводящийся в подмышечную впадину. Частота сердечных сокращений 119 в мин, артериальное давление 120/70 мм рт. ст., печень увеличена (15×12×10 см по Курлову).
На ЭКГ: синусовый ритм с одиночными желудочковыми экстрасистолами, блокада правой ножки пучка Гиса.
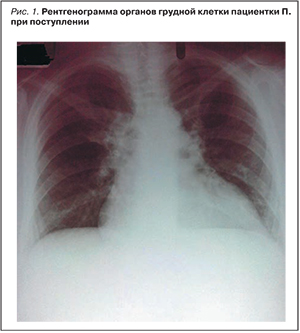
На рентгенограмме грудной клетки обращало на себя внимание значительное расширение тени сердца. При этом явных инфильтративных изменений в ткани легкого не прослеживалось (рис. 1).
Скорость клубочковой фильтрации составляла 71 мл/мин/1,73м2 (по формуле CKD-EPI).
 Диагноз «пневмония» был подвергнут сомнению, заподозрена патология сердца. Проведенная на 3-й день госпитализации эхокардиография показала: полости сердца не расширены, глобальная сократимость удовлетворительная, в полости перикарда жидкость до 250 мл, небольшая легочная гипертензия (систолическое давление в легочной артерии 46 мм рт. ст.), в полости правого желудочка (ПЖ) пристеночный тромб 15×17 мм, уплотнение створок аортального клапана, створки митрального и трикуспидального клапанов не изменены.
Диагноз «пневмония» был подвергнут сомнению, заподозрена патология сердца. Проведенная на 3-й день госпитализации эхокардиография показала: полости сердца не расширены, глобальная сократимость удовлетворительная, в полости перикарда жидкость до 250 мл, небольшая легочная гипертензия (систолическое давление в легочной артерии 46 мм рт. ст.), в полости правого желудочка (ПЖ) пристеночный тромб 15×17 мм, уплотнение створок аортального клапана, створки митрального и трикуспидального клапанов не изменены.
Руководствуясь критериями Джонса (T. Duckett Jones), выработанными более 70 лет назад [4] и не столько пересмотренными, сколько подтвержденными специалистами American Heart Association (AHA) в 1992 г. [5, 6], как основная была принята версия о наличии у пациентки острой ревматической лихорадки: признаки панкардита (большой критерий) сочетались с лихорадкой и повышением скорости оседания эритроцитов (СОЭ; 51 мм/ч), увеличением содержания С-реактивного белка в крови до 205,15 мг/дл (малые критерии).
Следует отметить, что в 2012 г. в Московской области был зарегистрирован 161 случай острой ревматической лихорадки. Наряду с Республикой Татарстан (162 случая) и Чеченской Республикой (154 случая) это один из самых высоких показателей среди субъектов Российской Федерации [7]. Потому диагноз, несмотря на возраст пациентки, имевшей скомпрометированный иммунологический фон, не выглядел маловероятным.
Было начато лечение большими дозами ацетилсалициловой кислоты и антибиотиком пенициллинового ряда, что позволило в течение 2-х сут добиться нормализации температуры тела. Кроме того, были назначены антикоагулянты, β-адреноблокаторы, ингибиторы протонной помпы.
В период временного улучшения продолжала накапливаться информация о состоянии больной. Диагноз «острая ревматическая лихорадка» был ведущим, но не единственным. Нельзя было не провести дифференциальную диагностику с бактериальным эндокардитом. Однако не было выявлено ни одного большого критерия заболевания из предложенных университетом Duke, а из малых в наличии была только лихорадка >38°С [8–11]. Отсутствие кожных проявлений, признаков поражения почек и артрита делало вероятность наличия у пациентки септического артрита, васкулита, системной красной волчанки чрезвычайно малой.
В то же время не находил подтверждения и диагноз «острая ревматическая лихорадка»: уровень антистрептолизина-О, повышенный у 80–85% пациентов с таким заболеванием [5], оказался нормальным, не отмечалось других больших критериев (полиартрит, кольцевидная эритема, хорея Сиденгама, подкожные узелки); более того, на 7-е сут стационарного лечения вновь появилась лихорадка, больная начала предъявлять жалобы на одышку при умеренных физических нагрузках. Эти явления стали показанием для проведения компьютерной томографии органов грудной клетки (КТ ОГК) с болюсным усилением для исключения/подтверждения тромбоэмболии легочной артерии (ТЭЛА). При КТ ОГК, проведенной на 10-й день стационарного лечения, были выявлены «признаки ТЭЛА», подтверждено наличие тромба в полости ПЖ, обнаружены большой очаг деструкции тела VI грудного позвонка, его правого поперечного отростка и прилежащей части VI ребра, множественные мягкотканные образования в плевре и паренхиме легких, внутригрудная лимфаденопатия, а также «гидроперикард с тенденцией к напряженному».
С этого момента диагноз «острая ревматическая лихорадка» потерял актуальность. Коллегиально с кардиохирургом было принято решение воздержаться от пункции полости перикарда ввиду высокого риска осложнений процедуры и кардинально различавшихся данных, полученных при КТ ОГК («гидроперикард с тенденцией к напряженному») и эхокардиографии, результаты которой не позволяли подозревать тампонаду сердца. Фактически имела место лихорадка неясного генеза, соответствовавшая диагностическим критериям, предложенным Petersdorf и Beeson еще в 1961 г. [12] и не потерявшим актуальность по сию пору [13, 14], а также синдром системной воспалительной реакции (ССВР), критерии которого были утверждены в 1992 г. [15]. Такой диагноз, а также наличие очага деструкции в грудном позвонке и множественные мягкотканные образования в легких и плевре заставили продолжить обследование пациентки с онконастороженностью и сменить схему антибактериальной терапии: больная стала получать ванкомицин и гентамицин. Эзофагогастродуоденоскопия, бронхоскопия, ультразвуковое исследование брюшной полости, забрюшинного пространства, органов малого таза не позволили выявить потенциальный источник метастазирования. Предположение о прогрессировании рака вульвы с учетом имевшихся сведений (стадия заболевания II; отсутствие опухолевых клеток в биоптате, полученном при пункции пахового лимфатического узла в июне 2015 г.), а также самого характера опухолевого заболевания, имеющего в целом благоприятный профиль (пятилетняя выживаемость в Западной Европе 64% против 38% при раке яичников) [16], отличающегося крайне низкой склонностью к гематогенному метастазированию (что соответствовало бы стадии IVB, ТхNxM1) [17], демонстрирующего крайне неблагоприятный прогноз лишь с момента двухстороннего метастазировании в паховые лимфатические узлы (стадия IVA, ТхN2M0), также рассматривали, но расценивали как маловероятное.
На 14-й день пребывания пациентки в стационаре лихорадка сменилась гипотермией (35,5–35,9°С). К этому моменту состояние больной значительно ухудшилось за счет нараставшей одышки; частота дыхательных движений в покое достигла 25 в мин, частота сердечных сокращений не снижалась менее 110 в мин, количество лейкоцитов выросло до 24,3×109/л (в дальнейшем, к 20-му дню лечения, их количество выросло до 43,0×109/л).
На 16-й день пребывания в стационаре были выявлены признаки абсцедирования пахового лимфатического узла, 3 мес назад подвергшегося пункционной биопсии. Незамедлительно было выполнено дренирование абсцесса. Казалось, что по законам гнойной хирургии это, наконец, приведет к улучшению состояния пациентки и перелому в течении заболевания. Однако и в дальнейшем состояние больной ухудшалось, что стало окончательным доводом в пользу того, что ССВР имеет неинфекционную природу, что пришлось столкнуться с драматическим прогрессированием опухолевого заболевания, что прогноз — крайне неблагоприятен. На 21-й день пребывания в стационаре при нарастающих явлениях сердечной и дыхательной недостаточности наступила смерть пациентки. Заключительный диагноз был сформулирован следующим образом:
Основной: 1. Прогрессирование неороговевающего плоскоклеточного рака вульвы, отдаленное метастазирование (легкие, позвоночник); 2. Абсцедирующий лимфаденит правой паховой области. Осложнения: Раковая интоксикация. Синдром системной воспалительной реакции. Тромбоз ПЖ, ТЭЛА. Дыхательная недостаточность III ст. Прогрессирующая сердечно-сосудистая недостаточность, отек легких, отек головного мозга.
При аутопсии:
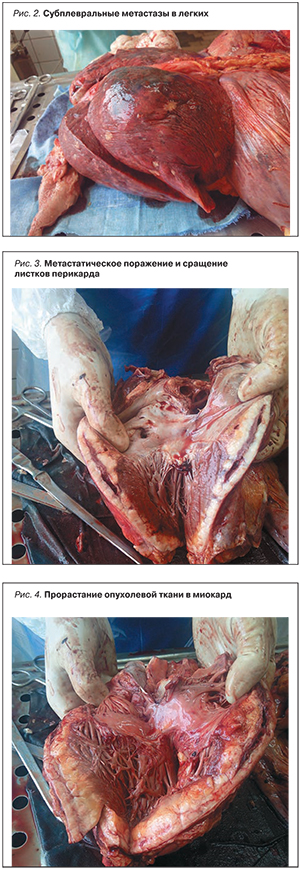
Основной диагноз: Низкодифференцированный (инвазивно растущий плоскоклеточный неороговевающий) рак вульвы. Состояние после комбинированной химиолучевой терапии и хирургического лечения. Множественные метастазы в мягкие ткани правой паховой области (в участках склерозированной соединительной и жировой ткани пласты опухолевых клеток низкодифференцированной раковой опухоли), в грудную клетку с разрушением наружной костной пластинки тела VI ребра справа и тела VI грудного позвонка справа, в лимфатические узлы средостения, под висцеральный листок плевры (рис. 2), в правую почку (единичный), в листки перикарда (толщина разрастания опухолевой метастатической ткани от 10 до 30 мм) (рис. 3, 4); Т2N1M1G3. Осложнения: Венозное полнокровие и дистрофические изменения внутренних органов. Некроз эпителия канальцев почек. Фиксированный к стенке тромб ПЖ (15×10×10 мм). Отек головного мозга. Отек легких. Сопутствующие заболевания: Атеросклероз аорты, сосудов головного мозга, сердца. Хронический бронхит, вне обострения. Диффузный сетчатый пневмосклероз. Хронический пиелонефрит вне обострения. Вскрытие абсцесса правой паховой области. Установлено совпадение клинического и патологоанатомического диагнозов.
В рамках обсуждения описанного случая небезынтересно будет отметить:
- Тромб ПЖ, выявленный при аутопсии, был фиксирован к стенке сердца в месте, где опухолевые разрастания глубоко врастали в миокард и приближались непосредственно к эндокарду. Это было сочтено достаточным основанием для того, чтобы признать причиной образования тромба реактивное воспаление эндокарда (тромбэндокардит). Возможность фиксации тромбоэмбола к стенке желудочка или формирование тромба в полости ПЖ по тому же механизму, который имеет место при тромбозе ушка левого предсердия при мерцательной аритмии, с последующей спонтанной его фиксацией к эндокарду признана крайне маловероятной.
- Аутопсия не подтвердила наличия у пациентки ТЭЛА. Принятые критерии лучевой диагностики ТЭЛА допускают вероятность ложноположительных заключений. В исследовании, посвященном сравнению алгоритмов лучевой диагностики ТЭЛА, приводятся такие данные: чувствительность КТ ОГК составила 91,7%, специфичность 96,4% [18]. В то же время КТ ОГК оказалась достаточно информативной для выявления метастатического поражения легких и плевры. Ультразвуковое исследование почек не показало их метастатического поражения, выявленного в дальнейшем при аутопсии; очевидно, из-за малого размера метастатического очага.
- Посмертно было выявлено обширное поражение мягких тканей правой паховой области опухолевыми разрастаниями. Наиболее вероятно, что не прямое прорастание, а метастатическое поражение регионарных лимфатических узлов с последующим их разрушением и вторичным прорастанием в окружающую клетчатку стало путем распространения опухоли, первичный очаг которой был когда-то удален. Многократные осмотры, пальпация паховой области лечащим врачом, заведующей отделением, двумя хирургами, двумя гинекологами не дали оснований заподозрить такой обширный опухолевый рост в указанной области, т.к. консистенция опухолевых разрастаний не отличалась от плотной жировой клетчатки. Лишь один лимфатический узел, описанный ранее, впоследствии дренированный, вызывал опасения. Возможно, ультразвуковое исследование мягких тканей этой области могло бы способствовать более быстрому установлению диагноза (но вряд ли излечению), но оно, увы, не было выполнено.
И в заключение важно отметить, что рак вульвы – заболевание, которое должно диагностироваться на самых ранних стадиях, т.к. может быть заподозрено при визуальном осмотре. Как разъяснение пользы самопальпации для раннего выявления новообразований молочных желез, о которой можно прочитать на информационных стендах в каждой женской консультации, так и информирование женщин о ранних признаках онкопатологии наружных половых органов для ранней ее диагностики должно быть, на наш взгляд, одной из важных тем санитарно-просветительской работы.


