Диагностика
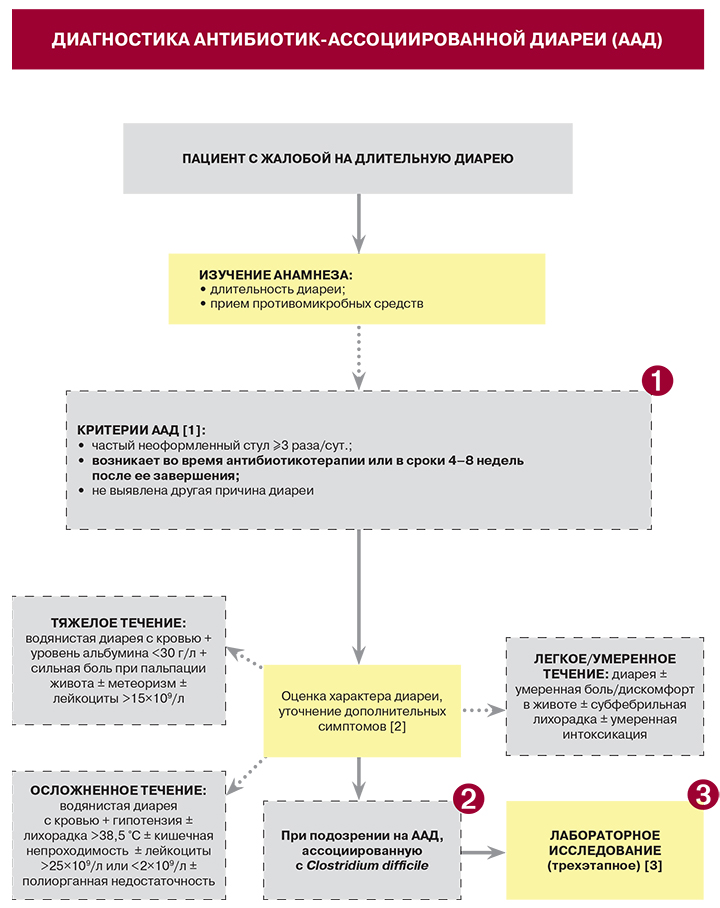
1. • 70–90% случаев антибиотик-ассоциированной диареи (ААД) не связано с Clostridium difficile (по МКБ-10 – неинфекционный гастроэнтерит, или неуточненный колит). На долю Cl. difficile приходится, соответственно, 10–30% случаев заболевания (псевдомембранозный колит, или, в соответствии с МКБ-10, энтероколит, вызванный Cl. difficile) [4, 5].
• Неуточненная ААД и диарея, ассоциированная с Cl. difficile, имеют схожие механизмы происхождения: – избыточный рост условно-патогенной флоры в результате угнетения облигатной интестинальной микрофлоры ЖКТ; – нежелательные эффекты противомикробных средств как таковых (аллергические, токсические, фармакологические), например, местное раздражающее действие в кишечнике; – нарушение метаболизма желчных кислот и углеводов в кишечнике, приводящее к осмотической диарее (в основном характерно для цефалоспоринов) [5, 6].
• Практически все противомикробные средства системного действия, особенно активные против анаэробов, способны провоцировать ААД. При этом согласно проспективному исследованию начала 21 в. с участием 2462 пациентов, повышенный риск ААД был сопряжен с применением цефалоспоринов, пенициллинов и клиндамицина [7].
2. К факторам риска энтероколита, вызванного Cl. difficile, относятся: – прием антибиотиков, длительно задерживающихся в просвете кишечника. Это в основном препараты, выводящиеся с желчью (например, эритромицин, цефтриаксон, линкамицин); – длительные или часто повторяющиеся курсы противомикробных средств, комбинирование нескольких системных антибиотиков; – возраст младше 5 и старше 60 лет; – длительная госпитализация больного в анамнезе, коморбидные заболевания [8–10].
3. • Анализ клинической картины и анамнеза позволяет лишь предположить ААД, ассоциированную с Cl. difficile, но не точно ее идентифицировать.
• Согласно федеральным рекомендациям, лабораторное исследование при подозрении на Cl. difficile должно проводиться в 3 этапа: иммуноферментный анализ (ИФА) образца просветленного кала, далее – ИФА токсинов A и B Cl. difficile, затем – культуральный метод (выделение токсигенной культуры Cl. difficile, определение ее цитотоксичности и чувствительности к противомикробным средствам) [3].
Лечение
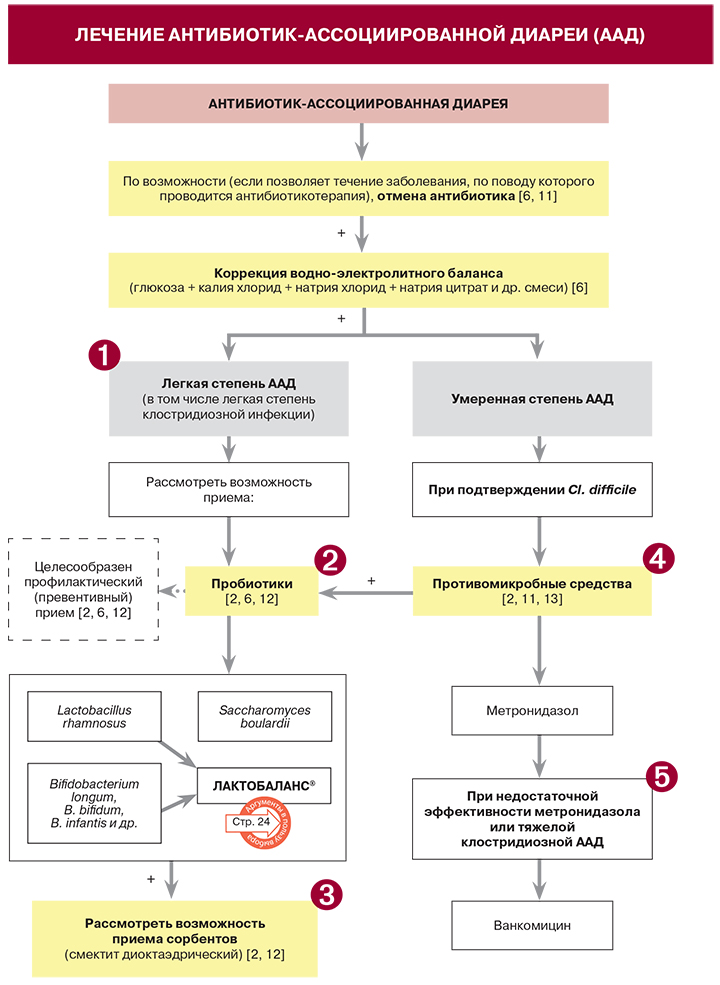
1. В ряде российских клинических гайдлайнов и научных публикаций говорится о том, что при легкой форме антибиотик-ассоциированной диареи (ААД), ассоциированной с Cl. difficile, можно обойтись без назначения специфических «противоклостридийных» антимикробных средств (метронидазол, ванкомицин) [2, 6]. Очевидно, что эта рекомендация относится и к неуточненной ААД. В то же время, если легкая ААД, вызванная Cl. difficile, сопровождается даже незначительным ухудшением состояния в течение 48 ч после отмены антибиотика, российские рекомендации оговаривают необходимость назначения метронидазола [2]. В американских гайдлайнах однозначно сказано о целесообразности приема метронидазола при легкой форме ААД, ассоциированной с Cl. difficile [11].
2. • В европейских и северо-американских рекомендациях по применению пробиотиков при ААД, а также в клинических рекомендациях Ассоциации колопроктологов России по диагностике, лечению и профилактике Cl. difficile-ассоциированной диареи к препаратам с наиболее высоким уровнем доказательности отнесены источники Lactobacillus rhamnosus и Saccharomyces boulardi [12, 13]. В свою очередь рекомендации Российской гастроэнтерологической ассоциации в качестве «эффективного препарата для лечения Cl. difficile-ассоциированной болезни» предлагают рассматривать комбинированный пробиотик, в состав которого входят штаммы Lactobacillus rhamnosus, Bifidobacterium longum, Bifidobacterium bifidum, Bifidobacterium infantis не менее 1×109 КОЕ/г [2].
• Прием пробиотиков оправдан как во время антибиотикотерапии (с учетом устойчивости пробиотических штаммов к антибиотикам), так и после завершения курса лечения Clostridium difficile-ассоциированной болезни метронидазолом или ванкомицином – для профилактики рецидива [2].
3. При использовании в комплексе с метронидазолом/ ванкомицином сорбенты следует принимать не ранее, чем через 1 ч после антибиотиков [2].
4. Стандартная схема приема метронидазола при Cl. difficile-ассоциированной диарее умеренной и легкой степени – 500 мг 3 раза/сут. в течение 10 дней. При неэффективности лечения через 5–7 дней рекомендовано заменить его на ванкомицин. Режим приема ванкомицина – 125 мг 4 раза/сут. на протяжении 10 дней [2, 11].
5. Ванкомицин служит средством первого ряда при тяжелом течении Clostridium difficile-ассоциированной диареи [11, 13]. В рекомендациях Российской гастроэнтерологической ассоциации по диагностике и лечению Clostridium difficile-ассоциированной болезни при тяжелой форме рассматривается комбинированное применение метронидазола и ванкомицина. Также эта комбинация показана при осложненном течении болезни [2].


