Диагностика
1.
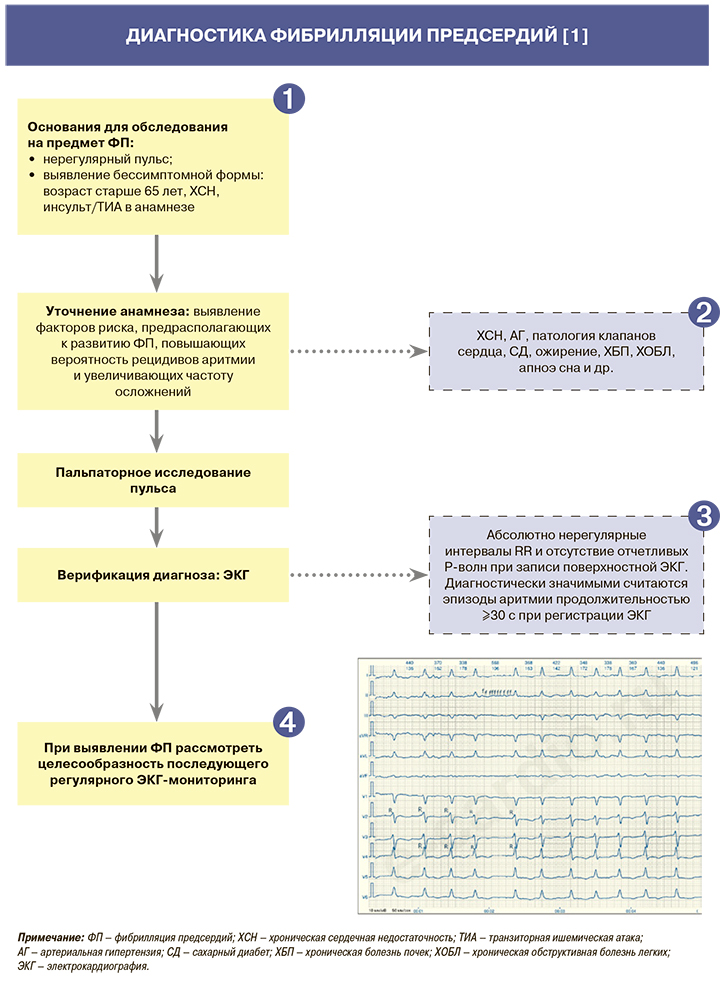
Как правило, фибрилляция предсердий (ФП) может иметь симптомное течение, либо не сопровождаться клиническими проявлениями (асимптомная ФП). Зачастую оба этих варианта сочетаются [1]. Асимптомная ФП особенно распространена в пожилом возрасте, а также у пациентов с хронической сердечной недостаточностью (ХСН) [1].
2.
• ФП развивается у многих больных ХСН, что связано с наличием общих факторов риска и схожими патофизиологическими механизмами, к которым относятся структурное ремоделирование сердца, активация нейрогормональных механизмов и ухудшение функции левого желудочка (ЛЖ) на фоне тахисистолии при ФП. Доказано, что пациенты с сопутствующей ХСН на фоне ФП имеют более неблагоприятный прогноз, включая увеличение смертности, независимо от показателей фракции выброса ЛЖ [1].
• Артериальная гипертензия (АГ) – значимый фактор риска инсульта при ФП. Неконтролируемое высокое артериальное давление (АД) увеличивает вероятность инсульта и геморрагических осложнений и может приводить к рецидивам аритмии. В связи с этим тщательный контроль АД должен быть неотъемлемой частью ведения пациентов с ФП.
• Патология клапанного аппарата сердца независимо ассоциируется с возникновением ФП. Около 30% пациентов с ФП имеют ту или иную форму поражения клапанов сердца, часто выявляемую только при проведении эхокардиографии. ФП ухудшает прогноз у пациентов с тяжелой степенью клапанной патологии. Клапанная болезнь сердца может быть связана с повышенным тромбоэмболическим риском, который, вероятно, также усиливает риск инсульта у больных ФП [1].
• ФП часто сочетается с сахарным диабетом (СД), так как эти заболевания имеют схожие факторы риска. Кроме того, СД увеличивает вероятность развития инсульта и других осложнений, связанных с аритмией. У пациентов с ФП длительный анамнез диабета, по всей видимости, повышает вероятность тромбоэмболических событий, хотя не оказывает влияния на риск кровотечений на фоне приема оральных антикоагулянтов [1].
• Ожирение способствует прогрессивному возрастанию риска развития ФП. К тому же избыточный вес может ассоциироваться с повышением риска ишемического инсульта, тромбоэмболий и смерти у пациентов с ФП [1].
• ФП регистрируется у 15–20% пациентов с хронической болезнью почек (ХБП) [1].
• Установлено, что ФП ассоциирована с синдромом обструктивного апноэ сна. На фоне этого заболевания усиливаются колебания внутригрудного давления, что может оказывать прямое или опосредованное через вагусную активацию влияние, вызывая укорочение потенциала действия миокарда предсердий и индукцию ФП [1].
• Препараты, используемые для снятия бронхоспазма при хронической обструктивной болезни легких (ХОБЛ), особенно теофиллины и агонисты бета-адренорецепторов, могут провоцировать возникновение ФП и затруднять контроль частоты желудочковых сокращений. При этом следует учитывать, что пациенты с ХОБЛ часто имеют сопутствующую предсердную тахикардию, которую необходимо дифференцировать от ФП с помощью ЭКГ-критериев [1].
3.
Типичное истмус-зависимое правопредсердное трепетание имеет характерный паттерн на электрокардиограмме (ЭКГ) и определенную частоту желудочковых сокращений. Распространенность трепетания предсердий примерно в 10 раз меньше, чем ФП, но в то же время эти состояния часто сосуществуют. При типичном трепетании предсердий на поверхностной ЭКГ волны P часто имеют «пилообразную» форму, особенно в нижних отведениях (II, III, aVF). Частота сокращений желудочков при типичном трепетании предсердий может быть различной (обычное соотношение предсердных и желудочковых сокращений от 4:1 до 2:1, в редких случаях 1:1), однако иногда стабильное проведение 2:1 может наблюдаться при других формах тахикардий по типу macro re-entry, которые могут остаться не диагностированными. Таким образом, вагусная стимуляция или внутривенное введение аденозина могут быть полезны для верификации трепетания предсердий. Левопредсердное или правопредсердное атипичное трепетание предсердий встречаются главным образом у пациентов после катетерной аблации или хирургического лечения ФП, а также после открытых кардиохирургических вмешательств [1].
4.
• После верификации диагноза ФП последующий ЭКГ-мониторинг может быть полезен в следующих ситуациях:
– для оценки динамики клинического статуса или выявления новых симптомов;
– при подозрении на прогрессирование ФП;
– для оценки влияния лекарственной терапии на частоту желудочковых сокращений;
– для мониторинга эффективности контроля ритма с помощью антиаритмических препаратов или катетерной аблации [1].
• Рекомендации по скринингу ФП приведены в таблице 1.

Лечение

1.
• Уровень заболеваемости инсультом у пациентов с фибрилляцией предсердий (ФП) значительно выше, чем при других сердечно-сосудистых патологиях. Так, по современным данным, у 20–30% пациентов с ишемическим инсультом выявляется ФП в анамнезе, а также остром периоде либо после выписки из стационара [1].
• Помимо профилактики инсульта, комплексная терапия ФП включает следующие направления [1]:
– контроль сопутствующих заболеваний (ожирения, артериальной гипертензии, хронической сердечной недостаточности, ишемической болезни сердца, сахарного диабета, клапанных пороков сердца, хронической обструктивной болезни легких, апноэ сна);
– контроль частоты сердечных сокращений (ЧСС);
– контроль ритма;
– обучение пациентов, формирование у них высокого комплаенса и навыков самоконтроля.
2.
• Принципы использования шкалы CHA2DS2-VASc, которая имеет наиболее высокий класс рекомендаций и уровень доказательности (IA) по прогнозированию риска инсульта и кровотечений при ФП [1], приведены в таблице 2.

• По сравнению с главными факторами риска инсульта при ФП, отраженными в таблице 1, меньшим доказанным влиянием на вероятность развития этого осложнения обладают:
– лабильное международное нормализованное отношение (МНО) и низкий процент времени нахождения его в терапевтическом диапазоне (TДВ) у пациентов, принимающих варфарин (антагонист витамина K);
– перенесенное кровотечение или анемия;
– избыточное употребление алкоголя и другие признаки плохой приверженности к терапии;
– сопутствующая хроническая болезнь почек (ХБП);
– повышенный уровень высокочувствительного тропонина и N-концевого натрийуретического пептида pro-B-типа.
3.
• В настоящее время доказано, что терапия оральными антикоагулянтами может предотвращать большинство ишемических инсультов у пациентов с ФП и способствует увеличению продолжительности жизни. Такой подход превосходит по эффективности терапию низкими дозами ацетилсалициловой кислоты или отсутствие приема антикоагулянтов у пациентов с различными факторами риска инсульта [1].
• Несмотря на убедительные доказательства эффективности оральных антикоагулянтов, до сих пор распространены ситуации их неназначения, неадекватного дозирования либо досрочного прекращения терапии. Самыми распространенными причинами для отмены антикоагулянтов становятся геморрагические осложнения (как тяжелые, так и незначительные), предполагаемый «высокий риск» кровотечений, а также неудобство лабораторного контроля и подбора дозы на фоне приема варфарина [1]. Тем не менее значительный риск инсульта в отсутствие приема оральных антикоагулянтов часто превышает риск кровотечения на фоне терапии этой группы препаратов, даже у пожилых и ослабленных пациентов, а также у людей с когнитивными нарушениями [1]. Риск кровотечений при приеме ацетилсалициловой кислоты не отличается от риска кровотечений на фоне приема варфарина или «новых» оральных антикоагулянтов, не являющихся антагонистами витамина K (НОАК) [1]. При этом, в отличие от ацетилсалициловой кислоты, оральные антикоагулянты эффективно предотвращают инсульты у пациентов с ФП [1].
• Контролируемые исследования, изучающие прием оральных антикоагулянтов у пациентов с ФП и повышенным риском развития инсульта, демонстрируют убедительные доказательства преимущества такой терапии при высоком количестве баллов по шкале CHA2DS2-VASc (≥2 баллов для мужчин и ≥3 баллов для женщин) [1]. В настоящее время идет накопление доказательной базы в отношении риска тромбоэмболических осложнений у пациентов с одним клиническим фактором риска инсульта (т.е. 1 балл для мужчин и 2 балла для женщин по CHA2DS2-VASc), хотя результаты и выводы во многом зависят от реальных показателей распространенности инсульта у пациентов, не получающих оральные антикоагулянты. Тем не менее получилось продемонстрировать клиническое преимущество антикоагулянтной терапии в группе больных с низким количеством баллов по шкале CHA2DS2-VASc [1].
• Частота инсультов и тромбоэмболий у больных ФП значительно различается при наличии 1 или ≥2 баллов, что обусловлено неоднородностью популяции пациентов, неодинаковым коагуляционным статусом и разными потенциальными исходами заболевания [1]. В случае с мужчинами и женщинами, имеющими один дополнительный фактор риска инсульта, назначение оральных антикоагулянтов следует рассматривать, исходя из ожидаемой эффективности в плане профилактики тромбоэмболий и кровотечений с учетом предпочтений больного. Важным является факт прогрессивного увеличения риска инсульта с возрастом (65 лет и старше), что также может усиливать негативное влияние других факторов риска (женский пол, хроническая сердечная недостаточность). Однако доказано, что при отсутствии других факторов риска инсульта женский пол не увеличивает вероятность этого сердечно-сосудистого события. Следовательно, при решении вопроса о назначении антикоагулянтной терапии пациентам только с одним ФР по шкале CHA2DS2- VASc (помимо женского пола) необходимо проводить индивидуализированную оценку вероятности осложнений, принимая во внимание выбор пациента [1].
4.
• В процессе антитромботической терапии необходима коррекция факторов риска кровотечений. При оценке риска кровотечения на фоне приема оральных антикоагулянтов следует иметь в виду, что некоторые соответствующие шкалы разработаны главным образом для пациентов, получающих терапию антагонистами витамина K. К таким шкалам, в частности, относится HAS-BLED (по 1 баллу за каждый фактор риска) (табл. 3).
• Прогнозируемый высокий риск кровотечений (≥3 баллов по HAS-BLED), как правило, не должен быть причиной для отказа от терапии ОАК [1, 2]. Скорее, необходимы выявление и модификация потенциально корригируемых факторов риска [1, 2].

5.
• НОАК, в отличие от антагонистов витамина K (варфарина), обладают предсказуемым эффектом (срок начала и пика действия) без необходимости регулярного мониторинга антикоагуляции. Испытания III фазы с участием НОАК были проведены с соблюдением необходимых этих препаратов, рекомендованных к рутинному использованию на практике [1].
• В исследовании ARISTOTLE [4] прямой ингибитор Ха фактора апиксабан в дозе 5 мг 2 раза/сут снижал угрозу развития инсульта или системной эмболии на 21% в сравнении с варфарином, плюс уменьшал риск больших кровотечений на 31% и снижал смертность от всех причин на 11% (статистически достоверные различия). Процент возникновения геморрагического инсульта и внутричерепного кровоизлияния, но не ишемического инсульта, также был ниже при приеме апиксабана. При этом частота гастродуоденальных кровотечений между группами исследования не отличалась.
• Апиксабан – единственный НОАК, который сравнивался с ацетилсалициловой кислотой у пациентов с ФП. Получены данные о существенном (на 55%) снижении риска инсульта или системных эмболий на 55% на фоне апиксабана с отсутствием или небольшим различием в плане количества эпизодов большого кровотечения или внутричерепного кровоизлияния [5].
• В исследовании RE-LY [6] прямой ингибитор тромбина дабигатрана этексилат в дозе 150 мг 2 раза/сут снижал развитие инсульта и системной эмболии на 35% в сравнении с варфарином без значимых различий по числу больших кровотечений. В дозе 110 мг 2 раза/сут этот НОАК не превосходил варфарин в предотвращении развития инсульта и системной эмболии, но на 20% снижал риск развития крупных кровотечений. Обе дозы дабигатрана этексилата существенно уменьшали частоту геморрагического инсульта и внутричерепного кровоизлияния. Препарат в дозе 150 мг 2 раза/сут значимо снижал вероятность развития ишемического инсульта (на 24%) и сосудистой смертности (на 12%), однако угроза желудочно-кишечных кровотечений при этом возрастала на 50%. При использовании обеих дозировок дабигатрана этексилата отмечалось недостоверное повышение частоты развития инфаркта миокарда, которое не было подтверждено в последующих крупных метаанализах [1]. Эти данные также подтвердили превосходство дабигатрана этексилата над варфарином, впервые продемонстрированное в исследовании RE-LY, у пациентов, которые, как правило, принимали полную дозу препарата (150 мг 2 раза/сут).
• Эффективность и безопасность приема прямого ингибитора Ха фактора ривароксабана в дозе 20 мг 1 раз/сут в сравнении с варфарином оценивалась в исследовании ROCKET-AF [7]. Доза ривароксабана была снижена до 15 мг ежедневно при уменьшении клиренса креатинина до 30–49 мл/мин по формуле Кокрофта–Голта. Ривароксабан был не хуже варфарина в профилактике инсульта и системных эмболий: он способствовал статистически значимому снижению их уровня на 21% относительно препарата сравнения. Тем не менее ривароксабан не снижал смертность, не изменял частоту развития ишемического инсульта или большого кровотечения в сравнении с варфарином. Кроме того, отмечалось увеличение общего количества желудочно-кишечных кровотечений, но число геморрагических инсультов и внутричерепных кровоизлияний на ривароксабане значимо снижалось в сравнении с варфарином.
• В исследовании ENGAGE AF TIMI 48 [8] прямой ингибитор Ха фактора эдоксабан в дозах 60 мг 1 раз/сут и 30 мг 1 раз/сут (с уменьшением дозы у определенных категорий пациентов) сравнивался с подобранной эффективной дозой варфарина. Эдоксабан в дозе 60 мг 1 раз/сут не уступал варфарину и значительно снижал вероятность развития инсультов и системных эмболий (на 21%), а также больших кровотечений (на 20%). В дозе 30 мг 1 раз/сут препарат также был эффективен в плане профилактики инсульта и системной эмболии, при этом частота больших кровотечений уменьшалась на 53%. Показатели сердечно-сосудистой смертности были ниже у всех пациентов, получающих эдоксабан, в сравнении с результатами терапии варфарином. Согласно решению большинства экспертных ассоциаций, только полная доза эдоксабана (60 мг) была одобрена для профилактики инсульта при ФП.
• Режим коррекции доз НОАК у определенных категорий пациентов представлен в таблице 4.

• Данные метаанализа наиболее крупных исследований, в которых сравнивалась терапия варфарином (29 272 пациента) и НОАК (42 411 пациентов) в полных дозах, продемонстрировали лучшую эффективность НОАК в плане снижения риска инсульта и системных эмболий на 19% (относительный риск (ОР) 0,81; 95% доверительный интервал (ДИ) 0,73–0,91; p <0,0001). Такой результат главным образом был достигнут за счет сокращения частоты геморрагического инсульта (ОР 0,49; 95% ДИ 0,38–0,64; p <0,0001). У пациентов, рандомизированных в группу терапии НОАК, смертность была на 10% ниже (ОР 0,90; 95% ДИ 0,85–0,95; p=0,0003), внутричерепные кровоизлияния сократились в 2 раза (ОР 0,48; 95% ДИ 0,39–0,59; p <0,0001), однако желудочно-кишечные кровотечения встречались чаще (ОР 1,25; 95% ДИ 1,01–1,55; p=0,04). Снижение количества инсультов при приеме НОАК наблюдалось во всех оцениваемых подгруппах, хотя возможно было предположить относительное уменьшение риска кровотечений на НОАК в центрах с неудовлетворительным контролем МНО (р=0,022). Тем не менее существенное снижение частоты внутричерепных кровоизлияний при приеме НОАК в сравнении с варфарином действительно доказано независимо от качества контроля МНО [1].
6.
Терапия антагонистами витамина K (варфарином) снижает риск инсульта на 60%, а смертность на 25% в сравнении с контрольной группой (терапия ацетилсалициловой кислотой или отсутствие терапии). Применение варфарина ограничено узким терапевтическим диапазоном, необходимостью частого мониторинга и коррекции дозы, но при достаточном ТДВ антагонисты витамина K эффективны для профилактики инсульта у пациентов с ФП. Пациенты, которые достигают эффективных результатов при лечении варфарином, имеют в среднем более высокий показатель ТДВ, чем пациенты с худшим ответом на терапию [1].
7.
Для больных ФП с ревматическим поражением митрального клапана и/или механическими протезами в настоящее время единственным методом лечения с доказанной безопасностью служит терапия антагонистами витамина K [1].


