Диагностика
1.
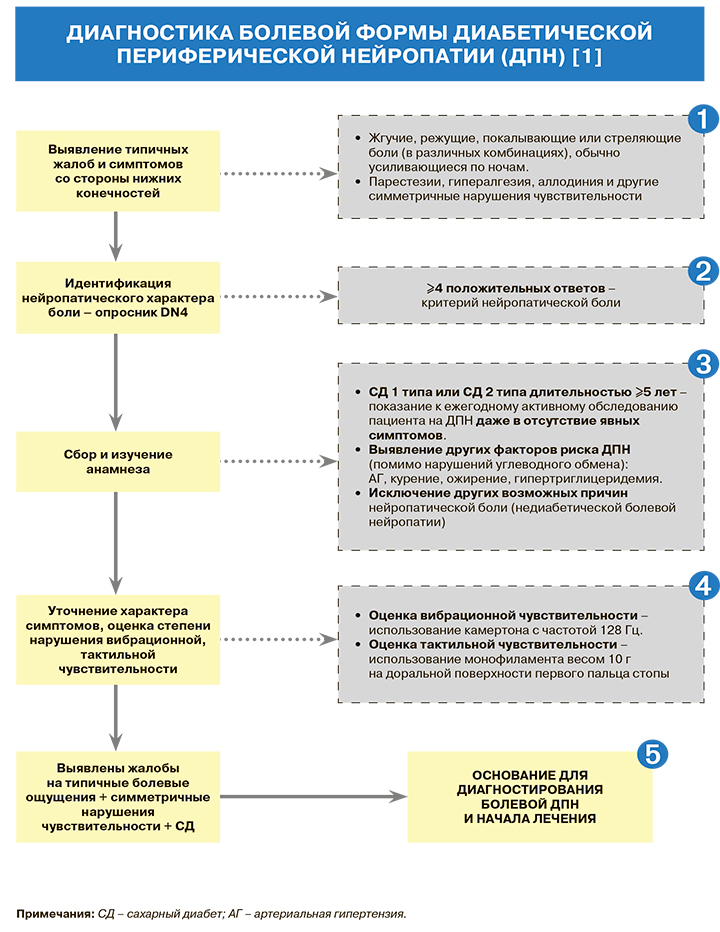
• Нейропатическая боль (табл. 1) может быть первым симптомом, побуждающим пациента обратиться к врачу, и присутствует почти у 25% лиц с диабетической периферической нейропатией (ДПН) [1–4]. Она может сопровождаться повышением ответа на болевые стимулы (гипералгезия) и болями, провоцируемыми контактом (аллодиния) [1].

• Симптомы ДПН могут варьировать в зависимости от того, какой класс волокон вовлечен в патологический процесс. Наиболее частые ранние симптомы, вызванными вовлечением волокон малого диаметра – боль и дизестезии [1, 5–7].
• О вовлечении в патологический процесс волокон большого диаметра может свидетельствовать чувство онемения, покалывания без болевого синдрома и утраты протективной чувствительности. Потеря протективной чувствительности – фактор риска образования диабетических язв стопы. Пациенты при этом часто описывают свои ощущения так, как будто стопа обернута шерстью или одета в толстые носки. Это свидетельствует о потере способности чувствовать боль и позволяет пациентам с нейропатическими язвами подошвенной поверхности стопы ходить при наличии повреждений, что приводит к хронизации процесса, зачастую осложняющегося инфекцией [1, 8].
• В зоне боли у пациентов с ДПН могут наблюдаться трофические изменения кожи, подкожной клетчатки, волос, ногтей, нарушение мышечного тонуса или локальные вегетативные расстройства, связанные с одновременным поражением вегетативных волокон в составе периферических нервов [1].
2.
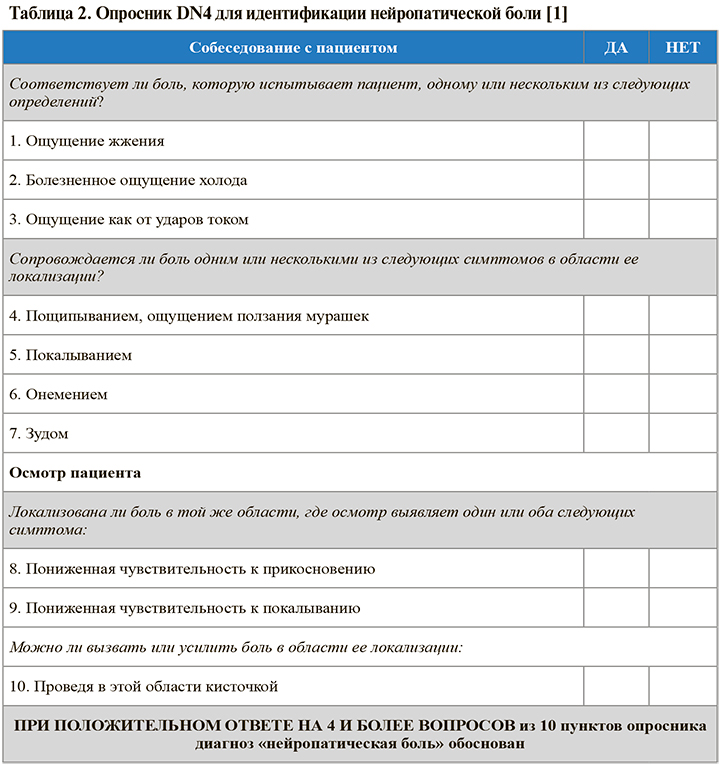
Структура опросника DN4, который в настоящее время считается одним из самых чувствительных в плане выявления нейропатической боли (чувствительность 80%), приведен в таблице 2.
3.
• Больные сахарным диабетом (СД) могут сами не предъявлять жалоб, однако при активном опросе указывают на онемение или другие симптомы ДПН. Выявление болевой ДПН у пациентов с СД должно носить активный характер и быть неотъемлемой частью сбора жалоб и анамнеза с уточнением наличия и характера боли. Всем пациентам необходимо выполнять оценку признаков и симптомов ДПН на момент установления диагноза СД 2 типа и каждые 5 лет после установления диагноза СД 1 типа с последующим ежегодным обследованием (уровень доказанности B) [1].
• Рассмотреть обследование пациента на предмет ДПН следует также у пациентов с предиабетом (нарушение толерантности к глюкозе, нарушенная гликемия натощак) при наличии симптомов периферической нейропатии (уровень доказанности B) [1].
• Повышение вероятности ДПН при наличии артериальной гипертонии (относительный риск [ОР] 1,5), большой длительности СД (ОР 1,4), гипергликемии и ее колебаниях (ОР 1,4 и 1,3 соответственно), курении (ОР 1,3), ожирении (ОР 1,2) и гипертриглицеридемии (ОР 1,2) было установлено в исследовании осложнений при СД 1 типа (Eurodiab) [1, 9].
• Болевая ДПН – диагноз исключения. У больных СД могут иметься и недиабетические болевые нейропатии, этиопатогенез которых не связан с СД [1, 34]. К возможным этиологическим факторам недиабетических болевых нейропатий относятся [1]:
– интоксикации (чаще всего злоупотребление алкоголем, реже отравление свинцом, ртутью);
– онкологические заболевания (бронхогенный рак легкого и др.);
– инфекции (ВИЧ, герпес и др.);
– дефицит витаминов В12, В6 и В1, амилоидоз, применение некоторых лекарств средств (изониазида, алкалоидов барвинка, противоопухолевых средств, антиретровирусных препаратов).
Большинство этих причинных факторов несложно установить или предположить путем тщательного сбора анамнеза и диагностики сопутствующих заболеваний у конкретного пациента [1].
• В рутинной клинической практике часто приходится дифференцировать болевой синдром, обусловленный ДПН, от болей в ногах, вызванных другой патологией. Как правило, больной СД на приеме предъявляет жалобы просто на «боли в ногах», не конкретизируя их. В таблице 3 представлены заболевания, сопровождающиеся болями в ногах и часто встречающиеся у больных СД. При этом следует помнить: диагностическая задача усложняется тем, что у многих больных СД встречается сочетание указанных в таблице видов патологии, например, чаще всего комбинация нейропатического и ишемическогохарактера поражения нижних конечностей. Тем не менее детальный расспрос и внимательное физикальное обследование и здесь помогают дифференцировать нейропатический и ишемический компонент болевого синдрома [1].
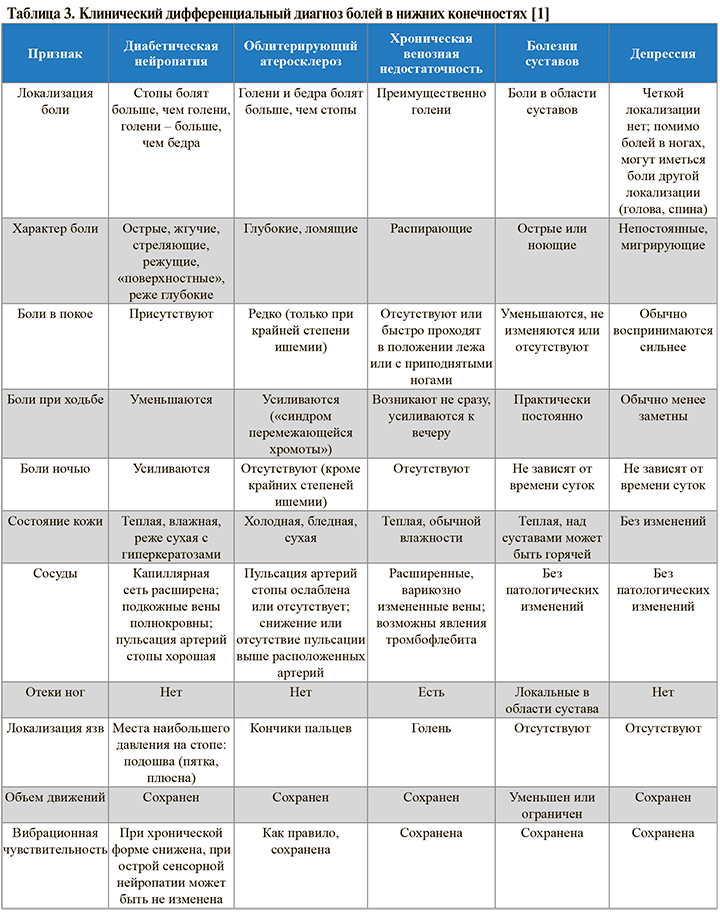
• При дифференциальной диагностике особенно важна высокая настороженность практических врачей в отношении депрессивных расстройств как возможной причины болевого синдрома. Распространенность депрессии у больных СД достигает 20–30%, при этом главными жалобами 45–95% пациентов выступают различного рода соматические, включая болевые, синдромы, в частности боли в ногах [1].
4.
• Оценка симптомов ДПН, наряду с тщательным сбором анамнеза и исследования температурной/болевой чувствительности, должна включать определение вибрационной чувствительности с использованием камертона 128 Гц (уровень доказанности B). Вибрационная чувствительность при ДПН, как правило, нарушается раньше, чем тактильная, болевая, позиционная и температурная, и гораздо раньше, чем появляются моторные симптомы в виде мышечной слабости. Снижение вибрационной чувствительности ниже возрастной границы нормы служит надежным, простым и удобным скрининговым тестом для диагностики ДПН. В ряде случаев, особенно при СД 2 типа, нарушение вибрационной чувствительности идет параллельно с повышением порогов к термическим раздражителям; такие пациенты нередко получают ожоги при «распаривании» ног, так как они не чувствуют высокой температуры воды [1].
• Всем пациентам необходимо выполнять ежегодное исследование с использованием монофиламента весом 10 г для оценки риска развития язв стопы и ампутации (уровень доказанности B). Тест с монофиламентом 10 г, включенный в программу ежегодного скрининга и диагностики ДПН, отличается от теста для диагностики «стопы высокого риска» в плане развития язв – позднего осложнения ДПН и требует исследования четырех областей (головки I, III и V плюсневых костей и подошвенная поверхность дистального сегмента большого пальца стопы) на каждой стопе [1, 10].
• Более тонкие методы оценки различных видов чувствительности могут быть использованы у пациентов с нейропатической болью, когда поражение трудно выявить по данным клинического обследования, для исключения других причин боли и изучения механизмов развития болевого синдрома. Как правило, для диагностики в повседневной клинической практике они не требуются [1].
5.
• В целом диагноз ДПН и болевой ДПН является преимущественно клиническим. Сочетания типичных жалоб на болевые ощущения и симметричных нарушений чувствительности обычно достаточно для постановки диагноза. У пациента с СД эти симптомы с большой степенью вероятности свидетельствуют о ДПН и могут не требовать дополнительного обследования или направления к специалисту [1].
• Электрофизиологическое исследование или направление к неврологу редко показано на этапе скрининга, за исключением ситуаций атипичных клинических признаков, неясного диагноза или подозрения на иную этиологию заболевания (уровень доказанности B). Атипичные признаки включают большую выраженность моторной нейропатии по сравнению с сенсорной, быстрое начало или асимметричную выраженность симптомов [1].
Лечение

1.
Полное купирование болевого синдрома при болевой ДПН не всегда достижимо, поэтому хорошим результатом лечения считается уменьшение его выраженности на 50% по визуальной аналоговой шкале (ВАШ), а удовлетворительным – на 30%. После уменьшения интенсивности болевого синдрома обычно достигается основная цель лечения – восстановление или улучшение функционирования больного и его качества жизни [1].
2.
• При выборе препаратов для обезболивания у пациентов с болевой ДПН следует исходить из следующих факторов [1]:
– доказанной эффективности при этом заболевании;
– переносимости с учетом профиля пациента;
– возраста пациента;
– сопутствующих заболеваний;
– сопутствующей медикаментозной терапии;
– стоимости лечения и предпочтений пациента.
• К первой линии терапии болевой ДПН относятся препараты с наиболее доказанной эффективностью и наилучшим соотношением эффективности и безопасности/переносимости [1]. Рекомендации по выбору препаратов для начальной терапии болевой ДПН приведены в таблице 4.

• При назначении каждого препарата следует придерживаться следующих правил [1]:
– постепенное увеличение (титрование) дозы для лучшей переносимости и выбора минимальной эффективной дозы;
– делать вывод о неэффективности того или иного препарата можно только при его приеме в максимальной переносимой дозе в течение времени, строго определенного для каждого препарата («продолжительность тестовой терапии»);
– отмену препаратов в большинстве случаев также желательно производить путем постепенного снижения дозы во избежание развития синдрома отмены и других побочных эффектов. Данное правило неприменимо к тем случаям, когда препарат отменяют из-за аллергических реакций или других тяжелых и серьезных побочных эффектов.
3.
• Габапентин – первый габапентиноид, внедренный в клиническую практику. Он продемонстрировал эффективность в многочисленных клинических исследованиях лечения боли при ДСПН. NNT1 габапентина равняется 3–7, т.е. как минимум удовлетворительный обезболивающий эффект (на 30–50%) достигается у 1 из 3–7 пациентов [1, 11].
• Наряду с обезболивающим действием, габапентин обладает противотревожным и седативным эффектом. Это может быть немаловажным в связи с тем, что патологическая тревога нередко сопутствует болевому синдрому при ДПН [1].
• Режим дозирования габапентина: начальная доза 300 мг 1 раз/сут, на 2-й день – 300 мг 2 раза/сут, на 3-й – 300 мг 3 раза/сут. В дальнейшем дозу постепенно увеличивают до достижения эффекта, вплоть до 1800–3600 мг/сут [1].
• Минимальная продолжительность тестовой терапии габапентином составляет от 3 до 8 нед титрования дозы, плюс не менее 2 нед приема в максимальной переносимой дозе.
• Габапентин относится к препаратам первой линии для симптоматического лечения болевой ДПН при большинстве сопутствующих заболеваний (табл. 5).

• Основные противопоказания к приему габапентина включают повышенную чувствительность к препарату, беременность и лактацию, возраст до 17 лет. Лекарственные взаимодействия габапентина с другими препаратами практически отсутствуют [1].
• Прегабалин – самый изученный при болевой ДПН препарат с обезболивающим эффектом, доказанным в большинстве исследований. Около 50% больных с этим заболеванием отмечают уменьшение боли на 50% и более на суточной дозе прегабалина 300 мг, а на дозе 600 мг/сут почти у 30% пациентов отмечается уменьшение болевого синдрома на 70% и более. Как правило, улучшение появляется уже в первую неделю лечения. NNT прегабалина равняется 3–8 [1, 11].
• Прегабалин, подлежащий предметно-количественному учету, имеет смысл назначать и тем пациентам, которые не ответили или недостаточно ответили на терапию габапентином или трициклическими антидепрессантами (ТЦА): у таких больных через 6 мес лечения прегабалином отмечается дополнительное уменьшение болевого синдрома примерно на 25% [1].
• Помимо обезболивающего действия, прегабалин вызывает стойкое улучшение сна и уменьшение хронической патологической тревоги [1].
• Режим дозирования прегабалина: начальная доза: 25–75 мг 1–2 раза/сут, с 3-го по 7-й день – по 150 мг 2 раза/сут, далее при необходимости по 300 мг 2 раза/сут [1]
• Минимальная продолжительность тестовой терапии прегабалином: 2–4 нед в максимальной переносимой дозе [1].
• Основные противопоказания к прегабалину, как и в случае габапентина, – повышенная чувствительность к препарату, беременность и лактация, возраст до 17 лет. При приеме препарата с седативными средствами возможно усиление эффекта последних. В первый или второй день лечения прегабалином у 21–46% больных возникают головокружения, у 14–46% – сонливость. Эти нежелательные явления проходят через 6–17 и 26–31 день соответственно, о чем заранее следует предупредить пациента [1].
4.
• В многоцентровых рандомизированных исследованиях была продемонстрирована эффективность селективного ингибитора обратного захвата серотонина и норадреналина дулоксетина в дозах 60–120 мг/сут в лечении болевой ДПН. NNT этого лекарственного средства составляет 1,7–7 [1, 11].
• Наряду с обезболивающим действием, дулоксетин проявляет антидепрессивный эффект, вызывает доказанное улучшение качества жизни, нарушенного в связи с болевой ДПН. При этом обезболивающий эффект препарата не зависит от антидепрессивного [1].
• Режим дозирования дулоксетина: начальная доза – 60 мг 1 раз/сут, эффективные обезболивающие дозы – 60 и 90 мг 1 раз/сут и 120 мг/сут в 2 приема. В связи с тем что в первые 1–2 нед приема дозы 60 мг у некоторых пациентов может появляться тревога, которая проявляется нарушением сна, тахикардией или легкой тошнотой («норадреналиновые эффекты»), можно начинать прием дулоксетина с 30 мг/сут с увеличением дозы до 60 мг через неделю. Альтернативой является прием комбинации 60 мг дулоксетина с небольшими дозами любого противотревожного препарата. Через 2–3 нед противотревожный препарат отменяют, а прием дулоксетина продолжают [1].
• Минимальная продолжительность тестовой терапии дулоксетином: не менее 4 нед в максимальной переносимой дозе. У большинства пациентов уменьшение болевого синдрома отмечается уже в первые дни приема препарата [1].
• Основные противопоказания к применению дулоксетина – повышенная чувствительность к препарату, лактация, декомпенсированная закрытоугольная глаукома. Одновременный прием препарата с потенциальными ингибиторами CYP1A2 (фторхинолоны) требует осторожности и снижения его доз. Не рекомендуется совместное использование дулоксетина с трициклическими антидепрессантами (ТЦА) и ингибиторами моноаминооксидазы [1].
• Другие зарегистрированные в России селективные ингибиторы обратного захвата серотонина и норадреналина, в отличие от дулоксетина, не содержат болевую ДПН среди показаний к применению в официальных инструкциях [12].
5.
• В нескольких рандомизированных слепых плацебо-контролируемых клинических исследованиях было показано значительное уменьшение выраженности нейропатической боли при приеме ТЦА. Вместе с тем последний Кокрановский обзор поставил под сомнение качество результатов исследований амитриптилина, указав на небольшие размеры выборки в большинстве случаев, и заключил, что в действительности нет ни убедительных доказательств положительного влияния амитриптилина на выраженность болевого синдрома при ДПН, ни доказательств отсутствия эффекта [1, 13]. И все же большой практический опыт применения ТЦА для лечения боли позволяет использовать эти препараты при болевой ДПН. NNT амитриптилина составляет 1,3–4 [1, 11].
• Помимо обезболивания, амитриптилин обладает антидепрессивным и противотревожным действием, способностью улучшать сон. Обезболивающий эффект ТЦА не зависит от антидепрессивного [1].
• Режим дозирования амитриптилина: начальная доза 5–10 мг/сут в 2 приема. При хорошей переносимости через 3–4 дня дозу увеличивают до 10–25 мг в 2 приема, дальнейшее увеличение проводится 1 раз в 10–14 дней до достижения терапевтической дозы 50–150 мг/сут в 2–3 приема [1].
• При выборе дозировки амитриптилина следует избегать следующих часто встречающихся ошибок [1]:
– назначения более высоких начальных доз или более быстрого увеличения дозы. Это может привести к отказу больного от дальнейшего приема препарата из-за побочных эффектов;
– назначения слишком малых доз амитриптилина (2,5–25 мг/сут), которые не купируют болевой синдром и вынуждают пациентов прекращать терапию из-за мнимой ее неэффективности.
• Минимальная продолжительность тестовой терапии амитриптилином: не менее 3 нед в максимальной переносимой дозе.
• Круг основных противопоказаний к приему амитриптилина довольно широк: острый и ранний восстановительный период после инфаркта миокарда, острая алкогольная интоксикация, острая интоксикация снотворными, анальгезирующими и психотропными лекарственными средствами, закрытоугольная глаукома, нарушения ритма и проводимости сердца, удлинение интервала QT на электрокардиограмме (ЭКГ), одновременный прием препаратов, удлиняющих интервал QT на ЭКГ, лактация, повышенная чувствительность к амитриптилину, гипертрофия предстательной железы.
• Из-за возможных нежелательных лекарственных взаимодействий аитриптилин не следует сочетать с препаратами, оказывающими угнетающее влияние на ЦНС, холинолитиками, симпатомиметиками, ингибиторами МАО, селективными ингибиторами обратного захвата серотонина (СИОЗС), этанолом. При совместном использовании амитриптилина с нейролептиками взаимно угнетается метаболизм, при этом происходит снижение порога судорожной готовности. При одновременном применении с антигипертензивными средствами (за исключением клонидина, гуанетидина и их производных) возможно усиление антигипертензивного действия и риска развития ортостатической гипотензии, при сочетании с карбамазепином – снижение эффекта амитриптилина вследствие повышения его метаболизма.
• Требуется крайняя осторожность при назначении амитриптилина больным старческого возраста (плохая переносимость). Препаратами первой линии для данной группы пациентов служат габапентин, прегабалин, реже дулоксетин. При этом нужно учитывать, что их побочные эффекты могут быть наиболее выражены именно в старческом возрасте; степень нежелательных явлений можно уменьшить за счет назначения меньших начальных доз препаратов и более медленного титрования [1].
• Следует иметь в виду, что большинство торговых наименований амитриптилина, зарегистрированных в России, имеют среди показаний в официальных инструкциях лишь депрессии. Только у отдельных препаратов в списке показаний содержится хронический болевой синдром (в том числе неврогенного характера) [12].
• Из других ТЦА, представленных в России, аналогичное показание присутствует в инструкциях к большинству препаратов кломипрамина. Доза этого средства подбирается индивидуально (10–150 мг/сут при пероральном приеме) с учетом сопутствующего приема обезболивающих препаратов [12].
6.
Рекомендации по оптимальному сочетанию препаратов для лечения болевой ДПН в случае неэффективности монотерапии и в отношении тех комбинаций, которых нужно избегать, отражены в таблице 6.

7.
• Трамадол – «мягкий» опиоидный анальгетик центрального действия, который может назначаться в качестве препарата 3-й линии терапии при болевой ДПН. Он обладает меньшим потенциалом развития зависимости и злоупотребления, чем другие опиоиды. Тем не менее трамадол следует использовать лишь в том случае, если все возможности обезболивания с помощью антиконвульсантовгабапетиноидов и антидепрессантов полностью исчерпаны. NNT препарата равняется 3–6 [1, 11].
• Режим дозирования трамадола: начальная доза 50 мг 1–2 раза/сут, с постепенным увеличением при необходимости до 100 мг 2–4 раза/сут. У пациентов старше 75 лет высшая суточная доза не должна превышать 300 мг в связи с риском нарушения сознания (спутанность) [1].
• Минимальная продолжительность тестовой терапии трамадолом: 4 нед приема максимальной переносимой дозы [1].
• Противопоказания к применению трамадола: повышенная чувствительность к препарату, острая интоксикация алкоголем и препаратами, оказывающими угнетающее влияние на ЦНС. Препарат не следует комбинировать с антидепрессантами, действующими на серотонин (группы СИОЗС, СИОЗСН, ТЦА), и ингибиторами МАО (опасность развития серотонинового синдрома) [1].
• К другим опиоидам, которые могут быть назначены в качестве 3-й линии терапии при болевой ДПН, относится тапентадол. Однако доказательная база по его эффективности тапентадола при нейропатической боли недостаточно убедительна (NNT неизвестно) [1, 11]. Тапентадол подлежит предметно-количественному учету.
• В отношении следующих препаратов доказана неэффективность или получены противоречивые результаты по эффективности, не позволяющие рекомендовать их при болевой ДПН [1, 11]: – из противосудорожных: ламотриджин, лакосамид, вальпроаты, топирамат, зонисамид; – из антидепрессантов: СИОЗС, миансерин, тразодон, ингибиторы МАО; – из прочих фармакологических групп: клонидин, пентоксифиллин, мексилетин, мемантин, каннабиноиды.
• В связи с побочными действиями для лечения болевой ДПН не рекомендуются следующие лекарственные средства: нестероидные противовоспалительные препараты, парацетамол, витамин В6, петидин, тримеперидин (промедол) [1].


