Диагностика

1.
При диагностике алкогольной болезни печени (АБП) следует учитывать склонность больных к неадекватной оценке своего состояния и частое их стремление к сокрытию злоупотребления спиртными напитками. Структура анкеты CAGE – опросника первой линии для выявления склонности пациента к злоупотреблению алкоголем – приведена в таблице 1. Чувствительность теста составляет 66%, специфичность ‒ 91,4% [1].

2.
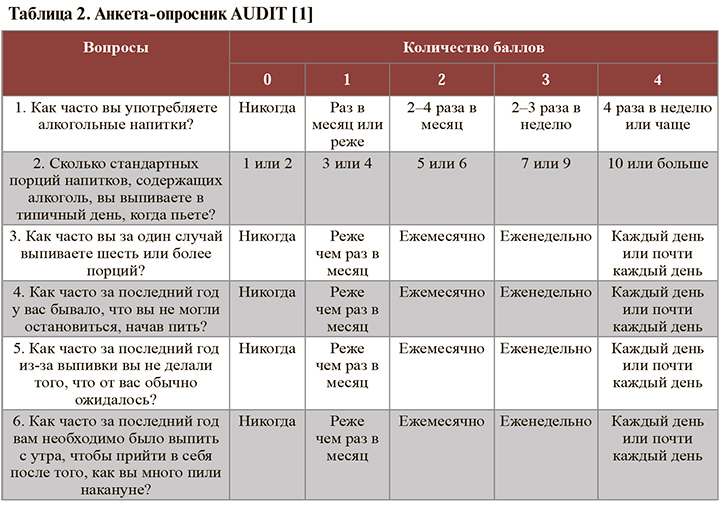
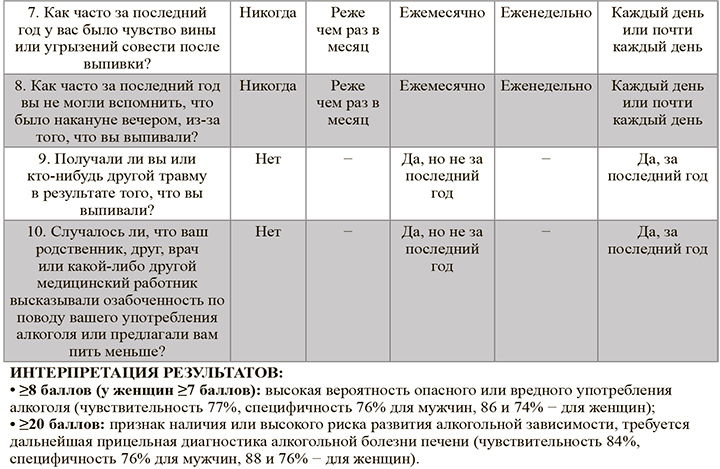
Международный стандартизованный тест AUDIT, рекомендованный для подтверждения/исключения факта алкоголизма при положительном результате CAGE (≥2 баллов), представлена в таблице 2. Продолжительность проведения и оценка AUDIT обычно не превышает 5 мин [1].
3.
• Клинические признаки АБП варьируют от полного отсутствия каких-либо симптомов (в большинстве случаев при алкогольном стеатозе) до классической картины тяжелых форм поражения печени с симптомами печеночной недостаточности и портальной гипертензии (при алкогольном циррозе) [1]. Ряд неспецифических симптомов, позволяющих заподозрить АБП, указан в таблице 3.

• При физикальном обследовании признаков, патогномоничных исключительно для АБП, не отмечается. При объективном исследовании следует обращать внимание на так называемые алкогольные стигмы: одутловатость лица, расширение сосудов носа и склер, увеличение околоушных слюнных желез, ринофиму, атрофию мышц плечевого пояса, яркие сосудистые звездочки, гинекомастия, контрактура Дюпюитрена, тремор пальцев рук, атрофия яичек, гепатомегалию, «мраморность» кожных покровов, повышенную потливость, раздражительность [1]. При этом следует учитывать, что дифференцировать АБП от других форм паренхиматозного повреждения печени только по физикальным данным невозможно (уровень убедительности рекомендаций А, уровень достоверности доказательств 1) [1].
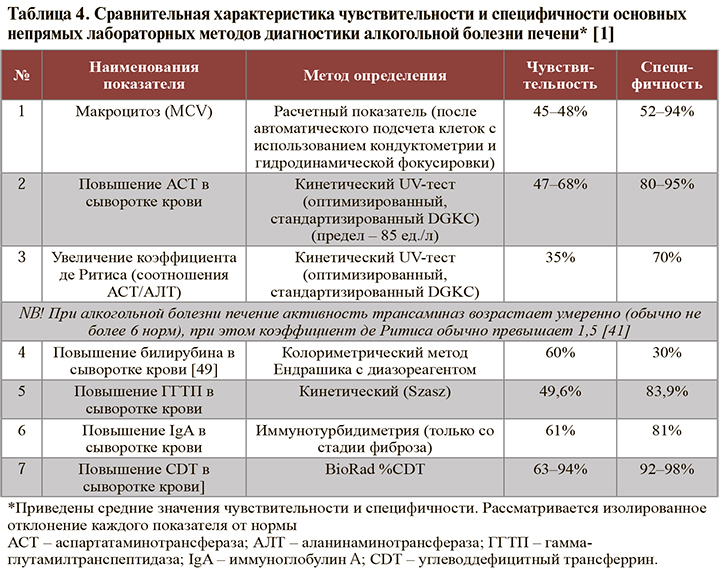
• При подозрении на АБП рекомендуется оценить клинический анализ крови. При выраженном воспалительном процессе в печени на фоне чрезмерного употребления алкоголя нередки лейкемоидные реакции, нейтрофильный лейкоцитоз до 15–20 × 109 /л, повышение скорости оседания эритроцитов (СОЭ) до 40–50 мм/ч [1]. Основные непрямые лабораторные маркеры АБП отражены в таблице 4. При всей важности определения этих маркеров нужно помнить, что ни один из них не может быть достоверным индикатором алкогольной этиологии заболевания печени.
4.
• Из инструментальных методов диагностики АБП в клинической практике наиболее распространено ультразвуковое исследование (УЗИ) (табл. 5). Оно рекомендуется для определения стеатоза и цирроза, но не позволяет установить этиологию и стадию поражения печени (уровень убедительности рекомендаций А, уровень достоверности доказательств 2) [1]. Чувствительность УЗИ при диагностике АБП составляет 85%, специфичность – 30% [1].

• Метод транзиентной эластографии рекомендуется для оценки степени плотности печени и ассоциированной с ней стадии фиброза печени по шкале Metavir (уровень убедительности рекомендаций В, уровень достоверности доказательств 2). Чувствительность метода при диагностике АБП составляет 86%, специфичность – 93%. Транзиентная эластография может давать погрешности вследствие точечного определения упругости печеночной ткани без оценки состояния паренхимы в целом. Кроме того, получение достоверных результатов невозможно при асците или ожирении [1].
5.
Чаще всего проводят дифференциальную диагностику АБП с неалкогольной жировой болезнью печени (характерные признаки – атерогенная дислипидемия, избыточный вес или ожирение, жировая инфильтрация печени при CDT <1,7%), а также с механической обструкцией желчевыводящих путей (гепатоцеллюлярная карцинома, билиарная обструкция, синдром Бадда–Киари), гепатитами (вирусным, аутоиммунным, лекарственно-индуцированным, ишемическим), первичным гемохроматозом и рядом других заболеваний гепатобилиарной системы. Обнаружение «второго» заболевания печени не исключает наличие АБП [1].
6.
Учитывая все имеющиеся методы диагностики, для установления диагноза АБП целесообразно использование сводной таблицы критериев, составленной на основе специфичности каждого используемого метода диагностики и рассчитанной с высокой степенью достоверности (табл. 6).

Лечение
1.
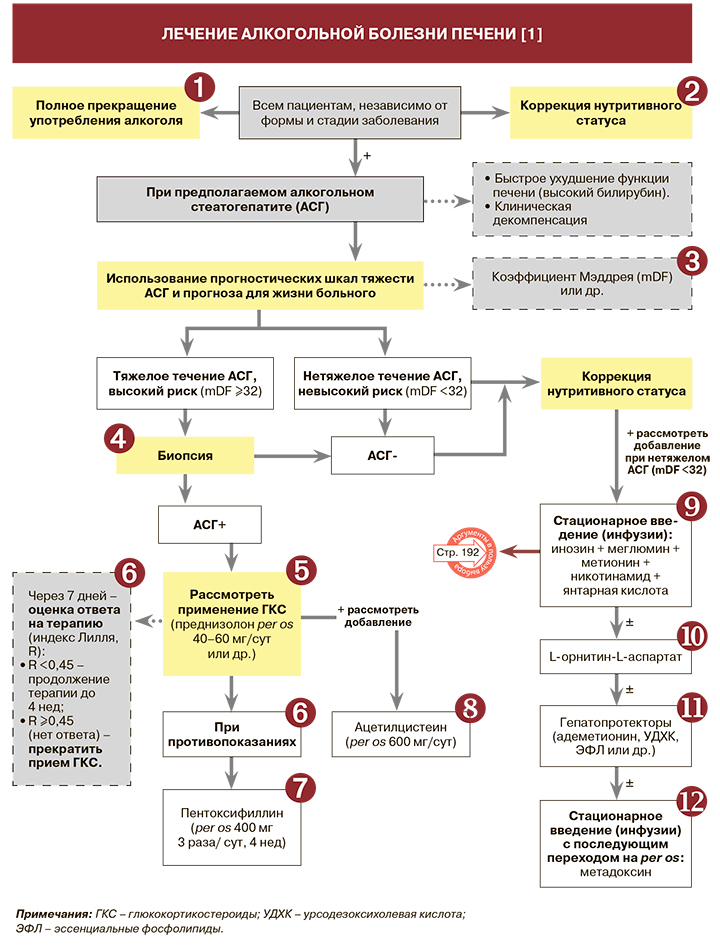
Ведение пациентов, страдающих алкогольной зависимостью, целесообразно осуществлять совместными усилиями специалистов соматического и наркологического звена. Первое и обязательное рекомендуемое условие лечения больных АБП – полное прекращение употребления алкоголя, в противном случае прогрессирование заболевания неизбежно (уровень убедительности рекомендаций А, уровень достоверности доказательств 1) [1, 2]. Во многих случаях выполнение только этого условия приводит к обратному развитию патологических изменений в печени. При наличии алкогольной зависимости желательно включение пациента в одну из программ социальной реабилитации алкоголиков [1].
2.
• Нарушение статуса питания и нутритивная недостаточность являются важной проблемой пациентов с АБП: дефицит поступления и усвоения микро-, макроэлементов и питательных веществ отмечается у большинства больных, злоупотребляющих алкоголем [1, 3]. Учитывая сниженный нутритивный статус злоупотребляющих алкоголем лиц, важным компонентом рекомендуемого лечения служит адекватное поступление питательных веществ [1, 4, 5].
• Энергетическая ценность рекомендуемой диеты должна быть не менее 2000 ккал в сутки, с достаточным количеством витаминов в составе продуктов или мультивитаминных препаратов (уровень убедительности рекомендаций А, уровень достоверности доказательств 1). Кроме исключения тугоплавких жиров и легкоусваиваемых углеводов, необходимо обеспечить достаточное содержание белка в дозе не менее 1–1,5 г на кг идеальной массы тела [1, 6]. Рекомендуются липотропные продукты, способствующие оттоку желчи – овсяная и гречневая крупы, изделия из творога, нежирные сорта рыбы. При анорексии применяется энтеральное зондовое или парентеральное питание. При легких и среднетяжелых формах АБП определенный эффект могут дать анаболические стероиды [1, 7].
3.
• Коэффициент Маддрея (mDF) вычисляется по формуле: DF=4,6 × (ПВбольного – ПВконтроля) + СБ, где: ПВ — протромбиновое время (с); СБ — уровень сывороточного билирубина (мг/дл). У больных со значением этого коэффициента ≥32 (тяжелое течение алкогольного стеатогепатита) вероятность летального исхода в ближайший месяц составляет от 35−50% (при отсутствии адекватной терапии) [1, 8−10].
• Из других прогностических шкал тяжести алкогольного стеатогепатита (АСГ) и прогноза для жизни больного могут использоваться MELD (Model for End-Stage Liver Disease) и GAHS (Glasgow Alcoholic Hepatitis Score). MELD ‒ модель терминальной стадии болезни печени для определения риска летального исхода в 90-дневный срок, ранее разработанная для больных, нуждающихся в трансплантации печени. MELD (в баллах) вычисляется по формуле: 11,2 × ln (МНО) + 9,57 × ln (креатинин, мг/дл) + 3,78 × ln (билирубин, мг/дл) + 6,43, где: ln — натуральный логарифм. Нижняя граница нормы для каждого показателя 1, максимальное значение для уровня креатинина ‒ 4. В случае если пациент находится на гемодиализе, уровень креатинина считают равным 4. Течение АСГ считают тяжелым, а прогноз на ближайшие 90 дней неблагоприятным при результате MELD ≥18 баллов [1, 11−13].
• В первый или седьмой день госпитализации по поводу предполагаемого АСГ рекомендуется оценивать показатели шкалы Глазго (GAHS) (табл. 7). 8 и более полученных баллов говорят о тяжелом АСГ и возможном летальном исходе в ближайшее время, при ≥9 баллах выживаемость к 28-му дню составляет 46%, к 84-му − 40% (уровень убедительности рекомендаций А, уровень достоверности доказательств 1) [1, 14, 15].

4.
• АСГ тяжелого течения, когда существует необходимость в специфической терапии (глюкокортикостероиды), − одно из основных показаний к выполнению биопсии печени [16]. Биопсия подтверждает наличие поражения печени, устанавливает его стадию и позволяет во многих случаях подтвердить алкогольный генез (чувствительность 91%, специфичность 97%) [1].
• Данные гистологического исследования позволяют четко определить прогноз заболевания у конкретного пациента. Например, морфологически подтвержденный диагноз АСГ сочетается с худшим долгосрочным прогнозом (смертность на 50% выше) в сравнении со стадией стеатоза [16].
5.
• Кроме преднизолона, при тяжелой форме АСГ возможно применение таких пероральных глюкокортикостероидов (ГКС), как метилпреднизолон в дозе 32 мг/сут, будесонид 9 мг/сут (уровень убедительности рекомендаций А, уровень достоверности доказательств 1) [1].
• В процессе лечения ГКС рекомендуется использовать индекс Лилля для оценки ответа на лечение: вероятность 6-месячного выживания пациентов с R ≥0,45 составляет в среднем 25%, пациентов с R <0,45 – 85% (уровень убедительности рекомендаций А (уровень достоверности доказательств 1). Расчет индекса Лилля проводят по формуле: R=3,19–0,101 × возраст + 0,147 × А0 + 0,0165 × (СБ1 – СБ7) – 0,206 × ПН – 0,0065 × СБ0 – 0,0096 × МНО, где: А0 – альбумин в день 0 (г/л); СБ0, СБ1, СБ7 — сывороточный билирубин в 0 -й, 1-й и 7-й дни соответственно; ПН – коэффициент, связанный с наличием или отсутствием почечной недостаточности: при уровне сывороточного креатинина ниже 115 мкмоль/л (1,3 мг/дл) или клиренсе креатинина менее 40 мл/мин ПН=0 (нет почечной недостаточности); при превышении указанных выше величин диагностируют почечную недостаточность (коэффициент ПН=1) [1].
• Интерпретация результатов лечения ГКС по индексу Лилля: R ≤0,16 – полный ответ; R=0,16–0,56 – частичный ответ на терапию; R≥0,56 – отсутствие ответа. Если на 7-й день лечения у больного индекс Лилля ≥0,45, рекомендуется прекратить прием ГКС [1, 17].
6.
ГКС противопоказаны больным с желудочно-кишечным кровотечением, сахарным диабетом, инфекционными процессами различной локализации, почечной недостаточностью (уровень убедительности рекомендаций А, уровень достоверности доказательств 1) [1].
7.
Пентоксифиллин рекомендуется пациентам с наличием противопоказаний к назначению ГКС (уровень убедительности рекомендаций В, уровень достоверности доказательств 2). Препарат назначается в дозировке 400 мг в 3 приема перорально длительно. Он способен лишь оказывать некоторое влияние на субъективное самочувствие пациента, но не влияет на выживаемость больных АБП [1, 18, 19].
8.
Ацетилцистеин в дозе 600 мг/сут в комбинации с ГКС может быть рекомендован при тяжелом течении АБП, поскольку способен улучшать краткосрочную выживаемость пациентов с алкогольным гепатитом тяжелого течения в сравнении с монотерапией ГКС (уровень убедительности рекомендаций С, уровень достоверности доказательств 3) [20].
9.
При АБП могут быть рекомендованы препараты на основе янтарной кислоты, которые в клинической практике значимо снижают выраженность синдромов цитолиза и холестаза, восстанавливают липидный обмен, улучшают субъективный статус пациентов (уровень убедительности рекомендаций С, уровень достоверности доказательств 3) [1, 21]. Янтарная кислота – универсальный энергосубстрат, входящий в цикл Кребса: она участвует в энергообеспечении и восстанавливает НАД-зависимое клеточное дыхание, обеспечивая утилизацию кислорода тканями и повышая устойчивость мембран гепатоцитов к перекисному окислению [1, 22]. Преимущества сукцината (аниона янтарной кислоты) наиболее выражены в условиях гипоксии, когда НАД-зависимое клеточное дыхание угнетено. В практической деятельности широко применяются инфузии полиионного сукцинат-метионинового комплекса на основе янтарной кислоты (янтарная кислота 5,28 г; N-метилглюкамин (меглюмин) 8,725 г; рибоксин (инозин) 2 г; метионин 0,75 г; никотинамид 0,25 г) [1].
10.
L-орнитин-L-аспартат рекомендуется для лечения больных с АБП, поскольку уменьшает эндотоксикоз и печеночную энцефалопатию за счет выраженного гипоаммониемического эффекта (уровень убедительности рекомендаций B, уровень достоверности доказательств 2) [1]. Участвуя в орнитиновом цикле, он утилизирует аммонийные группы в синтезе мочевины, снижая концентрацию аммиака в плазме крови. L-орнитин-L-аспартат способствует нормализации кислотно-щелочного состояния организма и выработке инсулина и соматотропного гормона [1, 23].
11.
• При АБП рекомендуется назначение адеметионина, который статистически значимо повышает выживаемость больных алкогольным циррозом (уровень убедительности рекомендаций B, уровень достоверности доказательств 2) [1, 24]. Исследования показали, что при АБП препарат купирует абстинентный синдром, улучшает общее самочувствие, уменьшает кожный зуд, снижает уровень сывороточного билирубина и активность трансаминаз. Адеметионин назначают вначале парентерально по 5–10 мл (400–800 мг) внутривенно или внутримышечно в течение 10–14 дней, а затем по 400–800 мг (1–2 таблетки) 2 раза в день. Продолжительность курса лечения составляет в среднем 2 мес. Препарат не следует назначать при азотемии [1].
• Рекомендуется применение эссенциальных фосфолипидов, которые при АБП способствуют быстрому купированию болевого и диспепсического синдромов, снижению клинико-биохимической активности, уменьшению размеров печени (уровень убедительности рекомендаций В, уровень достоверности доказательств 3) [1, 25].
• Применение урсодезоксихолевой кислоты (УДХК) рекомендуется с учетом имеющихся данных об улучшении клинико-биохимической и гистологической картины на фоне ее использования у больных АБП, что, вероятно, связано не только с антихолестатическим эффектом этого лекарственного средства, но и подавлением секреции провоспалительных цитокинов (Уровень убедительности рекомендаций В, уровень достоверности доказательств 3) [1, 26]. Режим дозирования УДХК при алкогольном стеатозе составляет 10 мг/кг/сут однократно в вечернее время, что в среднем соответствует 2–3 капсулам в день (500–750 мг), сроком на 3 мес. Не рекомендуется назначение УДХК в условиях прогрессирования цитолитического синдрома [1].
12.
• Метадоксин рекомендуется при АБП, поскольку активирует ферменты печени, участвующие в метаболизме этанола (алкогольдегидрогеназы и ацетальдегиддегидрогеназы), ускоряет процесс выведения этанола и ацетальдегида из организма и соответственно снижает их токсическое воздействие (уровень убедительности рекомендаций С, уровень достоверности доказательств 3) [1]. Лечение начинают с внутривенного, однократного в сутки введения 600–1200 мг препарата, длительностью до 4 нед, с последующим переходом на пероральный прием 1000–1500 мг/сут, продолжительностью до 3 мес [1].
• К прочим лекарственным средствам, которые могут потенциально полезными при АБП, относятся силимарин, таурин, гидролизат плаценты человека (Уровень убедительности рекомендаций С, уровень достоверности доказательств 4) [1].


