ВВЕДЕНИЕ
Подагра – системное аутовоспалительное заболевание, характеризующееся отложением в тканях кристаллов моноурата натрия (МУН) и развивающимся в связи с этим воспалением у лиц с гиперурикемией (ГУ), обусловленной внешнесредовыми и/или генетическими факторами [1]. Именно ГУ – наиболее важный фактор риска развития подагры: ей соответствует сывороточный уровень мочевой кислоты (МК) > 360 мкмоль/л, или > 6 мг/дл (т. е. выше порога насыщения, за которым в крови при температуре 35 °C происходит кристаллизация уратов) [2]. Классическим клиническим проявлением подагры выступает острый приступ артрита, который опосредован иммунным ответом, инициируемым кристаллами МУН.
«Золотым стандартом» диагностики подагры общепризнана поляризационная микроскопия синовиальной жидкости, позволяющая визуализировать кристаллы МУН, важными инструментальными методами – сонография суставов и двухэнергетическая компьютерная томография (ДЭКТ) [3]. Главной целью лечения заболевания служит достижение и длительное поддержание целевого уровня МК в крови (<360 мкмоль/л): это препятствует образованию новых и приводит к растворению уже имеющихся кристаллов МУН, тем самым предотвращая возможность развития приступов артрита.
ПАТОГЕНЕЗ
С современных позиций подагру следует рассматривать не как болезнь острого приступа, а как хроническое прогрессирующее заболевание и один из неблагоприятных исходов ГУ. Условно в развитии и течении подагры выделяют 4 последовательные стадии:
- ГУ;
- ГУ с депонированием кристаллов МУН (без приступов артрита!);
- клинические проявления подагры (дебют заболевания, как правило, в форме острого артрита);
- хроническая тофусная подагра (в случае непрерывной прогрессии заболевания при неадекватной терапии или ее отсутствии) [4].
Таким образом, бессимптомная ГУ и подагра не тождественные друг другу понятия, и к последней относят только тех пациентов, у которых был хотя бы один острый приступ артрита, характерный для заболевания [5].
При этом ГУ – непреложный, но не единственный фактор риска развития подагры, так как в большинстве случаев даже при длительном повышении уровня МК > 360 мкмоль/л (>6 мг/дл) заболевание не развивается (за 15 лет наблюдения – менее чем у 1 из 11 пациентов с исходно бессимптомной ГУ) [6]. В качестве «промежуточного звена» между ГУ и подагрой рассматривают ГУ с наличием кристаллов МУН, которые обнаруживают как минимум у каждого четвертого пациента с бессимптомной ГУ [7]. Помимо повышенной концентрации МК, вероятность кристаллизации уратов в биологической жидкости увеличивают низкие температуры (одна из причин того, почему вероятность развития артрита в 1-м плюснефаланговом суставе и суставах стоп в целом выше, чем в иных), рН в пределах 7–8, высокая концентрация ионов натрия, глюкозамингликаны, белки, липополисахариды, волокна коллагена, различные антитела [8].
Сформировавшиеся кристаллы МУН могут взаимодействовать с рецепторами клеточных мембран и фагоцитироваться, что служит пусковым механизмом острого приступа артрита, хотя даже наличие «молчащих» кристаллов связано с наличием вялотекущего микрокристаллического воспаления.
Механизмом, определяющим специфичность подагрического воспаления, является активация инфламмасомы в «иммунных» клетках (нейтрофилах, моноцитах/макрофагах, тучных клетках), включающая два этапа – неспецифическую «предактивацию» (priming – сигнал 1) и активацию (сигнал 2). Первый сигнал приводит к стимуляции фактора транскрипции NF-κB путем активации мембранных рецепторов Толл-подобных рецепторов (Toll-like receptors – TLR) 2 и 4, экспрессирующихся на моноцитах и макрофагах. NF-κB контролирует экспрессию компонентов, необходимых для сборки NLRP3-инфламмасомы, регулирующей образование «провоспалительных» белков-предшественников (проинтерлейкина 1 и проинтерлейкина 18, служащих субстратом для действия «воспалительной» каспазы-1) [9]. Сигнал 1 не является специфичным и недостаточен для полноценного «запуска» инфламмасома-зависимого воспаления. TLR регулируют подагрическое воспаление за счет распознавания широкого спектра лигандов, предактивирующих моноциты/макрофаги в отношении образования проинтерлейкина 1 (про-ИЛ-1). К ним относят S100F8, S100A9, длинные цепи свободных жирных кислот (при приеме пищи и алкоголя), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), анафилотоксин С5а, вакцины, кишечную микробиоту и др. [10–13].
Собственно кристаллы МУН активируют вторую сигнальную систему, вызывая сборку NLRP3 инфламмасомы и активацию каспазы-1, которая протеолизирует про-ИЛ-1β до интерлейкина 1β (ИЛ-1β). Последний взаимодействует с рецептором ИЛ-1β, инициируя процесс привлечения иммунных клеток (преимущественно нейтрофилов) к местам образования кристаллов МУН и синтез нейтрофилами множества провоспалительных цитокинов, что клинически проявляется в виде приступа подагры [9]. Поскольку указанный процесс двухэтапный, кристаллы МУН не обязательно приводят к острому воспалению (приступу артрита) и длительно могут быть интактными.
Интересен и процесс самокупирования приступа артрита при подагре. В нем основную роль играют те же иммунные клетки, что и в развитии острого воспаления. Процесс связан с формированием разрушенными нейтрофилами так называемых нейтрофильных ловушек, ингибирующих действие провоспалительных цитокинов, активацией AMPK (AMP-активируемая киназа) зависимого пути в макрофагах и синтезом ими антивоспалительных цитокинов [14].
В настоящее время претерпела изменения и классификация причин ГУ. В отличие от традиционной, но устаревшей градации, где выделяли три этиологических фактора ГУ (гиперпродукция МК, почечная гипоэкскреция МК, а также сочетание первой и второй), ныне выделяют четыре ее варианта [15].
- А. Вариант перегрузки почек:
- А1. Подвариант гиперпродукции (когда почки не справляются с избыточным количеством пуринов, поступающих в организм с пищей или продуцируемых в организме при ожирении, потреблении больших количеств фруктозы, миелопролиферативных заболеваниях, псориазе, редких наследственных заболеваниях);
- А2. Внепочечные варианты гипоэкскреции, обусловленные дисфункцией в кишечнике уратного транспортера ABCG2, нарушенным составом кишечной микробиоты, наличием воспалительных заболеваний кишечника;
- В. Вариант почечной гипоэкскреции, связанный с работой уратных транспортеров в почках (URAT1 (SLC22A12), OAT4 (SLC22A11), OAT10 (SLC22A13) и GLUT9 (SLC2A9) OAT1 (SLC22A6), OAT2 (SLC22A7), OAT3 (SLC22A8), GLUT9), почечной недостаточностью;
- С. Комбинированные варианты ГУ (перегрузка почек и почечная гипоэкскреция).
СОПУТСТВУЮЩИЕ ЗАБОЛЕВАНИЯ
Подагра, как и ГУ, часто ассоциирована с ожирением, нарушениями липидного и углеводного обмена, повышением артериального давления (которые могут обнаруживаться изолировано или совместно, в рамках метаболического синдрома), сердечно-сосудистыми заболеваниями, нарушением функции почек и уратным нефролитиазом, жировым гепатозом, некоторыми видами рака, заболеваниями щитовидной железы, эректильной дисфункцией и др. [16]. Продолжительность жизни пациентов с подагрой меньше популяционной как из-за коморбидных заболеваний, так и, собственно, из-за ГУ и микрокристаллического воспаления, не ограничивающегося суставами [17]. Наконец, рассматривается связь подагры с поражением суставного хряща кристаллами МУН: по предварительным данным исследования, проводимого в ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой», среди 188 пациентов с подагрой (169 мужчин (89,9%), средний возраст – 49,0 ± 11,7 года) наличие рентгенологических признаков остеоартрита коленных суставов было выявлено у 132 человек, что в процентном отношении (70,2%) существенно превышает соответствующие популяционные значения (13%) [18].
В целом же чем больше у пациентов сопутствующих заболеваний, тем тяжелее протекает подагра и тем сложнее проведение лекарственной терапии [19].
КЛИНИЧЕСКАЯ КАРТИНА ПОДАГРЫ
Типичное проявление подагры – крайне болезненный острый артрит, чаще всего поражающий суставы нижних конечностей. Приступ возникает почти молниеносно (время его развития обычно менее 12 ч), как при травме, и в течение нескольких часов боль становится нестерпимой. Как правило, в процесс вовлекается один, реже несколько суставов (олигоартрит). Длительность приступов обычно варьирует от нескольких дней до 2 нед., при этом они разрешаются даже без медикаментозного лечения. Далее наступает межприступный период, на протяжении которого пациент не предъявляет каких-либо жалоб, вплоть до нового обострения болезни. Помимо суставов, у пациентов могут поражаться суставные сумки (например, ахиллобурсит или бурсит локтевого сустава), сухожилия, в том числе в местах их прикрепления (энтезиты). Другими особенностями артрита при подагре являются отек различной интенсивности, локальная гипертермия и эритема. Боль при приступе столь интенсивна, что приводит к существенному ограничению возможности использовать пораженную область (проявляется функциональными нарушениями) и страху даже минимального физического контакта [20].
Острый артрит при подагре преимущественно поражает нижние конечности: по мере убывания частоты это 1-е плюснефаланговые суставы, суставы предплюсны, голеностопные, коленные суставы. Вместе с тем приступ, особенно при длительном неконтролируемом течении заболевания, может охватывать также суставы верхних конечностей и даже осевого скелета [21]. У женщин суставы верхних конечностей поражаются чаще, чем у мужчин [22]. Общие проявления обострения подагры включают лихорадку и озноб; в крови, помимо ожидаемого повышения скорости оседания эритроцитов (СОЭ) и сывороточного уровня С-реактивного белка, нередко наблюдаются лейкоцитоз с нейтрофилезом [23].
Триггерными факторами приступов подагрического артрита служат потребление продуктов, богатых пуринами, и алкоголя, травмы суставов, острые заболевания (например, COVID-19), а также резкое снижение уровня МК в крови, связанное с инициацией уратснижающей терапии (УСТ) [24–27]. Чем выше сывороточный уровень МК и чем дольше он сохраняется высоким, тем больше вероятность повторных приступов артрита [28]. Это связано с накоплением все большего количества кристаллов МУН, что со временем вызывает прогнозируемое нарастание частоты и длительности приступов и постепенно сводит к нулю длительность межприступных периодов. Таким образом, без адекватной терапии приступы рецидивируют, при этом поражаются новые суставы, формируются конгломераты кристаллов в виде подкожных, внутритканных отложений (тофусов), разрушается костная ткань, артрит становится хроническим [29].
Подкожные тофусы выглядят как мелообразные узлы под прозрачной кожей, нередко c вышележащей васкуляризацией (рис. 1). Они могут самопроизвольно вскрываться, и тогда из них через свищ выделяется творожистое (сметанообразное) содержимое, состоящее из кристаллов МУН. Размеры тофусов могут варьировать от небольших, размером с просяное зерно, до огромных. Наиболее типичные места локализации тофусов – суставы конечностей (чаще стоп), ушные раковины, бурса локтевого отростка, подушечки пальцев, сухожилия (например, ахилл) [30]. Тофусы являются твердыми на ощупь: это отличает их, к примеру, от узелков у пациентов с ревматоидным артритом, плотность которых при пальпации напоминает резину [31]. Тофусы обычно безболезненны даже в случае их воспаления. Они могут быть гиперемированы, хотя гипертермия при этом, как правило, не отмечается. При проведении эффективной УСТ тофусы могут размягчаться и постепенно рассасываются. «Естественное» течение нелеченой подагры может приводить к деформации и дефигурации суставов как за счет роста тофусов, так и по причине поражения костных структур, что влечет за собой серьезные функциональные нарушения.

ДИАГНОСТИКА
«Золотым стандартом» диагностики подагры считается визуализация кристаллов МУН в синовиальной жидкости или тофусах при поляризационной микроскопии. Кристаллы МУН имеют игольчатую форму, длину в диапазоне от 1 до 20 мкм, им свойственно двойное лучепреломление, что позволяет легко визуализировать их при поляризационной микроскопии (рис. 2) [32]. У пациентов с недифференцированным артритом обнаружения хотя бы одного кристалла достаточно для диагностирования подагры, однако, если кристаллы не найдены, это не исключает данного диагноза.
При диагностике подагры не следует полностью полагаться на сывороточный уровень МК. Вероятность кристаллизации уратов при содержании МК в крови < 360 мкмоль/л крайне низка, однако во время острого приступа артрита привычный для пациента уровень МК резко снижается из-за компенсаторного увеличения ее почечной экскреции. Этот уровень временно может быть ниже порога ГУ (<360 мкмоль/л), поэтому для корректной оценки концентрации МК в крови следует выбирать наиболее высокое значение показателя из имеющихся (если они есть) и проводить повторное исследование этого маркера через 2–4 нед. после разрешения приступа [3].
В случаях, когда выполнение поляризационной микроскопии невозможно или ее результат отрицательный, принципиально важно проведение ультрасонографии суставов (как правило, это суставы стоп, включая 1-е плюснефаланговые суставы) или ДЭКТ [3]. Оба метода обладают высокой специфичностью и чувствительностью, и их применение позволяет существенно уменьшить вероятность диагностической ошибки [33].
Если ДЭКТ еще не является общедоступной, то визуализация кристаллов при помощи ультразвукового исследования (УЗИ) – простой, неинвазивный, безопасный и дешевый метод инструментальной диагностики подагры. К сонографическим признакам отложения кристаллов МУН относят «двойной контур», внутрисуставные и периартикулярные тофусы, а также «вид метели», чувствительность и специфичность которого меньше. Изображение феномена «двойного контура» по результатам УЗИ 1-го плюснефалангового устава представлено на рисунке 3.
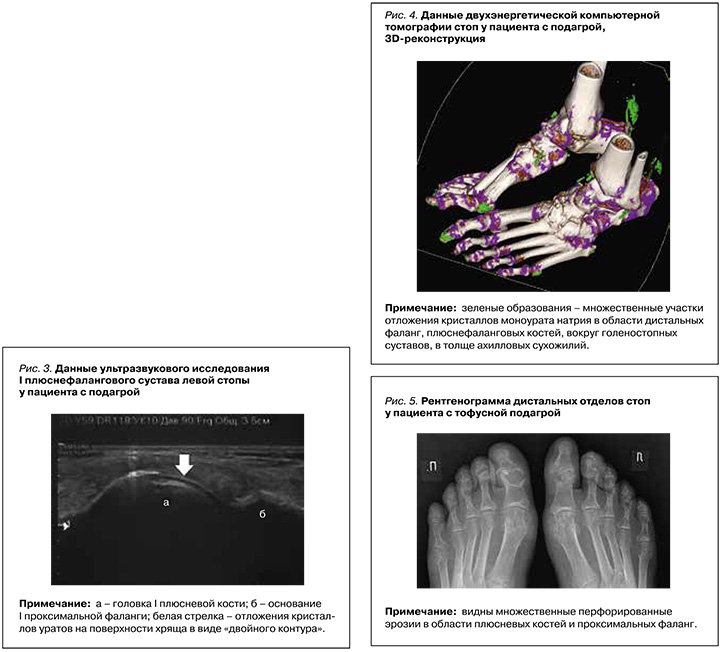
Для выявления отложения кристаллов МУН при помощи ДЭКТ используется метод двухматериальной декомпозиции, основанный на разложении полученных изображений по двух составляющим – кальцию и МК. В нашей стране для проведения этого метода обычно применяются аппараты, на которых кристаллы МУН имеют зеленую цветовую кодировку (рис. 4), кортикальная кость – синюю, а губчатая кость – розовую.
Как и в случае с поляризационной микроскопией, отсутствие признаков депонирования кристаллов МУН по результатам указанных методов лучевой диагностики отнюдь не гарантия отсутствия у пациента подагры, особенно при малой длительности заболевания.
Рутинное использование рентгенографии для верификации подагры признано малоинформативным и применяется, скорее, в целях дифференциальной диагностики (например, для исключения травмы, других ревматических заболеваний). Характерные для подагры рентгенологические признаки (четкие околосуставные перфорированные эрозии со склеротическим ободком и нависающими краями) обычно появляются поздно, через 6–12 лет от дебюта заболевания при его естественном течении [34]. На рисунке 5 приведена рентгенограмма стоп у пациента с длительным анамнезом подагры.
ТЕРАПИЯ ОСТРОГО ПРИСТУПА ПОДАГРИЧЕСКОГО АРТРИТА
Для купирования приступов артрита в качестве препаратов первой линии терапии используются нестероидные противовоспалительные препараты (НПВП), колхицин и глюкокортикоиды (внутрь или внутрисуставно). Выбор препарата, дозы и длительность применения должны быть индивидуальны и зависят от множества факторов: сопутствующих заболеваний, лимитирующих применение конкретного средства, абсолютных и относительных противопоказаний к применению лекарств, личного опыта пациента, тяжести артрита и т. д. В качестве вспомогательной терапии возможно локальное применение криотерапии (пакетов со льдом) [35].
Пациент должен быть обучен самостоятельно начинать лечение при первых же симптомах артрита, так как раннее начало терапии более действенно. Оценка эффективности лечения должна осуществляться в первые три дня от его начала. При неэффективности монотерапии возможно комбинированное применение НПВП, глюкокортикоидов и колхицина. При наличии противопоказаний и неэффективности этих средств может быть рассмотрено назначение ингибиторов ИЛ-1 [36, 37]. Основные принципы лечения острого приступа подагрического артрита отражены в таблице 1.

УРАТСНИЖАЮЩАЯ ТЕРАПИЯ
УСТ служит основой полного контроля подагры. Основная ее цель – достижение и постоянное поддержание целевого уровня МК сыворотки (<360 мкмоль/л). У пациентов с тяжелой тофусной подагрой целесообразно снижение концентрации МК < 300 мкмоль/л вплоть до полного растворения тофусов. Возможность назначения УСТ должна быть рассмотрена у всех без исключения пациентов с впервые установленным диагнозом (сразу после постановки диагноза).
УСТ проводится непрерывно, длительность ее не лимитируется временем, препараты должны использоваться в тех дозах, которые позволяют поддерживать сывороточный уровень МК ниже целевого. Уратснижающие лекарственные средства назначаются либо сразу, либо после купирования приступа артрита; исходно – в минимальной дозе, которая последовательно увеличивается по мере необходимости, в зависимости от показателей целевого уровня МК (при недостижении искомого значения МК в крови доза препарата увеличивается, вплоть до максимально допустимой).
В России, как и в большинстве стран мира, доступны два уратснижающих препарата – аллопуринол и фебуксостат. В основе действия обоих лежит ингибирование фермента ксантиноксидазы, регулирующего трансформацию гипоксантина в ксантин, а ксантина – в МК.
В качестве препарата первой линии терапии назначается аллопуринол в стартовой дозе 100 мг/сут., которую постепенно, каждые 2–4 нед., увеличивают в зависимости от концентрации МК в крови вплоть до достижения ее целевого уровня. Назначение аллопуринола в большей стартовой дозе сопряжено с многократным увеличением риска тяжелых кожных реакций, поэтому соблюдать указанные правила приема препарата нужно неукоснительно. При развитии любых кожных реакций препарат следует отменить и впредь данному пациенту не назначать. Максимальная суточная дозировка аллопуринола – 900 мг/сут. При правильном титровании его дозы риск побочных явлений почти не меняется и в целом низок. Вероятность снижения концентрации МК меньше 360 мкмоль/л (или меньше 300 мкмоль/л при наличии тофусов) на фоне терапии аллопуринолом весьма высока – 86% [38]. Средняя дозировка этого лекарственного средства, необходимая для достижения целевого значения МК (<360 мкмоль/л), составляет 400 мг/сут. [39]. Делить дозу на несколько приемов не нужно.
В случае недостижения целевого уровня МК в крови при приеме аллопуринола или наличии противопоказаний к нему пациентам со сниженной функцией почек назначается фебуксостат в стартовой дозе 40 или 80 мг/сут. При необходимости она может быть увеличена до 120 мг/сут. Для оценки эффективности достаточно двухнедельного курса приема препарата. Важно, что фебуксостат может с успехом использоваться при неэффективности аллопуринола, особенно в случае сниженной функции почек [40]. Главные принципы назначения уратснижающих препаратов обобщены в таблице 2.

Строгое соблюдение представленного алгоритма УСТ, который с некоторыми нюансами отражен в основных действующих рекомендациях по лечению подагры [37, 41–43], позволяет достичь целевых показателей МК (<360 или <300 мкмоль/л) у 92% больных [44]. Поскольку со временем сывороточная концентрация МК может меняться, следует контролировать ее даже после достижения целевого уровня, не реже 1 раза в 6 мес. [42]. Результатом длительного поддержания уровня МК ниже целевого будет растворение кристаллов МУН и полное прекращение приступов артрита.
ПРОФИЛАКТИКА ПРИСТУПОВ АРТРИТА ПРИ ИНИЦИАЦИИ УРАТСНИЖАЮЩЕЙ ТЕРАПИИ
В первые месяцы УСТ, независимо от используемого препарата, приводит к временному увеличению вероятности развития острых приступов подагрического артрита [45]. Поэтому для их профилактики совместно с УСТ рекомендуется назначать (в отсутствие противопоказаний) низкие дозы колхицина (0,5 мг/сут.), НПВП (например, напроксен 250–275 мг 2 р./сут., эторикоксиб 60 мг 1 р./сут., мелоксикам 7,5 мг 1 р./сут. или др.) или глюкокортикоиды (преднизолон 5 мг/сут.) [37]. Наиболее часто применяемым с этой целью (и наиболее хорошо изученным в этом аспекте) лекарственным средством является колхицин, который рассматривается как препарат первой линии.
В ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» был разработан и внедрен в практику алгоритм назначения препаратов для профилактики приступов подагрического артрита (рис. 6) [46]. В соответствии с ним пациентам, у которых колхицин не переносится, противопоказан или не эффективен, следует использовать НПВП, а при неэффективности или наличии противопоказаний и к этой группе препаратов – глюкокортикоиды.

Лекарственная профилактика приступов артрита должна быть неотъемлемым компонентом терапии подагры и назначаться в каждом случае, если у пациента нет противопоказаний к соответствующим препаратам. Отказ от нее приведет к увеличению частоты приступов артрита и, как следствие, к необходимости приема тех же лекарственных средств, но в более высоких дозах. Вероятность развития приступов при назначении профилактической медикаментозной терапии многократно снижается, а значительная часть пациентов их уже никогда не испытает. Если же приступ случается, он, как правило, менее тяжелый и продолжительный. При этом у больных возрастает приверженность к УСТ, а назначение низких доз колхицина не только уменьшает вероятность приступов и общие расходы на терапию, но также предупреждает развитие сердечно-сосудистых заболеваний и снижает связанную с ними смертность [47, 48].
Рекомендуемая длительность профилактической терапии составляет 6 мес., однако этот срок может быть бóльшим у пациентов с тяжелой тофусной подагрой, частыми приступами артрита.
ДИЕТА, ОБРАЗ ЖИЗНИ
Предполагается, что при всей важности влияния особенностей питания (потребления в больших количествах мяса, рыбы, подслащенных напитков, алкоголя) на повышение сывороточного уровня МК не меньшее значение в развитии подагры имеют генетические факторы [49]. Кроме того, хотя снижение массы тела и соблюдение низкопуриновой диеты приводят к снижению концентрации МК в крови, изолированного изменения рациона питания для достижения целевого уровня МК, как правило, недостаточно. Более того, жесткие требования строго следовать диетическим рекомендациям могут развить у больного ложное чувство вины и способствовать стигматизации [37].
Таким образом, пациенту с подагрой в рамках изменения образа жизни следует рекомендовать ограничение употребления алкоголя (особенно пива и крепких спиртных напитков), животных продуктов, богатых пуринами (мяса, морепродуктов, наваристых бульонов, субпродуктов и т. д.), подслащенных напитков (колы, дрожжевых напитков, соков с добавлением сахара и т. д.), а также по необходимости снижение веса. Однако эти рекомендации не должны быть навязчивыми, и, главное, как врачу, так и пациенту следует рассматривать их лишь в качестве дополнения, но ни в коем случае не альтернативы УСТ.
Добавим, что специальных диет при подагре к настоящему времени не разработано. Среди наиболее изученных систем питания более всего пациентам с этим заболеванием подходит DASH-диета (Dietary Approaches to Stop Hypertension) [50].
ЗАКЛЮЧЕНИЕ
Таким образом, подагру правильно рассматривать как хроническое воспалительное, непрерывно прогрессирующее в отсутствие лечения, но в то же время излечимое заболевание. В развитие этой болезни более весомый вклад, вероятно, вносят генетические факторы, а не особенности питания. Всем пациентам с подагрой, кроме диетических мер, необходимо рекомендовать прием уратснижающих препаратов для поддерживания сывороточного уровня МК в крови ниже как минимум 360 мкмоль/л, что является основой успешного контроля над заболеванием. Подобная терапия не проводится ограниченным курсом, а назначается на постоянной основе. Снизить вероятность развития приступов артрита в первые месяцы УСТ можно путем параллельного назначения низких доз колхицина, НПВП или глюкокортикоидов.



