В течение последних двух десятилетий значительный прогресс в понимании электрофизиологических основ внезапной аритмической смерти во многом был обусловлен интенсивными исследованиями синдрома удлиненного интервала QT (СУИQT), при котором имеется высокий риск внезапной сердечной смерти (ВСС) вследствие развития угрожающих жизни желудочковых аритмий. Данный синдром относится к первичным электрическим заболеваниям сердца [1] и характеризуется удлинением интервала QT на электрокардиограмме (ЭКГ) покоя, приступами потери сознания вследствие полиморфной желудочковой тахикардии (ЖТ), тахикардии типа «пируэт» или фибрилляции желудочков [2]. С момента открытия синдрома до настоящего времени это заболевание служит уникальной моделью для изучения патофизиологии, электрокардиографических проявлений, молекулярно-генетических механизмов, а также факторов риска внезапной аритмической смерти. Именно исследования СУИQT позволили понять механизмы так называемых первичных электрических заболеваний сердца, или каналопатий, проявляющихся злокачественными нарушениями ритма сердца (НРС) с высоким риском ВСС в отсутствие органических изменений сердечно-сосудистой системы. В основе этих заболеваний лежат мутации в генах, ответственных преимущественно за нарушение функций ионных каналов. Созданы и постоянно ведутся международные и локальные регистры случаев заболевания [3]. Существенно изменились взгляды на этиологию и патогенез синдрома — первоначальная теория сцепленного с полом наследования [4] уступила место представлениям о фенотипической и генотипической разнородности с дифференцированными подходами к лечению и принципиально отличающимся прогнозом при различных формах заболевания [2, 5]. Дальнейшее изучение молекулярно-генетических основ синдрома направлено на выявление новых мутаций, определение вклада генов-модификаторов и сочетанных мутаций в патогенез и прогноз заболевания. По возможности ранняя, доклиническая диагностика СУИQT и лечение с учетом молекулярно-генетического варианта синдрома, индивидуальных факторов и маркеров риска позволяют в большинстве случаев предотвратить ВСС, значительно повысить продолжительность и качество жизни больных.
История открытия синдрома
В 1957 г. A. Jervell и F. Lange-Nielsen [6] сообщили о норвежской семье, в которой 4 из 6 детей страдали врожденной тугоухостью и частыми приступами потери сознания, провоцируемыми эмоциями или физической нагрузкой, и имели удлинение интервала QT на ЭКГ покоя (табл. 1). В 1963 г. C. Romano [7] и в 1964 г. O.C. Ward [8] описали семьи, в которых удлинение интервала QT было выявлено у одного из родителей и нескольких детей без глухоты. Впоследствии было подтверждено существование 2 форм — синдрома Джервелла—Ланге-Нильсена (аутосомно-рецессивный тип наследования) и Романо—Уорда (аутосомно-доминантный тип наследования), получивших название по фамилии авторов, впервые их описавших [9].
Таблица 1. История изучения СУИQT
Примечание. Здесь и в табл. 2: СУИQT — синдром удлиненного интервала QT.
Наследственная природа синдрома была подтверждена методами молекулярно-генетического анализа только в начале 90-х годов ХХ века, когда М. Keating и соавт. выявили ген KCNQ1, ответственный за развитие наиболее распространенного молекулярно-генетического варианта синдрома (LQT1) [10]. В последующем были определены 12 генетических вариантов СУИQT (см. табл. 1; табл. 2). За развитие клинических проявлений СУИQT ответственны не менее 11 генов, получивших числовую нумерацию (вариант) согласно хронологии их открытия (LQT1—LQT12) [11]. Мутации идентифицируются у 50—70% больных с клинически установленным диагнозом [2], что предполагает существование и других неизвестных пока генов, связанных с этим синдромом.
Таблица 2. Молекулярно-генетические варианты СУИQT [11]
Примечание. АД — аутосомно-доминантный; АР — аутосомно-рецессивный; LQT — синдром удлиненного интервала QT; JLN — синдром Джервелла—Ланге-Нильсена; IKs — медленный калиевый ток задержанного выпрямления; IKr — быстрый калиевый ток задержанного выпрямления; IK1 — активируемый кальцием калиевый ток; INa — натриевый ток; INa,K — натриево-калиевый ток; ICaL — медленный кальциевый ток; ↓ — снижение; ↑ — повышение.
Синдром выявляется в европейской и американской популяциях с частотой до 1:2500—1:7000 при пенетрантности 90% [2, 12]. При этом распространенность молекулярно-генетических вариантов синдрома Романо—Уорда различна. Описаны семьи со спорадическими случаями СУИQT и очень низкой пенетрантностью, составляющие около 25% (LQT4—LQT12). Большинство пациентов с установленным молекулярно-генетическим диагнозом относятся к первым 3 вариантам синдрома, соответственно LQT1 выявляется в 50—55% случаев, LQT2 — 35—45%, LQT3 — 5—15% [2]. Синдром Джервелла—Ланге-Нильсена, при котором удлинение интервала QT сопровождается глухотой, в отличие от синдрома Романо—Уорда, является редкой патологией. Согласно данным G.R. Fraser, в Великобритании частота данного синдрома в популяции детей 4—10 лет оценивается в 1,6 на 1 млн [9].
В патогенезе СУИQT ведущая роль принадлежит генам, кодирующим трансмембранные ион-селективные каналы. При СУИQT мутации найдены в генах, кодирующих калиевые, натриевые и кальциевые каналы, мембранные переносчики, а также некоторые структурные белки, локализованные на 3, 4, 7, 11, 12, 17, 20 и 21-й хромосомах (см. табл. 2) [13]. Большинство идентифицированных генетических дефектов при СУИQT относится к мутациям, нарушающим структуру кодируемого белка. Молекулярно-генетические варианты синдрома и характер мутаций определяют электрофизиологические особенности и клиническую картину заболевания. В то же время, несмотря на различия, все варианты СУИQT объединяются общими фенотипическими проявлениями.
Клиническая диагностика синдрома основана на критериях, впервые предложенных в 1985 г. P. Schwartz и уточненных автором в 1993 г. (табл. 3) [14]. Диагноз складывается из: 1) анализа предшествующей истории обмороков («синкопальных эпизодов»); 2) семейного анамнеза, включающего случаи ВСС в возрасте моложе 40 лет; 3) оценки специфических изменений ЭКГ.
Таблица 3. Диагностические критерии синдрома удлиненного интервала QT (P. Schwartz и соавт., 2008 [2])
Примечание. ≤1 балла — низкая вероятность наличия СУИQT; 1—3 балла — промежуточная вероятность наличия СУИQT; ≥3,5 балла — высокая вероятность наличия СУИQT.
Еще до получения доказательства генетической природы заболевания были выделены 4 варианта клинического течения: 1) синкопальный с удлинением интервала QT; 2) бессинкопальный с удлинением интервала QT; 3) синкопальный с нормальной продолжительностью интервала QT; 4) немая (скрытая, латентная) форма. Третий и четвертый клинические варианты диагностируются, как правило, у членов семьи пациента с установленным диагнозом СУИQT по наличию признаков электрической нестабильности миокарда, а также у внезапно умерших членов семьи с СУИQT в отсутствие указаний на обмороки в анамнезе и удлинения QT на зарегистрированных ЭКГ [15]. Данная классификация не утратила значимости до настоящего времени, так как она отражает тяжесть течения синдрома и позволяет оценивать степень риска развития угрожающих жизни НРС (табл. 4). Кроме того, ориентация на выраженность клинических проявлений и семейный анамнез, предложенная в классификации, позволяет улучшить качество диагностики на этапе, предшествующем молекулярно-генетическому исследованию, в том числе в случаях с нетипичным фенотипом.
Таблица 4. Стратификация риска ВСС у пациентов с СУИQT на основании рекомендаций Американского и Европейского обществ кардиологов (цит. по [11])
Примечание. ВСС — внезапная сердечная смерть.
Важная роль принадлежит электрокардиографии, которая в 80% случаев позволяет установить или предположить наличие СУИQT.
Интервал QT рекомендуется оценивать на синусовом ритме при стабильной частоте сердечных сокращений (ЧСС), в отсутствие выраженной синусовой аритмии во II стандартном или грудных отведениях. Волна U из измерения, как правило, исключается [16] (рис. 1).
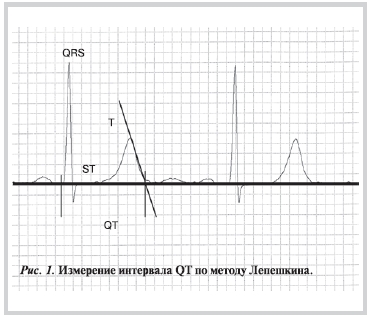
При наличии двуфазной волны Т или комплекса TU с высокой амплитудой волны U (более ⅓ амплитуды Т-волны) измеряется также интервал TU. В норме интервал QT находится в пределах от 350 до 440 мс. С учетом высокой корреляции между интервалами QT и RR была предложена стандартизация или коррекция интервала QT по ЧСС. Это позволяет оценить относительно независимую от ЧСС продолжительность интервала QT. Существует несколько формул для оценки корригированного интервала QT (табл. 5) [17—22]. Оптимальной признана модифицированная формула Базетта: QTc=QT/√RR (абсолютная продолжительность интервала QT в миллисекундах, деленная на корень квадратный из предшествующего интервала RR в секундах). Удлиненным считается QTc≥480 мс. После пубертатного периода у женщин в норме продолжительность интервала QTc в среднем на 10 мс больше, чем у мужчин, что послужило причиной разработки дифференцированных критериев оценки QT в зависимости от пола [23, 24]. Отсутствие очевидного удлинения интервала QT еще не исключает СУИQT у членов семьи пациента с верифицированным диагнозом, так как показано, что обмороки могут возникать у членов семей с нормальным интервалом QT на ЭКГ покоя [12, 25].
Таблица 5. Измерение корригированного интервала QT
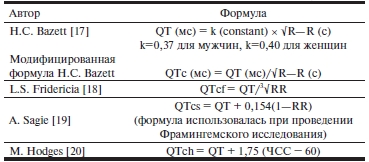
Примечание. ЧСС — частота сердечных сокращений.
Оценка других маркеров электрической нестабильности миокарда важна как для диагностики, так и для стратификации риска и контроля эффективности терапии. Аномалии в виде снижения амплитуды, инверсии, зазубренности или двуфазности волны T наиболее часто наблюдаются в грудных отведениях и служат дополнительным диагностическим критерием. A. Moss и соавт. впервые предположили, что морфология волны Т и сегмента ST у больных с СУИQT отражают определенный молекулярно-генетический вариант синдрома [26]. Нашими исследованиями также подтверждено наличие различий в морфологии волны Т у больных с LQT1, LQT2 и LQT3 [4] (рис. 2). Данные нарушения реполяризации могут быть непостоянными, проявляясь только в момент физического или психоэмоционального стресса, а также предшествовать развитию угрожающих жизни желудочковых аритмий (рис. 3).
Методика электрокардиографического картирования с одномоментной регистрацией потенциалов от 80 униполярных отведений с поверхности грудной клетки, 12 стандартных и 3 ортогональных отведений у больных с СУИQT позволяет выявлять характерные электрофизиологические типы распределения потенциалов в зависимости от молекулярно-генетического варианта синдрома. Согласно одной из существующих теорий патогенеза СУИQT обнаруженная анизотропия электрофизиологических процессов в сердце может быть следствием симпатического дисбаланса иннервации, характерного для данного заболевания [27].
24-часовое мониторирование ЭКГ по Холтеру (ХМЭКГ) является важным диагностическим методом при обследовании пациентов с СУИQT, в том числе для дифференциальной диагностики вторичного удлинения интервала QT. Помимо оценки продолжительности интервала QT, его максимальных значений и адаптации интервала QT к меняющейся ЧСС, с целью уточнения прогноза заболевания активно изучаются показатели вариабельности ритма сердца, дисперсия интервала QT, вариабельность интервалов QT/QTc и их производной QTpeak. Оценка морфологии волны Т в различные периоды суток важна с точки зрения уточнения молекулярно-генетического варианта и выявления альтернации Т-волны [29].
Классическая альтернация волны Т — это электрокардиографический феномен, характеризующий изменение полярности и амплитуды волны Т в последовательных сердечных циклах на синусовом ритме [29]. Альтернация волны Т у больных с СУИQT в наших исследованиях регистрировалась редко и только у больных с высоким риском развития угрожающих жизни желудочковых аритмий (рис. 4).
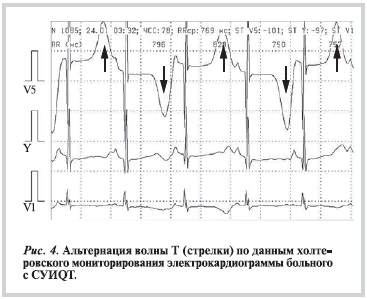
Дополнительными признаками электрической нестабильности миокарда по данным ХМЭКГ при СУИQT служат желудочковая эктопическая активность, удлинение интервалов QT и QTc непосредственно перед экстрасистолией и нарушение адаптации интервала QT к ЧСС [4]. К преимуществам длительной регистрации ЭКГ у больных с СУИQT относятся возможности автоматического анализа продолжительности интервала QT, QTс, а также определение процентной представленности QTc, превышающих нормативные значения.
Роль тестов с физической нагрузкой у больных с СУИQT обусловлена в большей степени их значением для дифференциальной диагностики как самого синдрома, так и его вариантов. Систематизация данных клинических исследований показала, что больные с СУИQT отличаются неадекватной изменению ЧСС динамикой продолжительности интервала QT (QTc) на фоне нагрузки [30].
Оценка вероятности диагноза. С 1985 г., когда P. Schwartz были разработаны большие (QTc≥440 мс, наличие обмороков, провоцируемых стрессом, наличие членов семьи с подтвержденным СУИQT) и малые (врожденная глухота, эпизоды альтернации волны Т, редкий для соответствующего возраста ритм сердца, а также нарушения реполяризации) критерии диагностики СУИQT [31] и предложена их балльная оценка [14], число диагностических критериев несколько расширилось и изменилось экспертное отношение к их клинической значимости. Так, вероятность наличия у больного наследственного СУИQT рекомендуется оценивать в баллах на основании выраженности изменений ЭКГ, клинических проявлений и отягощенности семейного анамнеза (см. табл. 3).
Дифференциальный диагноз. Наследственные варианты синдрома следует в первую очередь дифференцировать от приобретенного, в том числе лекарственно-индуцированного удлинения интервала QT [32].
К факторам, предрасполагающим к удлинению интервала QT, относятся следующие [11, 33]:
• комбинация лекарственных препаратов, действующих на одну молекулярную мишень (калиевый канал) и удлиняющих интервал QT;
• женский пол;
• пожилой возраст;
• наличие сердечной недостаточности (фракция выброса ≤40%);
• электролитные нарушения:
• гипокалиемия (терапия диуретиками, cиндром Кона);
• гипомагниемия («мягкая» питьевая вода; острая ишемия миокарда — снижение активности Na/K-АТФазы);
• гипокальциемия;
• хронический алкоголизм;
• брадикардия;
• наличие АВ-блокады III степени;
• гипотиреоз;
• нарушение мозгового кровообращения;
• автономная нейропатия;
• нарушение белкового питания, голодание, диеты для снижения массы тела;
• наркотические вещества (кокаин).
Удлинение интервала QT наиболее часто развивается на фоне приема антипсихотических средств, ряда антибиотиков (табл. 6). Структурные заболевания сердца, такие как гипертрофия, ишемия миокарда, а также сердечная недостаточность, нарушения метаболизма (ацидоз, гипокалиемия, гиперкальциемия), могут сопровождаться удлинением интервала QT на ЭКГ [33].
Таблица 6. Препараты, удлиняющие интервал QT на ЭКГ [www.torsades.org]
Примечание. * — документировано удлинение интервала QT, риск развития TdP неизвестен.
Клинически обмороки («синкопальные эпизоды») у многих больных с СУИQT имеют сходство с эпилептическими приступами. В таких случаях пациенты с СУИQT длительно наблюдаются неврологами с ошибочным диагнозом «эпилепсия» и получают терапию противосудорожными препаратами, неэффективными в профилактике повторных приступов потери сознания [4]. Дифференциальный диагноз с эпилепсией проводится на основании данных ЭКГ, семейного анамнеза и углубленного анализа клинических характеристик обмороков. Для больных с СУИQT, в отличие от пациентов, страдающих эпилептическими приступами, характерна провокация обмороков физическим или эмоциональным стрессом (LQT1, LQT2), быстрое восстановление сознания и самочувствия после приступа, отсутствие прикусывания языка, специфических изменений личности. Для пациентов с СУИQT также не характерна сонливость после приступа, типичная для больных с эпилепсией [4].
Дифференциальная диагностика наиболее распространенных молекулярно-генетических вариантов СУИQT. Накопленная информация о фенотипических проявлениях синдрома позволяет с большой вероятностью предположить один из трех основных молекулярно-генетических вариантов СУИQT. Наиболее значимыми дифференциально-диагностическими признаками служат структура провоцирующих обмороки факторов, морфология волны Т на ЭКГ покоя, динамика интервала QT (QTc) на фоне физической нагрузки, динамика де- и реполяризации по данным поверхностного электрокардиографического картирования (табл. 7). Такой подход позволяет назначить патогенетическую терапию до получения результатов генетического анализа.
Таблица 7. Сравнительная клинико-электрокардиографическая характеристика трех наиболее распространенных вариантов СУИQT
Примечание. ААП — антиаритмические препараты; НРС — нарушения ритма сердца; ЧСС — частота сердечных сокращений
Согласно результатам недавних исследований, достоверные дифференциально-диагностические критерии LQT1 и LQT2 были получены при проведении поверхностного электрокардиографического картирования. Абсолютное большинство больных с LQT1 отличают феномен расщепления отрицательного экстремума в ходе деполяризации с появлением дополнительных экстремумов (так называемая мультипольность) [27]. При LQT2 реполяризация отличается обширной зоной отрицательных потенциалов в зоне проекции правого желудочка, межжелудочковой перегородки, верхушки, задней стенки левого желудочка. Данное нарушение электрического поля сердца регистрируется в течение всего процесса реполяризации и сопровождается появлением дополнительных отрицательных (70% случаев) и иногда положительных экстремумов (30% случаев) [27]. Наличие мультипольного распределения потенциалов подтверждает нестабильность электрофизиологических процессов в миокарде желудочков больных с LQT1 и LQT2.
Динамика продолжительности интервала QT при проведении теста с физической нагрузкой также различна в зависимости от молекулярно-генетического варианта СУИQT (см. табл. 7). Так, у больных с LQT1 укорочение интервала QT на фоне нагрузки слабо выражено или отсутствует. P. Schwartz и соавт. выявили, что пациенты с LQT2 характеризуются нормальным приростом ЧСС и меньшей степенью укорочения интервала QT по сравнению с больными с вариантом LQT3 [30]. Максимальная ЧСС, достигнутая в ходе нагрузки у пациентов с первым вариантом синдрома, достоверно ниже, чем у пациентов со вторым вариантом.
Показания к проведению генетического тестирования у больных СУИQT представлены в табл. 8 [34].
Таблица 8. Показания к молекулярно-генетическому тестированию при СУИQT (цит. по [11])
Стратификация риска ВСС. Риск развития угрожающих жизни состояний у пациентов с СУИQT определяет тактику лечения. S. Priori и соавт. предложили схему стратификации риска развития обмороков и ВСС с учетом оценки продолжительности интервала QTc, генотипа, возраста и пола больных (см. табл. 4) [11]. Установлено, что вероятность развития обмороков у больных LQT1 и LQT2 выше, чем при LQT3, а наибольшая вероятность летального исхода отмечена при LQT3. С высоким риском ВСС ассоциируется QTc ≥ 500 мс [35]. Альтернация волны Т также относится к критериям высокого риска [36, 37]. Кроме того, предикторами угрожающих жизни ситуаций являются предшествующие эпизоды обмороков. Вероятность ВСС при LQT2 выше у женщин, а при LQT1 — у мужчин. У 36% больных с LQT1 выявляются так называемые немые мутации, не сопровождающиеся увеличением интервала QT на ЭКГ. Установлено, что риск развития аритмий в случае «немого носительства» ниже [2, 11].
Все больные с CУИQT должны находиться на постоянном мониторном наблюдении с контролем числа и выраженности индивидуальных факторов риска развития обмороков и внезапной аритмической смерти, которые целесообразно разделять на модифицируемые и немодифицируемые [4]. Базовый риск внезапной смерти при СУИQT обусловлен суммарным воздействием этих факторов риска. Немодифицируемые факторы риска представлены молекулярно-генетическим вариантом синдрома (более высокий риск при LQT3, синдроме Джервелла—Ланге-Нильсена), полом, ранним возрастом клинических проявлений синдрома, наличием в семье случаев ВСС в молодом возрасте. Обмороки, степень удлинения интервала QT, альтернация зубца Т и другие признаки электрической нестабильности миокарда относятся к условно модифицируемым маркерам риска, по изменению которых судят как о тяжести синдрома, так и об эффективности лечения.
Терапия считается эффективной, если она позволяет предотвратить рецидивы обмороков и уменьшить число модифицируемых факторов риска обмороков и ВСС [16].
Сохранение высокого риска ВСС на фоне терапии служит показанием к имплантации кардиовертера-дефибриллятора (ИКД) [38]. Эффективность ИКД-терапии оценивается на основании общепринятых алгоритмов, включая мотивированные и немотивированные шоковые воздействия. Оптимальная стратегия профилактики ВСС у больных с СУИQT заключается в определении базового риска на основании суммарной оценки модифицируемых и немодифицируемых факторов и маркеров риска и последующего мониторинга больных в соответствии с установленным индивидуальным профилем риска.
Тактика лечения наследственного СУИQT. Лечение больных с синкопальной формой СУИQT заключается в исключении специфических для каждого пациента факторов, которые запускают угрожающие жизни аритмии, исключении препаратов, способных удлинять интервал QT (см. табл. 7), а также в обязательном длительном (пожизненном) назначении антиаритмических препаратов. Разработаны специфические для генотипа подходы к терапии синдрома, что нашло отражение в международных рекомендациях по профилактике ВСС [37]. Рекомендации по образу жизни для разных генотипических вариантов синдрома, такие, как избегание резкого звукового раздражителя у больных с LQT2, исключение плаванья для больных с LQT1, могут способствовать предотвращению опасных для жизни аритмий. Препаратами первого ряда являются β-адреноблокаторы — пропранолол, атенолол, метопролол или надолол. Эти препараты особенно эффективны при LQT1 (81%), при котором риск ВСС прямо связан с реакцией на симпатическую стимуляцию. При втором и третьем вариантах синдрома β-адреноблокаторы менее эффективны (53 и 50% соответственно). Терапию у больных с LQT2 было предложено усиливать назначением препаратов калия. Содержание электролита в плазме крови желательно поддерживать на максимально допустимом уровне, что достигается сочетанием с калийсберегающими диуретиками. При LQT3 β-адреноблокаторы должны применяться с осторожностью под контролем ЧСС, так как выраженное снижение ее повышает дисперсию реполяризации и может облегчать возникновение тахикардии типа «пируэт». P. Schwartz первым в 1995 г. предложил назначение антиаритмического препарата IB класса мексилетина (блокатор натриевых каналов) больным с LQT3 [39]. Экспериментально было подтверждено, что антиаритмический эффект мексилетина в отношении предупреждения развития тахикардии типа «пируэт» обнаруживается при всех 3 основных вариантах синдрома (LQT1—QT3). Препарат эффективен и у больных с синдромом Тимоти (LQT8). Блокатор натриевых каналов IC класса флекаинид также продемонстрировал эффективность у больных с LQT3 [40], на основании чего в настоящее время может быть рекомендовано дополнительное назначение блокатора натриевых каналов как дополнение к базовой терапии у больных с третьим вариантом синдрома. Современные подходы к специфической для данного генотипа терапии суммированы в табл. 9.
Таблица 9. Генотип-специфическая терапия СУИQT [4, 11]
Примечание. * — на стадии экспериментальных работ.
Сохранение обмороков или эпизодов ВСС на фоне терапии β-адреноблокаторами является абсолютным показанием к ИКД. При имплантации современного антиаритмического устройства наряду с функциями дефибриллятора нередко используется функция электрокардиостимуляции, что позволяет избежать выраженной брадикардии у больных с брадизависимыми аритмиями, а также при необходимости назначения высоких доз β-адреноблокаторов [41—3].
В 1971 г. A. Moss впервые применил левостороннюю симпатэктомию у больного со злокачественным, резистентным к лекарственной терапии течением СУИQT [44]. Затем P. Schwartz и A. Malliani экспериментально доказали связь удлинения интервала QT со стимуляцией левого звездчатого ганглия [45]. Учитывая роль повышенной симпатической активности в патогенезе СУИQT, в качестве одного из дополнительных ресурсов лечения у больных с тяжелым течением заболевания рассматривают левостороннюю симпатическую денервацию.
Таким образом, вопреки первоначальным предположениям, наследственный синдром удлиненного интервала QT является достаточно распространенным в популяции (1:2500) заболеванием с высоким риском внезапной аритмической смерти. Высокая частота выявления синдрома у лиц, внезапно умерших с недиагностированной при жизни патологией сердца [46], а также обнаружение больных с СУИQT среди жертв синдрома внезапной смерти детей грудного возраста
свидетельствуют о том, что роль СУИQT в структуре ВСС существенно выше, чем предполагалось ранее. Доказана генетическая неоднородность заболевания и повсеместно в экономически развитых странах вошла в повседневную клиническую практику ДНК-диагностика основных молекулярно-генетических вариантов синдрома. В нашей стране этот вопрос пока остается нерешенным и нуждается в серьезном изучении. Кроме того, актуальными являются поиск новых мутаций и диагностика так называемых немых форм патологии. Сопоставление данных генетических исследований с фенотипическими проявлениями различных молекулярно-генетических вариантов синдрома позволило усовершенствовать их диагностику на этапе, предшествующем генотипированию, и тем самым ускорить назначение адекватной терапии. Лечение больных с СУИQT во многих случаях остается трудной задачей, наиболее успешно решенной для больных с LQT1 и LQT2. Необходимы доказательные исследования по эффективности применения антиаритмических препаратов I класса у больных с LQT3. Широкое внедрение в клиническую практику верифицированных критериев диагностики СУИQT, дифференциальной диагностики вариантов синдрома, стратификации риска ВСС и современных методов лечения является одним из направлений в решении глобального вопроса — в профилактике ВСС.



