При определении риска внезапной сердечной смерти (ВСС) у больных, перенесших инфаркт миокарда (ИМ), традиционно в качестве основного фактора рассматривается фракция выброса (ФВ) левого желудочка (ЛЖ). Согласно европейским и отечественным рекомендациям [1, 2], у больных данной категории снижение ФВ ЛЖ менее 30—35% является самостоятельным показанием к имплантации кардиовертера-дефибриллятора (класс Ia) с целью первичной профилактики ВСС. В последние годы при оценке функции ЛЖ также большое внимание уделяется диастолическим нарушениям. О диастолической дисфункции (ДД) в первую очередь судят по изменениям скорости трансмитрального кровотока при эхокардиографии (ЭхоКГ) [3]. Диастолический резерв, определяемый таким образом, характеризует компенсаторные возможности сердца. В 1976 г. E. Braunwald и соавт. высказали предположение, что повышение конечного диастолического давления ЛЖ у больных с хронической сердечной недостаточностью (ХСН) во время приступа стенокардии может быть обусловлено изменениями диастолической функции миокарда, независимо от его сократительной функции [4]. В последующем это подтвердилось результатами исследований, согласно которым диастолические нарушения играют существенную, а часто ведущую роль в гемодинамической картине ХСН при хронических формах ишемической болезни сердца [5, 6]. Недавние исследования также показали прогностическое значение нарушений диастолической функции ЛЖ при ИМ [7, 8]. Так, K. Sakata и соавт. [9] продемонстрировали самую низкую 5-летнюю выживаемость у больных при сниженном пике А по сравнению с его нормальными значениями (р<0,001). F. Nijland и соавт. [10] показали, что рестриктивный тип ДД через 32 мес после ИМ среди множества других клинико-функциональных факторов оказался единственным независимым предиктором ВСС. Вместе с тем вопрос о влиянии ДД на риск развития ВСС у больных, перенесших ИМ, изучен недостаточно. В единичных работах имеется информация о большей частоте ВСС у пациентов с сохраненной ФВ ЛЖ и ДД по сравнению с таковой у пациентов без ДД [11].
Целью настоящего исследования явилось изучение прогностической роли ДД ЛЖ в отношении ВСС у больных, перенесших ИМ.
Материал и методы
Всего в исследование были включены 603 больных ИМ (табл. 1).
Таблица 1. Характеристика обследованных больных (n=603)
Примечание. Здесь и в табл. 3: ИМ — инфаркт миокарда; ГБ — гипертоническая болезнь; СД — сахарный диабет; Q-ИМ — инфаркт миокарда с патологическим зубцом Q на электрокардиограмме; ЛЖ — левый желудочек; ХСН — хроническая сердечная недостаточность; ФК — функциональный класс; NYHA — Нью-Йоркская кардиологическая ассоциация; ФВ — фракция выброса.
На 10—14-й день ИМ всем больным выполняли ЭхоКГ в одномерном, двухмерном и допплеровском режимах. Для анализа диастолической функции ЛЖ использовали традиционный метод оценки трансмитрального кровотока и легочных потоков. Выделяли следующие типы ДД: ригидный, псевдонормальный и рестриктивный [12, 13]. Вариабельность ритма сердца (ВРС) и поздние потенциалы желудочков (ППЖ) определяли на кардиоанализаторе Кардис 310 (Геолинк Электроникс, Москва) с программным обеспечением Ритмон-1М (Биосигнал, Санкт-Петербург). Ритмокардиограммы регистрировали в течение 5 мин в горизонтальном положении больного в покое, а также во время вегетативных проб: проба с глубоким дыханием и активная ортостатическая проба [14]. Оценку ВРС осуществляли в соответствии с международными стандартами [15]; кроме того, использовали процентный вклад спектральных величин в общую мощность спектра: %LF, %HF, %VLF. ППЖ определяли с помощью электрокардиографии высокого разрешения по стандартной методике, утвержденной в 1991 г. международными экспертами [16].
Исследование чувствительности кардиохронотропного компонента артериального барорефлекса (ЧБР) осуществляли в соответствии с «Оксфордским методом» на фоне внутривенного капельного введения нитроглицерина (0,1% раствор со скоростью 20 мкг/мин) [17]. Оценивали степень уменьшения интервалов RR в ответ на снижение среднего артериального давления. Итоговый показатель ЧБР рассчитывали как средний из трех измерений.
Проспективное наблюдение осуществляли в сроки от 1 года до 7 лет (средняя длительность наблюдения 2,9 года), все больные проходили ежегодное повторное обследование. В случае летального исхода информацию об обстоятельствах смерти получали от родственников пациента и из медицинской документации (патологоанатомические заключения, амбулаторные карты, посмертные справки).
Обработку полученных результатов исследований проводили с использованием параметрических и непараметрических методов: однофакторный дисперсионный анализ, критерий Крускала—Уоллиса, корреляции Пирсона (r) и Спирмена (ρ). Анализ качественных признаков проводили на основе построения таблиц сопряженности. Для оценки выживаемости пациентов после ИМ строили кривые выживаемости Каплана—Мейера. Для оценки риска ВСС применяли регрессионный анализ пропорционального риска Кокса [18].
Результаты и обсуждение
По результатам однофакторного регрессионного анализа Кокса, проведенного на всей выборке, было выявлено, что среди показателей ЭхоКГ, влияющих на риск ВСС, наряду с такими показателями как гипертрофия левого желудочка (ГЛЖ), диаметр левого предсердия (ЛП), конечный диастолический размер (КДР) ЛЖ, конечный систолический размер (КСР) ЛЖ, ФВ ЛЖ оказалась и ДД (табл. 2).
Таблица 2. Относительный риск некоторых эхокардиографических показателей для ВСС в модели пропорционального риска Кокса
Примечание. ЛП — левое предсердие; ДД — диастолическая дисфункция; ГЛЖ — гипертрофия левого желудочка; КСР — конечный систолический размер; ЛЖ — левый желудочек; КДР — конечный диастолический размер; ФВ — фракция выброса; ОР — относительный риск; ДИ — доверительный интервал; ВСС – внезапная сердечная смерть.
Следует отметить, что при проведении многофакторного регрессионного анализа Кокса, в который включали не только показатели ЭхоКГ, но и клинико-эпидемиологические данные (всего 135 параметров), ДД не вошла в число факторов, независимо влияющих на риск ВСС, так как была «поглощена» более мощными предикторами. К ним относились острая левожелудочковая недостаточность III—IV по Killip (β=1,09; отношение рисков (ОР) 2,99 при 95% доверительном интервале (ДИ) от 1,44 до 6,18; ρ=0,003), КДР ЛЖ (β=0,05; ОР 2,46 при 95% ДИ от 1,07 до 2,68; р=0,02), ФВ ЛЖ (β=–0,03; ОР 1,63 при 95% ДИ от 0,40 до 1,75; ρ=0,05), зоны акинезии ЛЖ (β=–0,88; ОР 2,42 при 95% ДИ от 1,30 до 5,41; ρ=0,006).
Вместе с тем при анализе смертности в зависимости от типа нарушений диастолической функции установлено, что при рестриктивном типе частота ВСС была достоверно (ρ=0,002) выше (16,7%), чем среди пациентов, у которых определялся нерестриктивный тип (5,0%) или не было нарушений диастолической функции (7,5%). При построении кривых выживаемости Каплан—Мейера (рис. 1) подтверждено, что выживаемость больных с рестриктивным типом ДД также была достоверно ниже, чем у больных с нерестриктивным типом и без ДД. Поэтому представляло интерес изучить прогностическое значение ДД в отношении ВСС, тем более что в конечную прогностическую модель вошли такие параметры, как КДР ЛЖ и зоны акинезии, которые влияют на диастолическую функцию ЛЖ.
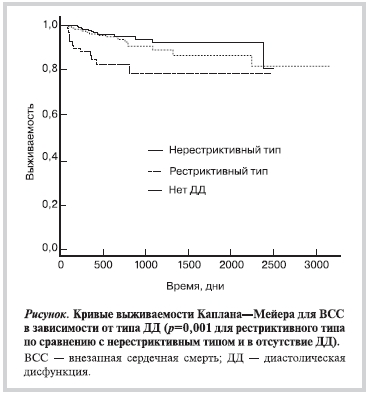
Для дальнейшего анализа использовали результаты обследования пациентов с сохранной систолической функцией ЛЖ. В зависимости от типа ДД были выделены 3 группы: 1-я — пациенты без ДД (n=250; 45,4%), 2-я — пациенты с нерестриктивным типом ДД, которая включала ригидный и псевдонормальный варианты ДД (n=242; 43,9%), 3-я — пациенты с рестриктивным типом ДД (n=59; 10,7%).
При оценке клинико-функциональных показателей в зависимости от типа ДД выявлено, что пациенты, у которых определялась ДД, были старше, в то время как различий по полу, локализации и формированию зубца Q при ИМ, а также наличию сахарного диабета, перенесенного ранее ИМ, развитию рецидива и ранней постинфарктной стенокардии не получено (табл. 3). У пациентов с рестриктивным типом ДД по сравнению с пациентами без ДД или с ее нерестриктивным вариантом течение ИМ достоверно чаще осложнялось развитием ХСН. Следует отметить высокую частоту регистрации ГЛЖ при рестриктивном типе ДД. Таким образом, полученные данные свидетельствуют о более выраженных структурно-функциональных изменениях при рестриктивном типе ДД.
Таблица 3. Сравнительная характеристика пациентов в зависимости от типа ДД ЛЖ
Примечание. РПС — ранняя постинфарктная стенокардия.
Представлялось важным понять, путем каких механизмов ДД могла способствовать развитию ВСС. Мы проанализировали взаимосвязь ДД с такими известными предикторами ВСС, как желудочковые нарушения ритма (ЖНР), ППЖ, снижение ВРС и ЧБР. Так, желудочковая экстрасистолия III—V класса по Lown (по результатам суточного мониторирования электрокардиограммы) у больных с рестриктивным типом ДД встречалась достоверно (ρ=0,004) чаще (в 63,0% случаев), чем у больных с нерестриктивным типом ДД (35,4%) и без нарушений диастолической функции (29,1%). Различий по частоте выявления ППЖ в зависимости от типа ДД не выявлено: ППЖ регистрировались у 23,2% больных без ДД, при нерестриктивном типе у 25,6%; при рестриктивном — у 28,8%. В литературе снижение прогностической ценности ППЖ при ИМ объясняется более широким использованием в последние годы ранней реперфузионной терапии [19].
Известно, что у всех больных, перенесших ИМ, находят нарушения ВРС, заключающиеся в снижении общей изменчивости синусового ритма и повышении симпатических влияний [20, 21]. Ранее мы описали связь ВРС и ФВ ЛЖ [22], которая заключалась в том, что по мере нарастания систолической дисфункции увеличивался вегетативный дисбаланc; вклад ДД нами не рассматривался. Поэтому представляло интерес изучить изменения ВРС при ДД. В связи с этим мы сравнили ВРС у больных с ДД без нарушения систолической функции, с ВРС у пациентов без нарушений как систолической, так и диастолической функции. При этом выявлено (табл. 4), что при ДД общая изменчивость синусового ритма была достоверно меньше, о чем свидетельствовали показатели SD и TP. В то же время нарушения вегетативного баланса у этих больных были более выраженными, причем преимущественно за счет более значительного снижения парасимпатической активности (NN50, PNN50).
Таблица 4. Показатели ВРС в покое у больных с ДД
Примечание. ВРС — вариабельность ритма сердца; nu — нормализованные единицы; нд — недостоверно.
В литературе нам встретились лишь несколько работ, в которых оценивались изменения ВРС при ДД [23]. В них также указывается на нарушения вегетативного баланса у больных с ДД, причем наиболее выраженные изменения, заключающиеся в повышении симпатических влияний, отмечены у больных с рестриктивным вариантом ДД. В отличие от цитируемых авторов, мы имели возможность оценить не только временны`е, но и спектральные показатели ВРС. Они убедительно свидетельствовали не только о повышении симпатической активности у больных с ДД, но и о снижении вагусной активности, что было подтверждено также результатами пробы с глубоким дыханием, направленной на изучение именно парасимпатического отдела вегетативной нервной системы: SD при ДД 36,0±24,3 мс против 43,3±21,3 мс (ρ<0,05); ТР при ДД — 2011,5±1466,4 мс² против 2443,6±2157,4 мс² (ρ<0,05).
Эти данные представляются особенно важными, так как не только повышение влияния симпатического отдела вегетативной нервной системы, но и снижение защитного вагусного действия чаще всего рассматриваются в качестве триггера злокачественных ЖНР. Таким образом, результаты изучения ВРС показали, что при ДД имеются нарушения вегетативного баланса, способствующие развитию угрожающих жизни аритмий. Вероятно, это объясняется тем, что развивающиеся при ИМ структурные изменения миокарда приводят как к возникновению повышенной «жесткости» последнего (что способствует ДД), так и к возникновению зон вегетативной денервации. Это приводит, с одной стороны, к нарушению вегетативной регуляции, а с другой — к увеличению чувствительности к симпатическим влияниям. Проведенный корреляционный анализ также подтвердил взаимосвязь ДД с такими прогностическими факторами, как ЖНР (ρ=0,5; ρ<0,5) и ВРС (для RR ρ=–0,5; ρ<0,05; для SD ρ=0,4; ρ<0,05).
Другим важным показателем, характеризующим вегетативный дисбаланс, является сниженная ЧБР. По данным крупных исследований [24, 25], этот показатель по прогностической значимости в отношении ВСС у больных, перенесших ИМ, был сравним с ФВ ЛЖ и превосходил ВРС. По нашим данным, ЧБР у обследованных больных в 1-е сутки ИМ также снижалась [17] и были выявлены умеренные, но достоверные корреляции ЧБР с ДД (ρ=–0,4; р<0,05) и размерами ЛП (r=–0,4; ρ<0,05). К 10—14-м суткам достоверных корреляций не выявлено.
Следует отметить, что такой показатель, как артериальная гипотензия при активной ортостатической пробе (снижение артериального давления — АД на 20 мм рт.ст. и более на 3-й минуте ортостаза), который, по данным наших предыдущих работ [26], оказался в числе значимых факторов риска ВСС, также имел корреляции с рестриктивной ДД (ρ=0,5; ρ<0,05) и размерами ЛП (r=0,9; ρ<0,05). Мы считаем, что результаты активной ортостатической пробы косвенно отражают чувствительность артериального барорефлекса.
Вероятно, полученные данные в определенной степени могут свидетельствовать о том, что процессы апоптоза имеют значение для формирования ДД у больных ИМ.
Заключение
Несмотря на то что настоящая работа имеет определенные ограничения (определение диастолической дисфункции проводили только традиционным методом по оценке трансмитрального кровотока, диастолические нарушения не исследованы до развития инфаркта миокарда), полученные данные свидетельствуют о том, что у больных, перенесших инфаркт миокарда, диастолическая дисфункция повышает риск внезапной смерти. Известно, что для развития фатальных аритмий у больных ишемической болезнью сердца необходимо наличие двух главных факторов: структурных изменений в миокарде и пусковых механизмов. Как показали полученные результаты, у больных с диастолической дисфункцией, особенно при ее рестриктивном варианте, были более выражены признаки, отражающие структурные изменения в миокарде. В то же время в качестве триггера угрожающих жизни аритмий могли выступать чаще встречающиеся при диастолической дисфункции желудочковые нарушения ритма и более выраженные явления вегетативного дисбаланса.
Таким образом, по результатам настоящего исследования фракция выброса левого желудочка оказалась независимым предиктором внезапной сердечной смерти, что соответствует данным литературы. Вместе с тем нельзя недооценивать неблагоприятное прогностическое влияние диастолической дисфункции и не учитывать ее при стратификации риска внезапной сердечной смерти у больных, перенесших инфаркт миокарда.



