Cиндром Вольфа—Паркинсона—Уайта (WPW) — сочетание электрокардиографического феномена, иллюстрирующего предвозбуждение желудочков сердца по дополнительному (аномальному) атриовентрикулярному соединению (ДАВС) и пароксизмальной атриовентрикулярной реципрокной (re-entry) тахикардии (АВРТ), возникающей в результате реализации механизма повторного входа электрического возбуждения, структурными составляющими компонентами которого являются врожденное ДАВС, атриовентрикулярное соединение, миокард предсердий и миокард желудочков [1].
Синдром WPW выявляется во всех возрастных группах, его распространенность в общей популяции колеблется от 0,15 до 0,25%, причем у больных с врожденными пороками сердца она несколько выше — 0,5%. Соотношение между мужчинами и женщинами составляет 3:2. В большинстве случаев клинические проявления синдрома WPW возникают в молодом возрасте (от 10 до 20 лет) и гораздо реже — у лиц старшей возрастной группы [1—4].
Принято считать, что АВРТ при синдроме WPW является патогномичной относительно доброкачественной аритмией, не сопровождающейся структурной патологией миокарда и изменениями показателей центральной гемодинамики. Однако известно, что у пациентов с тахиаритмиями с высокой частотой сердечных сокращений (ЧСС) на фоне пароксизмов тахикардии может возникнуть сначала диастолическая, а затем и систолическая дисфункция миокарда с последующим развитием дилатационной (аритмогенной) кардиомиопатии и, в конечном итоге, сердечной недостаточности, что повышает риск развития тромбоэмболических осложнений [2—4].
Ухудшение клинического течения АВРТ у больных с синдромом WPW в ряде случаев отмечается при присоединении трепетания предсердий и/или фибрилляции предсердий (ФП). При этом возникает риск развития желудочковой тахикардии и/или фибрилляции желудочков, обусловленных развитием предсердно-желудочкового проведения 1:1 с частотой до 340 в минуту [1—3, 5, 6]. Вероятность подобного развития событий у пациентов данной категории в течение 10 лет наблюдения составляет от 0,15 до 0,39%, что выше общепопуляционного риска развития фибрилляции желудочков и внезапной сердечной смерти [2, 7].
В настоящее время радиочастотная катетерная абляция (РЧА) ДАВС в виду своей высокой эффективности и безопасности является методом выбора при лечении больных с АВРТ и единственным противопоказанием к ее проведению является предпочтение больным приема антиаритмических препаратов и нежелание выполнять эту процедуру [1, 15]. Первичная эффективность РЧА ДАВС при синдроме WPW составляет 95%. Повторные сессии РЧА, как правило, позволяют достигнуть показателей абсолютной эффективности при лечении этого заболевания. Выполнение интервенционного вмешательства ассоциируется со значительным улучшением параметров качества жизни пациентов и не требует в дальнейшем проведения антиаритмической терапии [1, 8—11].
Является ли улучшение качества жизни пациентов с синдромом WPW следствием обратимости структурного аритмогенно-обусловленного ремоделирования миокарда вследствие эффективного лечения методом РЧА, неизвестно. В этой связи нам представляются актуальными оценка центральной гемодинамики методом трансторакальной эхокардиографии (ЭхоКГ) у пациентов с синдромом WPW в межприступном периоде до проведения РЧА ДАВС, а также динамическая оценка изучаемых параметров в течение года после выполнения операции в условиях клинического мониторирования данной группы пациентов.
Целью настоящего исследования явилось изучение морфофункциональных характеристик миокарда методом трансторакальной ЭхоКГ у пациентов с синдромом WPW и оценка изменений изучаемых показателей до и в течение года после РЧА ДАВС в сравнении их с аналогичными параметрами у лиц контрольной группы.
Материал и методы
Клиническая характеристика пациентов. Под нашим наблюдением находились 160 пациентов, которые были разделены на 2 группы: основную и клинического сравнения. Основную группу составили 140 (87,5%) пациентов с синдромом WPW, из них 114 (81,4%) мужчин, 26 (18,6%) женщин, средний возраст 39,5±15,3 года. В группу клинического сравнения вошли 20 практически здоровых лиц: 15 (75,0%) мужчин, 5 (25,0%) женщин, средний возраст 41,9±5,3 года, у которых в результате проведенного нами обследования не было выявлено структурной патологии сердечно-сосудистой системы. Обе группы были сопоставимы по возрасту и полу.
Аритмический анамнез составил 10,7±8,5 года. У 22,9% больных приступы аритмии возникали после физического или эмоционального перенапряжения; в 3,5% случаев была выявлена четкая связь с употреблением алкоголя. В большинстве случаев конкретные факторы, провоцирующие возникновение аритмии не были выявлены. Средняя ЧСС на фоне пароксизма АВРТ составила 169±12 уд/мин. Основными жалобами пациентов во время приступа АВРТ являлись ощущения приступообразных, ритмичных сердцебиений и замирания в области сердца, начинавшиеся и заканчивавшиеся внезапно. Нередко клиническая картина была представлена сочетанием нескольких симптомов. Реже приступы сопровождались развитием предобморочных состояний и обмороков, кардиалгией, ощущением нехватки воздуха (табл. 1) [1, 2, 8, 10].
Таблица 1. Клинические характеристики пациентов с синдромом WPW (n=140)
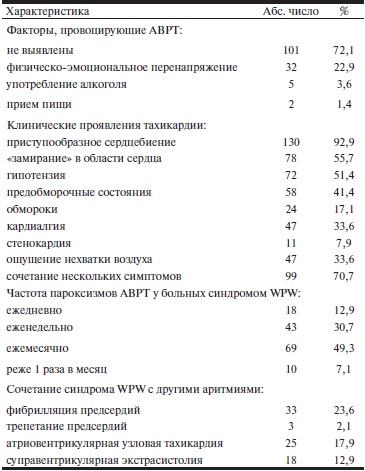
Примечание. WPW — синдром Вольфа—Паркинсона—Уайта; АВРТ — атриовентрикулярная реципрокная тахикардия.
Как представлено в табл. 1, в большинстве случаев приступы АВРТ возникали ежемесячно. У 56,4% пациентов синдром WPW сочетался с другими аритмиями, такими как ФП (23,6%), атриовентрикулярная узловая реципрокная тахикардия (АВУРТ) (17,9%), суправентрикулярная экстрасистолия (12,9%), трепетание предсердий (2,1%).
Приступ аритмии мог продолжаться от нескольких секунд до нескольких часов и купироваться самостоятельно или с помощью рефлекторных приемов. В 82,9% случаев пароксизмы АВРТ были затяжные, продолжались в течение нескольких часов и обусловливали необходимость врачебного вмешательства [2, 4, 8, 10].
У 72,1% пациентов синдром WPW был манифестирующим, у 27,9% пациентов — скрытым (табл. 2). В группе с манифестирующим синдромом WPW левосторонняя локализация ДАВС была верифицирована у 38,6% пациентов, правосторонняя локализация ДАВС — у 6,4%, септальная — у 27,1%. Среди пациентов со скрытым синдромом WPW левосторонние ДАВС выявлялись у 56,4%, септальные — у 17,9%, правосторонние — у 25,6%.
Таблица 2. Локализация дополнительного атриовентрикулярного соединения у обследованных больных (n=140)
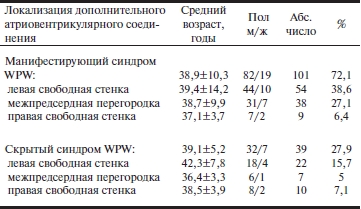
Примечание. По возрасту и полу группы (манифестирующий и скрытый синдром WPW) и подгруппы в этих группах (локализация ДАВС) были сопоставимы. WPW — синдром Вольфа—Паркинсона—Уайта; ДАВС — дополнительное атриовентрикулярное соединение.
Всем пациентам после получения письменного согласия и отмены антиаритмических препаратов (за 6 периодов полувыведения) было выполнено эндокардиальное электрофизиологическое исследование (эндоЭФИ) и РЧА ДАВС. В послеоперационном периоде антиаритмическая терапия (ААТ) не назначалась.
Методика эндоЭФИ и РЧА. Под местной анестезией 60 мл 0,5% раствора новокаина по методике Сельдингера выполняли пункцию левой подключичной вены, правой и левой общей бедренной вен. В левую общую бедренную вену устанавливали интродъюсер трипорт диаметром 12 Fr. В правую общую бедренную вену, в левую подключичную вену устанавливали интродъюсеры диаметром 8 Fr. Через интродъюсер трипорт диаметром 14 Fr вводили 3 диагностических электрода, которые устанавливали в верхнелатеральном отделе правого предсердия, области пучка Гиса и верхушке правого желудочка (ПЖ). Через подключичный интродъюсер диаметром 8 Fr вводили диагностический электрод, который устанавливали в коронарном синусе (10-полюсный электрод).
Протокол эндоЭФИ у пациентов с АВРТ включал в себя определение значений антероградного и ретроградного эффективных рефрактерных периодов АВС и ДАВС, величины антероградной точки Венкебаха, режима индукции и купирования тахикардии, методику введения синхронизированного желудочкового экстрастимула из верхушки ПЖ, парагисиальную стимуляцию для верификации и дифференциальной диагностики с другими видами тахиаритмий. При отсутствии индукции АВРТ протокол эндоЭФИ повторяли после внутривенного введения атропина сульфата в дозе 0,02—0,04 мг/кг массы тела больного.
После подтверждения диагноза синдрома WPW и уточнения локализации ДАВС переходили к следующему этапу операции — РЧА ДАВС.
Область интереса для нанесения эффективной РЧ-аппликации определяли на основании данных активационного картирования на фоне синусового ритма, АВРТ, и/или асинхронной желудочковой стимуляции. При достижении оптимального позиционирования и стабилизации абляционного электрода наносились РЧ-воздействия.
При использовании конвенционного абляционного электрода у 110 (78,6%) больных применяли следующие параметры РЧА: средняя мощность — 45±5 Вт, средняя температура –50±5 °С. У 30 (21,4%) пациентов указанные действия не приводили к эффективной РЧА ДАВС. В этих случаях дополнительно использовали орошаемые абляционные электроды с предустановленным лимитом по мощности и температуре 40 Вт и 43 °С соответственно.
Для проведения РЧА левосторонних ДАВС применяли трансаортальный ретроградный доступ у 64 (84,2%) пациентов и транссептальный доступ у 12 (15,8%) пациентов.
Методика изучения параметров центральной гемодинамики у больных с синдромом WPW. Для комплексного изучения параметров центральной гемодинамики в обеих группах применяли трансторакальную ЭхоКГ, которую проводили на аппаратах ACUSON 512 SEQUOIA (ACUSON, США) и Vivid-3 (GE, США). Обследование выполняли в М-режиме, 2D-режиме, PW, в режиме CW (цветового допплеровского картирования кровотока). ЭхоКГ выполняли в положении больного лежа на левом боку по общепринятой методике. Для получения изображений использовали парастернальный доступ в третьем—четвертом межребере слева от грудины (по длинной и короткой оси сердца) и апикальный доступ в области максимального верхушечного толчка. Для вычисления размеров и объемов левого желудочка (ЛЖ) помимо парастернальной позиции по длинной оси использовали двухкамерную и четырехкамерную апикальные позиции. Обработка изображений проводилась с помощью специального пакета программ для кардиологических расчетов, установленного на соответствующем ультразвуковом аппарате. Анализировали следующие параметры: конечный диастолический диаметр (КДД) ЛЖ, конечный систолический диаметр (КСД) ЛЖ, конечный диастолический объем (КДО) ЛЖ, конечный систолический объем (КСО) ЛЖ, фракция выброса (ФВ) ЛЖ по формуле Тейхольца, систолодиастолическое укорочение (СДУ) ЛЖ, конечный диастолический диаметр (КДД) ПЖ, размер левого предсердия (ЛП).
Пациентам группы исследования ЭхоКГ проводили на фоне синусового ритма до РЧА ДАВС и через 2, 6 и 12 мес после нее, а пациентам контрольной группы — однократно.
Статистическую обработку результатов исследования выполняли с помощью пакета программ Statistica 6.0 for Windows. Для оценки количественных показателей применяли непараметрические критерии Вилкоксона, Ньюмена—Кейлса. Данные представлены в виде среднего значения ± стандартное отклонение. Различия считали статистически значимыми при р<0,05.
Результаты
Эффективность РЧА за 1 год наблюдения составила 85,7%. Рецидив АВРТ в течение года наблюдения отмечался у 20 (14,3%) больных. Проведение этим больным повторных РЧА ДАВС позволило добиться стойкого прекращения проведения по ДАВС во всех случаях.
В ближайшем послеоперационном периоде у одного (0,7%) больного сформировалась ложная аневризма бедренной артерии, потребовавшая проведения хирургического вмешательства — ушивание дефекта сосудистой стенки. Других осложнений от проведенного лечения методом РЧА ДАВС не отмечено.
У 83% пациентов приступы аритмии были затяжные, продолжались в течение нескольких часов и обусловливали необходимость врачебного вмешательства для купирования (см. табл. 1). Нами установлено, что аритмический синдром в большинстве случаев характеризовался выраженной гемодинамической значимостью (гипотензия — 51,4%, предобморок — 41,4%, обморок — 17,1%), вероятно, в связи с выраженностью тахисистолии (средняя ЧСС во время пароксизма АВРТ 169±11 уд/мин). Анализ клинических характеристик пациентов исследуемой группы показал, что у 25,7% пациентов была диагностирована структурная патология системы органов кровообращения, в том числе гипертоническая болезнь в 21,4% случаев, ишемическая болезнь сердца (ИБС) — в 7,9%, аномалия Эбштейна — в 0,7%. Тем не менее, у этих больных отсутствовали выраженные признаки аритмогенно-обусловленного структурного ремоделирования миокарда.
Оценка параметров ЭхоКГ у больных с синдромом WPW до РЧА ДАВС и через 2, 6 и 12 мес после нее. Анализ параметров центральной гемодинамики, изученных методом трансторакальной ЭхоКГ у 140 больных с синдромом WPW до и через 2, 6 и 12 мес после РЧА ДАВС, продемонстрировал, что до выполнения хирургического вмешательства не было выявлено достоверных различий в изучаемых параметрах по сравнению с аналогичными характеристиками группы сравнения (табл. 3).
Таблица 3. Показатели центральной гемодинамики у больных синдромом WPW до оперативного лечения методом РЧА ДАВС и пациентов группы клинического сравнения*
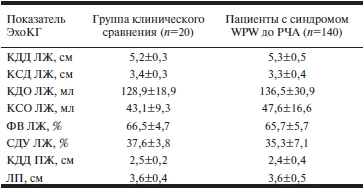
Примечание. * — р>0,05 для всех сравнений. ЭхоКГ — эхокардиография; РЧА — радиочастотная абляция; ДАВС — дополнительное атриовентрикулярное соединение; ЛЖ — левый желудочек; КДД — конечный диастолический диаметр; КСД — конечный систолический диаметр; КДО— конечный диастолический объем; КСО — конечный систолический объем; ФВ — фракция выброса; СДУ — систолодиастолическое укорочение; ПЖ — правый желудочек; ЛП — левое предсердие.
За весь период наблюдения (2, 6 и 12 мес после выполненной РЧА ДАВС) у больных с синдромом WPW изучаемые параметры центральной гемодинамики не претерпели существенных изменений по сравнению с исходными характеристиками (рис. 1, 2).
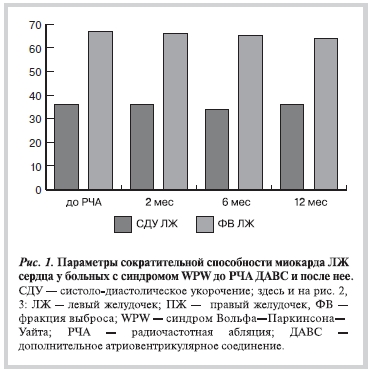
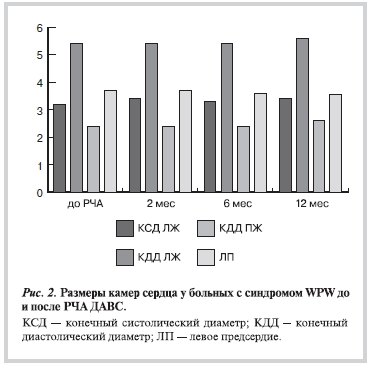
Ни в одном случае не было выявлено локальных нарушений кинетики миокарда, изменений клапанного аппарата и подклапанных структур сердца, которые можно было бы связать с проведенным хирургическим лечением.
«Малые аномалии» развития соединительной ткани сердца у пациентов с синдромом WPW. В ходе ЭхоКГ у пациентов с синдромом WPW так называемые малые аномалии развития соединительной ткани сердца были диагностированы у 69 (49,3%) пациентов. Самым распространенным из них являлось наличие добавочной хорды, которая диагностировалась в 25 (35%) случаев. Кроме того, были верифицированы такие аномалии развития соединительной ткани, как пролапс митрального клапана (n=23), пролапс трикуспидального клапана (n=3), повышенная трабекулярность (n=10), удлиненная заслонка евстахиева клапана (n=6) (рис. 3), открытое овальное окно (n=2).
В табл. 4 представлен спектр «малых» аномалий сердца, верифицированных у пациентов группы клинического сравнения и больных с синдромом WPW.
Таблица 4. Наличие «малых аномалий» сердца у пациентов группы клинического сравнения и больных с синдромом WPW
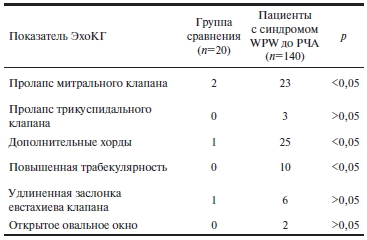
У пациентов с синдромом WPW достоверно чаще встречались пролапс митрального клапана, дополнительные хорды ЛЖ, повышенная трабекулярность. Ни у одного из обследуемых нами больных с синдромом WPW не было выявлено ни тромбов в камерах сердца, ни феномена спонтанного эхоконтрастирования, хотя у 23 (16,4%) из них была диагностирована пароксизмальная форма ФП, которую мы рассматривали как вторичную по отношению к синдрому WPW. После проведения РЧА ДАВС у пациентов с вторичной ФП в последующий период наблюдения аритмия не рецидивировала и не требовала назначения ААТ.
Нам не удалось выявить достоверные различия показателей ЭхоКГ у больных с синдромом WPW в зависимости от электрофизиологических свойств ДАВС (скрытый, манифестирующий) и от локализации ДАВС (правый, левый, септальный).
Обсуждение
Современный тактический подход к лечению пациентов с синдромом WPW основан на результатах нескольких крупных многоцентровых исследований, посвященных клинической оценке эффективности и безопасности РЧА ДАВС в ближайшем и отдаленном периодах наблюдения. Динамическое наблюдение за этой категорией пациентов продемонстрировало, что эффективность РЧА ДАВС составляет 95%, частота развития осложнений не превышает 5% (включая развитие полной атриовентрикулярной блокады, тампонады сердца, формирование артериовенозной фистулы и др.) [1—2, 8—12]. Кроме того, интервенционное вмешательство, как правило, ассоциируется со значительным улучшением параметров качества жизни пациентов и не требует проведения поддерживающей ААТ [8, 10, 15]. Однако дизайн подобных исследований не включал проведение трансторакальной ЭхоКГ у пациентов с синдромом WPW в межприступном периоде до и после РЧА ДАВС.
В выполненной нами работе, включавшей в комплексное обследование пациентов трансторакальную ЭхоКГ, было продемонстрировано, что у большинства пациентов пароксизмы АВРТ были затяжные, сопровождались серьезными нарушениями центральной гемодинамики (артериальная гипотензия, предобморочные состояния, стенокардия), продолжались в течение нескольких часов и, как правило, требовали врачебного вмешательства. Возможным объяснением такого клинического варианта течения АВРТ, являются возраст наших больных (около 40 лет), давность аритмии (анамнез АВРТ около 10 лет) и/или высокая ЧСС на фоне аритмического эпизода (средняя 169 уд/мин). Однако структурная патология сердца для этой категории пациентов скорее не была характерна (выявлялась только у ¼ пациентов). Сходные результаты были также нами получены в сопоставимой по возрасту группе пациентов с типичной формой АВУРТ [12].
При сравнительном анализе ЭхоКГ-параметров центральной гемодинамики больных с синдромом WPW со здоровыми добровольцами нами установлено, что на фоне синусового ритма отсутствуют достоверные различия по основным морфофункциональным характеристикам сердца. Исключение составляют «малые» аномалии сердца. Практически у каждого второго пациента c синдромом WPW трансторакальная ЭхоКГ позволила визуализировать «малые аномалии» развития соединительной ткани сердца (пролапс митрального клапана, удлиненная заслонка нижней полой вены, ложные хорды желудочков и др.), которые следует трактовать в рамках синдрома дисплазии соединительной ткани. Полученные нами данные согласуются с результатами обследования группы больных пароксизмальными реципрокными тахикардиями (АВУРТ и АВРТ), проведенного M. Josephson и соавт., в котором было показано, что признаки дисплазии соединительной ткани (пролапс митрального клапана, ложные хорды ЛЖ, бикуспидальная аорта) верифицируются у 40—60% больных с реципрокными тахикардиями. Тем не менее авторы считают, что сама аритмия (АВУРТ или АВРТ) не является признаком дисплазии соединительной ткани [13].
В настоящий момент отсутствуют убедительные данные о том, что «малые аномалии» развития соединительной ткани сердца у больных с АВРТ при синдроме WPW влияют на клиническое течение аритмии и отдаленный прогноз. Полученные нами данные не позволяют утверждать, что наличие или отсутствие «малых аномалий» сердца определяет выраженность клинических проявлений АВРТ при синдроме WPW, по крайней мере, в исследованной нами возрастной группе пациентов с 10-летним аритмическим анамнезом АВРТ. Следует подчеркнуть, что несмотря на 10-летний анамнез аритмии в исследуемой нами выборке, выраженность гемодинамического компромисса на фоне приступов (гипотензия — 51,4%, предобморочные состояния — 41,4%, обмороки 17,1%, одышка — 33,6%, сочетание симптомов — 70,7%) нами не было выявлено достоверных различий в изучаемых морфофункциональных характеристиках миокарда между больными с синдромом WPW и здоровыми лицами ни до, ни после лечения методом РЧА. Можно предположить, что это положение будет дискутабельным по мере увеличения возраста больных с синдромом WPW и длительности их аритмического анамнеза.
Локализация ДАВС и их электрофизиологические свойства, а также наличие вторичных аритмий (ФП у 23,6% пациентов) по нашим данным также не имеют взаимосвязи с наличием или отсутствием «малых аномалий» развития соединительной ткани. Тем не менее, их верификация с помощью ЭхоКГ требует от лечащего врача, по крайней мере, настороженного отношения к пациентам этой категории [14—16].
Все перечисленное позволяет рассматривать АВРТ при синдроме WPW как относительно доброкачественную аритмию. Полученные результаты мы представляем как научное обоснование общепринятого мнения об относительной доброкачественности клинического течения синдрома WPW, накопленного эмпирическим опытом. Как известно, выраженный гемодинамический компромисс на фоне аритмического синдрома у пациентов этой категории (гипотензия, обморок, предобморок, головокружение, стенокардия, нарастание проявлений хронической сердечной недостаточности) не является предиктором риска развития неблагоприятных кардиальных исходов. Возможное исключение составляют клинические случаи сочетания врожденного синдрома WPW с присоединившимися структурными заболеваниями миокарда (например, ИБС). Однако анализировать исходы клинического течения синдрома WPW в данной подгруппе пациентов нам не представлялось возможным в связи с ее немногочисленностью.
Очевидно, что РЧА ДАВС является щадящим, малотравмирующим методом, который не приводит к дилатации камер сердца и снижению его инотропной функции, не наносит повреждение клапанным и подклапанным структурам, а также не сопровождается тромбообразованием в камерах сердца. Данные факты подтверждены отсутствием достоверных различий в показателях центральной гемодинамики у больных с синдромом WPW и группы здоровых добровольцев на протяжении 12-месячного клинического мониторирования после успешного интервенционного лечения.
Заключение
Изученные методом трансторакальной эхокардиографии морфофункциональные характеристики миокарда у пациентов с синдромом Вольфа—Паркинсона—Уайта сопоставимы с аналогичными параметрами здоровых лиц и остаются без изменений в течение одного года наблюдения после проведения операции радиочастотной абляции дополнительного атриовентрикулярного соединения.
Клиническое мониторирование и оценка морфофункциональных характеристик миокарда у больных с синдромом Вольфа—Паркинсона—Уайта на протяжении года после эффективного интервенционного лечения аритмии методом радиочастотной абляции свидетельствует о его безопасности и малой травматичности, что позволяет считать его методом выбора в лечении пациентов с этой патологией.



