В современной аритмологии катетерная радиочастотная абляция (РЧА) является наиболее перспективным и стремительно развивающимся методом лечения фибрилляции предсердий (ФП) [1, 2]. В 2009 г. были опубликованы результаты выполненных в 90 центрах по всему миру РЧА, полученные при лечении более 16 000 пациентов с ФП; эти результаты свидетельствуют о том, что эффективность процедуры составляет от 71 до 84% [3]. Наиболее часто в клинической практике для лечения пароксизмальной и персистирующей форм ФП используются методики остиальной радиочастотной (РЧ-) изоляции устьев легочных вен (УЛВ) с использованием катетера LASSO и периметрической РЧА с использованием систем нефлюороскопического картирования, доля которых составляет соответственно 27 и 48% [3]. Характеристики эффективности РЧА у пациентов с пароксизмальной формой ФП при использовании остиальной изоляции УЛВ и периметрической абляции достоверно не различаются [3]. Тем не менее, обращает внимание практически двукратное превосходство использования методики нефлюороскопического картирования у больных с мерцательной аритмией (МА). Данный факт, вероятно, объясняется ее более высокой эффективностью по сравнению с остиальной РЧА в отдаленном периоде наблюдения, что продемонстрировано в ряде клинических исследований [4, 5].
В настоящее время выбор той или иной методики РЧА у больных с ФП в большей степени основан на эмпирическом подходе и определяется зачастую клиническим опытом и предпочтением оперирующего хирурга и/или традициями клинического центра. Существующее научное обоснование интраоперационной тактики нанесения РЧ-воздействий не является исчерпывающим и не удовлетворяет требованием времени. Отчасти это может быть связано с относительной новизной данного клинического метода лечения ФП (первые клинические работы датируются 1996 г. [6]). Ключевое же значение, на наш взгляд, принадлежит патогенезу МА предсердий, который едва ли можно считать достаточно ясным и полностью изученным. Очевидно также, что ФП у каждого отдельного больного имеет яркие индивидуальные особенности с точки зрения как патогенеза, так и клинической значимости. В этой связи следует признать, что унифицированный подход к РЧА при ФП не существует (и едва ли будет сформирован в ближайшем будущем). Попытки же научно обосновать тот или иной вариант нанесения РЧ-воздействий при лечении ФП, доказать право на его существование в условиях высокотехнологичного интервенционного вмешательства, безусловно, оправданы.
Возможность теоретического обоснования эффективности РЧА, по нашему мнению, находится на стыке специальностей, в частности клинической аритмологии и математики. Нам представляется, что использование математической модели ФП в виде автоволновых процессов в двумерной активной среде с использованием методики сканирования с учетом геометрии предсердий и последующим проведением абляционного форматирования (АФ) с помощью создания невозбудимых линий, имитирующих лечебные РЧ-воздействия, позволит определить оптимальный методический подход к проведению РЧА при МА в повседневной клинической практике, в конечном итоге приблизиться к унификации РЧА при ФП.
Цель исследования — сравнение теоретических возможностей элиминации ФП (на модели четырехволнового re-entry) в условиях математического моделирования с использованием методики сканирования при выполнении циркулярных и линейных воздействий, имитирующих лечебные РЧ-повреждения у больных с ФП и сопоставить полученные результаты с клиническими данными.
Материал и методы
Дефиниции. Существующая методика проведения РЧА в левом предсердии (ЛП) при лечении ФП предполагает последовательное нанесение РЧ-воздействий в различных областях интереса (периметр УЛВ, свод ЛП, митральный перешеек и т.д.). Строго говоря, любая РЧ-аппликация приводит к развитию локального повреждения участка миокарда диаметром около 5 мм, где развивается асептический некроз и становится невозможным проведение электрического импульса. Нанесение нескольких точечных воздействий, в ходе которых область последующего нанесенного РЧ-повреждения связана с предыдущим, приводит к формированию линейного РЧ-повреждения. В клинической практике под линейной РЧА понимают создание повреждений между двумя участками или анатомическими ориентирами (такими как периметр митрального клапана, УЛВ, ушко ЛП, верхняя и нижняя полые вены, устье коронарного синуса, рубцовые поля), которые отграничены от других отделов миокарда (например, в ходе предшествующей РЧА) таким образом, что отсутствует возможность проведения электрического импульса между этим самым участком и прилежащими отделами миокарда. Примером могут служить линейные РЧ-воздействия между рубцовыми зонами миокарда или между рубцовыми участками и анатомическими образованиями, не обладающими свойствами электрической проводимости (например, между рубцовой областью и кольцом митрального клапана). В том случае, если последняя и первая точки, формирующие это линейное повреждение, оказываются непосредственно связанными друг с другом, то можно говорить о циркулярном РЧ-повреждении (например, циркулярная РЧ-изоляция УЛВ, изоляция ушка ЛП и т.п.).
Клинический этап. В настоящее исследование включены 20 пациентов (6 женщин, средний возраст 51,4±13,6 года), страдающих пароксизмальной формой ФП, которым выполнялись процедуры РЧА в ЛП. Пациенты были разделены на 2 группы, сопоставимые по возрасту, полу, длительности аритмического анамнеза и характеру антиаритмической терапии (ААТ).
В 1-й группе РЧ-изоляцию УЛВ осуществляли с использованием диагностического электрода LASSO и абляционного электрода [6—8]. Данная методика подробно описана ранее [6—8] и, по сути, заключается в создании циркулярных РЧ-повреждений в области УЛВ (рис. 1, а, см. цветную вклейку).
Во 2-й группе с помощью системы нефлюороскопического картирования CARTO XP (Biosense Webster) картирующим электродом (NAVYStar, Biosense Webster) осуществляли трехмерную реконструкцию ЛП и РЧ-воздействия выполняли вокруг УЛВ (циркулярная изоляция), которые дополняли линейными РЧ-воздействиями в области свода ЛП (между устьями верхних левой и правой легочных вен), между устьем левой нижней легочной вены и кольцом митрального клапана (в области так называемого митрального перешейка) [7, 8] (см. рис. 1, в, см. цветную вклейку). Данную методику РЧА, сочетающую в себе циркулярную изоляцию УЛВ и линейную РЧА, здесь и далее мы называем линейной РЧА.
В течение 3 мес после операции все пациенты продолжали принимать антиаритмические препараты III класса и варфарин под контролем международного нормализованного отношения с последующей их отменой.
Клиническое наблюдение заключалось в оценке жалоб пациента, проведении физикального осмотра, регистрации электрокардиограммы в 12 отведениях и ее холтеровского мониторирования через 2, 6 и 12 мес после выполнения РЧА.
В случае появления наджелудочковых аритмий в раннем или позднем послеоперационном периодах пациентам выполняли медикаментозную и/или электрическую кардиоверсию. При стойкой тенденции к рецидиву аритмического синдрома пациентам проводили повторную операцию РЧА.
Математическое моделирование. На первом этапе в ходе вычислительного эксперимента реализовали заданный автоволновый процесс возбудимой ткани ЛП и производили моделирование ФП с использованием уравнения Фитцхью—Нагумо, позволяющие учитывать электрическую неоднородность предсердий (УЛВ) [9].
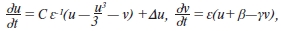
где ε=0,03, β=0,7, γ=0,8.
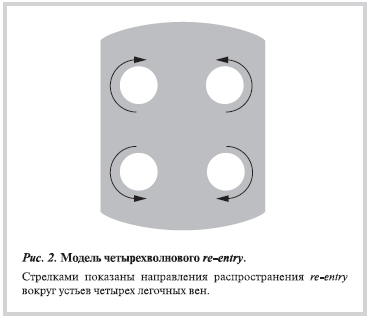
Выбор использованной математической модели был основан на создании модели четырехволнового re-entry, в которой направление вращения re-entry определялось базовыми свойствами синхронизации вращения круговых волн (рис. 2) [10—13]. Для вычисления характеристик автоволновых процессов в двумерной математической модели предсердий использовали специально разработанный метод сканирования, позволяющий производить эффективные подсчеты в случае сложных границ области и ее гетерогенности [10—13]. В этих целях применяли сеточную схему метода прямых в сочетании с методом сканирования в программной среде MATLAB7, что позволяет эффективно исследовать автоволновые процессы при наличии сложных границ области и ее гетерогенности. Метод сканирования позволял оперативно моделировать геометрию исследуемой области с учетом наличия устьев четырех легочных вен и линий, препятствующих распространению фронта деполяризации, моделирующих абляционные воздействия.
Для графического представления автоволн электрического возбуждения красным цветом отображалась область нарастания электрического возбуждения, желтым — область спадания, бирюзовым — область медленного нарастания, относящаяся к фазе рефрактерности возбуждения, зеленым — отсутствие возбуждения. Вторым этапом с помощью процедуры, реализуемой с использованием метода сканирования, производили моделирование циркулярных (соответствующих методике РЧА, использовавшейся у пациентов 1-й группы) и линейных воздействий (соответствующих методике РЧА, использовавшейся у пациентов 2-й группы) (см. рис. 1, б, г, см. цветную вклейку).
Результаты
Клинические результаты. В раннем послеоперационном периоде (в период до 3 мес после последней повторной процедуры РЧА) у 7 пациентов 1-й группы (у которых использовалась методика РЧА изоляции УЛВ с помощью катетера LASSO, что соответствовало математическому моделированию циркулярных повреждений) и 4 пациентов 2-й группы (у которых проводилась РЧА с помощью системы нефлюороскопического картирования, что соответствовало математическому моделированию линейных повреждений) регистрировались наджелудочковые нарушения ритма (ФП, атипичное трепетание предсердий), которые были эффективно купированы дополнительным назначением кордарона в 3 случаях или проведением электрической кардиоверсии в 6 случаях (рис. 3).
В 1-й группе через 12 мес наблюдения отсутствие рецидивов МА на фоне отмены ААТ отмечалось у 2 пациентов, в 3 случаях пароксизмы МА стали эффективнее контролироваться ААТ. В 5 случаях РЧА не повлияла на течение аритмического синдрома. Проведение повторных сессий РЧА по поводу МА с использованием системы CARTO потребовалась 6 пациентам через 12 мес после проведения первичной процедуры РЧА.
Во 2-й группе через 12 мес наблюдения отсутствие рецидивов МА на фоне отмены ААТ отмечалось в 8 случаях, в 2 случаях пароксизмы аритмии отсутствуют на фоне ААТ. Повторные сессии РЧА по поводу атипичного перимитрального ТП проводились 2 пациентам через 4 и 7 мес после первичного интервенционного вмешательства.
Таким образом, проведение РЧА методом линейных воздействий у пациентов с пароксизмальной формой ФП ассоциируется с более высокой вероятностью поддержания устойчивого синусового ритма, чем проведение РЧ-изоляции УЛВ (8 пациентов и 2 пациента соответственно; р=0,003).
Результаты математического моделирования. Результаты вычислительного моделирования re-entry вокруг УЛВ и эффективность проведения циркулярного абляционного форматирования представлены на рис. 4 (см. цветную вклейку). Через период времени, равный периоду re-entry после проведения циркулярного абляционного форматирования, отмечается отсутствие элиминации как четырехволнового re-entry, вокруг УЛВ, так и вызванных ими вихревых волн в распределенной двумерной среде предсердий. Таким образом, циркулярное абляционное форматирование не влияет на re-entry вокруг УЛВ и, следовательно, не подавляет МА.
Результаты вычислительного моделирования re-entry вокруг УЛВ и эффективность линейного абляционного форматирования представлены на рис. 5 ( см. цветную вклейку). Рассчитано, что линейное абляционное форматирование эффективно подавляет аритмию, обусловленную re-entry в легочных венах.
Обсуждение
В ходе математического моделирования ФП, которое осуществлялось на основании реализации заданного автоволнового процесса с использованием уравнения Фитцхью—Нагумо, и последующего абляционного форматирования, имитирующего линейную РЧА ЛП с помощью системы нефлюороскопического картирования, нами установлено, что проведение линейных РЧ-повреждений в ЛП приводит к элиминации четырехволнового re-entry вокруг УЛВ. В то же время циркулярное абляционное форматирование не подавляет данную модель ФП. Полученные результаты клинического наблюдения за пациентами, перенесшими интервенционные вмешательства по поводу ФП, соответствуют данным вычислительного эксперимента и свидетельствуют о том, что рецидивы ФП через 12 мес после выполнения линейной РЧА в ЛП возникали достоверно реже, чем при использовании циркулярной изоляции УЛВ.
Современные методики РЧА при ФП предполагают возможность достижения устойчивого синусового ритма в течение 1 года у 70% пациентов. В настоящее время существует множество объяснений, почему в ряде случаев выполнение РЧА при ФП не приводит к удовлетворительным клиническим результатам. Среди наиболее часто обсуждаемых причин — восстановление проведения в участках нанесения циркулярных и/или линейных РЧ-повреждений [14], заинтересованность эпикардиальных волокон миокарда предсердий и отсутствие трансмурального повреждения [15, 16], а также вовлеченность в генез ФП правого предсердия [17], ушка ЛП [18], структур коронарного синуса [19].
В нашей работе мы попытались научно обосновать ответ на вопрос, почему у ряда больных МА можно эффективно контролировать, и какие методические подходы в проведении интервенционной процедуры предпочтительнее и предполагают достижение лучшего клинического результата.
Эволюция методических подходов РЧА при ФП во многом связана с понятием линейности повреждения. В работах, выполненных группой M. Haissaguerre в начале 2000 гг., показано, что нанесение дополнительных линейных воздействий в области свода ЛП и/или митрального перешейка сопровождается уменьшением частоты рецидивов ФП после РЧА [20, 21]. То, что создание линейных повреждений в ЛП положительно влияет на ФП, подтверждено данными проспективного рандомизированного исследования, в котором приняли участие 204 пациента, оперированных методом РЧА по поводу пароксизмальной формы ФП [4]. Полученные результаты свидетельствуют о том, что дополнение циркулярной РЧ-изоляции УЛВ линейными РЧ-воздействиями в области свода ЛП и митрального перешейка ассоциируется с отсутствием рецидивов ФП на фоне отмены ААТ у 56 и 53% пациентов через 1 и 3 года клинического наблюдения соответственно. При этом выполнение только циркулярной РЧ-изоляции легочных вен без дополнительных линейных воздействий в ЛП обеспечивает устойчивый синусовый ритм через 1 год клинического наблюдения у 46% пациентов, а через 3 года — лишь в 29% случаев [4]. Полученное в нашей работе соответствие клинических данных и результатов вычислительного эксперимента свидетельствует о преимуществе линейной РЧА над циркулярной при лечении пароксизмальной ФП при условии, что механизм аритмии реализуется в виде четырехволнового re-entry в УЛВ.
Проведение дальнейшей работы в этом направлении, как нам представляется, позволит приблизиться к решению одной из основных задач современной электрофизиологии — унификации метода интервенционного лечения МА.
Заключение
Математическое моделирование фибрилляции предсердий в виде четырехволнового re-entry с использованием методики сканирования показало, что выполнение циркулярного абляционного форматирования, имитирующего радиочастотную изоляцию устьев легочных вен, уступает линейному, имитирующему линейную же радиочастотную абляцию в левом предсердии. Результаты математического моделирования соответствуют данным клинического наблюдения в течение 1 года клинического мониторирования за пациентами с пароксизмальной формой фибрилляции предсердий, оперированными с использованием соответствующих клинических техник радиочастотной абляции при мерцательной аритмии.



