Фибрилляция предсердий (ФП) — наиболее распространенное нарушение ритма сердца, которое обусловливает 1/3 госпитализаций, связанных с аритмиями. По различным оценкам, распространенность ФП достигает 1—2% в общей популяции, увеличиваясь до 8% у лиц пожилого возраста [1]. ФП является важнейшим фактором риска развития инсульта, сердечной недостаточности и смерти от любых причин. Частота развития инсультов у пациентов с ФП в 4—5 раз выше, чем при синусовом ритме. Количество инсультов, связанных с ФП, возрастает с 1,5% в возрасте 50—59 лет до 23,5% в возрасте 88—89 лет [2].
Более того, инсульт на фоне ФП протекает с более выраженными неврологическими расстройствами и более высоким риском рецидивов, чем при синусовом ритме [3]. Основным способом профилактики тромбоэмболических осложнений является постоянная бессрочная пероральная антикоагулянтная терапия (АКТ) с помощью антагонистов витамина К либо новых прямых пероральных антикоагулянтов (НОАК), таких как дабигатрана этексилат, ривароксабан и апиксабан [4].
Первым прямым ингибитором фактора Xa, зарегистрированным к клиническому применению по показаниям профилактики инсульта и системных тромбоэмболий при неклапанной ФП, стал ривароксабан. Ривароксабан (ксарелто), прямой ингибитор фактора Ха, может обеспечить более надежный и прогнозируемый антикоагулянтный эффект, чем варфарин. По результатам исследования ROCKET AF [5], ривароксабан по сравнению с варфарином дополнительно снижает риск развития инсульта и системных эмболий, при этом количество больших и небольших клинически значимых кровотечений было таким же, как и на фоне лечения варфарином, а число внутримозговых кровоизлияний и кровотечений с летальным исходом – значительно меньше.
Известно, что наличие в анамнезе ишемического инсульта (ИИ) либо транзиторной ишемической атаки (ТИА) у пациентов с неклапанной ФП в 2,5 раза увеличивает риск повторного инсульта [6]. Вместе с этим на фоне длительной пероральной АКТ может увеличиваться риск кровотечений, включая внутричерепные кровоизлияния, что для больных, перенесших ИИ, сопряжено с инвалидизирующими последствиями [7]. Косвенное сопоставление результатов лечения варфарином больных неклапанной ФП в рамках первичной и вторичной профилактики инсульта продемонстрировало, что варфарин у больных, перенесших инсульт, был эффективнее и приводил к трехкратному снижению риска повторного инсульта наряду с сопоставимым риском внутричерепных кровотечений.
При этом суммарная эффективность лечения варфарином после ИИ была выше [8—10].
Несомненный интерес представляет изучение клинической эффективности НОАК во вторичной профилактике кардиоэмболического инсульта. Анализ в подгруппах исследования ROCKET AF, в котором 52% пациентов до рандомизации имели в анамнезе указания на перенесенные ИИ либо ТИА, показал, что после анализа эффектов взаимодействия показатели эффективности и безопасности ривароксабана у пациентов с неклапанной ФП и ИИ/ТИА в анамнезе соответствует таковым полученным для популяции ROCKET AF в целом [11].

При этом риск развития всех геморрагических осложнений в группе ривароксабана был несколько меньше, чем в группе больных, получающих варфарин.
Стандарты АКТ в разных странах отличаются. Продолжение АКТ пациентами с ФП с целью вторичной профилактики инсульта на амбулаторном этапе до сих пор не является правилом. Это связано с недостаточной осведомленностью врачей амбулаторной сети о современных стандартах лечения. В данном исследовании основной целью явилось изучение схемы назначения неврологами ривароксабана с целью вторичной профилактики инсульта и всех системных эмболических осложнений у пациентов с ФП, перенесших ИИ или ТИА.
Материал и методы
Исследование Neuro-Xar представляет собой проспективное когортное многоцентровое наблюдательное исследование, в котором участвовало 14 клинических организаций Российской Федерации. Протокол исследования одобрен Министерством здравоохранения РФ и локальными этическими комитетами клиник.
В исследование были включены пациенты в возрасте 18 лет и старше с неклапанной ФП, перенесшие инсульт или ТИА не ранее чем за 14 дней до первого визита. АКТ больным ранее не проводилась.
 Учитывали демографические данные пациента (пол, возраст, расовую принадлежность), данные объективного осмотра (масса тела, рост, индекс массы тела, артериальное давление — АД), злоупотребление алкоголем, табакокурение, наличие артериальной гипертензии (АГ). Анализировали клинико-инструментальные характеристики церебрального поражения, сопутствующие заболевания (инфаркт миокарда в анамнезе, стенокардия, заболевания периферических артерий, вмешательства на артериях и т.д.), способы диагностики и форму ФП. Проводили оценку риска развития эмболических осложнений и кровотечений по шкалам CHA2DS2VASC и HAS-BLED. Осуществляли лабораторную диагностику (гемоглобин, гематокрит, тромбоциты, клиренс креатинина — КК), инструментальное обследование (электрокардиография – ЭКГ, эхокардиография — ЭхоКГ, магнитно-резонансная/компьютерная томография головы). Учитывали сопутствующую терапию.
Учитывали демографические данные пациента (пол, возраст, расовую принадлежность), данные объективного осмотра (масса тела, рост, индекс массы тела, артериальное давление — АД), злоупотребление алкоголем, табакокурение, наличие артериальной гипертензии (АГ). Анализировали клинико-инструментальные характеристики церебрального поражения, сопутствующие заболевания (инфаркт миокарда в анамнезе, стенокардия, заболевания периферических артерий, вмешательства на артериях и т.д.), способы диагностики и форму ФП. Проводили оценку риска развития эмболических осложнений и кровотечений по шкалам CHA2DS2VASC и HAS-BLED. Осуществляли лабораторную диагностику (гемоглобин, гематокрит, тромбоциты, клиренс креатинина — КК), инструментальное обследование (электрокардиография – ЭКГ, эхокардиография — ЭхоКГ, магнитно-резонансная/компьютерная томография головы). Учитывали сопутствующую терапию.
Перед включением пациента в исследование врачи ознакомились с инструкцией по применению ривароксабана, особенно с информацией о безопасности. В исследовании было запланировано 4 визита — один, на котором пациент был включен в исследование, и 3 визита наблюдения, приблизительно через каждые 2 мес. Визит включения в исследование проводился после ишемического осложнения (более 72 ч после ТИА или более 2 нед после негеморрагического инсульта) и после того, как невролог принимал решение о назначении ривароксабана.
Все процедуры и лечение проводились в соответствии со стандартами оказания медицинской помощи, предусмотренными в данном лечебном учреждении. Критериями отказа от включения в исследование явились противопоказания к назначению ривароксабана, ранее проводимая терапия антикоагулянтами с целью профилактики ИИ/ТИА. Решение о начале терапии и ее продолжительности принимал исследователь. По желанию пациент мог быть выведен из исследования в любое время, при этом отказ от дальнейшего участия в исследовании не влиял на характер проводимой терапии.
В исследовательской документации отражали прием ривароксабана, его дозировку, название препарата в случае перехода на другой антикоагулянт, другие лекарственные препараты для лечения сопутствующих заболеваний и нежелательных явлений.
Основные и дополнительные критерии оценки лечения. В качестве основного критерия оценивали временно'й промежуток между перенесенным инсультом или ТИА и назначением ривароксабана; частоту прекращения/перерывов в лечении ривароксабаном; время до прекращения/перерывов в лечении ривароксабаном; причину прекращения/перерывов в лечении ривароксабаном (с использованием формализованного списка критериев).
В качестве дополнительного критерия оценивали время начала АКТ непосредственно после ишемического осложнения (инсульта или ТИА); частоту и причину, по которой пациенты прекращали прием ривароксабана; характеристику нежелательных явлений, включая частоту, степень тяжести, связь с антитромботической терапией, лечение и исходы.
Методы оценки безопасности. Нежелательным явлением считали любое неблагоприятное проявление (включая отклонение лабораторных показателей), симптом или заболевание, возникновение которого по времени совпадало с приемом исследуемого лекарственного препарата. Термин «нежелательные явления» также включает клинически значимые изменения лабораторных показателей. К тяжелым нежелательным явлениям относили смерть, состояния, угрожающие жизни, обусловившие необходимость госпитализации пациента или приведшие к значительной утрате трудоспособности, либо к инвалидности.
Статистический анализ данных. Результаты были суммированы для всех пациентов, а также для различных клинических подгрупп. Для непрерывных переменных были рассчитаны средние значения, стандартное отклонение, медиана, нижний и верхний квартили, минимальное и максимальное значения. Данные в таблицах представлены в виде абсолютного числа больных (%) или медианы с указанием 25-го и 75-го процентилей их распределения — Ме (25%; 75%). Для дискретных переменных рассчитаны показатели частоты, процентное соотношение. В целях оценки лечения, рекомендуемого неврологами в условиях клинической практики для вторичной профилактики инсульта и системной эмболии у пациентов с ФП, перенесших инсульт или ТИА, применялись методы описательной статистики. Данные о нежелательных явлениях для группы пациентов, вошедших в анализ безопасности, обработаны с помощью методов описательной статистики.
 Исходные характеристики пациентов. Всего в исследование были включены 214 пациентов (табл. 1), из них 179 (83,6%) перенесли ИИ, 35 (16,4%) — ТИА. До конца исследования наблюдался 201 (93,9%) пациент. Умерли 2 пациента, 11 выбыли досрочно. Число мужчин и женщин было сопоставимо.
Исходные характеристики пациентов. Всего в исследование были включены 214 пациентов (табл. 1), из них 179 (83,6%) перенесли ИИ, 35 (16,4%) — ТИА. До конца исследования наблюдался 201 (93,9%) пациент. Умерли 2 пациента, 11 выбыли досрочно. Число мужчин и женщин было сопоставимо.
В основном пациенты относились к лицам пожилого возраста, имели избыточную массу тела. ФП была представлена всеми формами, средняя оценка по шкале CHA2DS2VASc свидетельствовала о высоком риске развития тромбоэмболических осложнений, по шкале HAS-BLED — об умеренном риске кровотечений. При включении в исследование ФП зафиксирована на электрокардиограмме у 175 (81,8%) пациентов. С помощью ЭхоКГ на скрининге тромбы в полостях сердца визуализированы у 4 (1,9%) пациентов. Фракция выброса левого желудочка составила в среднем 62 (55; 66) %. Исходно КК 50 мл/мин и выше зафиксирован у 133 (62,2%) больных, у остальных пациентов КК был ниже 50 мл/мин, но не достигал уровня менее 30 мл
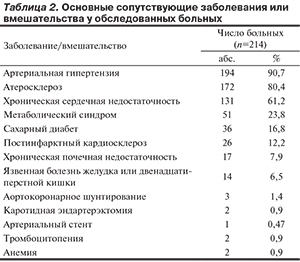
В табл. 2 представлены основные сопутствующие заболевания. У большинства пациентов имелись АГ, атеросклероз с поражением различных сосудистых бассейнов и хроническая сердечная недостаточность, преимущественно диастолическая. Реже отмечались метаболический синдром, сахарный диабет, постинфарктный кардиосклероз, хроническая почечная недостаточность и язвенная болезнь желудка или двенадцатиперстной кишки. Нескольким больным выполнены хирургические вмешательства на коронарных и сонных артериях. Признаки умеренной анемии или тромбоцитопении зарегистрированы у 4 пациентов.
Лечение и данные лабораторного и инструментального обследований пациентов в динамике. Большинство пациентов получали комбинированную терапию, включая антигипертензивные, антиаритмические, гиполипидемические, антиангинальные, сахароснижающие средства. При этом 33 (15,4)% больных наряду с ривароксабаном получали терапию антитромбоцитарными препаратами (клопидогрел, ацетилсалициловая кислота).
На визите включения 187 (87,5%) больным был рекомендован прием ривароксабана 20 мг однократно в сутки (табл. 3), 16 (7,4%) пациентам —15 мг ривароксабана, 11 (5,1%) больным на первом визите ривароксабан назначен в дозе 10 мг в сутки, что объяснялось субъективным решением врача.
При этом в ходе динамического наблюдения у 195 (91,1%) больных дозировка не менялась, а у 18 (8,4%) повышена с 10 до 15 мг и с 15 до 20 мг. И только у 1 пациента произошло снижение дозы с 20 до 15 мг.
В ходе наблюдения за пациентами не выявлено клинически значимых изменений уровней гемоглобина, гематокрита, тромбоцитов и КК. В динамике контролю подвергались уровни АД. У ряда пациентов анализировали результаты повторно выполненных ЭКГ, ЭхоКГ, магнитно-резонансной/компьютерной томографии головы. Клинически значимых изменений результатов электрокардиографии и ЭхоКГ не отмечено, при этом у 3 из 4 пациентов уже на втором визите не визуализированы признаки имевшегося ранее тромбоза полостей сердца.
Постоянство терапии ривароксабаном. Продолжали терапию ривароксабаном через 6 мес 189 (94%) пациентов из 201. Всего в ходе исследования описаны причины отказа от приема ривароксабана у 16 пациентов. Так, замена препарата дабигатраном зарегистрирована у 2 пациентов, при этом у одного пациента «был большой запас дабигатрана», во втором случае причина не указана. В 11 случаях отказ от ривароксабана был мотивирован недоступностью препарата. Еще у 3 больных в основе отмены лежало субъективное решение пациента («не прошло головокружение» и т.д.).
Оценка безопасности. Всего в исследовании было сообщено о 15 (7%) нежелательных явлениях, 4 (26,7%) из которых расценены как тяжелые. Умерли 2 больных по причине повторного ИИ и непроходимости кишечника. В последнем случае смерть наступила от перитонита, осложнившегося полиорганной недостаточностью. В других двух случаях (пароксизм ФП и декомпенсация неврологической симптоматики после ранее перенесенного инсульта) пациенты были госпитализированы. Было зафиксировано два случая кровоточивости: из прямой кишки (на фоне одновременного приема ривароксабана и ацетилсалициловой кислоты 75 мг) и однократная макрогематурия. В обоих случаях тромбопрофилактика была приостановлена и в последующем было возобновлено лечение ривароксабаном. Кровотечения прекращались спонтанно. С использованием ривароксабана были связаны, по мнению исследователей, появление кожного зуда (купированного на фоне применения антигистаминных препаратов) и атопического дерматита (ривароксабан был отменен). Кроме того, у одного из пациентов были зафиксированы повышение уровней аланинаминотрансферазы до 120 ед/л и аспартатаминотрансферазы до 58 ед/л, связанные, по мнению исследователя, с применением ривароксабана.
Обсуждение
Профилактика инсульта и системных тромбоэмболических осложнений при неклапанной ФП за последние 5 лет вышла на новый качественный уровень. В настоящее время новые прямые пероральные антикоагулянты занимают ведущие позиции в качестве средств выбора при неклапанной ФП [12]. Фиксированный режим дозирования, прогнозируемая антикоагуляция, отсутствие необходимости регулярного контроля свертываемости крови и перманентного подбора дозы сделали препараты лидерами среди антитромботических средств, используемых для профилактики ИИ [13]. Однако в пожилом возрасте наряду с увеличением частоты развития неклапанной ФП появляются другие хронические заболевания, требующие соответствующей терапии.
При этом увеличивается риск полипрагмазии и нежелательных лекарственных взаимодействий. Кроме того, сопутствующая коронарная патология, плановое или экстренное чрескожное вмешательство на артериях, нарушение функции печени или почек может внести свои коррективы в антикоагулянтную терапию. В связи с этим несомненную ценность приобретают данные клинической практики применения НОАК, где могут быть учтены различные ситуации, не предусмотренные в рандомизированных клинических испытаниях.
Основной целью исследования Neuro-Xar были изучение и описание применяемых неврологами схем назначения ривароксабана с целью вторичной профилактики инсульта и системной эмболии у пациентов с ФП, перенесших ИИ или ТИА. В ходе данной программы наблюдения оценивались конечные точки, характеризующие особенности вторичной профилактики инсульта. В связи с тем что данная программа была наблюдательной и несравнительной, объем выборки был рассчитан исходя из значения допускаемой погрешности окончательных расчетов.
Пациенты, включенные в исследование, были пожилого возраста, перенесли острое нарушение мозгового кровообращение, что обусловило высокий риск развития тромбоэмболических осложнений. Кроме этого, у большинства больных имелась сочетанная патология, включая АГ, атеросклероз, хроническую сердечную недостаточность, увеличивающую риск мозговых катастроф. Нельзя не учитывать также то, что большинство пациентов принимали одновременно 4 лекарственных препаратов и более, включая тромбоцитарные антиагреганты, что уменьшает приверженность терапии и увеличивает риск развития тромбоэмболических осложнений.
Тем не менее результаты исследования Neuro-Xar подтвердили эффективность и безопасность применения ривароксабана в клинической практике для вторичной профилактики инсульта. Из прошедших заключительный визит 94% пациентов продолжили прием ривароксабана, что вселяет надежду на сохранение подобной приверженности. Хорошая переносимость терапии, стабильные лабораторные показатели наряду с низкой частотой кровотечений и побочных явлений свидетельствовали в пользу безопасности терапии. Несмотря на высокий риск развития тромбоэмболических осложнений, только у 2 (0,9%) больных были зафиксированы ишемические церебральные нарушения, одно из которых закончилось летальным исходом. При этом в данном наблюдении повторный фатальный ИИ, по мнению исследователей, мог быть связан с отказом пациента принимать ривароксабан.
Дозы ривароксабана, используемые в исследовании, в основном соответствовали рекомендациям, где в качестве дозировки выбора выступает 20 мг/сут, тогда как 15 мг/сут рекомендуется больным с клиренсом креатиниа 49—30 мл/мин [4].Следует отметить, что 11 больным на визите включения без достаточных на то оснований был назначен ривароксабан в дозе 10 мг/сут, что можно объяснить распространенной на практике переоценкой риска развития кровотечений. Тем не менее в последующие визиты у всех из них дозировка была увеличена до 20 мг/сут.
Заключение
Таким образом, накапливающийся опыт успешного пострегистрационного клинического применения ривароксабана подтверждает благоприятное соотношение польза и риска при условии соблюдения всех рекомендаций по показаниям к лечению и режиму дозирования.



