В настоящее время фибрилляция предсердий (ФП) является наиболее распространенным нарушением ритма сердца. Распространенность ФП в общей популяции составляет около 2% и увеличивается от <0,5% в возрасте 40—50 лет до 5—15% в возрасте 80 лет [1]. У мужчин ФП развивается чаще, чем у женщин. Риск развития ФП на протяжении жизни составляет около 25% в возрасте 40 лет [2]. Заболеваемость ФП увеличилась на 13% за 20 лет [3].
Ежегодно в мире регистрируется около 15 млн инсультов, из них примерно 5 млн фатальных и 5 млн инсультов, приводящих к тяжелым инвалидизирующим последствиям. ФП увеличивает риск развития инсульта в 5 раз и обусловливает возникновение каждого пятого инсульта. При этом у больных с ФП увеличивается риск развития инсульта с возрастом: у больных 50—59 лет он составляет 1,5% в год, в возрасте 80—89 лет повышается до 23,5% [4]. Ишемический инсульт у больных с ФП часто заканчивается смертью и по сравнению с инсультом другой природы приводит к более выраженной инвалидизации, чаще рецидивирует. Риск развития инсульта с последующим летальным исходом у больных с ФП в 2 раза выше, чем в обычной популяции больных, а затраты на лечение возрастают в 1,5 раза [3]. Известно, что в более 90% случаев тромбоэмболий у пациентов с неклапанной ФП тромбы образовывались в ушке левого предсердия (УЛП) [5].
 Многочисленные клинические исследования показали эффективность антитромботической терапии у больных с ФП. Из антикоагулянтов непрямого действия варфарин является препаратом, клиническая эффективность которого у больных с ФП наиболее хорошо установлена в крупных рандомизированных исследованиях [6]. Однако при применении антикоагулянтной терапии (АКТ) существует ряд проблем. Несмотря на точность лабораторного контроля и наличие схем тщательного подбора дозы, главной опасностью при назначении варфарина остается возможность развития кровотечений, частота которых, по данным крупных исследований, составляет от 9 до 26%, из них «больших» (приводящих к смерти, госпитализации) — от 0,3 до 4,2% в год [7]. Применение АКТ требует регулярного контроля протромбина с расчетом международного нормализованного отношения (МНО). Риск развития кровотечений напрямую зависит от уровня МНО и возрастает в 1,37 раза с его превышением на каждые 0,5 единицы. При этом бессимптомное повышение МНО может происходить не только на этапе насыщения, но и при длительном применении непрямых антикоагулянтов [8]. Еще одной проблемой является приверженность пациентов к АКТ. Сложность контроля уровня МНО приводит к тому, что больные отказываются от приема варфарина, а это увеличивает риск развития тромбоэмболических осложнений ФП.
Многочисленные клинические исследования показали эффективность антитромботической терапии у больных с ФП. Из антикоагулянтов непрямого действия варфарин является препаратом, клиническая эффективность которого у больных с ФП наиболее хорошо установлена в крупных рандомизированных исследованиях [6]. Однако при применении антикоагулянтной терапии (АКТ) существует ряд проблем. Несмотря на точность лабораторного контроля и наличие схем тщательного подбора дозы, главной опасностью при назначении варфарина остается возможность развития кровотечений, частота которых, по данным крупных исследований, составляет от 9 до 26%, из них «больших» (приводящих к смерти, госпитализации) — от 0,3 до 4,2% в год [7]. Применение АКТ требует регулярного контроля протромбина с расчетом международного нормализованного отношения (МНО). Риск развития кровотечений напрямую зависит от уровня МНО и возрастает в 1,37 раза с его превышением на каждые 0,5 единицы. При этом бессимптомное повышение МНО может происходить не только на этапе насыщения, но и при длительном применении непрямых антикоагулянтов [8]. Еще одной проблемой является приверженность пациентов к АКТ. Сложность контроля уровня МНО приводит к тому, что больные отказываются от приема варфарина, а это увеличивает риск развития тромбоэмболических осложнений ФП.
В настоящее время одним из методов уменьшения риска развития мозгового инсульта считается эндоваскулярная изоляция УЛП. Существует несколько устройств, с помощью которых она выполняется, различающихся как по конструкции, так и по уровню доказательной базы в отношении эффективности и безопасности [9]. Одно из них — устройство WATCHMAN [10].
В ходе крупного рандомизированного исследования PROTECT AF было показано, что имплантация устройства WATCHMAN не менее эффективна, чем применение варфарина, в отношении предупреждения всех инсультов, сердечно-сосудистой смерти и системной эмболии. В отдаленных результатах исследования (за 4 года) отмечалось снижение общей, сердечно-сосудистой смерти и риска геморрагического инсульта в группе устройства WATCHMAN [4, 11].
 Цель нашего исследования — показать эффективность эндоваскулярной окклюзии УЛП пациентам с ФП и высоким риском геморрагических осложнений при приеме АКТ.
Цель нашего исследования — показать эффективность эндоваскулярной окклюзии УЛП пациентам с ФП и высоким риском геморрагических осложнений при приеме АКТ.
Материал и методы
Выбор пациентов осуществлялся по следующим критериям:
- наличие ФП и кровотечений в анамнезе при употреблении варфарина;
- наличие ФП и кровотечений в анамнезе, предшествующих использованию варфарина;
- ФП и высокий риск развития тромбоэмболических осложнений по шкале CHA2DS2-VASc (2 балла и более);
- ФП и высокий риск развития геморрагических осложнений по шкале HAS-BLED (3 балла и более);
- ФП и нежелание принимать АКТ.
Противопоказаниями к имплантации устройства считали стеноз митрального клапана, наличие тромботических масс в УЛП, наличие у больного окклюдера межпредсердной перегородки.
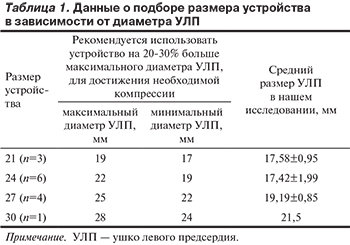
С декабря 2012 г. по май 2014 г. было выполнено 14 имплантаций окклюдеров у 15 больных с ФП. Показанием к имплантации устройства являлись у 12 (80%) больных высокий риск развития геморрагических осложнений по шкале HAS-BLED (3 балла и более), а у 3 (20%) пациентов нежелание принимать АКТ. Во всех случаях закрытие УЛП выполняли в рентгеноперационной под контролем чреспищеводной эхокардиографии. Размер устройства подбирался на 20—30% больше диаметра УЛП (табл. 1).
В 3 (21,4%) случаях имплантировано устройство диаметром 21 мм, в 6 (42,8%) — 24 мм, в 4 (28,6%) — 27 мм и в 1 (7,2%) случае 30 мм. Три (20%) пациента были в возрасте от 60 до 70 лет, 4 (26,6%) — от 70 до 80 лет и 8 (53,4%) больных старше 80 лет. После имплантации пациенты продолжали прием варфарина, который был отменен через 45 дней в зависимости от результатов чреспищеводной эхокардиографии.
Результаты
В табл. 2 представлены основные характеристики пациентов, которым проводилась имплантация устройства WATCHMAN.
Положение устройства и наличие параокклюдерных потоков оценивалось по данным чреспищеводной эхокардио-графии интраоперационно, а также через 45 дней, 6 и 12 мес. Непосредственно после имплантации и через 1 мес наблюдения у 6 (42,8%) больных резидуальный кровоток отсутствовал, у 6 (42,8%) составил менее 5 мм, у 2 (14,4%) был равен 5 мм. Через 6—12 мес у 13 (92,8%) больных УЛП было полностью изолировано, а у 1 (7,2%) параокклюдерный поток составил 3 мм. Для сравнения, в исследовании PROTECT AF 37% пациентов имели резидуальный кровоток >1 мм [7]. В 1 (7,2%) случае через 45 дней на поверхности устройства был выявлен тромб 12 мм, который при контрольном исследовании через 1 мес после приема низкомолекулярного гепарина не определялся.
В исследовании PROTECT AF было показано, что тромбы на поверхности устройства образовывались в 4,2% случаев, при этом у 15% этих пациентов произошла тромбоэмболия [7]. За период наблюдения ни у одного пациента дислокации устройства, тромбоэмболических осложнений и острых нарушений мозгового кровообращения не было.
Летальный исход отмечался в одном случае, причиной которого явился гемоперикард как следствие перфорации аорты. Кроме того, зарегистрирован один случай сердечно-сосудистой смерти через 6 мес после имплантации, не связанный с устройством.
Заключение
Несмотря на риск интра- и послеоперационных осложнений, эндоваскулярная изоляция ушка левого предсердия устройством WATCHMAN является эффективным методом профилактики тромбоэмболических осложнений и может стать альтернативой приему антикоагулянтной терапии у пациентов с фибрилляцией предсердий с высоким риском развития геморрагических осложнений. Возможно, что применение новых антикоагулянтов в период эпителизации устройства поможет избежать образования тромбов на его поверхности, но пока таких исследований не проводилось.



