Фибрилляция предсердий (ФП) — самое частое нарушение ритма сердца [1, 2], с которым ассоциировано 5-кратное повышение риска развития инфаркта головного мозга [3]. Применение новых пероральных антикоагулянтов улучшило клинические исходы, связанные с ФП [4]. Однако выявление пациентов, у которых антикоагулянтная терапия будет наиболее эффективной и безопасной, остается сложной задачей, несмотря на совершенствование подходов к прогнозированию риска развития тромбоэмболических осложнений (ТЭО) [5]. Считается, что пациенты с неклапанной ФП в варианте пароксизмального, персистирующего или постоянного течения в равной степени подвержены риску развития ТЭО [6—10], однако в нескольких проспективных исследованиях было показано, что у больных, получающих антикоагулянтную терапию, при пароксизмальной ФП риск развития ТЭО ниже, чем при персистирующей или постоянной форме [11—13].
Раскрытие представлений о связях между структурой и функцией сердца, характером течения аритмии сердца и риском развития ТЭО способствует оптимизации лечения пациентов с ФП. Результаты выполненных исследований в отношении таких ассоциаций неоднозначны. В более ранних исследованиях придавалось значение структуре левого предсердий (ЛП) [14—16], тогда как в последнее время особое внимание отводится нарушениям функции ЛП [17—19].
Новая эхокардиографическая методика speckle-tracking, определяющая скорость движения миокарда по перемещению пятнистых структур, которые представляют собой естественные акустические маркеры, позволяет выявлять ранние изменения функции миокарда [20, 21]. Целью нашего исследования являлось изучение структурных и функциональных особенностей миокарда ЛП и левого желудочка (ЛЖ) у пациентов с ФП в зависимости от ее варианта течения и риска развития ТЭО по шкале CHA2DS2VASc.

Материал и методы
В исследование были включены 60 пациентов — 45% мужчин, средний возраст 65 (61; 72) лет с неклапанной рецидивирующей формой ФП (длительностью >6 мес) и стабильной формой ишемической болезни сердца, синусовым ритмом и документированным эпизодом ФП в течение предшествующих 3 мес. Все пациенты относились к группе умеренного или высокого риска развития ТЭО по шкале CHA2DS2VASc [1, 2], в соответствии с которой они были разделены на 3 группы: 1, 2 и ≥3 баллов.
Всем больным выполнялась эхокардиография (ЭхоКГ, Vivid 7, GE, США) с оценкой диастолической функции ЛЖ, переднезаднего размера (ПЗР) ЛП, конечного систолического объема (КСО) и индекса объема (ИО) ЛП. Нормальными считались ПЗР ЛП≤4 см и ИОЛП<29 мл/м2. Фракция выброса (ФВ) ЛЖ оценивали по Симпсону. Массу миокарда ЛЖ (ММЛЖ) рассчитывали по формуле R. Devereux и индексировали к площади поверхности тела. Критериями гипертрофии ЛЖ считали индекс ММЛЖ (ИММЛЖ)≥95 г/м2 у женщин, ≥115 г/м2 у мужчин. Для анализа диастолической функции ЛЖ применяли традиционный метод исследования трансмитрального потока (ТМП) в импульсноволновом допплеровском режиме, а также анализ движения фиброзного кольца (ФК) митрального клапана (МК) методом тканевой допплеровской визуализации. Определяли индекс ИОЛП по биплановому методу. Глобальную деформацию ЛП оценивали в фазе наполнения (ГДЛПн, %) и сокращения (ГДЛПс, %) по 6 сегментам в 4-камерной позиции и по 6 сегментам в 2-камерной позиции. Для определения глобальной продольной деформации левого желудочка (ГДЛЖ, %) использовали 3 стандартных апикальных доступа: 3-, 4- и 2-камерную позиции с использованием 16-сегментной модели строения ЛЖ.
Статистический анализ данных проводили с помощью пакета статистических программ Statistica 8.0. Для описания количественных производных использовали медиану (Ме) и 25-й и 75-й процентили (межквартильный интервал — МИ). Достоверность различий оценивали по непараметрическим критериям Вилкоксона и Манна—Уитни. О различиях качественных признаков судили по χ2-критерию с поправкой Йетса. Для построения прогностических моделей использовали логистический регрессионный анализ. Различия средних величин и корреляции считали статистически значимыми при р<0,05.

Результаты
Пароксизмальная форма ФП наблюдалась у 26 (43%) больных, тогда как персистирующая ФП — у 34 (57%). В подгруппе пациентов с персистирующей ФП по сравнению с подгруппой лиц с пароксизмальной ФП достоверно больше был объем талии и ниже скорость клубочковой фильтрации — СКФ (табл. 1). По другим клинико-демографическим показателям пациенты обеих подгрупп были сопоставимы. Один балл по шкале CHA2DS2VASc имели 4 (15%) пациента с пароксизмальной ФП и 3 (9%) больных персистирующей ФП (р=0,70). Кроме того, в обеих подгруппах были сопо-ставимы доли пациентов с высоким риском кровотечений по шкале HAS-BLED.
Хотя ФВ у пациентов с пароксизмальной ФП была достоверно ниже, чем у больных персистирующей ФП (60 против 62%; р=0,02), первые характеризовались достоверно более низкими величинами диастолических объема и размера ЛЖ, переднезаднего размера и систолического объема ЛП, а также ИОЛП (табл. 2). При пароксизмальной ФП у всех больных ПЗР ЛП был нормальным, а при персистирующей ФП — выше нормы у 31 (91%) больного (р<0,000001). ИММЛЖ у пациентов с пароксизмальной ФП был меньше, чем у больных персистирующей ФП (121 против 136 г/м2; р=0,006).
При допплеровском исследовании величина волны Е и показатель E/E' были сопоставимы в обеих подгруппах, но пик скорости позднего наполнения ЛЖ А у больных пароксизмальной ФП был выше, чем при персистирующей ФП (0,71 против 0,60 м/с; р=0,01).
У больных пароксизмальной формой ФП по сравнению с пациентами с персистирующей ФП были лучше ГДЛПн (15,1 против 11,2%; р=0,0002) и ГДЛПс (-15 против -12%; р=0,0002), но ГДЛЖ была сопоставима.
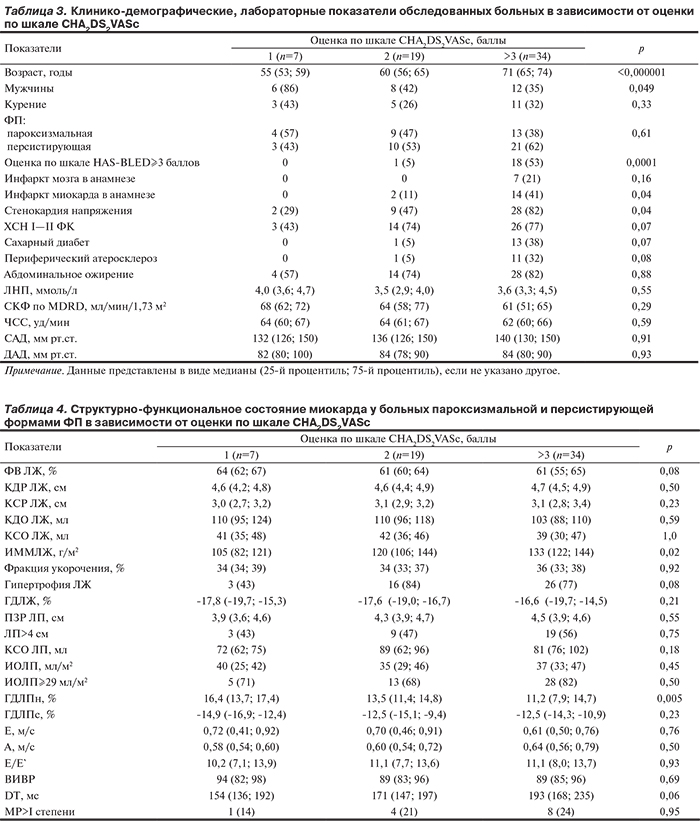
По шкале CHA2DS2VASc индекс, равный 1, 2 и 3—7 баллам, наблюдался у 7 (12%), 19 (31%) и 34 (57%) больных пароксизмальной и персистирующей ФП (табл. 3). Закономерно возраст, доля пациентов с инфарктом головного мозга, стенокардией напряжения, сахарным диабетом 2-го типа, периферическим атеросклерозом увеличивались пропорционально тяжести риска развития ТЭО по шкале CHA2DS2VASc.
Из 19 пациентов с высоким риском кровотечений по шкале HAS-BLED 18 относились к подгруппе с оценкой по шкале CHA2DS2VASc≥3 баллов.
При анализе параметров ЭхоКГ не наблюдалось пропорционального с ростом оценки по шкале CHA2DS2VASc увеличения размера и объема ЛП, как и ИОЛП (табл. 4).
Принадлежность больных ФП к разным группам риска развития ТЭО по шкале CHA2DS2VASc обусловила достоверные межгрупповые различия по ИММЛЖ (р=0,02) и ГДЛПн (р=0,005), при этом ГДЛПс и ГДЛЖ были сопоставимы.
Нелинейный логистический регрессионный анализ модели, включавшей ФВ и КСР ЛЖ, КСО ЛП, ИОЛП, ИММЛЖ и ГДЛПн, продемонстрировал единственную достоверную связь более высокого ГДЛПн с более низкими оценками по шкале CHA2DS2VASc (относительный риск 0,61 при 95% доверительном интервале — ДИ от 0,38 до 0,97; p=0,03).
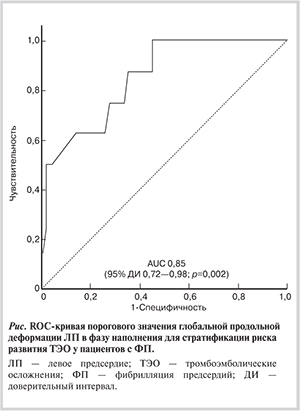
С целью применения значения ГДЛПн для разделения пациентов с умеренным и высоким риском развития ТЭО было рассчитано эффективное пороговое значение для ГДЛПн, которое составило 16,7% (чувствительность 62,5%; специфичность 39%) с площадью под ROC-кривой 0,85 (при 95% ДИ от 0,72 до 0,98; p=0,002) (см. рисунок).
Из 7 больных с умеренным риском (CHA2DS2VASc 1 балл) значение ГДЛПн менее 16,7% имелось в 2 (29%) случаях, во 2-й подгруппе (CHA2DS2VASc 2 балла) — 18 (95%), в 3-й подгруппе — у 33 (97%) больных. Среди пациентов с невысоким риском кровотечений (HAS-BLED<3 балла) снижение ГДЛПн отмечено в 35 (85%) случаях, тогда как при высоком риске кровотечений — в 18 (95%).
Обсуждение
В связи с отсутствием различий, согласно данным ранее проведенных исследований [6—10], по частоте развития ТЭО при рецидивирующей и постоянной формах ФП текущие руководства рекомендуют назначение антитромбоцитарной терапии вне зависимости от формы ФП по результатам оценки только клинических факторов риска развития ТЭО [1, 2, 11].
Однако в ряде последних исследований, сравнивающих эффективность новых пероральных антикоагулянтов с варфарином, было установлено, что частота развития ТЭО у больных пароксизмальной ФП ниже, чем у пациентов с персистирующей или постоянной ФП [12, 13]. В исследовании SPORTIF III и V у больных пароксизмальной ФП (n=836) годичная частота развития инфаркта головного мозга и системных тромбоэмболий была на 87% ниже (р=0,037), чем у пациентов с персистирующей ФП (n=6493), причем обе группы были сопоставимы по риску развития ТЭО [12].
 В то же время у пациентов в подгруппе высокого риска частота развития ТЭО составила 1,27% при пароксизмальной ФП и 2,08% при персистирующей ФП (р=0,098) [12]. В исследовании ARISTOTLE частота ТЭО была достоверно ниже у больных пароксизмальной ФП (n=836), чем у пациентов с персистирующей/постоянной ФП (n=6493) (0,98 против 1,52% соответственно; скорректированный р=0,015) [25]. Таким образом, создается впечатление, что развитие ТЭО может быть связано с выраженностью электрического ремоделирования ЛП, которое в свою очередь зависит от его структурной перестройки. Вместе с тем данные о зависимости риска развития ТЭО от структурно-функциональных изменений ЛП противоречивы [14—19]. Высказывается предположение, что не столько морфологические, сколько нарушения функции ЛП определяют предрасположенность к тромбозу [22].
В то же время у пациентов в подгруппе высокого риска частота развития ТЭО составила 1,27% при пароксизмальной ФП и 2,08% при персистирующей ФП (р=0,098) [12]. В исследовании ARISTOTLE частота ТЭО была достоверно ниже у больных пароксизмальной ФП (n=836), чем у пациентов с персистирующей/постоянной ФП (n=6493) (0,98 против 1,52% соответственно; скорректированный р=0,015) [25]. Таким образом, создается впечатление, что развитие ТЭО может быть связано с выраженностью электрического ремоделирования ЛП, которое в свою очередь зависит от его структурной перестройки. Вместе с тем данные о зависимости риска развития ТЭО от структурно-функциональных изменений ЛП противоречивы [14—19]. Высказывается предположение, что не столько морфологические, сколько нарушения функции ЛП определяют предрасположенность к тромбозу [22].
В нашей работе у пациентов с более тяжелым вариантом клинического течения ФП наблюдались более выраженные структурно-функциональные изменения миокарда ЛП и ЛЖ.
У всех пациентов с пароксизмальной ФП размер ЛП не превышал нормы, но ИОЛП у 17 (65%) был повышенным. Представительство пациентов с повышенным линейным размером ЛП и увеличенным ИОЛП при персистирующей ФП можно назвать паритетным: 91 и 85%. Поэтому ИОЛП может служить более точным маркером структурного ремоделирования ЛП, чем ПЗР ЛП, что подтверждают последние исследования [18, 19].
ТМС волны А как косвенный показатель сократимости ЛП у больных пароксизмальной ФП была выше, чем у лиц с персистирующей ФП (р=0,01). Но, пожалуй, более очевидной иллюстрацией лучшей сохранности сократительной функции ЛП при пароксизмальной ФП может рассматриваться то, что, согласно данным ЭхоКГ методом speckle-tracking, ГДЛП как в фазу наполнения, так и в фазу сокращения при этом варианте аритмии была достоверно выше, чем в группе пациентов с персистирующей ФП (р=0,0002). Отсутствие существенных межгрупповых различий по медианам E/E', DT и ВИВР, свидетельствующее об определенной сопоставимости спектра диастолических расстройств, по-видимому, может рассматриваться в качестве аргумента в пользу того, что тяжесть ФП оказывает самостоятельное дополнительное влияние на формирование структурно-функциональных расстройств ЛП.
При этом несмотря на такие отличия в структуре и функции ЛП, пациенты с пароксизмальной и персистирующей формами ФП не имели статистически значимых различий по представительству категорий риска развития ТЭО. Однако данное обстоятельство, скорее всего, не исключает связи формы ФП с вероятностью развития ТЭО, так как формирование групп по риску в нашем исследовании осуществлялось в соответствии с действующим алгоритмом, не учитывающим состояние ЛП.
Оценка риска развития ТЭО у больных ФП основана на использовании клинических характеристик, что делает ее простой и доступной в большинстве случаев [15]. Шкала CHADS2 была валидизирована в 2001 г. применительно к популяции США, шкала CHA2DS2VASc появилась спустя 9 лет и ориентрована на европейскую популяцию. Мета-анализ, выполненный J.-Y. Chen и соавт. и включавший 317 389 больных ФП, показал, что C-статистическая прогностическая мощность обеих шкал сопоставима: для CHADS2 она составляла 0,683 (при 95% ДИ от 0,60 до 0,80), а для шкалы CHA2DS2VASc — 0,673 (при 95% ДИ от 0,64 до 0,79) [23]. Вместе с этим при оценке риска по шкале CHA2DS2VASc≥1 балла чувствительность шкалы достигает 100%, что делает ее прогностическую ценность выше, чем шкалы CHADS2, в отношении больных ФП с «истинно» низким риском развития ТЭО [24]. Между тем при анализе категориальных показателей шкала CHADS2 является более мощным прогностическим инструментом, так как при индексировании по шкале CHA2DS2VASc больше пациентов попадают в категорию высокого риска развития ТЭО, что уменьшает долю больных ФП с умеренным риском [23]. Поскольку шкала CHA2DS2VASc учитывает половую принад-лежность, вполне логично, что женщины с ФП и умеренным риском развития ТЭО по шкале CHADS2 при использовании шкалы CHA2DS2VASc перейдут в категорию высокого риска, что увеличит долю пациентов женского пола, получающих антикоагулянты, по сравнению с лицами мужского пола.
Так как клинические шкалы обладают лишь умеренной дискриминационной способностью в отношении риска развития ТЭО, одной из центральных задач является поиск новых предикторов риска у больных ФП. Так, некоторые показатели, отражающие физиологические процессы, связанные с ФП и инфарктом головного мозга, при добавлении к клиническим шкалам позволяют усилить их прогностическую значимость [25]. К ним можно отнести маркеры тромбоза (фактор Виллебранда, D-димер), функции почек (СКФ, расчитанная по клиренсу креатинина или цистатину С, протеинурия), некроза миокарда (тропонины), воспаления (интерлейкин-6), натрийуретические пептиды (NT-proBNP, BNP) [25, 26].
В последние годы в связи с возросшей доступностью ЭхоКГ и своершенствованием оценки структурно-функциональных характеристик ЛП повысился интерес к уточнению их прогностической значимости. При этом особое внимание уделяется параметрам сократительной активности ЛП, в том числе новым, определяемым методом speckle-tracking [20, 21].
Так, в некоторых исследованиях выявлялись ассоциации между продольной деформацией ЛП и риском развития инфаркта головного мозга. В работе J. Shih и соавт., включавшей 66 больных постоянной ФП, независимыми предикторами инфаркта головного мозга были продольная деформация ЛП в фазу наполнения и скорость продольной деформации в резервуарную фазу [27]. В исследовании S. Saha и соавт. сопоставлялись исходы у 36 больных с неклапанной ФП по сравнению с 41 пациентом без ФП: сниженная ГДЛП являлась предиктором высокого риска развития ТЭО (ОР 0,86; р=0,02) у лиц с ФП [28].
В нашем исследовании больные с оценкой по шкале CHA2DS2VASc≥2 баллов имели достоверно более высокий ИММЛЖ при сопоставимых значениях ГДЛЖ во всех 3 подгруппах риска развития ТЭО. Более интересным представляется то, что при повышении риска развития ТЭО по шкале CHA2DS2VASc линейные и объемные характристики ЛП оставались соизмеримыми, а функциональные нарушения ЛП усугублялись.
В соответствии с текущими рекомендациями по лечению ФП [1, 2] пациенты с оценкой по CHA2DS2VASc 1 балл могут получать для профилактики ТЭО дезагреганты, но более предпочтительным является применение антикоагулянтов. Выявленная нами достоверная связь между более высокой ГДЛПн и более низким индексом CHA2DS2VASc свидетельствует о возможности использования значений ГДЛПн для облегчения выбора между дезагрегантами и антикоагулянтами у больных данной категории. С целью определения критериальных значений этого показателя нами проведен ROC-анализ, который продемонстрировал, что эффективное пороговое значение ГДЛП в фазе наполнения менее 16,7% позволяет выделить группу пациентов с ФП и высоким риском развития ТЭО с чувствительностью 62,5% и специфичностью 39%, при этом площадь под ROC-кривой 0,85 (при 95% ДИ от 0,72 до 0,98; p=0,002) дает основание расценить дискриминационную мощность данной модели как умеренную, т.е. имеющую клиническую значимость. Оказалось, что у 2 из 7 пациентов с умеренным риском развития ТЭО ГДЛПн была ниже 16,7%, что может быть использовано в качестве дополнительного аргумента в пользу выбора у них антикоагулянтов, как средства профилактики ТЭО. Усилить мотивацию к назначению препаратов этой группы данный показатель может, по-видимому, и в ситуации, когда у пациента имеется повышенный риск кровотечений.
Заключение
Таким образом, более тяжелое течение рецидивирующей фибрилляции предсердий ассоциируется с более выраженными структурно-функциональными изменениями левого предсердия. Наряду с этим нормальные линейные размеры левого предсердия не исключают его структурного ремоделирования, более точной оценкой которого является индекс объема левого предсердия. Cнижение глобальной деформации левого предсердия в фазу наполнения служит независимым предиктором повышения индекса риска тромбоэмболических осложнений. При этом полученное в ходе ROC-анализа эффективное пороговое значение глобальной деформации левого предсердия, равное 16,7%, позволяет разграничить пациентов с умеренным и высоким риском развития тромбоэмболических осложнений, что может иметь практическое значение для выбора тактики назначения пероральных антикоагулянтов у больных с оценкой по шкале CHA2DS2VASc 1 балл и пациентов с высоким риском кровотечений.



