Главным фактором риска развития сердечно-сосудистых заболеваний (ССЗ) с точки зрения причин летальных исходов эксперты признают повышенное артериальное давление (13% общего числа летальных исходов в мире), курение (9%), повышенный уровень глюкозы в крови (6%), низкую физическую активность (6%) и ожирение (5%) [1, 2]. Повышенный уровень ХС в крови также значительно увеличивают риск развития ишемической болезни сердца (ИБС) и инсульта [1—3]. Данные доказательной медицины свидетельствуют о существенном улучшении прогноза жизни за счет использования гиполипидемических лекарственных средств [4, 5]. Поэтому в последние годы научный фармацевтический потенциал активно направил свои усилия на создание нескольких новых классов препаратов, снижающих уровень ХС. Так, в июле и августе 2015 г. получили рекомендации к одобрению от Управления по контролю за качеством пищевых продуктов и лекарственных препаратов США (FDA) и Европейского агентства по лекарственным средствам (EMA) моноклональные антитела к ферменту пропротеин конвертаза субтилизин/кексина 9-го типа препараты алирокумаб и эволокумаб [6, 7], снижающие уровень липопротеинов низкой плотности (ЛНП) более чем на 60%; продолжают изучаться ингибиторы белка — переносчика эфиров ХС, блокаторы синтеза апопротеина В, производные тиреоидных гормонов. В то же время врач в практической медицине при выборе препаратов руководствуется, прежде всего, клиническими рекомендациями, результатами доказательной медицины и ограничительными списками лекарственных средств. В Российских рекомендациях «Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза» представлены статины, фибраты, cеквестранты желчных кислот, ингибиторы всасывания ХС в кишечнике, ниацин и препараты, содержащие ω-3-полиненасыщенные жирные кислоты (ПНЖК) [8]. Статины являются наиболее эффективными и хорошо переносимыми препаратами для коррекции повышенного уровня общего ХС, триглицеридов (ТГ), и, что особенно ценно, ЛНП. Экспертами проведено ранжирование статинов по силе действия с акцентом на наибольшую эффективность розувастатина [8], а, следовательно, прогнозируемость достижения целевых уровней ключевых составляющих липидного обмена. Базовые принципы применения статинов для первичной и вторичной профилактики сердечно-сосудистых заболеваний и их осложнений отражены в клинических рекомендациях ведущих европейских, американских и отечественных кардиологических сообществ и не имеют принципиальных различий в основе принятия решения о назначении гиполипидемической терапии (ГЛТ), ориентируя врачей на степени риска развития сердечно-сосудистых осложнений (ССО), рассчитанные по общеизвестным шкалам [8—10]. В то же время в клинической практике целенаправленные исследования по ряду нозологий доказали, что тактика и стратегия врачебных решений в отношении различных клинико-фармакологических групп лекарственных средств нередко весьма далеки от современных клинических рекомендаций [11—18].
 Цель: в рамках фармакоэпидемиологического исследования изучить тактику врачебных назначений гиполипидемических лекарственных средств у пациентов с гипертонической болезнью (ГБ) и дислипидемией.
Цель: в рамках фармакоэпидемиологического исследования изучить тактику врачебных назначений гиполипидемических лекарственных средств у пациентов с гипертонической болезнью (ГБ) и дислипидемией.
Материал и методы
Проведен ретроспективный фармакоэпидемиологический анализ назначения статинов по данным источников первичной медицинской документации за 2013—2014 гг. методом сплошной последовательной выборки историй болезни и амбулаторных карт пациентов с верифицированной ГБ. В выборку включены все последовательно поступившие 482 пациента в течение одного из месяцев 2013—2014 гг. в нескольких стационарах, поликлиниках и центральных районных больницах Краснодарского края. Анализировали врачебные назначения больным ГБ в рекомендациях при выписке из стационара и на амбулаторном этапе лечения. Для обобщения первичных результатов использовали методы описательной статистики с представлением абсолютных (n) и относительных (%) переменных.
Результаты
Средний возраст пациентов составил 62,2±8,7 года, из них 41,7% мужчины. По сведениям из медицинской документации более 50% пациентов курили, ожирение и избыточную массу тела имели 36,3%, однако ключевые антропометрические показатели, в том числе окружность талии, в более половине документов не указаны или не мониторировались. Сахарным диабетом 2-го типа страдали 11,4% пациентов, ИБС — 29,5%, инсульт перенесли 11%, фибрилляция предсердий (ФП) указана у 5,8% пациентов.
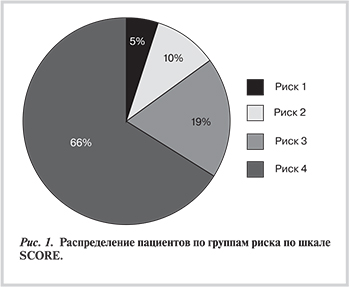
Уровень общего ХС и ТГ в сыворотке крови исследован у всех пациентов. Фракции ХС определены менее чем у 50% пациентов. Калькуляция риска развития ССЗ по шкале SCORE (Systematic Coronary Risk Estimation) указана у 88,2%, преимущественно у пациентов из группы высокого и очень высокого риска. По данным из медицинской документации нами проведен пересчет степени риска у всех пациентов в соответствии с рекомендациями Российского общества кардиологов [8], максимальное совпадение с записью врача регистрировалось у пациентов из группы высокого и очень высокого рисков (84,6 и 75% соответственно), минимальное — в группе умеренного риска (16%). Распределение пациентов по группам риска по шкале SCORE представлено на рис. 1.
Следует отметить, что почти у 1/4 пациентов однократно указанный в амбулаторной карте уровень риска не пересчитывался ни разу, несмотря на изменение возраста, медикаментозную компенсацию систолического давления и снижение уровня ХС.
Для более 80% пациентов в качестве ГЛТ врачами рекомендовалась монотерапия статинами.
Результаты анализа всей выборки для оценки назначения гиполипидемических схем свидетельствуют об использовании врачами нескольких вариантов лечения (табл. 1).
В нашем исследовании у большинства пациентов врачи инициировали назначение розувастатина с 5 мг/сут, аторвастатина и симвастатина с 10 мг/сут, несмотря на уровни атерогенных липидов, существенно превосходивших возможности минимальных доз этих препаратов в отношении достижения целевых значений.
 Фибрат назначен в виде монотерапии 3,8% пациентов, причем за исключением 3 человек препарат применялся без предшествующего статина, несмотря на наличие повышения уровней как ЛНП, так и ТГ. Имелись единичные назначения комбинации статина и фибрата, статина и омакора. У 2 пациентов эзетимиб добавлен в отсутствие достижения целевых уровней на фоне максимальной дозы статинов, у 4 — на фоне начальной и средней дозы. Чаще всего врачи выписывали генерические препараты — 84,2%. Антиагреганты назначены у 63,1% больных, антикоагулянты — у 8,9%. Все пациенты получали антигипертензивную терапию: ингибиторы ангиотензинпревращающего фермента (АПФ) — 59,3%, сартаны — 31,1%, антагонисты кальция — 34,9%, β-адреноблокаторы — 58,1%, диуретики — 23,9%, альфа1-адреноблокаторы — 7,9%, центральные агонисты адренергических систем — 9,9%, фиксированную комбинацию антигипертензивных лекарственных средств получали 21,6% пациентов (рис. 2).
Фибрат назначен в виде монотерапии 3,8% пациентов, причем за исключением 3 человек препарат применялся без предшествующего статина, несмотря на наличие повышения уровней как ЛНП, так и ТГ. Имелись единичные назначения комбинации статина и фибрата, статина и омакора. У 2 пациентов эзетимиб добавлен в отсутствие достижения целевых уровней на фоне максимальной дозы статинов, у 4 — на фоне начальной и средней дозы. Чаще всего врачи выписывали генерические препараты — 84,2%. Антиагреганты назначены у 63,1% больных, антикоагулянты — у 8,9%. Все пациенты получали антигипертензивную терапию: ингибиторы ангиотензинпревращающего фермента (АПФ) — 59,3%, сартаны — 31,1%, антагонисты кальция — 34,9%, β-адреноблокаторы — 58,1%, диуретики — 23,9%, альфа1-адреноблокаторы — 7,9%, центральные агонисты адренергических систем — 9,9%, фиксированную комбинацию антигипертензивных лекарственных средств получали 21,6% пациентов (рис. 2).
Оригинальные антигипертензивные препараты указаны у 17,4% пациентов. Не применялись опасные и нерациональные комбинации препаратов. Комбинация антагониста кальция с симвастатином в нежелательной дозе (более 20 мг/сут) отмечена у 6 пациентов.
Обсуждение
Стратегически важным аспектом внимания практического врача должна быть нацеленность на снижение риска развития инвалидности и смерти, связанной с атеротромботическими процессами. Анализ историй болезни и амбулаторных карт пациентов с ГБ показал понимание и принятие врачебным сообществом региона, в котором проведено исследование, основных современных подходов к решению этой задачи, озвученных в согласительных клинических рекомендациях отечественных и зарубежных экспертов [8—10]. По европейской шкале SCORE определение суммарного риска развития ССЗ и их осложнений основано на следующих параметрах: возраст, пол, уровень общего ХС, статус курения, систолическое артериальное давление [8, 10]. У большинства пациентов в нашей выборке указаны риски развития сердечно-сосудистых осложнений, учтены модифицируемые и немодифицируемые факторы, у всех имеются данные об уровне общего ХС и ТГ. Сравнение степени риска, определенное врачом, со степенью риска в контрольном подсчете по шкале SCORE показало максимальное совпадение для высокого и очень высокого риска, что, по-видимому, связано с простотой определения этих степеней риска при наличии у пациента в анамнезе клинических проявлений атеросклероза. Кроме того, в этих подгруппах более часто определялись фракции ХС. Общеизвестно, что в алгоритмах оценки риска допускается использование уровня общего ХС [8, 10], однако с учетом многочисленных сведений о разнонаправленности действия отдельных фракций ХС, а также выбора в европейских и отечественных руководствах ЛНП в качестве терапевтической цели ГЛТ [8, 10], представляется необходимым усилить информированность врачей и нацеленность лечебно-профилактических учреждений на определении фракций ХС, применении лекарственных средств с наивысшей доказательной базой. Проблема внедрения данных доказательной медицины в клиническую практику является предметом пристального внимания клинических фармакологов. Несомненно, способствовать этому процессу будут мероприятия по повышению информированности врачей, в частности, открытие в России в 2015 г. филиала Северного Кокрейновского Центра — Кокрейн Россия [19].
Особенно важно знание уровня ЛНП у пациентов с низким и умеренным риском, так как ключевым критерием в решении вопроса о начале ГЛТ в данном случае будет именно этот показатель [8]. Между тем данные нашего исследования указывают на более поверхностный подход к верификации дислипидемии именно у пациентов с низким и умеренным риском, информации в большинстве документов о них недостаточно для правильного решения о назначении ГЛТ.
В наше исследование включены два пациента с артериальной гипертензией (АГ) и ортотопической трансплантацией печени. Несмотря на выраженную дислипидемию, они не получали ГЛТ, что, вероятно, связано с распространенным мнением врачей об опасности применения статинов при патологии печени. Гиперхолестеринемия нехарактерна для пациентов с циррозом в связи со снижением синтеза ХС в печени. У 45—60% пациентов развивается дислипидемия после трансплантации, что требует обязательного назначения ГЛТ. Имеющиеся данные наблюдения за пациентами с донорскими органами показывают существенное повышение ССЗ, связанных с ятрогенными нарушениями липидного обмена, вызванными применением иммуносупрессивной терапии [20—23].
Отдельного внимания заслуживает проблема адекватности контроля ГЛТ. Клиницисты, во-первых, не всегда помнят о том, что в отличие от ЛНП общий ХС является лишь ориентировочным критерием эффективности препаратов, во-вторых, нередко игнорируют титрование дозы и применение комбинации гиполипидемических препаратов до целевых значений липидного профиля. В результате даже амбулаторные больные, наблюдающиеся в течение нескольких лет с указанным риском развития ССО, не имеют тех шансов на сохранение жизни и трудоспособности, которые продемонстрированы в многоцентровых рандомизированных плацебо-контролируемых исследованиях. Задача достижения целевых уровней ЛНП наиболее просто и надежно решается при применении розувастатина. Данные авторитетных исследований свидетельствуют о неоспоримом преимуществе розувастатина по степени снижения уровня ХС в сравнении с аторвастатином, симвастатином, правастатином. В исследовании STELLAR (Statin Therapies for Elevated Lipid Levels compared Across doses to Rosuvastatin) продемонстрирована высокая гиполипидемическая эффективность всех доз розувастатина в сравнении с вышеперечисленными препаратами у пациентов с дислипидемией и клиническими проявлениями атеросклероза: ИБС, инфарктом миокарда в анамнезе, цереброваскулярными заболеваниями, транзитопными ишемическими атаками, заболеваниями периферических и коронарных артерий, сахарным диабетом [24, 25]. Результаты мета-анализа свидетельствуют, что 10 мг розувастатина снижают уровень ЛНП аналогично 30 мг аторвастатина [26]. Информация о наивысшей фармакодинамической активности розувастатина в сравнении с другими статинами проанализирована и подчеркнута экспертами в клиническом руководстве [8]. Результаты нашего фармакоэпидемиологического исследования свидетельствуют о приоритетах выбора аторвастатина и симвастатина, несмотря на большое число в выборке пациентов, имеющих существенные риски развития ССО и показания к более интенсивной ГЛТ. Определяющими факторами этого тактического диссонанса является, прежде всего, более давний выход на фармацевтический рынок аторвастатина и симвастатина, что обеспечило в настоящее время высокое информационное насыщение субъектов обращения лекарственных средств и наличие большого количества дженериков этих препаратов. Общеизвестно, что в последние годы выписывать лекарственное средство лечащему врачу приходится, учитывая не только данные о его эффективности, но и о его цене. Поэтому нередко основной причиной, сдерживающей применение статинов, является их высокая стоимость [27]. После окончания срока патентной защиты на фармацевтическом рынке представлены несколько дженерических препаратов розувастатина, что позволяет сделать это лекарственное вещество доступнее для пациента как в розничном отпуске, так и в условиях современного финансирования лечебно-профилактических учреждений. В ряде случаев врачи указывали торговое наименование препарата, что позволило выявить приоритетность назначения дженериков. В дальнейших исследованиях, вероятно, не будет возможности с помощью используемого нами метода оценки фармакотерапии по первичной медицинской документации ориентироваться в структуре назначения оригинальных и дженерических лекарственных средств в связи с необходимостью с июля 2013 г. в соответствии с Приказом №1175 [28] выписывать препараты по международному непатентованному названию. Мы сравнили прямую стоимость лечения с некоторыми взаимозаменяемыми препаратами розувастатина, упоминающимися в первичной медицинской документации нашего исследования (рис. 3).
Данные о ценах на препараты получены одномоментно из базы «Аналоги лекарств» от 25.06.2015 [29]. Обращает внимание ценовое преимущество препарата тевастор — розувастатин компании «Тева»*, Израиль. В базе данных FDA большинство препаратов этой компании находятся в ранге кода «AB», обозначающего максимальную эквивалентность оригинальному препарату. Тевастор — единственный розувастатин, зарегистрированный в FDA помимо оригинального препарата [7]. В России тевастор представлен в полном спектре дозировок (5, 10, 20 и 40 мг), в упаковках на 30 дней и 90 дней приема, что обеспечивает лучшую ценовую доступность и в начале лечения оптимизирует подбор дозы, повышая приверженность пациента к лечению. Вкупе с данными о стоимостной доступности тевастор в настоящее время в условиях ограниченного финансирования здравоохранения может быть рекомендован в качестве доминирующей альтернативы в линейке розувастатинов, так как оригинальный препарат более чем в 5 раз дороже, а ближайшие изученные в нашем исследовании аналоги розарт, розукат и роксера дороже на 27,5, 47,5 и 57,3% соответственно. Высокая эффективность розувастатина в отношении снижения атерогенных фракций ХС, ТГ [8] обеспечивает выраженный профилактический эффект в отношении ССО атеросклеротического генеза. В дозе 10 мг розувастатин снижал содержание ТГ на 20% и повышал уровень ЛНП на 8%, снижал уровень ХС ЛП на 46%, в то время как аторвастатин в дозе 20 мг — на 43%, симвастатин в дозе 40 мг — на 39% и правастатин в дозе 40 мг — на 30% соответственно. В среднем прием розувастатина обеспечивает снижение уровня ЛНП на 52—63% для доз 10—40 мг соответственно [24, 25].
В исследовании JUPITER (Justification for the Use of statins in Prevention: anIntervention Trial Evaluating Rosuvastatin) выяснялась способность розувастатина к первичной профилактике ССЗ у более 17 тыс. пациентов без клинических симптомов, рандомизированных в 2 группы терапии — розувастатином 20 мг/сут и плацебо с максимальной продолжительностью динамического наблюдения 5 лет. Доказано снижение частоты развития фатального/нефатального инфаркта миокарда, фатального/нефатального инсульта [30]. Значительное снижение уровня ЛНП и повышение концентрации липопротеидов высокой плотности у пациентов с ИБС показано в исследовании ASTEROID (A Study To Evaluate the Effect of Rosuvastatin on Intravascular Ultrasound-Derived Coronary Atheroma Burden). Розувастатин назначали в течение 2 лет в дозе 40 мг с целевым уровнем ЛНП менее 1,8 ммоль/л. В результате лечения при повторной ангиографии выявлено уменьшение объема атеросклеротической бляшки в наиболее суженном сегменте в среднем на 9,1% [31]. Эти и ряд других исследований позволили обосновать выбор розувастатина как для первичной (в том числе у пациентов без клинических признаков ИБС), так и для вторичной профилактики ССЗ [8—10, 32].
 Факторы риска развития основных фатальных сердечно-сосудистых катастроф, связанных с атеротромботическим процессом, в большинстве своем совпадают. В частности, АГ и дислипидемия редко встречаются изолированно ввиду их широкой распространенности и частого сочетания и являются ведущими факторами риска развития ИБС, атеротромботических осложнений. Уникальна дуальность значимости АГ в судьбе пациента; в отличие от других факторов риска развития атеросклеротических ССЗ АГ является одновременно их и причиной, и следствием. В современных согласительных документах ведущих международных организаций АГ представлена и как фактор, стимулирующий процесс атеросклероза, и как ССЗ, развивающееся в результате атеросклероза [2]. Возможность медикаментозной модификации этого важнейшего патологического состояния должна быть максимально использована в лечебно-профилактическом учреждении любого профиля. В нашем исследовании показано, что и в историях болезни стационарных пациентов, и в амбулаторном звене оказания медицинской помощи всем пациентам рекомендовались антигипертензивные препараты с представленностью всех клинико-фармакологических групп за исключением прямого блокатора ренина. Приоритетом пользуются ингибиторы АПФ, что согласуется с данными других авторов [15, 33]. Понятен выбор врачей в отношении препаратов этих классов как максимально интактных в прогрессировании нарушений липидного обмена, с положительным влиянием на регуляторно-адаптивный статус пациентов [32, 34, 35]. Велика доля больных, получающих антагонисты кальция, также влияющих позитивно на липидный и углеводный обмен [32]. В контексте широкой распространенности дислипидемии и АГ следует отметить недавно выявленную негативность комбинации верапамила и симвастатина, не позволяющую в клинической практике увеличивать дозу симвастатина выше 20 мг из-за существенного повышения вероятности неблагоприятных эффектов этого препарата [32]. Поскольку аторвастатин также метаболизируется CYP3A4, его концентрация при применении в дозе 40 мг может увеличится на фоне дилтиазема в дозе 240 мг [32]. В отличие от симвастатина и аторвастатина розувастатин клинически значимо не взаимодействует с изоферментами цитохрома P450 [32], поэтому при применении этого препарата отмечается низкая вероятность нежелательных лекарственных взаимодействий, что особенно важно в условиях вынужденной полипрагмазии. Важно отметить, что в ряде исследований у пациентов с ФП статины продемонстрировали позитивный эффект. Их изучение в крупном мета-анализе 15 рандомизированных исследований показало, что использование статинов снизило риск развития любой формы ФП на 45%, впервые выявленной ФП — на 32%, рецидивов ФП — на 57%, рецидивов ФП после кардиоверсии — на 42% и послеоперационной ФП — на 58% снижения количества рецидивов пароксизмальной ФП [36]. Факты и механизмы антиаритмического действия статинов активно обсуждаются в последние годы [37—40]. В исследовании GISSI HF использование розувастатина по сравнению с плацебо у пациентов с хронической сердечной недостаточностью без пароксизмов ФП в анамнезе снижало частоту впервые выявленной ФП [41]. Как известно, у пациентов с ФП и рядом других нарушений ритма сердца амиодарон является препаратом выбора с целью профилактики и лечения аритмии. В нашем исследовании более 20 пациентов получали амиодарон и симвастатин. Известно, что для пациентов, принимающих амиодарон, верапамил, амлодипин или дилтиазем одновременно с симвастатином, суточная доза симвастатина не должна превышать 20 мг [32]. С учетом данных инструкции о минимизации дозы симвастатина в комбинации с амиодароном, а, следовательно, снижении шансов достичь целевых уровней ЛНП, более рациональным выбором в таких случаях являются статины, не вступающих в негативное фармакокинетическое взаимодействие с амиодароном, в частности, розувастатин, который не является ни ингибитором, ни индуктором изоферментов цитохрома Р450 [32].
Факторы риска развития основных фатальных сердечно-сосудистых катастроф, связанных с атеротромботическим процессом, в большинстве своем совпадают. В частности, АГ и дислипидемия редко встречаются изолированно ввиду их широкой распространенности и частого сочетания и являются ведущими факторами риска развития ИБС, атеротромботических осложнений. Уникальна дуальность значимости АГ в судьбе пациента; в отличие от других факторов риска развития атеросклеротических ССЗ АГ является одновременно их и причиной, и следствием. В современных согласительных документах ведущих международных организаций АГ представлена и как фактор, стимулирующий процесс атеросклероза, и как ССЗ, развивающееся в результате атеросклероза [2]. Возможность медикаментозной модификации этого важнейшего патологического состояния должна быть максимально использована в лечебно-профилактическом учреждении любого профиля. В нашем исследовании показано, что и в историях болезни стационарных пациентов, и в амбулаторном звене оказания медицинской помощи всем пациентам рекомендовались антигипертензивные препараты с представленностью всех клинико-фармакологических групп за исключением прямого блокатора ренина. Приоритетом пользуются ингибиторы АПФ, что согласуется с данными других авторов [15, 33]. Понятен выбор врачей в отношении препаратов этих классов как максимально интактных в прогрессировании нарушений липидного обмена, с положительным влиянием на регуляторно-адаптивный статус пациентов [32, 34, 35]. Велика доля больных, получающих антагонисты кальция, также влияющих позитивно на липидный и углеводный обмен [32]. В контексте широкой распространенности дислипидемии и АГ следует отметить недавно выявленную негативность комбинации верапамила и симвастатина, не позволяющую в клинической практике увеличивать дозу симвастатина выше 20 мг из-за существенного повышения вероятности неблагоприятных эффектов этого препарата [32]. Поскольку аторвастатин также метаболизируется CYP3A4, его концентрация при применении в дозе 40 мг может увеличится на фоне дилтиазема в дозе 240 мг [32]. В отличие от симвастатина и аторвастатина розувастатин клинически значимо не взаимодействует с изоферментами цитохрома P450 [32], поэтому при применении этого препарата отмечается низкая вероятность нежелательных лекарственных взаимодействий, что особенно важно в условиях вынужденной полипрагмазии. Важно отметить, что в ряде исследований у пациентов с ФП статины продемонстрировали позитивный эффект. Их изучение в крупном мета-анализе 15 рандомизированных исследований показало, что использование статинов снизило риск развития любой формы ФП на 45%, впервые выявленной ФП — на 32%, рецидивов ФП — на 57%, рецидивов ФП после кардиоверсии — на 42% и послеоперационной ФП — на 58% снижения количества рецидивов пароксизмальной ФП [36]. Факты и механизмы антиаритмического действия статинов активно обсуждаются в последние годы [37—40]. В исследовании GISSI HF использование розувастатина по сравнению с плацебо у пациентов с хронической сердечной недостаточностью без пароксизмов ФП в анамнезе снижало частоту впервые выявленной ФП [41]. Как известно, у пациентов с ФП и рядом других нарушений ритма сердца амиодарон является препаратом выбора с целью профилактики и лечения аритмии. В нашем исследовании более 20 пациентов получали амиодарон и симвастатин. Известно, что для пациентов, принимающих амиодарон, верапамил, амлодипин или дилтиазем одновременно с симвастатином, суточная доза симвастатина не должна превышать 20 мг [32]. С учетом данных инструкции о минимизации дозы симвастатина в комбинации с амиодароном, а, следовательно, снижении шансов достичь целевых уровней ЛНП, более рациональным выбором в таких случаях являются статины, не вступающих в негативное фармакокинетическое взаимодействие с амиодароном, в частности, розувастатин, который не является ни ингибитором, ни индуктором изоферментов цитохрома Р450 [32].
Заключение
Таким образом, розувастатин как для первичной, так и для вторичной профилактики ССЗ у многих пациентов является доминирующей альтернативой выбора не только в связи с наиболее выраженным ХС-снижающим действием, но и в связи с высокой безопасностью при вынужденной полипрагмазии и/или в сочетании с рядом препаратов с высоким риском опасного взаимодействия с другими статинами. Сравнение в нашей работе розувастатина нескольких производителей по прямой стоимости показывает фармакоэкономическое преимущество тевастора, что обеспечивает и его лучшую ценовую доступность для субъектов обращения лекарственных средств и укрепление приверженности пациентов к лечению. Наше фармакоэпидемиологическое исследование сформировано на базе ключевого фактора — диагноза ГБ у пациентов, находящихся на стационарном и амбулаторном лечении. В целом врачи соблюдают принципы верификации риска развития ССО, большинству пациентов назначена ГЛТ. В то же время следует обратить внимание на необходимость определения уровня ЛНП и как маркера начала ГЛТ при умеренном и низком рисках и как контроля эффективности ГЛТ у всех пациентов. Не зафиксировано назначение препаратов вне показаний и при наличии противопоказаний, не выявлено превышения доз и нерациональных комбинаций ни в одной из применяемых клинико-фармакологических групп препаратов, за исключением превышения дозы симвастатина в комбинации с верапамилом. В данной публикации оценивались лишь фармакоэпидемиологические приоритеты ГЛТ. В последующем будут обсуждаться вопросы достижения целевых значений ключевых параметров липидного обмена, регулярность контроля эффективности и безопасности статинов и их комбинаций с другими гиполипидемическими средствами. Анализ современных отечественных и зарубежных рекомендаций по дислипидемии, а также данные доказательной медицины свидетельствуют о том, что использование статинов является устойчивой долговременной тенденцией первичной и вторичной профилактики ССО. В связи с этим необходимо продолжить работу по оценке фармакоэкономических показателей этой клинико-фармакологической группы препаратов, повысить информированность врачей, усилить контроль качества оказания медицинской помощи пациентам с ССЗ.



