В последнее время среди нарушений электролитного баланса дефицит магния становится все более распространенным. По данным разных авторов, дефицит магния встречается у 15—33% населения [1, 2]. У больных с сердечно-сосудистыми заболеваниями распространенность данной патологии минерального обмена колеблется еще в более широких пределах (от 10 до 70%), особенно при лечении петлевыми диуретиками и сердечными гликозидами [3—7]. Кроме того, дефицит магния часто встречается при алкоголизме, сахарном диабете, ожирении, пролапсе митрального клапана [8—11]. Влияние дефицита магния на аритмогенный порог достаточно изучено [12—14], в то время как кардиодинамические эффекты магния, по мнению различных авторов, неоднозначны [14—17]. Кроме того, в литературе отсутствуют данные об изменении функциональных резервов миокарда в условиях алиментарного магниевого дефицита.
Целью исследования являлась оценка функциональных резервов миокарда у животных с дефицитом магния при проведении нагрузочных тестов.
Материал и методы
Эксперименты выполнены на 39 крысах-самцах массой 200—240 г. Животных содержали в условиях вивария согласно правилам лабораторной практики при проведении доклинических исследований в РФ (ГОСТ Р 50258-92, ГОСТ З 51000.3-96 и 51000.4-96), с соблюдением международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997). Эксперименты были одобрены комитетом по этической экспертизе исследований Волгоградского ГМУ. Интактная группа животных составляла контроль (n=21). У 18 крыс вызывали магнийдефицитное состояние, для моделирования которого использовали специальную магнийдефицитную диету. В состав диеты входили казеин (20%), крахмал (70%), DL-метионин (0,3%), холина битартрат (0,2%), кукурузное масло (5%), поливитаминная смесь (1%) и полиминеральная смесь, не содержащая магний (3,5%), аналогичная полиминеральной смеси AIN-76 фирмы MP Biomedicals (США).
Весь рацион готовили на деионизированной воде, эту же воду в ходе эксперимента использовали в качестве питьевой для животных, находящихся на диете. Интактные животные получали полноценную диету, содержащую 0,84 г MgO на 1 кг рациона, что соответствовало 0,5 г элементарного магния на 1 кг рациона.
Скорость и глубину развития гипомагниемии контролировали, определяя содержание магния в эритроцитах животных по цветной реакции с титановым желтым [18]. При снижении концентрации магния менее 1,4 ммоль/л в эритроцитах считали, что у животных развилась гипомагниемия средней тяжести. На 71-й день диеты проводили регистрацию основных показателей кардио- и гемодинамики. Животных предварительно наркотизировали (этаминал натрия 40 мг/кг, внутрибрюшинно), в условиях искусственной вентиляции легких выполняли торакотомию и перикардотомию. Для измерения внутрижелудочкового давления и его первой производной (+dp/dt и –dp/dt), частоты сердечных сокращений (ЧСС) через верхушку сердца в полость левого желудочка вводили катетер — иглу, соединенную с датчиком (Элема, Швеция). Для измерения систолического и диастолического артериального давления (АД) катетеризировали общую сонную артерию, катетер также соединяли с датчиком. Данные показатели записывали и обрабатывали с помощью универсальной компьютерной многоканальной системы обработки сигналов в реальном времени ВЕАТ (Москва, 2000). Интенсивность функционирования структур получали расчетным способом по формуле [19, 20]:
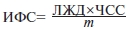
где m — масса левого желудочка + 2/3 массы межжелудочковой перегородки в миллиграммах, ИФС — интенсивность функционирования структур.
Коэффициент массы сердца рассчитывали как отношение массы сердца к массе тела.
После периода стабилизации регистрируемых показателей (10 мин) поочередно проводили функциональные пробы: нагрузка объемом, дозированная стимуляция адренорецепторов сердца, максимальная изометрическая нагрузка. В качестве нагрузки объемом использовали быстрое внутривенное введение (в течение 1 с) изотонического раствора хлорида натрия 0,3 мл на 100 г массы животного [20]. Дозированную стимуляцию адренорецепторов сердца осуществляли путем введения адреналина внутривенно в разведении 10–6 г/л из расчета 0,1 мл/100 г массы тела. Максимальную изометрическую нагрузку (пережатие восходящей части дуги аорты) обеспечивали в течение 20 с [19, 20]. Используемые функциональные пробы позволяли выявить ино- и хронотропные резервы сердца.
Статистическую обработку данных проводили с помощью программы Statistica 6.0. Для сравнения средних значений показателей использовали критерий Манна—Уитни. Различия считали статистически значимыми при p<0,05.
Результаты
У крыс, находящихся на магнийдефицитной диете, к концу 10-й недели наблюдалось достоверное снижение уровня магния в эритроцитах в среднем на 54% (с 2,01±0,09 до 0,92±0,07 ммоль/л) в сравнении с группой интактных крыс (p<0,05). Снижение концентрации магния в эритроцитах сопровождалось изменением внешнего вида животных (потускнение шерстного покрова, гиперемия открытых участков тела — ушных раковин, хвоста и лап). Полученные данные подтверждают ранее полученные результаты работ других авторов в условиях дефицита магния [7].
У животных с дефицитом магния до проведения нагрузочных тестов отмечалась тенденция к росту левожелудочкового давления на 13,5% (с 94±3,2 до 107,7±4,0 мм рт.ст.), скорости сокращения — на 10% (с 2489,7±125,2 до 2740,8±174,3 мм рт.ст. в секунду), скорости расслабления — на 6,7% (с 1804,3±61,76 до 1925±49,7 мм рт.ст. в секунду) по сравнению с контрольной группой. Систолическое АД достоверно превышало на 17% (100±6 и 85±3 мм рт.ст.), а диастолическое — на 27% (79±4 и 62±4 мм рт.ст.), аналогичные показатели у интактных животных, ЧСС превышала контрольные значения на 9% (р<0,05). Коэффициенты массы сердца у контрольных и магнийдефицитных животных статически значимо не различались (0,40±0,03 и 0,39±0,03 соответственно).
В условиях алиментарного дефицита магния у животных наблюдались следующие изменения кардиогемодинамики при проведении нагрузочных тестов.
Нагрузка объемом, имитирующая увеличение преднагрузки (рис. 1), у животных с дефицитом магния по сравнению с животными контрольной группы привела к значительно меньшему увеличению левожелудочкового давления, максимальных скоростей сокращения и расслабления. Максимальный прирост левожелудочкового давления в группе животных, получавших безмагниевую диету, отмечался на 30-й секунде и был достоверно в 2,6 раза ниже, чем в группе контрольных животных. Степень прироста скорости сокращения миокарда на 30-й секунде в группе животных с дефицитом магния была в 1,7 раза меньше (p<0,05), чем в группе интактных животных, а прирост скорости расслабления был ниже в 2,6 раза. У животных, получавших магнийдефицитную диету, в отличие от контрольной группы, при нагрузке объемом не отмечено выраженного подъема АД (см. рис. 1), что, очевидно, обусловлено отсутствием увеличения сердечного выброса, несмотря на увеличение ЧСС, которое наблюдается в норме [20]. У животных с дефицитом магния прирост интенсивности функционирования структур был в 3,1 раза ниже, чем в группе контроля (p<0,05).
В ответ на введение адреналина (рис. 2) прирост левожелудочкового давления, максимальной скорости сокращения и расслабления миокарда у животных с дефицитом магния был, соответственно, в 2,3, 2,25 и 2,6 раза меньше, чем в группе контроля.
Систолическое АД возрастало в группе животных с дефицитом магния также достоверно меньше, чем в группе интактных животных (см. рис. 2). Интенсивность функционирования структур миокарда была значительно ниже в группе магнийдефицитных животных. Так, на 60-й секунде после введения адреналина интенсивность функционирования структур была в 2,8 раза ниже, чем в группе контроля.
В условиях максимальной изометрической нагрузки у животных с алиментарным дефицитом магния прирост левожелудочкового давления, скорости сокращения и расслабления миокарда был в 1,7, 2 и 2,12 раза меньше, чем в группе контроля (см. таблицу). Во время этой пробы интенсивность функционирования структур миокарда у магнийдефицитных животных возрастала только на 92,6%, тогда как у контрольных животных — на 172,3%, т.е. в 1,9 раза меньше.
Таблица. Показатели кардио- и гемодинамики крыс с дефицитом магния при пережатии восходящей части дуги аорты (М±м)
Примечание. * — p<0,05 при сравнении с контрольной группой (интактные животные). ЛЖД — левожелудочковое давление; ИФС — интенсивность функционирования структур; dp/dt — первая производная внутрижелудочкового давления; ЧСС — частота сердечных сокращений.
Обсуждение
Таким образом, перед функциональными пробами у животных с дефицитом магния по сравнению с интактной группой АД имело тенденцию к повышению. Эти результаты согласуются с данными, полученными другими исследователями. Так, T.M. Paravicini и соавт. показали, что у животных с генетически обусловленной гипомагниемией наблюдается более высокое систолическое АД [22]. В основе данного явления может лежать активация симпатико-адреналовой и ренин-ангиотензин-альдостероновой систем [23], о чем также свидетельствует более высокая ЧСС у магнийдефицитных животных по сравнению с таковой в интактной группе.
При нагрузке объемом, введении адреналина и в условиях максимальной изометрической нагрузки (пережатие аорты) у животных с дефицитом магния отмечался меньший прирост левожелудочкового давления, скорости сокращения и расслабления миокарда, интенсивности функционирования структур миокарда.
Описанные изменения кардиогемодинамики свидетельствуют о снижении функциональных резервов сердца у магнийдефицитных животных. При этом можно предположить, что дефицит магния способствует формированию латентной сердечной недостаточности, проявления которой можно наблюдать в условиях нагрузочных тестов.
Как известно, дефицит магния приводит к развитию системной иммуновоспалительной реакции. Происходят повышение тромбогенного потенциала сосудистой стенки, усиление экспрессии молекул межклеточной адгезии и стимуляция пролиферации гладких мышечных клеток [24]. По данным литературы, низкий уровень внеклеточного магния стимулирует синтез молекул адгезии — маркера воспаления, который взаимодействует с интегрином VLA-4 (very late activation antigen-4), экспрессируемым моноцитами и лимфоцитами. Местная же адгезия лейкоцитов к стенкам капилляров является одним из ключевых этапов воспаления и иммунного ответа. После адгезии лейкоциты пенетрируют сосудистую стенку под действием цитокинов, вырабатываемых эндотелием. При дефиците магния отмечается повышение концентраций факторов роста интерлейкина-1 и интерлейкина-6, задействованных в формировании реакции острой фазы воспаления [25]. Наблюдается также увеличение диаметра и проницаемости сосудистой стенки, что облегчает хемотаксис лейкоцитов и может служить пусковым механизмом воспалительно-дистрофических изменений во многих органах и тканях, в том числе в миокарде [26—28].
Кроме того, полученные результаты могут объясняться важной метаболической ролью магния. Он входит в состав кофакторов ферментов, регулирующих энергетический обмен и содержание макроэргических соединений в клетках. Так, магний участвует в активации АТФаз, регулирует активность ряда ионных каналов, а также участвует в процессах синтеза нуклеиновых кислот, транскрипции и трансляции благодаря способности образовывать устойчивые трехкомпонентные комплексы с нуклеотидами [29—31]. В анаэробном цикле превращения глюкозы в пируват 7 ферментов являются магнийзависимыми [32]. Кроме того, дефицит магния сопровождается изменением соотношения Ca2+/Mg2+, что также влияет на сократимость миокарда.
Ишемия миокарда сопровождается потерей кардиомиоцитами как магния, так и АТФ [33]. Учитывая, что дефицит магния связан с ростом риска развития ишемии сердечной мышцы [34], можно предположить, что именно данное патологическое состояние в той или иной степени развивается у магнийдефицитных животных в условиях нагрузочных тестов.
У животных с дефицитом магния адреналин не приводил к столь выраженному увеличению левожелудочкового давления, сократимости и расслабления, систолического и диастолического АД, как у интактных животных. По мнению L.T. Williams и соавт., M.S. Skorodin и соавт., W.J. Mroczek и соавт., магний необходим для активации аденилатциклазы и синтеза цАМФ. цАМФ обеспечивает фосфорилирование протеинкиназы, что в кардиомиоцитах приводит к открытию кальциевых каналов и повышению сократительной активности. Иначе говоря, магний необходим для реализации инотропного эффекта адреналина [17, 35, 36].
Заключение
Таким образом, у крыс, находящихся на безмагниевой диете в течение 10 нед, отмечается выраженное снижение уровня магния в эритроцитах (с 2,01 до 0,9 ммоль/л). У животных с алиментарным дефицитом магния в сравнении с группой контроля в ответ на нагрузочные пробы (нагрузка объемом, на адренореактивность и при максимальной изометрической нагрузке) в значительно меньшей степени увеличиваются скорости сокращения и расслабления сердца, внутрижелудочковое давление, интенсивность функционирования структур миокарда. Выявленное снижение реактивности миокарда в условиях изометрической нагрузки, а также нагрузки объемом, адреналином может лежать в основе генеза сердечной недостаточности при дефиците магния. Можно предположить, что сердечная недостаточность при алкоголизме, метаболическом синдроме, пролапсе митрального клапана является в том числе следствием магниевого дефицита, часто сопровождающего данные заболевания.
Работа выполнена при поддержке гранта президента РФ для молодых кандидатов наук 2010 года (проект МК-4935.2010.7 «Дефицит магния и его коррекция в патогенезе заболеваний сердечно-сосудистой системы»)



