ВВЕДЕНИЕ
Распространенность коморбидной патологии закономерно увеличивается с возрастом как среди мужского, так и женского населения. При этом особенно возрастает процент кардиоваскулярных заболеваний, а именно артериальной гипертензии (АГ) и хронической сердечной недостаточности (ХСН). Так, около 80% больных ХСН составляют лица старше 75 лет [1, 2]. Кроме того, эпидемиология этого заболевания в России имеет четкую гендерную составляющую: 72,5% всех пациентов с выставленным диагнозом ХСН – женщины [3].
Результаты многих исследований свидетельствуют, что среди пациентов пожилого возраста развивается возрастное ремоделирование, которое имеет дезадаптивный характер и значимые различия у мужчин и женщин [4, 5]. Отметим, что такие дезадаптивные изменения чаще выявляют у пожилых людей с синдромом старческой астении (ССА), к основным клиническим проявлениям которого относятся снижение силы, выносливости и физиологического функционирования, повышение риска зависимости от посторонней помощи и смерти. По данным некоторых исследователей, распространенность ССА среди лиц от 80 до 84 лет достигает 16%, в возрасте более 85 лет – 26% [6].
В то же время в литературе практически отсутствуют данные о гендерных особенностях клинического течения ХСН у пожилых пациентов в зависимости от наличия ССА.
Цель исследования – выявить гендерные особенности факторов риска (ФР), сопутствующей патологии, клинических симптомов и когнитивных функций у пожилых пациентов с АГ и ХСН с учетом наличия ССА.
МАТЕРИАЛ И МЕТОДЫ
В исследование был включен 161 пациент с АГ и ХСН в возрасте 80 лет и старше. В зависимости от наличия ССА все участники были ранжированы на две группы: 1-я – 84 пациента (44 женщины и 40 мужчин) с АГ, ХСН и ССА, 2-я – 77 пациентов (38 женщин и 39 мужчин) с АГ и ХСН, но без ССА.
Критерии невключения: ишемическая болезнь сердца в анамнезе, острое нарушение мозгового кровообращения или транзиторная ишемическая атака в течение последних 6 мес., гемодинамически значимые пороки сердца, имплантированный электрокардиостимулятор, тяжелая патология печени или почек, злокачественные новообразования.
Диагноз АГ устанавливался с учетом анамнеза заболевания пациента, данных амбулаторной карты, а также результатов офисного измерения артериального давления (АД).
Наличие ХСН определяли, анализируя симптомы и клинические признаки, уровень маркера сердечной недостаточности (N-концевого пропептида натрийуретического гормона В-типа, NT-proBNP), а также данные эхокардиографии в соответствии с национальными клиническими рекомендациями по диагностике и лечению ХСН от 2020 г. [3]. Степень выраженности клинических признаков ХСН оценивалась с помощью шкалы оценки клинического состояния (ШОКС в модификации В.Ю. Мареева, 2000 г.) [3]. Тест 6-минутной ходьбы (ТШХ) использовался для определения переносимости пациентами физической нагрузки.
Причиной развития ХСН у пациентов, включенных в исследование, являлась АГ.
Для скрининга ССА применялся опросник «Возраст не помеха». Если пациент набирал ≥ 3 балла, то с высокой долей вероятности предполагалось наличие ССА. Мышечная сила измерялась посредством кистевой динамометрии [6].
Когнитивные функции оценивались методом нейропсихологического тестирования при помощи краткой шкалы MMSE (Mini Mental State Examination), характеризующей психический статус пациента. Конечный результат ее представляет собой сумму баллов по каждому из пунктов опросника. Максимально в тесте MMSE можно набрать 30 баллов. Чем ниже итоговый балл, тем более выражен когнитивный дефицит. Данные теста интерпретируют следующим образом: 28–30 баллов – нет нарушений когнитивных функций; 24–27 баллов – преддементные когнитивные нарушения; 20–23 балла – деменция легкой степени выраженности; 11–19 баллов – деменция умеренной степени выраженности; 0–10 баллов – тяжелая деменция.
Наличие ФР, сопутствующей патологии, данные физикального осмотра, а также результаты лабораторно-инструментальных методов исследования, тестов, шкал и опросников у каждого пациента отражались в анкете. Схема проведения исследования представлена на рисунке 1.
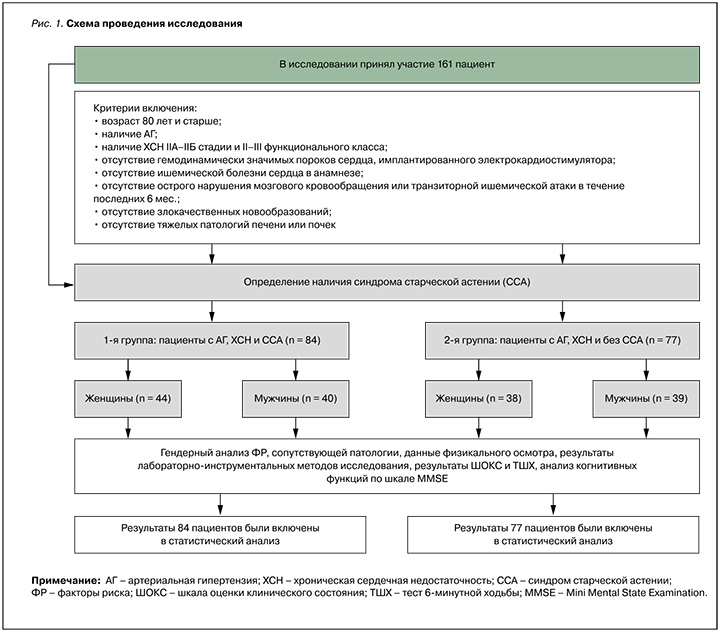
Статистическая обработка полученных результатов выполнялась при помощи прикладной программы Statistica 12.0 (производитель StatSoft Inc., CША). Проверка выборки на соответствие нормальному распределению осуществлялась с применением критерия Шапиро – Уилка. Количественные данные, соответствующие нормальному распределению, приведены в виде среднего и стандартного отклонения (M ± m). Количественные данные, отличающиеся от нормального распределения, описаны медианой и интерквартильным размахом (Me [Q1–Q3]). Качественные переменные представлены в виде абсолютных (n) и относительных (%) величин. Сравнение групп по качественным признакам проводилось посредством критерия Хи-квадрат с поправкой Йетса, по количественным признакам – с помощью критерия Манна – Уитни для двух независимых групп. Для сравнения четырех групп пациентов использовался критерий ANOVA Краскела – Уоллиса. За критический уровень достоверности нулевой статистической гипотезы принимали рmg < 0,05.
Исследование выполнялось в условиях Ростовской областной клинической больницы г. Ростова-на-Дону. Работа соответствовала стандартам Хельсинской декларации, была одобрена независимым этическим комитетом ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России (протокол № 13/19 от 05.09.2019). Все лица, вошедшие в исследование, подписали письменное информированное добровольное согласие на участие в нем.
РЕЗУЛЬТАТЫ
В исследовании приняли участие 50,9% женщин и 49,1% мужчин в возрасте 84,7 ± 1,5 года. Длительность АГ среди исследуемых больных составила 22,1 ± 2,2 года, продолжительность течения ХСН – 8,4 ± 3,6 года.
По данным скринингового опросника «Возраст не помеха», ССА был диагностирован у 52,2% обследованных. По гендерному распределению в 1-й группе по сравнению со 2-й показатель ССА был статистически значимо выше как среди женщин, так и среди мужчин (p < 0,001; табл. 1). Полученные результаты согласуются с данными литературы, которые свидетельствуют о том, что у «хрупких» женщин по сравнению с «хрупкими» мужчинами отмечается более выраженная астения (р = 0,021).

Оценку мышечной силы выполняли при помощи кистевой динамометрии. Как известно, критерии низкой силы пожатия при проведении этого метода зависят от пола. Гендерный анализ показателей кистевой динамометрии в исследуемых группах продемонстрировал, что как у «хрупких», так и «крепких» женщин по сравнению с «хрупкими» и «крепкими» мужчинами мышечная сила была выражена слабее (р < 0,001; табл. 2).
Частота встречаемости ФР и сопутствующих заболеваний у исследованных пациентов представлена в таблице 3.
При анализе клинической характеристики пациентов с АГ и ХСН в зависимости от наличия ССА было обнаружено, что в 1-й группе пациентов по сравнению со 2-й вдвое чаще регистрировалась фибрилляция предсердий (ФП, р < 0,001) и на 26,4% чаще – хроническая болезнь почек (ХБП, р < 0,001). В свою очередь, «крепкие» пациенты с АГ и ХСН имели больший индекс массы тела (ИМТ) в сравнении с «хрупкими» больными с АГ и ХСН (p = 0,029); также во 2-й группе оказался в 2,4 раза выше процент пациентов с ожирением (p = 0,032).
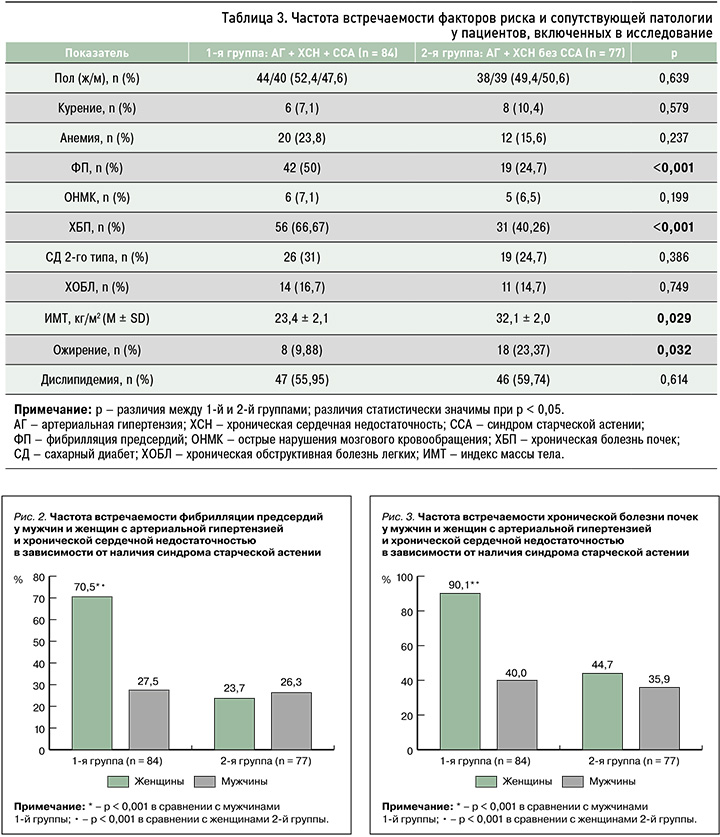
Важно подчеркнуть, что гендерный анализ выявил значимо более высокий процент встречаемости фибрилляции предсердий (ФП) и хронической болезни почек (ХБП) у женщин с АГ, ХСН и ССА не только в сравнении с мужчинами этой же группы (на 43 и 50,1% соответственно, р < 0,001), но и женщинами, имеющими АГ, ХСН без ССА (на 46,8 и 45,4% соответственно, р < 0,001; рис. 2, 3). Частота ФП и ХБП у мужчин с АГ и ХСН в сравниваемых группах была сопоставимой независимо от наличия ССА.
Также мы установили, что у «хрупких» женщин статистически значимо чаще встречалась анемия по сравнению с «хрупкими» мужчинами (на 16,8%, р = 0,036), а вот при их сопоставлении с «крепкими» женщинами статистически значимых отличий по этому показателю найдено не было (рис. 4).
Среди пациентов, включенных в исследование, у женщин с АГ и ХСН без ССА статистически значимо чаще наблюдалось ожирение по сравнению как с мужчинами этой же группы (31,6 против 15,4%, p = 0,031), так и женщинами с АГ, ХСН и наличием ССА (31,6 против 11,4%, p < 0,001; рис. 5).
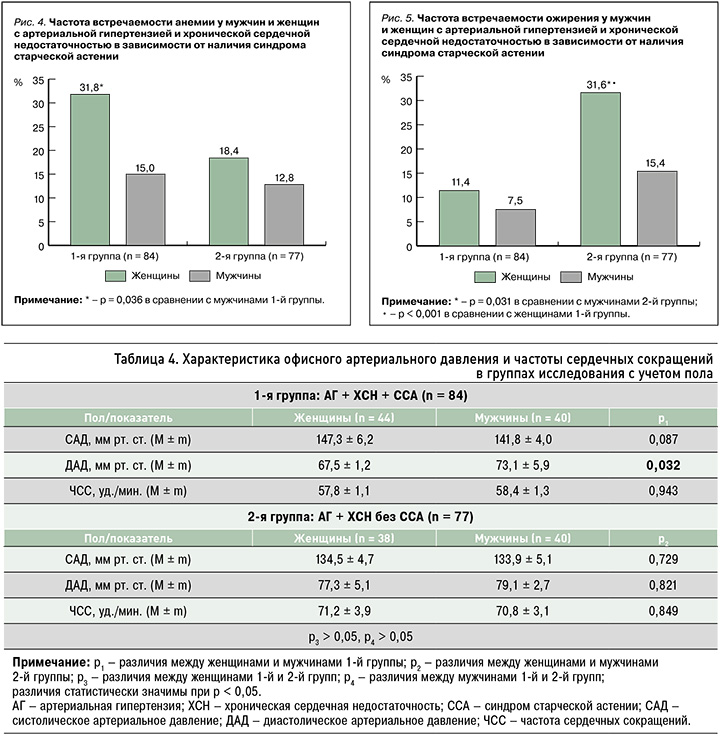
Все участники исследования получали антигипертензивную терапию, что позволяет судить о степени достигнутого АД, при этом ни в одной из групп не было пациентов с целевыми значениями этого параметра. У всех больных при офисном измерении АД регистрировалиcь его показатели, соответствующие 1-й степени АГ. Все пациенты имели III стадию гипертонической болезни и очень высокий сердечно-сосудистый риск.
Гендерный анализ внутри групп показал, что у «хрупких» женщин с ХСН отмечалась отчетливая тенденция к более высоким цифрам САД (p = 0,087) и статистически значимо более низкие величины диастолического АД (ДАД, p = 0,032) в сравнении с «хрупкими» мужчинами этой же группы (табл. 4).
Были выявлены клинические различия между пациентами мужского и женского пола с ХСН (табл. 5). Так, у «хрупких» женщин отмечался статистически значимо более высокий средний балл по шкале ШОКС относительно мужчин этой же группы (p = 0,037).

Вместе с тем выраженность клинических проявлений ХСН при гендерном сравнении в группе пациентов без ССА статистически значимо не отличалась (p = 0,747). Следует отметить, что при сопоставлении как женщин 1-й и 2-й групп (p < 0,001), так и «хрупких» и «крепких» мужчин (p = 0,017) статистически значимо больший балл по ШОКС наблюдался в группе пациентов с ССА.
При подробном сравнительном анализе клинических проявлений ХСН (табл. 6) у «хрупких» мужчин статистически значимо чаще, чем у «хрупких» женщин, регистрировалось увеличение печени более 5 см (на 27,72%, р = 0,033). В свою очередь, у «крепких» мужчин относительно «крепких» женщин статистически значимо чаще выявлялись хрипы в нижних отделах легких (на 25%, р = 0,020) и показатели САД <100 мм рт. ст. (на 22,9%, р = 0,019).
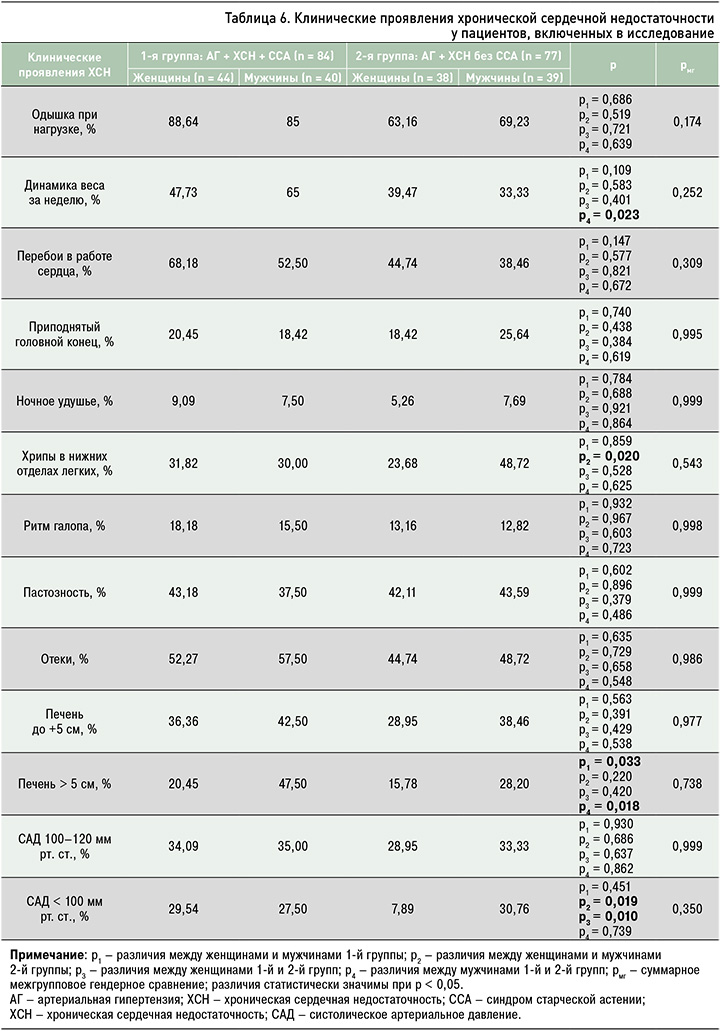
При межгрупповом гендерном сравнении у женщин 1-й группы статистически значимо чаще, чем у женщин 2-й группы, фиксировалось САД <100 мм рт. ст. (на 22,9%, р = 0,010). У «хрупких» мужчин чаще, чем у «крепких», имели место прибавка в весе в течение недели (р = 0,023) и увеличение печени более 5 см (р = 0,018).
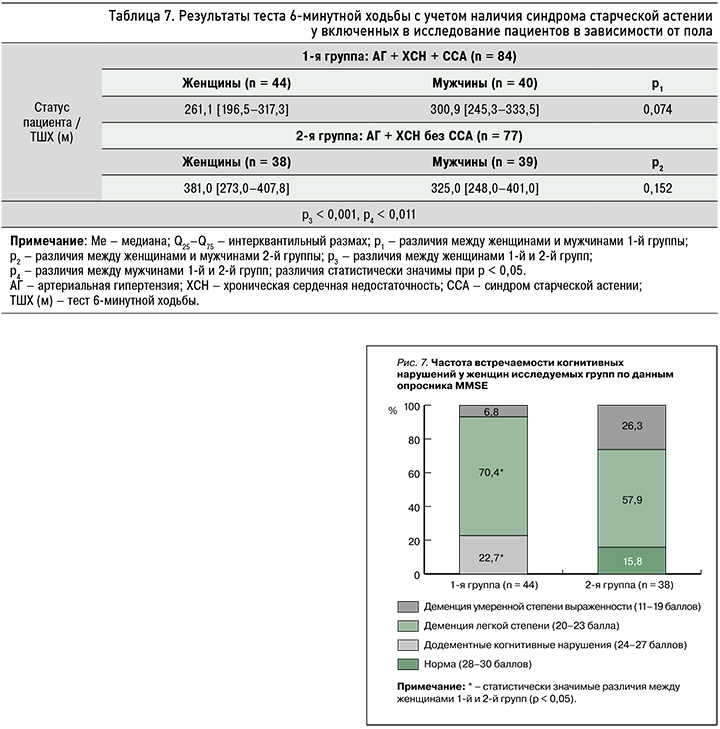
Оценка результатов ТШХ (табл. 7) позволила заключить, что у «хрупких» женщин выявлялась отчетливая тенденция к более низкой толерантности к физической нагрузке, чем у «хрупких» мужчин (р = 0,074). В группе «крепких» пациентов результаты ТШХ статистически значимо не отличались (p = 0,152). Сравнение результатов у мужчин и женщин в зависимости от наличия ССА продемонстрировало, что статистически значимо более низкая толерантность к физической нагрузке имела место у «хрупких» женщин (p < 0,001) и «хрупких» мужчин (p < 0,011), нежели у «крепких» пациентов соответствующего пола.
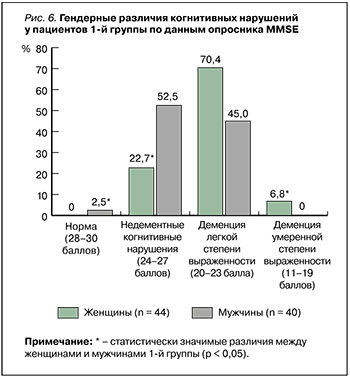
При сравнительном анализе когнитивных расстройств в соответствии с данными опросника MMSE среди «хрупких» пациентов наблюдались гендерные различия (рис. 6). Так, у женщин 1-й группы в сравнении с мужчинами прослеживалась отчетливая тенденция к более частой встречаемости деменции легкой степени выраженности (на 25,4%, р = 0,068), а у мужчин статистически значимо чаще фиксировались недементные когнитивные нарушения (на 29,8%, р = 0,050). Кроме того, у 6,8% женщин этой группы наблюдалась деменция умеренной степени выраженности (р < 0,001), тогда как 2,5% мужчин вообще не имели когнитивных нарушений (р < 0,001).
Среди пациентов с АГ и ХСН, но без ССА гендерных различий по частоте когнитивных нарушений обнаружено не было.
По результатам сравнения женщин 1-й и 2-й групп у «хрупких» пациенток статистически значимо чаще верифицировалась деменция легкой степени выраженности (на 44,1%, р < 0,001) и значимо реже – додементные когнитивные нарушения (на 35,2%, р = 0,014). Женщины с АГ, ХСН без ССА в 15,8% случаев вообще не страдали когнитивными расстройствами (р < 0,001), тогда как у 6,8% «хрупких» пациенток была установлена деменция умеренной степени выраженности (р < 0,001; рис. 7).
Сравнительный анализ данных опросника MMSE среди мужчин 1-й и 2-й групп различий не выявил.
ОБСУЖДЕНИЕ
В соответствии с результатами нашего исследования распространенность ССА у пациентов с АГ и ХСН в возрасте 80 лет и старше составила 52,2% случаев, причем у «хрупких» женщин по сравнению с «хрупкими» мужчинами наблюдалась более выраженная астения (р = 0,021). Схожие результаты были получены и в работах других авторов, которые также наблюдали возрастание частоты ССА с возрастом и преимущественно у женщин. Например, в исследовании К.В. Айрапетова с соавт. у пациентов 75 лет и старше ССА встречался в 48% случаев [7]. Л.В. Мачехина с соавт. обнаружили, что этот синдром был достоверно более распространен среди женщин [8].
Среди диагностических инструментов оценки мышечной силы динамометрия является простым и достаточно информативным методом в клинической практике. Ряд исследователей подтверждает связь снижения силы хвата кисти не только с возрастом, но и полом. Так, Д.П. Курмаев в своем исследовании продемонстрировал большее снижение мышечной силы у женщин относительно мужчин [9]. В нашем исследовании у женщин по сравнению с мужчинами независимо от наличия ССА мышечная сила также была выражена слабее (р < 0,001).
Полученные данные позволили судить и о гендерных особенностях ФР, а также о сопутствующей патологии у пациентов с АГ и ХСН в зависимости от наличия ССА. Так, в нашем исследовании выявлена статистически значимо более частая встречаемость ФП и ХБП у пациентов с ССА, причем у «хрупких» женщин эта патология фиксировалась чаще, чем у «хрупких» мужчин (p = 0,0002).
По данным литературы, ФП – одно из наиболее распространенных нарушений ритма сердца среди пожилого населения, при этом чем старше пациент, тем больше вероятность обнаружить у него аритмию [10]. Основные заболевания или факторы риска развития ФП в старших возрастных группах – АГ и ХСН. Кроме того, результаты крупных исследований ONTARGET и TRANSCEND указывают на вклад ССА в развитие и тяжесть ФП у пожилых пациентов [11].
За последние два десятилетия резко увеличилось количество пожилых пациентов с ХБП [12]. Наибольшая распространенность этого заболевания имеет место у лиц старше 70 лет, достигая 37–47%; у пациентов с АГ ее частота составляет 15,2%, с ХСН – от 44 до 66% [13]. Ассоциация между ССА и ХБП подтверждается многими данными. Например, в исследовании InCHIANTI выявлена предсказывающая способность расчетной скорости клубочковой фильтрации в отношении снижения показателя повседневной активности (ADL) у пожилых людей в течение 6 лет [14]. Кроме того, в соответствии с данными Д.П. Курмаева [9], частота встречаемости различных стадий ХБП различалась по гендерному признаку. В целом у женщин по сравнению с мужчинами статистически значимо чаще наблюдались более тяжелые стадии ХБП. В настоящем исследовании у пациентов с АГ и ХСН при наличии ССА сопутствующая ХБП также выявлялась значительно чаще, чем у пациентов без ССА. При этом гендерный анализ показал, что у «хрупких» женщин (с АГ, ХСН и ССА) отмечался статистически значимо больший процент случаев ХБП в сравнении как с «хрупкими» мужчинами, так и «крепкими» женщинами.
Результаты многих международных исследований говорят о высокой распространенности анемии среди пациентов с ХСН, которая находится в пределах 37–70% [6]. При ХСН анемия чаще обнаруживается у женщин, больных пожилого возраста, пациентов, имеющих ухудшение функции почек, и ассоциируется с выраженным ремоделированием миокарда, воспалением и перегрузкой объемом [15]. В нашем исследовании анемия также статистически значимо чаще встречалась у женщин с АГ, ХСН и ССА по сравнению с мужчинами с тем же сочетанием заболеваний.
В литературе последних лет накоплено достаточно данных о том, что взаимосвязь ожирения с показателями здоровья у лиц молодого возраста не всегда может быть спроецирована на пациентов старших возрастных групп, имеющих полиморбидную патологию. Так, установлено, что риск смерти от всех причин и смерти вследствие ухудшения течения ХСН был ниже в группе пациентов с избыточной массой тела и ожирением [16]. Помимо этого, доказано, что минимальная летальность среди женщин пожилого и старческого возраста отмечается при ИМТ 31,7 кг/м2, среди мужчин того же возраста – при 28,8 кг/м2 [17]. Следует добавить, что у больных старческого возраста (75 лет и старше) любое снижение веса (намеренное или нет) может иметь потенциально опасные последствия в виде развития и/или прогрессирования саркопении, мальнутриции, потери костной массы и повышения смертности. В нашем исследовании среди пациентов с ССА наблюдались статистически значимо меньший ИМТ (p = 0,029) и более низкая частота ожирения (на 13,6%, р = 0,032) по сравнению с пациентами без ССА; это также может подтверждать факт существования «парадокса ожирения» у пациентов с гериатрическими синдромами. Кроме того, «крепкие» женщины статистически значимо чаще имели ожирение по сравнению как с «крепкими» мужчинами (p = 0,031), так и «хрупкими» женщинами (p < 0,001).
Известно, что низкое АД у пожилых с ССА может вызывать состояние физиологической слабости, которое часто усугубляется наличием полипрагмазии и сопутствующей коморбидной патологии [18]. В связи с этим можно считать, что высокое АД у пожилых людей с ССА служит компенсаторным механизмом для поддержания перфузии органов и хорошим прогностическим признаком, в конечном итоге предотвращающим заболеваемость и дальнейшее снижение функционального статуса [19]. Снижение ДАД при высоком САД способствует также снижению коронарной перфузии и влияет на кровоснабжение миокарда. Результаты нескольких исследований позволяют заключить, что уровень ДАД ниже 70 мм рт. ст. ассоциирован со значимым повышением риска смерти [20].
Выявленные нами различия в показателях САД и ДАД и в исследуемых группах согласуются с данными литературы о более высоких цифрах САД и более низких значениях ДАД среди пациентов с ССА, причем у «хрупких» женщин в большей степени, чем у «хрупких» мужчин.
Гендерный анализ клинических проявлений ХСН по ШОКС и степени ограничения физических возможностей показал, что у «хрупких» женщин по сравнению с «хрупкими» мужчинами и «крепкими» женщинами регистрировались более высокий средний балл по ШОКС и более низкая толерантность к физической нагрузке. В работе Е.Б. Александровой также были продемонстрированы аналогичные статистически значимые гендерные различия среди пожилых пациентов: у женщин статистически чаще фиксировался более высокий средний балл по ШОКС [21].
Выявленные различия показателей по ШОКС позволяют говорить о более выраженных клинических проявлениях ХСН у «хрупких» пациентов. Согласно литературным данным, это может быть обусловлено как влиянием ССА, так и наличием синдрома мальнутриции, при котором происходит постепенное снижение физиологического резерва организма, что может значительно ускорять процесс развития ССА. Снижение интенсивности метаболических процессов и физической активности – закономерное следствие синдрома мальнутриции и саркопении, объясняющее полученные нами данные о сниженных показателях ТШХ у пациентов с ССА (р < 0,001) [3].
У пациентов с АГ нарушения кровообращения в головном мозге в дальнейшем способствуют снижению когнитивных функций [22]. Так, в роттердамском и гетенбергском исследованиях с участием около 600 пожилых пациентов с АГ была обнаружена обратная (отрицательная) корреляция уровня САД и показателей когнитивных функций по шкале MMSE [23].
Механизм развития когнитивных нарушений при ХСН до конца не изучен, но предполагается, что она приводит к ухудшению кровоснабжения и развитию микроэмболий сосудов головного мозга, способствуя снижению когнитивных функций. В целом пациенты с сердечной недостаточностью характеризуются более высоким риском развития когнитивных нарушений [24].
Как известно, ССА способствует замедлению метаболических процессов и уменьшению физической активности пожилых, что, в свою очередь, также создает предпосылки к снижению когнитивных функций [3]. Анализ результатов опросника MMSE продемонстрировал, что среди «хрупких» женщин по сравнению с «хрупкими» мужчинами и «крепкими» женщинами наблюдался статистически значимо больший процент деменции легкой степени выраженности (р = 0,068 и р < 0,001 соответственно), при этом у 6,8% «хрупких» женщин регистрировалась деменция умеренной степени выраженности (р < 0,001). Вместе с тем 2,5% «хрупких» мужчин и 15,8% «крепких» женщин вообще не страдали когнитивными нарушениями (р < 0,001) и значимо реже имели додементные когнитивные нарушения (р < 0,001 и р = 0,014 соответственно). Такие результаты, полученные в нашем исследовании, согласуются с данными других работ, в которых почти 60% больных деменцией были лицами женского пола [25].
ЗАКЛЮЧЕНИЕ
Таким образом, в нашем исследовании установлено, что у больных с АГ, ХСН и ССА по сравнению с пациентами с АГ, ХСН без ССА статистически значимо чаще встречались ФП и ХБП, определялись более высокие величины САД и более низкие значения ДАД, а также более низкие значения ЧСС. В свою очередь, «крепкие» пациенты с АГ и ХСН отличались от «хрупких» больных с тем же сочетанием заболеванием большим ИМТ и более высокой частотой встречаемости ожирения. Кроме того, у «хрупких» женщин в сравнении не только с «хрупкими» мужчинами, но и «крепкими» женщинами отмечалась более выраженная астения, статистически значимо чаще регистрировались ФП и ХБП. В сравнении с «хрупкими» мужчинами у «хрупких» женщин статистически значимо чаще наблюдались анемия, более высокие цифры САД и более низкие показатели ДАД. При этом «крепкие» женщины статистически значимо чаще страдали ожирением по сравнению как с «крепкими» мужчинами, так и с «хрупкими» женщинами.
Сравнительный анализ результатов ШОКС и ТШХ показал, что пациенты с ХСН и ССА имели статистически значимо более выраженные симптомы и признаки ХСН, причем у них чаще отмечались одышка при физической нагрузке и более низкая переносимость физической нагрузки относительно больных ХСН без ССА. При гендерном анализе было выявлено, что у «хрупких» женщин в сравнении не только с «хрупкими» мужчинами, но и «крепкими» женщинами имели место более высокий балл по ШОКС (в частности, чаще фиксировалось систолическое АД < 100 мм рт. ст.) и более низкая толерантность к физической нагрузке. У «хрупких» мужчин в сравнении с «крепкими» чаще фиксировались прибавка в весе в течение недели и увеличение печени более 5 см, а у «крепких» мужчин в сравнении с «крепкими» женщинами статистически значимо чаще обнаруживались хрипы в нижних отделах легких и уровень систолического АД < 100 мм рт. ст.
У пациентов с АГ, ХСН и ССА статистически значимо реже отмечалось отсутствие когнитивных расстройств и наличие додементных когнитивных нарушений, а также наблюдалась более высокая встречаемость деменции легкой степени тяжести в сравнении с пациентами с АГ и ХСН, но без ССА. По данным гендерного анализа, у «хрупких» женщин в сравнении не только с «хрупкими» мужчинами, но и «крепкими» женщинами более часто диагностировалась деменция легкой степени выраженности.
Результаты выполненного исследования позволяют судить, с одной стороны, о влиянии ССА на клинические проявления у пациентов с АГ и ХСН, а с другой – о гендерных особенностях клинических проявлений у больных с АГ и ХСН в зависимости от наличия ССА.



