Ежегодно в мире проводится более 230 млн сложных хирургических операций [1], и это число постоянно растет. По данным обширных когортных исследований, летальность в течение 30 дней при некардиальных операциях умеренного и высокого риска составляет около 2% [2—4] и превышает 5% у больных с высоким риском развития кардиальных осложнений [5]. Хотя точные показатели периоперационных осложнений в Европе неизвестны, считается, что при ежегодном выполнении в Европе 40 млн хирургических вмешательств происходит почти 400 тыс. инфарктов миокарда
(ИМ) и почти 133 тыс. летальных исходов вследствие кардиальных осложнений [6]. Кардиальные факторы являются наиболее частой причиной послеоперационных осложнений и смертности [4, 7], существенно влияя на продолжительность и стоимость пребывания больных в стационаре [8]. Высокая частота развития кардиальных осложнений объясняется высокой распространенностью ишемической болезни сердца (ИБС) в общей популяции, на которую накладывается дополнительный стресс хирургического вмешательства. В связи с этим постоянно ведется поиск оптимальной стратегии оценки
и снижения риска развития периоперационных кардиоваскулярных осложнений. Действия зарубежных врачей в этой ситуации регламентируются соответствующими рекомендациями [9—12]. В США рекомендации АСС/АНА по данному вопросу впервые вышли в свет в 1996 г. [9], последняя редакция выпущена в 2009 г. [11]. Кроме того, в 2009 г. вышли в свет рекомендации Европейского общества кардиологов (ЕОК) [12], перевод которых на русский язык опубликован недавно [13, 14]. Первые
комментарии отечественных специалистов не содержат принципиальных замечаний, и встает вопрос о возможности широкого внедрения данных рекомендаций в российских условиях [15].
Пошаговый алгоритм диагностических и тактических действий по оценке риска развития кардиальных осложнений перед некардиальными операциями
Результатом работы экспертов стал четкий пошаговый алгоритм действий по оценке риска развития кардиальных осложнений в предоперационном периоде, необходимых диагностических и лечебных процедур для его снижения, состоящий из 7 этапов.
1-й этап — оценка неотложности хирургического вмешательства. При необходимости выполнения экстренных операций возможность дополнительной диагностики и лечения сопутствующей сердечно-сосудистой патологии существенно сокращена. Консультант-кардиолог (терапевт) дает рекомендации по периоперационному медикаментозному лечению и продолжению назначенной ранее постоянной терапии. Необходимо обсудить возможность продолжения ранее назначенной терапии ацетилсалициловой кислотой (АСК); прекращение такой терапии следует рекомендовать только больным, у которых возможны трудности с периоперационным гемостазом при невозможности компрессии [16]. Доказано, что отмена АСК ведет к увеличению риска развития тромботических осложнений в 3 раза [17], в то же время продолжение приема АСК может приводить к повышению риска кровотечений в ходе операций в 1,5 раза, но не ведет к повышению тяжести кровопотери [18]. Назначение АСК в периоперационный период снижало риск развития сердечно-сосудистых осложнений (ССО) с 9,0% в группе плацебо до 1,8% (р=0,02) [19]. Результаты мета-анализа [20] также свидетельствуют в пользу продолжения в периоперационном периоде терапии АСК у больных
с сосудистыми операциями. При высокой вероятности развития кровотечений возможна инфузия тромбоцитной массы и других прогемостатических препаратов [12, 13]. Соответственно рекомендация ЕОК заключается в продолжении в периоперационном периоде ранее назначенной терапии АСК (класс IIa B). Прекращение терапии АСК у больных, получавших его, следует рекомендовать только в случаях, когда гемостаз во время операции трудно контролировать (класс IIa B).
Плановый характер хирургического вмешательства предполагает переход ко второму шагу алгоритма.
На 2-м этапе оценивается наличие у пациента острых или нестабильных кардиальных состояний. К последним авторы руководства относят нестабильную и тяжелую (IV функциональный класс) стенокардию, недавний ИМ (<30 дней) и наличие остаточной ишемии миокарда, декомпенсированную сердечную недостаточность, серьезные нарушения ритма, тяжелые клапанные поражения.
При таких состояниях требуется отложить плановую операцию и стабилизировать состояние пациента (провести реваскуляризацию миокарда, компенсировать сердечную недостаточность, провести коррекцию клапанного поражения и т.д.). При этом возможности лечения должны обсуждаться мультидисциплинарной командой, включая всех врачей хирургического этапа, поскольку различные
предоперационные вмешательства могут влиять на выбор дальнейшей анестезиологической и хирургической тактики. Например, установка стента в коронарную артерию (КА) в связи с необходимостью приема клопидогрела может привести к переносу сроков некардиальной операции либо проведении ее в условиях повышенного риска кровотечения (или тромбоза стента).
В отсутствие у пациента неотложных кардиологических состояний возможен переход на 3-й этап алгоритма. На этом этапе следует оценить вид операции и риск развития периоперационных кардиальных осложнений [21, 22]. По степени риска операции делят на 3 категории (табл. 1): низкого риска (кардиальные осложнения встречаются менее чем в 1% случаев), промежуточного риска (осложнения встречаются в 1—5% случаев) и высокого риска (осложнения чаще, чем в 5% случаев). Если операция относится к низкому риску развития кардиальных осложнений, то рекомендуется проведение вмешательства без дополнительного обследования (класс IIa B). При этом консультант-кардиолог с целью улучшения отдаленных результатов лечения определяет факторы риска (ФР)
развития ССО и обсуждает рекомендации по изменению образа жизни и медикаментозной терапии в послеоперационном периоде.
При выполнении операций промежуточного и высокого риска следует переходить к 4-му шагу алгорит-
ма, на котором оценивается функциональное состояние пациентов. Для этого предлагается задать несколько вопросов, ответы на которые отражают различный уровень функциональной активности больных (от 1 до 10 метаболических единиц и более). При хорошем физическом состоянии (способности пациентов без симптомов подниматься на 2 пролета лестницы, совершить короткую пробежку) рекомендуется проведение операции без дополнительного обследования (класс IIa B). При этом есть необходимость выявления ИБС, ФР ее развития и назначить пациенту статины.
В дооперационном периоде рекомендуется также начало терапии низкими дозами β-адреноблокаторов. В исследованиях, проведенных в последние годы с использованием бисопролола и метопролола, не всегда отмечали снижение частоты развития кардиальных осложнений в периоперационный период [23—28]. Однако результаты мета-анализа с включением большого числа рандомизированных исследований (от 5 до 33) убедительно показали благоприятное влияние β-адреноблокаторов [29—31].
Таблица 1. Классификация хирургических вмешательств по вероятности развития кардиальных осложнений* в периоперационный период.
В одном из исследований, POISE [28], отмечено возрастание частоты развития периоперационных инсультов при назначении метопролола. Причиной этого, как считают, было развитие гипотонии в периоперационном периоде на фоне приема высоких доз метопролола (400 мг) в день операции. В связи с этим подчеркивается необходимость титрования дозы β-адреноблокаторов; терапия должна
быть начата за 30 дней (минимум за неделю) до плановой операции. Рекомендуется начинать с суточной дозы бисопролола 2,5 мг или метопролола сукцината 50 мг и затем повышать дозу препаратов до достижения частоты сердечных сокращений (ЧСС) в покое между 60 и 70 уд/мин при систолическом артериальном давлении (АД) > 100 мм рт.ст. (класс I В). При этом β-адреноблокаторы не рекомендуют назначать в предоперационном периоде больным без ФР при операциях низкого риска (класс III B).
Более определенной является ситуация со статинами, эффективность которых доказана в обсервационных и рандомизированных клинических исследованиях (РКИ) [32—34]. В недавней работе DECREASE III 497 больных перед сосудистыми операциями в течение месяца до операции получали либо флувастатин, либо плацебо. Частота развития ишемии миокарда составила в группе флувастатина 10,8% против 19,0% в группе плацебо (относительный риск — ОР 0,55 при 95% доверительном интервале — ДИ от 0,34 до 0,88). Частота кардиальной смерти или развития ИМ составила 4,8 и 10,2% соответственно (ОР 0,47 при 95%ДИ от 0,24 до 0,94) [35]. В настоящее время рекомендуется назначать статины больным при операциях высокого риска в оптимальном
случае за 30 дней или, по крайней мере, за неделю до операции (класс I B). Кроме того, рекомендуется продолжать ранее назначенную терапию статинами периоперационно (класс I C). Подробно проблема медикаментозной терапии при некардиальных операциях освещена в обзоре Ю.М. Лопатина, опубликованного в 2009 г. [36].
У больных с низким и средним функциональным состоянием сердечно-сосудистой системы на 5-м этапе
алгоритма рекомендуется вновь вернуться к оценке риска собственно хирургического вмешательства. При операциях промежуточного риска рекомендуется проводить вмешательство после минимального обследования: эхокардиографии (ЭхоКГ) для выявления систолической дисфункции левого желудочка (ЛЖ); электрокардиографии в покое — при наличии одного и более ФР развития кардиальных осложнений (класс IIa B). В плане медикаментозной терапии сохраняются рекомендации по назначению статинов и титрованию β-адреноблокаторов с низких доз, при систолической дисфункции ЛЖ рекомендуются ингибиторы ангиотензинпревращающего фермента (АПФ).
При операциях высокого риска следует переходить к 6-му шагу алгоритма — оценке ФР развития кардиальных осложнений (табл. 2). При анализе 1,2 млн процедур к таковым отнесли ИМ в анамнезе, наличие стенокардии, сахарного диабета, почечной недостаточности, инсульт или транзиторную ишемическую атаку в анамнезе, наличие симптомов сердечной недостаточности в настоящий
момент или в анамнезе [22]. При наличии 2 ФР и менее дополнительное обследование не требуется (класс I B), хирургическое лечение рекомендуется выполнять на фоне терапии статинами, титрования β-адреноблокаторов с низких доз и назначения ингибиторов АПФ при систолической дисфункции ЛЖ.
Если у пациента выявляется 3 ФР развития кардиальных осложнений и более, то в этом случае рекомендуется переход на 7-ю ступень алгоритма, на которой проводится кардиальный стресс-тест (обычно рекомендуются нагрузочная ЭхоКГ или перфузионная сцинтиграфия миокарда) [37—40]. В отсутствие ишемии или умеренной стресс-индуцированной ишемии миокарда рекомендуется проведение операции (класс I B) на фоне медикаментозной терапии (статины, β-адреноблокаторы, при необходимости — ингибиторы АПФ). Только наличие обширной ишемии миокарда (более 5 из 16 сегментов по данным нагрузочной ЭхоКГ [41]) дает основание перейти к следующему шагу, на котором рассматривается вопрос о превентивной реваскуляризации миокарда.
Таблица 2. Клинические ФР развития кардиологических осложнений при некардиальных операциях.
Вопрос эффективности превентивной реваскуляризации миокарда перед некардиальными операциями носит дискуссионный характер. Результаты нерандомизированных когортных исследований [10, 42, 43] свидетельствуют в пользу превентивной реваскуляризации. В то же время в 2 рандомизированных клинических исследованиях (CARP и DECREASE-V) не выявлена польза от профилактической реваскуляризации миокарда [41, 44]. Объяснение тому эксперты ЕОК видят в том, что в патофизиологии периоперационного ИМ преобладающую роль играет не дисбаланс между доставкой и потреблением кислорода миокардом, а разрыв атеросклеротической бляшки и образование тромба (как и при развитии спонтанных ИМ). Периоперационный стресс может способствовать тромбозу КА как при гемодинамически значимых, так и при незначимых коронарных стенозах за счет таких факторов, как гемодинамический стресс, вазоспазм, активация тромбоцитов, гиперкоагуляция, изменение фибринолитической активности. Поэтому при выборе между местной (превентивная реваскуляри-
зация миокарда) или системной терапией авторы рекомендаций отдают предпочтение последней, т.е. назначению статинов и β-адреноблокаторов до операции. При этом показания к профилактической реваскуляризации миокарда существенно сужаются: она может быть проведена перед операциями высокого риска у больных с доказанной ИБС (класс IIb B), но не рекомендуется у таких больных перед операциями промежуточного (класс III B) и низкого (класс III С) риска. При принятии решения о необходимости превентивной реваскуляризации миокарда необходимо индивидуально взвесить пользу процедуры, риск неблагоприятного исхода, эффект препаратов или реваскуляризации миокарда. Следует также учесть сроки, рекомендуемые после проведения процедур реваскуляризации миокарда до некардиальной операции [45, 46]. Так, только после баллонной ангиопластики возможно проведение операции через 2 нед, при имплантации стентов без покрытия двухкомпонентная антитромбоцитарная терапия (АСК + клопидогрел) назначается до некардиальной операции, проведение которой возможно через 6 нед, оптимальный срок — 3 мес. При использовании стентов с лекарственным покрытием срок некардиальной операции сдвигается на 12 мес, в течение которых проводится терапия дезагрегантами. При более раннем проведении плановых некардиальных операций приходится сталкиваться с непростой дилеммой: продолжение приема клопидогрела приводит к повышенному риску кровотечений [47], прекращение его приема при незавершенности эпителизации стента — к существенному риску тромбоза стентов, развития ИМ и летального исхода [48, 49]. Такие ограничения отсутствуют при коронарном шунтировании (КШ). Следует отметить минимальную задержку времени до некардиальной операции при проведении баллонной ангиопластики. Однако последнее вмешательство вряд ли следует рекомендовать из-за большого числа осложнений в отдаленные сроки наблюдения [50]. В этом плане перспективным выглядит использование новых стентов с повышенной скоростью эпителизации (типа GENOUS), когда
отмена клопидогрела возможна уже через месяц после имплантации стента [51].
Авторы рекомендаций подчеркивают, что они содержат следующие новые положения: 1) интеграция
ФР развития кардиальных осложнений, физической работоспособно сти и риска хирургической процедуры; 2) стратификация риска развития послеоперационных осложнений у больных на низкий (<1%), промежуточный (1—5%) и высокий (>5%); 3) дополнительные кардиальные стресс-тесты рекомендуются только для больных с 3 ФР и более перед операциями высокого риска; 4) медикаментозная вторичная профилактика ССО начинается до операции, поскольку улучшает как
непосредственные, так и отдаленные результаты хирургического лечения; 5) имеются рекомендации по периоперационной антиагрегантной терапии и титрации β-адреноблокаторов. Преимущества новых рекомендаций ЕОК состоит в том, что ими предусматриваются: 1) эффективная дооперационная работа (медикаментозная терапия, сокращение предоперационных кардиальных
тестов, сокращение профилактической реваскуляризации КА); 2) рекомендации по медикаментозной терапии (β-адреноблокаторы, статины, АСК, клопидогрел, ингибиторы АПФ); 3) начало вторичной профилактики до операции.
Можно согласиться с мнением, что публикация первых рекомендаций ЕОК по оценке риска развития ССО у больных, которым выполняют хирургические операции, не связанные с вмешательством на сердце, а также по тактике ведения таких больных, является важным событием [15]. Однако в печати продолжаются дискуссии по отдель ным положениям как рекомендаций ЕОК, так и последних американских рекомендаций (АСС/АНА) [52—57]. Если сомнения по поводу медикаментозной терапии, возникшие из-за результатов исследования POISE [53], были сняты после появления рекомендации титрования дозы β-адреноблокаторов [11—13], то вопросы объема предоперационного обследования
и профилактической реваскуляризации миокарда при операциях промежуточного и высокого риска остаются предметом обсуждения. Некоторые авторы высказывают недовольство по поводу некоторой неконкретности имеющихся рекомендаций (частое употребление оборотов «может быть» и т.д.), что затрудняет выбор врачами тактики у конкретного больного [54]. Другие исследователи высказывают сомнение в правомерности сокращения объема обследования и превентивной реваскуляризации миокарда [52, 57]. Случайна ли эта полемика? Попробуем понять это при рассмотрении клинического случая.
Клинический случай
Пациент К., 62 лет, поступил для обследования в отделение кардиологии НИИ КПССЗ 06.02.2008. Диагноз при поступлении: периферический атеросклероз. Хроническая ишемия IIб степени. Гипертоническая болезнь III стадии, риск 4. Поводом для госпитализации послужили клинические проявления ишемии нижних конечностей.
При госпитализации больной предъявлял жалобы на боль в икроножных мышцах, возникавшую при ходьбе на расстояние до 200 м, купировавшуюся в покое. При данной нагрузке стенокардия и одышка не беспокоили. На протяжении 5 лет пациент страдал артериальной гипертензией с максимальным повышением АД до 160 мм рт.ст., антигипертензивные препараты принимал нерегулярно. ИМ и острое нарушение мозгового кровообращения в анамнезе отсутствовали. Симптомы ишемии нижних конечностей беспокоили в течение 3 лет, за это время расстояние безболевой ходьбы уменьшилось
с 600 до 200 м. Курил в течение 30 лет по 20 сигарет в сутки.
При осмотре состояние больного удовлетворительное. Телосложение нормостеническое. В легких дыхание везикулярное, хрипы не выслушиваются. Тоны сердца ясные, ритмичные, ЧСС 84 уд/мин, АД 140/80 мм рт.ст. Над обеими сонными артериями выслушивается систолический шум. Пульс на периферических артериях отсутствует до паховой складки, где он симметричен, резко ослаблен.
Пульсация на артериях верхних конечностей сохранена, отчетливая и симметричная.
По данным основных лабораторных тестов патология не выявлена. По данным ЭКГ: синусовый ритм с ЧСС 60 уд/мин. Изменения, которые могли бы свидетельствовать о наличии ишемии миокарда, не зарегистрированы. По данным ЭхоКГ: фракция выброса (ФВ) ЛЖ 66%, отделы сердца не изменены. В створках аортального клапана склеротические изменения, без нарушения гемодинамики. На рентгенограмме органов грудной клетки признаки артериальной легочной гипертензии, застоя, инфильтративных и очаговых изменений отсутствуют. При цветовом дуплексном сканировании выявляется утолщение комплекса интима—медиа до 1,5 мм. Правая внутренняя сонная артерия (ВСА) стенозирована на 50%, левая ВСА окклюзирована. Подвздошные артерии имеют ряд гемодинамически незначимых стенозов (до 35%). При ультразвуковом исследовании периферических артерий
выявлены окклюзии бедренных артерий справа и двусторонние протяженные стенозы берцовых артерий от 50 до 70%, более выраженные справа.
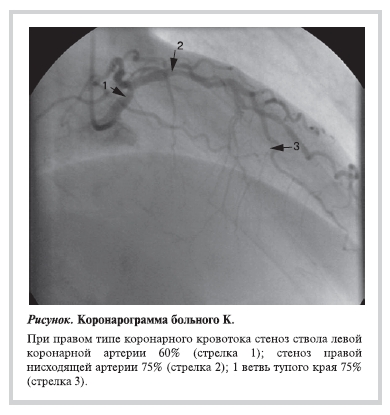
Итак, согласно рекомендациям ЕОК и пошаговому алгоритму пациенту следует выполнять реконструктивную операцию на артериях нижних конечностей без проведения нагрузочных тестов (плановая операция, отсутствие неотложного кардиологического состояния, низкий функциональный класс, высокий риск операции, но отсутствие ФР развития кардиальных осложнений). Вместе с тем согласно принятому в нашей клинике алгоритму обследования перед сосудистыми операциями
больному проведена коронарография (КГ), на которой выявлены (см. рисунок) стеноз ствола левой КА 60%, серия стенозов передней нисходящей артерии (ПНА) до 75% и 1-й ветви тупого края (ВТК) до 80%.
Что следует делать при выявлении такого поражения КА согласно рекомендациям ЕОК? Они гласят следующее: «Профилактическая реваскуляризация миокарда перед операциями высокого риска может быть проведена у больных с доказанной ИБС (класс IIb B)». Отмечаем первое противоречие предложенной концепции: у больного возможно проведение реваскуляризации миокарда при наличии доказанной ИБС, но по предложенному алгоритму предоперационной оценки выявление ИБС перед хирургическим вмешательством не является обосно ванным! Следующее противоречие — класс
рекомендаций (IIb) подразумевает, что реваскуляризация миокарда возможна, но эффективность ее сомнительна. Данное утверждение врач может трактовать и в пользу отказа от превентивного вмешательства на КА. В рекомендациях ЕОК не представлены случаи, когда такие процедуры необходимы. Следует отметить, что этот недостаток отсутствует в рекомендациях АСС/АНА [11],
где отмечены четкие показания. Так, к рекомендациям I класса при плановых некардиальных операциях относят следующие положения: 1. Коронарная реваскуляризация перед некардиальной
операцией показана для больных со стабильной стенокардией при наличии гемодинамически значимого стеноза ствола левой КА (уровень доказательности А). 2. Коронарная реваскуляризация перед некардиальной операцией показана для больных со стабильной стенокардией и трехсосудистым поражением КА (особенно при ФВ ЛЖ <50%) (уровень доказательности А). 3. Коронарная реваскуляризация перед некардиальной операцией показана для больных со стабильной стенокардией при наличии двухсосудистого поражения с существенным проксимальным стенозом ПНА и либо с ФВ ЛЖ <50%, либо с наличием ишемии при неинвазивных тестах (уровень доказательности А).
Соответственно в нашем клиническом случае проведены следующие этапы хирургического лечения:
07.02.2008 выполнено КШ (маммарокоронарный анастомоз, аортокоронарное шунтирование огибающей артерии и 2-й ВТК аутовенозной). Вторым этапом 13.03.2008 проведены эндартерэктомия на подвздошных и бедренных артериях, подвздошно-бедренное протезирование (протезом «Басекс») и поясничная симпатэктомия справа, протезно-подколенное биопротезирование справа. Послеоперационный период протекал без осложнений. Расстояние безболевой ходьбы увеличилось до 1000 м. Степень хронической ишемии нижних конечностей уменьшилась до I.
Насколько типичной является ситуация, отраженная в данном клиническом наблюдении? Для ответа на этот вопрос мы проанализировали результаты обследования перед сосудистыми операциями (т.е. операциями промежуточного и высокого риска), в которое входила и предоперационная КГ [58]. При ретроспективном анализе 388 историй болезни пациентов, подвергшихся хирургическим вмешательствам на каротидном бассейне, аорте и артериях нижних конечностей, отмечено преобладание среди них пациентов (79%), которым согласно последним рекомендациям ЕОК не требовалось дополнительное обследование перед операцией. Тем не менее при проведении КГ у 23,1% из этих больных выявлены трехсосудистое поражение КА и/или стеноз ствола левой КА (у остальных больных данная патология выявлена в 27,5% случаев). Превентивная реваскуляризация миокарда проведена у 94 (24,2%) больных. Периоперационные ИМ развились у 3 (0,8%) больных, умерли от кардиальных причин 2 (0,5%), причем именно из числа больных, которым по рекомендациям ЕОК не были показаны стресс-тесты и реваскуляризация миокарда. Насколько эти результаты отражают общую картину в российских условиях, судить трудно. По зарубежным данным, при повседневном проведении КГ перед сосудистыми операциями частота выявления ИБС очень высока — от 37 до 78% [59—61]. Отсутствие поражения КА при таких исследованиях встречалось нечасто и составляло от 9 до 20% [59]. При этом поражение хотя бы одного коронарного сосуда выявлялось в 60—67% случаев, трех — в 18—26% случаев, а поражение ствола левой КА — в 4—8% [59—62].
В исследовании N.R. Hertzer и соавт. [59] частота выявления значимых стенозов КА, поддающихся хирургической коррекции, составила 26%, что очень близко к данным, полученным в нашей работе.
Превентивная реваскуляризация миокарда перед некардиальными операциями
Эти данные и послужили основой стратегии по превентивной реваскуляризации миокарда, доказавшей свою эффективность в ретроспективных когортных исследованиях [42, 43], и от которой решено отказаться после двух вышеупомянутых РКИ — CARP и DECREASE-V [41, 44]. Отказ от реваскуляризации привел к следующему логичному шагу — сокращению объема обследования: зачем обследовать больных, если в итоге не будет вмешательства? Однако конечный результат — пошаговый алгоритм — оказался весьма противоречивым, что продемонстрировано в клиническом случае и в нашем ретроспективном анализе. В чем причина такого результата? Проанализируем два исследования, перевернувшие взгляды экспертов ЕОК на необходимость превентивной реваскуляризации миокарда.
В исследовании CARP не отмечено улучшения отдаленных результатов лечения при превентивной реваскуляризации у пациентов, оперированных на некоронарных артериальных бассейнах [44]. При наличии ФР развития ССО и ишемии по данным неинвазивных стресс-тестов (по мнению кардиолога-консультанта) были рандомизированы 510 больных. Группы не различались по долговременной смертности в течение 2,7 года: 22% в группе реваскуляризации и 23% (при медикаментозной терапии) (р=0,92). Более того, не было различий и по частоте развития периоперационного ИМ: 12 и 14% соответственно (р=0,37). Однако в этом исследовании не было единого метода оценки периоперационного риска, поэтому среди включенных пациентов перфузионная сцинтиграфия
миокарда проведена только у 62% и только у 44% имелась выраженная или обширная ишемия. Трехсосудистое поражение имелось только у 32% пациентов, включенных в исследование, или у 2,9% из всех 5859 включенных в скрининг (это существенно меньше ожидаемых 18%, судя по данным N.R. Hertzer и соавт. [59]). Таким образом, большинство пациентов с трехсосудистым поражением (основные претенденты на реваскуляризацию) в исследовании CARP не выявлены в процессе обследования или были исключены из него [52]. Кроме того, поражение ствола левой КА или низкая ФВ ЛЖ исходно
были критериями исключения из исследования. Можно прийти к выводу о том, что пациенты в исследовании CARP были более «легкими», чем обычно встречающиеся в клинической практике, и его результаты нельзя распространять на всю популяцию больных.
Исследование DECREASE-V было призвано заполнить бреши в исследовании CARP и включало пациентов очень высокого риска со значительным объемом ишемизированного миокарда при неинвазивном стресс-тесте [41]. Тем не менее в развернувшейся дискуссии [52] подчеркиваются существенные ограничения этого исследования, главным из которых является крайне высокая
30-дневная летальность как в группе превентивной реваскуляризации миокарда (22%), так и в группе медикаментозного лечения (11%). Это объясняется очень большим числом периоперационных ИМ (35 и 31% соответственно), причем все они были Q-образующими. Это наводит на мысль, что вероятной их причиной были тромбозы стентов, поскольку обычно среди периоперационных ИМ преобладают не-Q-образующие [62, 63], во всяком случае их число не менее 50% [64, 65]. Можно предположить,
что в исследовании DECREASE-V после превентивного стентирования КА не были оптимальными либо тактика антикоагулянтной терапии [48], либо сроки проведения сосудистой операции после реваскуляризации миокарда. Обращает внимание также проведение коронарной реваскуляризации всем пациентам со значительной ишемией по данным стресс-теста, хотя в реальной клинической
практике примерно в ⅓ случаев не удается провести полную реваскуляризацию миокарда в связи с анатомическими особенностями. Поэтому можно думать, что у отдельных пациентов реваскуляризация миокарда проведена неоптимальным способом, учитывая, что такие факторы, как «плохое» периферическое русло (особенно у больных сахарным диабетом), множественное протяженное поражение артерий сердца делают невозможным чрескатетерное вмешательство у пациентов, состояние которых слишком тяжелое для проведения КШ. В итоге у пациентов, подвергшихся реваскуляризации, 30-дневная смертность после сосудистого вмешательства оказалась в 2 раза больше, чем в группе контроля. Эти данные противоречат множеству сообщений об уменьшении
смертности и частоты развития послеоперационных ИМ у пациентов с предшествующей успешной реваскуляризацией миокарда, особенно при КШ [5, 42, 66]. В целом складывается впечатление, что пациенты в исследовании CARP были слишком «легкими», а в исследовании DECREASE-V — слишком «тяжелыми», чтобы полноценно оценить эффективность предоперационной реваскуляризации миокарда перед сосудистыми операциями.
Каким образом тщательно спланированные РКИ продемонстрировали весьма противоречивые результаты? По-видимому, наблюдается ограничение возможностей самих РКИ. Эти исследования позволяют получить оптимальные научные результаты, когда есть только один возможный ответ — да или нет — при контроле всех сопутствующих факторов. В реальности при сложных клинических ситуациях имеется более одного возможного ответа и решение должно приниматься для каждого отдельного пациента с учетом всей комбинации проявлений основного и сопутствующих заболеваний. В таких случаях нет лучшей альтернативы, чем проводить когортные исследования, а в случае решения вопроса о коронарной дооперационной реваскуляризации мы сталкиваемся именно с такой ситуацией [52]. Таким образом, РКИ из-за неизбежных ограничений в данной ситуации не имеют никакого преимущества в степени доказательности перед когортными исследованиями, поэтому мы
не можем отказываться от результатов когортных исследований по превентивной реваскуляризации миокарда.
Неинвазивные стресс-тесты перед некардиальными операциями
Неинвазивное нагрузочное тестирование пришло на смену повседневной КГ во многих центрах с целью уменьшения инвазивности предоперационного обследования [39, 40, 67]. Это помогло уменьшить число предоперационных КГ, но при этом возросли сроки и объем предоперационного обследования, сохранялось достаточно большим и число периоперационных осложнений [22, 68]. Не в последнюю очередь, поэтому последние рекомендации ЕОК настаивают на сокращении числа
нагрузочных тестов перед операцией. Логика экспертов понятна — в РКИ не доказана эффективность превентивной реваскуляризации миокарда, так зачем выявлять ишемию миокарда? Однако, как мы уже показали ранее, отказ от предоперационного обследования приводит к существенному сокращению числа пациентов с выявленным коронарным атеросклерозом, в том числе таких, у которых реваскуляризация показана и необходима. Следует отметить, что американские коллеги не столь
категоричны в этом вопросе [11]. При наличии 1—2 ФР они рекомендуют либо проведение операции на фоне применения препаратов, либо проведение нагрузочных тестов (но при условии, что они приведут к изменению терапии). Тем не менее возникает закономерный вопрос — как узнать до нагрузочных тестов, приведет ли это обследование в конечном итоге к необходимости реваскуляризации миокарда? Иными словами, и в этом случае, очевидно, придется склониться к обычному проведению нагрузочных тестов.
Решению этого вопроса посвящена работа D.N. Wijeysundera и соавт. [69], оценивших проведение
предоперационных нагрузочных тестов в 10-летнем популяционном исследовании. Среди 271 082 больных старше 40 лет, у которых проводилась плановая некардиальная операция промежуточного или высокого риска, неинвазивные нагрузочные тесты проведены у 23 991 (8,9%). После выделения сопоставимой контрольной когорты (n=46 120) проведение тестов было связано с улучшением годичной выживаемости (ОР 0,92 при 95% ДИ от 0,86 до 0,99; р=0,03) и снижением средней длительности пребывания в стационаре на 0,24 дня (95% ДИ
от –0,07 до –0,43 дня; р<0,001). Отмечено при этом, что проведение тестов повышало число осложнений в 1,35 раза у больных без клинических ФР (95% ДИ от 1,05 до 1,74). В то же время предоперационные стресс-тесты снижали риск развития кардиологических осложнений у больных промежуточного (при наличии 1—2 ФР; ОР 0,92 при 95% ДИ от 0,85 до 0,99) или высокого (при 3—6
ФР; ОР 0,80 при 95% ДИ от 0,67 до 0,97) риска. Тем не менее критика практики повседневного проведения неинвазивных стресс-тестов развивается и с другой стороны. Так, M.R. Back и соавт. [70] показали, что наличие трехсосудистого поражения КА при КГ являлось предиктором кардиальных осложнений при операциях на некоронарных сосудистых бассейнах, в то время как индуцируемая ишемия при стресс-тестах — нет. По данным мета-анализа с включением 8008 пациентов, у больных
с нормальными результатами нагрузочных тестов ежегодно развивались ИМ в 0,5% случаев и в 1,25% случаев проводилась реваскуляризация миокарда или возникала нестабильная стенокардии [71]. Хотя тесты с перфузией миокарда предоставляют достаточно точную клиническую информацию, есть случаи, когда при наличии угрожающего жизни поражения КА нет существенных изменений при нагрузочных теcтах [72]. Так, среди 110 больных с отрицательными результатами нагрузочной
ЭхоКГ у 8 (7%) отмечались признаки некроза миокарда при операциях на брюшной аорте. Таким образом, прогностическая ценность отрицательного результата нагрузочной ЭхоКГ составила лишь 92,7%, что существенно ниже, чем во многих других исследованиях [73]. J.A. Diamond и соавт. [74] сообщили о наличии в 29% случаев существенного поражения КА (в 9,1% — ствола левой КА и/или трехсосудистое поражение) у больных с нормальным перфузионным тестом, у которых проводили КГ в течение 6 мес после стресс-теста. У пациентов с однососудистым поражением часто выявляются негативные нагрузочные тесты [75]. Более того, среди старших возрастных групп негативные ненвазивные тесты не исключают наличие заметного поражения КА [76]. Наконец, пациенты с сосудистыми заболеваниями часто неспособны выполнить адекватные физические тесты, у них может быть наблюдаться сопутствующее поражение легких, что затрудняет проведение и оценку результатов нагрузочной ЭхоКГ, и они с меньшей вероятностью могут отказаться от лекарственных препаратов при проведении тестов. Можно сделать вывод, что неинвазивные тесты как средство прогнозирования и снижения периоперационного риска могут оставаться неоптимальной тактикой
у больных некоторых категорий, поскольку не позволяют выявить отдельных больных с ИБС.
Обычное проведение КГ перед некардиальными операциями
Возникает мысль о целесообразности обычного проведения КГ перед некардиологическими операциями промежуточного и высокого риска. Результаты когортных исследований, выполненных в прошлые годы [59, 60], как и опыт нашей клиники [58], свидетельствуют в пользу такого подхода. Однако ретроспективный характер исследований не давал возможности обосновать эту стратегию, что, в конечном счете, привело к резкому сокращению показаний к использованию данного метода обследования в последних рекомендациях ЕОК [12]. Поэтому знаковыми можно считать два исследования из Италии, опубликованные после выхода в свет данных рекомендаций [77, 78]. Обе эти работы сравнивали две различные диагностические стратегии, одной из которых было обычное проведение в предоперационном периоде КГ.
В исследовании M. Monaco и соавт. [77] обследованы 208 больных перед сосудистыми операциями промежуточного и высокого риска при наличии 2 ФР развития кардиальных осложнений и более. Все больные были рандомизированы либо в группу селективной КГ (только по результатам неинвазивных стресс-тестов) — группа А (n=104), либо в группу систематического проведения КГ у всех пациентов (группа В; n=105). В группе систематического проведения КГ существенно чаще выявляли ИБС (61,9%) по сравнению с группой с селективным проведением КГ (44,7%; р=0,02). Соответственно существенные различия отмечались и по частоте проведения превентивной реваскуляризации миокарда (58,1 и 40,1%; р=0,01). При анализе 30-дневных результатов двух диагностических стратегий в группе систематической КГ по сравнению с селективной КГ отмечалась тенденция к меньшему числу ИМ (1,9 и 3,9%; р=0,6), кардиальной смертности (1,9 и 6,8%; р=0,08) и тяжелых неблагоприятных исходов (4,8% и 11,7%; р=0,1). При длительном наблюдении (100 мес) выживаемость в группе больных систематического проведения КГ была выше, чем при селективной КГ (р=0,01). Еще более значимым было различие по выживаемости без тяжелых кардиальных осложнений (р=0,003).
В работе G. Illuminati и соавт. [78] обследованы 426 больных перед операцией каротидной эндартерэктомии (КЭЭ) в отсутствие ИБС в анамнезе и без изменений ЭКГ и данных ЭхоКГ. Больные были рандомизированы в группу предварительной КГ (n=216) и группу операции без КГ. Все больные перед КЭЭ получали аторвастатин, 65% больных группы А и 72% больных группы В получали β-адреноблокаторы. Признаки бессимптомного поражения КА выявлены на КГ у 68 больных 1-й группы. Эти стенозы подверглись реваскуляризации перед КЭЭ — у 66 больных выполнено стентирование КА, у 2 больных — операция КШ. Особенностью реваскуляризации миокарда у этих больных было проведение КЭЭ в среднем через 4 дня (1—8 дней) после стентирования КА. При стентировании вводили внутривенно болюсом тирофибан, после процедуры назначали двухкомпонентную антитромбоцитарную терапию (100 мг АСК + 75 мг клопидогрела), которую прерывали
только утром в день КЭЭ и продолжали вечером после операции. Такая тактика позволила избежать периоперационных тромботических осложнений, а периоперационная кровопотеря в группах была сопоставимой (126±42 и 112±36 мл; р=0,78). Хотя группы не различались по частоте летальных исходов и фатальных ИМ, в группе КГ и превентивной реваскуляризации миокарда таких случаев не было вообще. Кроме того, в этой группе не было и ишемических осложнений КЭЭ, в то время как в группе без КГ их было 4,3% (р=0,01). При однофакторном анализе по влиянию ФР на развитие
послеоперационных ишемических осложнений курение приводило к возрастанию риска развития осложнений в 2,98 раза (р=0,04), а проведение КГ снижало риск в 4 раза (р=0,01). При проведении множественного логистического регрессионного анализа только выполнение КГ обладало независимым влиянием на риск развития периоперационных ишемических осложнений (ОР 0,22 при 95% ДИ от 0,06 до 0,81; р=0,02). По результатам этих исследований можно сделать вывод, что отказ от обычного выполнения КГ приводит к недостаточному выявлению ИБС перед сосудистыми операциями промежуточного и высокого риска. Потенциально это могло служить причиной меньшей эффективности профилактической реваскуляризации миокарда в проведенных ранее РКИ, основанных на стратегии селективного выполнения КГ. Возможной заменой обычной КГ является мультиспиральная компьютерная томография КА [79—81], однако ее применение в предоперационной оценке риска развития кардиологических осложнений еще недостаточно изучено [81, 82].
Заключение
Новые рекомендации Европейского общества кардиологов по оценке и снижению риска развития
периоперационных осложнений подробно регламентируют действия врача в данной ситуации. Они позволяют избегать излишних неоправданных обследований и медикаментозной терапии при операциях с низким риском развития кардиальных осложнений, подчеркивают значимость периоперационного медикаментозного лечения. Однако проведенный анализ ставит под сомнение некоторые положения новых европейских рекомендаций, таких как сокращение предоперационных нагрузочных тестов и сокращение профилактической реваскуляризации коронарных артерий у больных перед операциями с промежуточным и высоким риском развития кардиальных осложнений. На это необходимо обратить особое внимание, поскольку в российских условиях с учетом имеющейся ограниченности диагностических и лечебных ресурсов у врачей появляется соблазн буквально следовать новым рекомендациям Европейского общества кардиологов. На наш взгляд, есть потребность в разработке отечественных рекомендаций по данной тематике, в которых необходимо
отразить следующие положения:
• Перед некардиальными операциями промежуточного и высокого риска необходима активная так-
тика предоперационного обследования больных для выявления поражения коронарных артерий (стресстесты, оптимально — проведение коронарографии).
• При выявлении поражения коронарных артерий выбор тактики реваскуляризации миокарда и этап-
ности хирургического лечения должен осуществляться командой специалистов с включением кардиологов, анестезиологов, хирургов и эндоваскулярных хирургов.
• Возможно проведение мультиспиральной компьютерной томографии коронарных артерий вместо
инвазивной коронарографии в отсутствие клинических симптомов ишемической болезни сердца.



