ВВЕДЕНИЕ
За последние годы в России вырос процент назначений ингибиторов натрий-глюкозного ко-транспортера 2-го типа (иНГЛТ-2, или глифлозинов), поскольку они имеют приоритет перед другими сахароснижающими средствами за счет своей способности замедлять прогрессирование хронической сердечной недостаточности (ХСН) и хронической болезни почек (ХБП) [1]. Кардио- и нефропротективные эффекты этого класса препаратов доказаны в многочисленных исследованиях [2, 3].
Наиболее широко глифлозины применяются у пациентов с сахарным диабетом 2-го типа (СД 2) старшего возраста. Являясь одной из групп сахароснижающих препаратов, не влияющих на секрецию инсулина, они позволяют избежать назначения высоких доз инсулиномиметиков и тем самым снизить риск гипогликемий.
Несмотря на множество плюсов иНГЛТ-2, на практике иногда приходится сталкиваться со снижением приверженности к приему этой группы препаратов, особенно среди пожилых пациентов с СД 2. Одна из причин этого – расстройства мочеиспускания: поллакиурия, никтурия, инфекции мочевыводящих путей (МВП). Следует сказать, что при приеме иНГЛТ-2 происходит увеличение частоты мочеиспусканий на 1–2 в сутки, однако большинство больных этого не замечает. Возрастные пациенты предрасположены к развитию гиперактивного мочевого пузыря (ГАМП), частота встречаемости которого выше среди лиц с СД 2 по сравнению с общей популяцией [4, 5]. Не исключено, что иНГЛТ-2 способны усугублять проявления гиперактивности мочевого пузыря. В инструкциях к применению глифлозинов нет данных об относительных или абсолютных противопоказаниях к их приему у пациентов с расстройствами мочеиспускания. В связи с этим больные, которым рекомендованы иНГЛТ-2 в рутинной клинической практике, как правило, не обследуются на наличие ГАМП.
В настоящее время работ, посвященных использованию иНГЛТ-2 у пациентов с ГАМП, мало. Ряд исследований продемонстрировал повышение частоты инфекций МВП на фоне терапии иНГЛТ-2, однако данные об обследовании участвовавших в них пациентов на наличие/отсутствие ГАМП отсутствуют [6, 7].
Цель исследования – оценить влияние терапии иНГЛТ-2 на течение ГАМП у пожилых пациенток с СД 2, а также возможность использования растительного уросептика для снижения риска инфекционных осложнений МВП на фоне применения дапаглифлозина.
МАТЕРИАЛ И МЕТОДЫ
Амбулаторно обследованы 18 пациенток с СД 2, у которых ГАМП выявлен при активном расспросе с помощью анкеты расстройств мочеиспускания DAN-IPSS и подтвержден дневниками мочеиспусканий. Медиана возраста пациенток равнялась 72 (68–79), длительность СД 2 – 10 (7–15) годам. Все пациентки получали сахароснижающую терапию, но без достижения целевых значений гликированного гемоглобина (HbA1c, %). Среди них 5 человек принимали метформин, 4 – комбинацию иДПП-4 и метформина, 6 – комбинацию производных сульфонилмочевины и метформина, 2 – инсулин и препарат сульфонилмочевины и 1 – комбинацию инсулина, иДПП-4 и метформина. Медиана HbA1c составила 7,9 (7,6–8,6) %. Все участницы ранее не получали терапию иНГЛТ-2, хотя имели показания к их назначению – ХСН и/или ХБП.
Исходно и спустя месяц применения дапаглифлозина в дозе 10 мг оценивались общий анализ мочи, уровень глюкозы плазмы натощак, дневники мочеиспусканий. Контрольное анкетирование, оценка дневников мочеиспускания, общий анализ мочи (ОАМ) выполнялись через 1, 2 и 3 мес. применения иНГЛТ-2.
Все пациентки подписывали информированное согласие на участие в исследовании.
Критерии исключения: наличие противопоказаний к приему иНГЛТ-2, когнитивные нарушения средней и тяжелой степени, затруднение самообслуживания, длительный прием петлевых диуретиков.
Статистическая обработка результатов осуществлялась с помощью программы Statistica 6,0. Количественные признаки представлены в виде медианы и интерквартильного размаха, соответствующего интервалу между 25 и 75 перцентилями. Оценка достоверности различий проводилась с использованием непараметрических методов сравнения по количественным признакам (критерий Манна – Уитни). Различия показателей считались достоверными при уровне значимости р < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При анализе анкет DAN-IPSS легкая степень тяжести расстройств мочеиспускания (1–12 баллов) исходно была установлена у 11, средняя степень (13–24 балла) – у 7 пациенток. Нарушения оттока мочи, признаки гипотонии мочевого пузыря, определяемые по вопросам 1–4, болезненности при мочеиспускании, непроизвольное выделение мочи (без позыва и физической нагрузки) отсутствовали. У всех пациенток наибольший промежуток между мочеиспусканиями составил 2–3 ч (1 балл), также во всех случаях отмечалась частота ночных мочеиспусканий 1–2 раза за ночь (1 балл). Ургентные позывы к мочеиспусканию, оцениваемые 2 баллами (не чаще 1 раза в день), регистрировались у 11 человек, 1 баллом (бывают редко) – у 7 пациенток. 3 участницы со средней степенью тяжести расстройств мочеиспускания отмечали потерю мочи после позыва не чаще 1 раза в день (2 балла). При исходном анализе дневников мочеиспусканий было установлено, что медиана частоты микций за сутки равнялась 10 (8–12) эпизодам, минимальный объем выделенной мочи – 70 (55–100) мл, максимальный – 235 (215–300) мл. Признаки инфекции в соответствии с ОАМ отсутствовали.
Перед назначением дапаглифлозина пациентки были проинформированы о необходимости соблюдать правила личной гигиены после каждого мочеиспускания.
Через месяц приема дапаглифлозина выполнилось повторное анкетирование, оценивались контрольные дневники мочеиспусканий. При анализе второго анкетирования у 6 пациенток нарушения мочеиспускания оценивались 25–36 баллами, что соответствует тяжелой степени расстройств, при исходной средней степени тяжести. Эти женщины отмечали учащение эпизодов недержания мочи чаще 1 раза в день и никтурию более 2 раз за ночь. Тяжесть расстройств мочеиспускания, характерных для ГАМП, исходно и на фоне терапии дапаглифлозином представлена на рисунке.
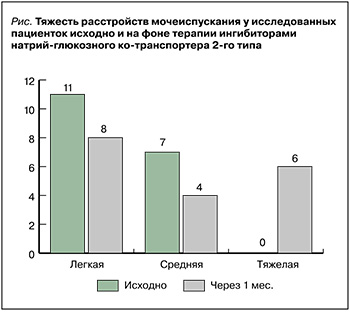
При оценке повторных дневников мочеиспусканий медиана частоты мочеиспусканий за сутки составила 12 (9–15) раз, минимального объема выделенной мочи – 50 (20–70) мл, максимального – 205 (165–235) мл. Было отмечено статистически значимое увеличение частоты мочеиспусканий на фоне приема дапаглифлозина (р = 0,025), снижение максимального и минимального объемов мочи (р = 0,02 и 0,009 соответственно). У всех пациенток с тяжелой степенью расстройств мочеиспускания и у 1 пациентки со средней степенью (n = 7) была обнаружена инфекция нижних МВП (значимая бактериурия и лейкоцитурия), что позволило диагностировать осложненный цистит, ставший показанием к отмене иНГЛТ-2 и назначению эмпирической антибактериальной терапии. В качестве антибактериального препарата был рекомендован цефиксим в дозе 400 мг 1 раз/сут. в течение 5 дней. Напомним, что, согласно рекомендациям по лечению осложненного цистита, в качестве первой линии терапии следует использовать бета-лактамные антибиотики (амоксициллин/цефалоспорин 2-го поколения) в комбинации с аминогликозидом [8]. Однако последний является неблагоприятным с точки зрения развития побочных эффектов, в частности нефротоксичности. Парентеральное введение антибиотика представлялось затруднительным, поэтому было отдано предпочтение терапии пероральным цефалоспорином 3-го поколения.
У 3 женщин со средней степенью тяжести расстройств мочеиспускания и у 4 с легкой степенью была выявлена бессимптомная бактериурия. Этим пациенткам назначили фосфомицин 3 г однократно без отмены дапаглифлозина. Из 7 пациенток с осложненным циститом после курса антибактериальной терапии 3 возобновили прием сахароснижающего препарата, 4 отказались. Всем пациенткам (n = 14), продолжившим терапию иНГЛТ-2, был рекомендован профилактический прием уросептического фитопрепарата, содержащего экстракты золототысячника травы, любистока лекарственного корней и розмарина листьев, по 10 дней в течение каждого месяца.
Дополнительное контрольное обследование, включавшее оценку ОАМ и повторное анкетирование, проводилось через 3 мес. У 10 пациенток была верифицирована легкая степень тяжести расстройств мочеиспускания, у 4 – средняя степень. Ни в одном случае не были выявлены лейкоцитурия и значимая бактериурия. Уровень гликированного гемоглобина через 3 мес. достоверно снизился с 7,9 (7,6–8,6) до 7,2 (6,9–8,0) % (р < 0,05).
Таким образом, из 18 женщин с СД 2, имевших ГАМП и получавших иНГЛТ-2 в течение месяца, у 8 пациенток (44,4%) появились бактериальные осложнения (значимая бактериурия и лейкоцитурия), в то время как во время клинических исследований этот показатель составлял 9,1% [9]. Данный феномен обусловлен механизмом действия иНГЛТ-2: индуцируемая ими глюкозурия благоприятна для активизации патогенной микрофлоры и развития воспалительного процесса в МВП. Следовательно, можно предположить, что иНГЛТ-2 отягощают течение ГАМП за счет присоединения бактериальной инфекции, и это снижает комплаентность пациенток к сахароснижающей терапии. В нашем исследовании 4 (22%) из 18 участниц отказались от дальнейшего приема глифлозина. Профилактическое применение растительного уросептика, наряду с соблюдением правил личной гигиены, способствует улучшению переносимости терапии иНГЛТ-2 за счет снижения частоты рецидивов инфекций МВП. Полученные нами результаты по применению фитопрепарата, содержащего экстракты золототысячника травы, любистока лекарственного корней и розмарина листьев, сопоставимы с данными других исследователей, продемонстрировавших, что добавление этого уросептика уменьшает частоту и выраженность дизурии у пациенток с СД 2 и рецидивирующим циститом на фоне терапии иНГЛТ-2 [10, 11].
ЗАКЛЮЧЕНИЕ
Применение иНГЛТ-2 у пациенток пожилого возраста с СД 2 и ГАМП повышает риск развития инфекционных осложнений со стороны МВП и может усугубить клинику расстройств мочеиспускания. Для выявления расстройств мочеиспускания у всех женщин с СД 2 старше 60 лет следует использовать опросник DAN-IPSS. Пациенткам с легкой степенью расстройств мочеиспускания на фоне приема иНГЛТ-2 целесообразно рекомендовать применение растительных уросептиков по схеме 10 дней в течение каждого месяца для снижения риска возникновения осложненного цистита и рецидивирующей инфекции нижних МВП. У больных со средней и тяжелой степенью расстройств мочеиспускания для достижения целевых значений гликемии предпочтительно использование препаратов инкретиновой терапии. При необходимости назначения иНГЛТ-2 требуется контроль за общим состоянием и анализом мочи пациента.



