Диабетическая кардиомиопатия (ДКМ) — особая нозологическая форма, индуцированная интерстициальным фиброзом, потерей кардиомиоцитов, нарушением использования энергии, патологией мелких сосудов и невропатией. Благодаря значительному росту заболевания сахарным диабетом (СД), в последующие десятилетия распространенность ДКМ, по-видимому, будет являться важной клинической проблемой [1].
Клинико-морфологические особенности заболеваний сердца у больных артериальной гипертензией (АГ) с СД являются более серьезными, чем у пациентов только с СД или АГ. Исследования показали, что сочетание СД и АГ приводит к большему вкладу интерстиция в состав ткани, чем наличие каждого заболевания по отдельности [2]. Кроме того, мало известно о влиянии гипергликемического ответа в течение 1-го часа (≥200 мг/дл) на пероральный тест на толерантность к глюкозе (ПТТГ), который до сих пор не является приемлемым критерием для постановки диагноза СД 2-го типа. Цель данного исследования — изучение различных признаков ДКМ у пациентов с контролируемой АГ в отсутствие СД и с гипергликемическим ответом в течение 1-го часа на ПТТГ.
Материал и методы
 Настоящее исследование проводилось в Научно-исследовательском медицинском центре Numune, Адана, Турция в соответствии с рекомендациями, предложенными в Хельсинкской декларации. Протокол и дизайн исследования одобрены Этическим комитетом центра.
Настоящее исследование проводилось в Научно-исследовательском медицинском центре Numune, Адана, Турция в соответствии с рекомендациями, предложенными в Хельсинкской декларации. Протокол и дизайн исследования одобрены Этическим комитетом центра.
Популяция исследования. Всего в исследовании приняли участие 47 пациентов с контролируемой эссенциальной АГ. Пациенты поступали в клинику на контрольное амбулаторное обследование. Каждым пациентом было подписано информированное согласие. Контролируемую АГ определяли при артериальном давлении (АД) менее 130/80 мм рт.ст. в случае измерения в домашних условиях и менее 140/90 мм рт.ст. — в больничных. Были отобраны пациенты старше 18 лет без коррекции антигипертензивной терапии в течение последних 3 мес.
У всех пациентов измеряли массу тела, рост и окружность талии (ОТ); рассчитывали индекс массы тела (ИМТ). Критериями исключения из исследования были наличие СД, ишемической болезни сердца, сердечной недостаточности, средней и тяжелой степени тяжести порока сердца, почечной недостаточности и использование лекарственных средств, влияющих на проводящую систему сердца.
Лабораторные тесты. Лабораторные исследования выполнены после 12-часового периода голодания. У всех пациентов измерены уровень глюкозы крови, липопротеинов низкой плотности (ЛНП), липопротеинов высокой плотности (ЛВП) и триглицеридов.
ПТТГ. Все испытуемые подвергались ПТТГ с 75 г глюкозы, принимаемой внутрь в течение 5 мин. Глюкозодегидрогеназным методом определен уровень глюкозы натощак, через 1 и 2 ч. Пациенты были сгруппированы в соответствии с результатами ответа в течение 1-го часа ПТТГ. Пациенты с уровнем глюкозы <200 мг/дл в течение 1-го часа ПТТГ составили 1-ю группу, в то время как во 2-й группе пациентов содержание глюкозы было ≥200 мг/дл. Пациенты с диагностированным нарушением толерантности к глюкозе по результатам ПТТГ (уровень глюкозы через 2 ч ≥140 мг/дл) исключены из исследования.
Эхокардиографическое исследование. Эхокардиографию (ЭхоКГ) проводили на аппарате Vivid 7. Размеры левого желудочка, толщина перегородки в диастолу (SWTd), внутренний диастолический размер левого желудочка (LVIDd) и толщина задней стенки ЛЖ в диастолу (PWTd) измерены в плоскости длинной оси. Массу левого желудочка (LVmass) рассчитывали по формуле [3]: LVmass=0,8 х {[1,04 х (SWTd + LVIDd + PWTd)3] – (LVIDd)3} + 0,6 г.
Параметры диастолической функции измерены в соответствии с Практическим руководством Американского общества по ЭхоКГ [4]. Максимальные значения волны кольцевого раннего диастолического наполнения (Е) и волны сокращения предсердий (А) измеряли в апикальной четырехкамерной позиции (А4С) в импульсно-волновом режиме (PW) допплера. Рассчитывали отношение E/А. Тканевую допплер-ЭхоКГ (TDI) проводили в проекции септальной и боковой створок митрального клапана с помощью PW TDI. Волна раннего диастолического наполнения (е′), волна сокращения предсердия (а') и систолическая волна (с) измерены на обоих кольцах в плоскости A4C. Для каждой переменной расчеты выполняли на основе средних измерений перегородки и боковых кольцевых миокардиальных скоростей. Соотношение кольцо—волна миокардиального раннего наполнения (E/е) и соотношение миокардиальное раннее заполнение—сокращение предсердия (е′/а′) были рассчитаны для каждого пациента.
 Оценка вариабельности ритма сердца (ВРС). Функция вегетативной нервной системы (ВНС) оценена по ВРС во время 24-часовой записи электрокардиограммы (ЭКГ). Все холтеровские записи проводили с помощью 12-канального рекордера. Артефакты и аритмии были исключены. Функция ВНС проанализирована в соответствии с рекомендациями Рабочей группы Европейского общества кардиологов и Североамериканского общества кардиостимуляции и электрофизиологии [5]. Исследование продолжалось в течение 24 ч с интервалами по 5 мин. Период наблюдения был поделен на 2 части: ночь (с 24 ч до 8 ч утра) и день (с 9 ч до 21 ч). Во время анализа домена измерено стандартное отклонение величин нормальных интервалов RR (SDNN, мс). При оценке частоты анализа домена использовано быстрое преобразование Фурье для получения мощности спектральной оценки ВРС. Суммарная мощность в диапазоне частот (0—0,40 Гц) была разделена на низкие частоты (НЧ: 0,04—0,15 Гц, модулируемые симпатической нервной системой) и высокие частоты (ВЧ: 0,15—0,40 Гц, модулируемые парасимпатической частью ВНС). Мощность НЧ и ВЧ компонентов рассмотрена в нормализованных единицах (н.ед.). Отношение НЧ/ВЧ рассчитано с использованием нормализованных единиц этих параметров. Анализ данных проведен с помощью программы Cardioscan 2 (DM Software).
Оценка вариабельности ритма сердца (ВРС). Функция вегетативной нервной системы (ВНС) оценена по ВРС во время 24-часовой записи электрокардиограммы (ЭКГ). Все холтеровские записи проводили с помощью 12-канального рекордера. Артефакты и аритмии были исключены. Функция ВНС проанализирована в соответствии с рекомендациями Рабочей группы Европейского общества кардиологов и Североамериканского общества кардиостимуляции и электрофизиологии [5]. Исследование продолжалось в течение 24 ч с интервалами по 5 мин. Период наблюдения был поделен на 2 части: ночь (с 24 ч до 8 ч утра) и день (с 9 ч до 21 ч). Во время анализа домена измерено стандартное отклонение величин нормальных интервалов RR (SDNN, мс). При оценке частоты анализа домена использовано быстрое преобразование Фурье для получения мощности спектральной оценки ВРС. Суммарная мощность в диапазоне частот (0—0,40 Гц) была разделена на низкие частоты (НЧ: 0,04—0,15 Гц, модулируемые симпатической нервной системой) и высокие частоты (ВЧ: 0,15—0,40 Гц, модулируемые парасимпатической частью ВНС). Мощность НЧ и ВЧ компонентов рассмотрена в нормализованных единицах (н.ед.). Отношение НЧ/ВЧ рассчитано с использованием нормализованных единиц этих параметров. Анализ данных проведен с помощью программы Cardioscan 2 (DM Software).
Статистический анализ. Статистический анализ выполнен по SPSS для Windows 14,0 (SPSS Inc, Chicago, IL). Исчисляемые показатели сравнивали с независимыми выборками критерия Стьюдента, в то время как неисчисляемые — по критерию χ2. Числовые переменные представлены в виде средних значений ± стандартное отклонение, а порядковые значения — числом случаев (n) и процентами (%). Статистически значимый порог определен как р≤0,05. Линейный регрессионный анализ проведен для определения переменных, независимо связанных с дневными и ночными значениями SDNN.
Результаты
Описательные переменные и результаты лабораторных исследований обеих групп приведены в табл. 1. Пациенты 2-й группы были значительно старше (47,6±5,7 года против 41,8±7,5 года; р=0,004), окружность талии в этой группе была также больше, чем в 1-й группе (115,8±7,8 см против 109,3±12,4 см; р=0,036), хотя ИМТ были одинаковыми в обеих группах. Процент использования блокаторов ренин-ангиотензин-альдостероновой системы (РААС) был значительно ниже среди пациентов 2-й группы (72,7% против 96%; р=0,04).
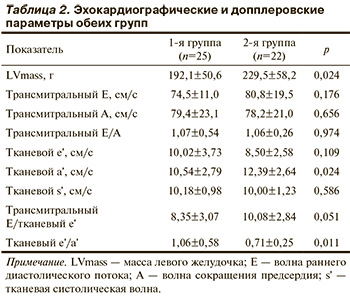
Сравнение эхокардиографических и допплеровских параметров в обеих группах представлено в табл. 2. Значение LVmass (229,5±58,2 г против 192,1±50,6 г; р=0,036) и данные е′/а′ (0,71±0,25 против 1,06±0,58; р=0,011) были значительно выше во 2-й группе. Соотношение Е/е′ также было выше во 2-й группе (10,08±2,84 против 8,35±3,07; р=0,051), и результат был практически значимым.
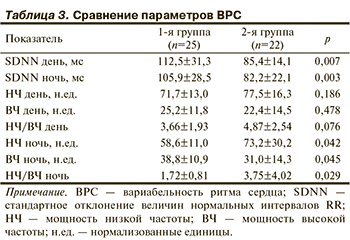
При оценке ВРС (табл. 3) установлено, что SDNN во 2-й группе значительно ниже как в дневное (85,4±14,1 мс против 112,5±31,3 мс; р=0,007), так и в ночное (82,2±22,1 мс против 105,9±28,5 мс; р=0,004) время. Соотношение мощности НЧ/ВЧ в ночное время также было достоверно выше во 2-й группе (3,75±4,02 против 1,72±0,81; р=0,029).
Обсуждение
В настоящем исследовании изучались признаки ДКМ у пациентов с контролируемой АГ и гипергликемическим ответом в течение 1-го часа ПТТГ. У данной популяции пациентов обнаружены увеличение LVmass, нарушение диастолической функции левого желудочка и снижение ВРС.
 Диастолическая дисфункция (ДД) — ранний, а возможно и первый признак ДКМ [1, 6, 7]. Это часто наблюдаемый симптом у больных СД без явных сердечно-сосудистых заболеваний (ССЗ) [8]. Частота ДД у пациентов среднего возраста с бессимптомным СД 2-го типа достигает 30% [9, 10]. На последующих этапах страдает систолическая функция и развивается вегетативная невропатия сердца [1]. ДД, наблюдаемая при СД, демонстрирует связь с региональной симпатической целостностью и клиническими маркерами вегетативной невропатии сердца [11]. У пациентов с пограничной АГ наблюдаются аналогичные связи между степенью ДД и параметрами ВРС [12].
Диастолическая дисфункция (ДД) — ранний, а возможно и первый признак ДКМ [1, 6, 7]. Это часто наблюдаемый симптом у больных СД без явных сердечно-сосудистых заболеваний (ССЗ) [8]. Частота ДД у пациентов среднего возраста с бессимптомным СД 2-го типа достигает 30% [9, 10]. На последующих этапах страдает систолическая функция и развивается вегетативная невропатия сердца [1]. ДД, наблюдаемая при СД, демонстрирует связь с региональной симпатической целостностью и клиническими маркерами вегетативной невропатии сердца [11]. У пациентов с пограничной АГ наблюдаются аналогичные связи между степенью ДД и параметрами ВРС [12].
Нарушенная вегетативная функция связана со всеми причинами, а сердечно-сосудистая смертность и риск смерти от ССЗ повышаются у пациентов с СД и АГ [13]. Снижение ВРС также связано с быстрым прогрессированием атеросклероза коронарных артерий [14], повышенным риском развития осложнений ССЗ [14] и инсульта [15]. Нарушение ВРС начинается на ранних стадиях диабетических изменений [16]. Резистентность к инсулину вызывает глобальную дисфункцию ВНС и изменение вегетативного баланса и выявляется даже у пациентов с недиабетическим уровнем глюкозы в крови натощак [17, 18]. Об измененной функции ВНС также часто сообщалось у пациентов с АГ. Среди мужчин с нормальным АД снижение ВРС связано с большим риском развития АГ [19]. У пациентов с тяжелой АГ установлено существенное изменение ВРС по сравнению с больными с легкой АГ [20]. У таких больных степень гипертрофии левого желудочка коррелирует с повышенным риском развития предсердных и желудочковых аритмий [21].
Как мы уже отмечали ранее, наличие СД и АГ повышает риск заболевания сердца по сравнению с таковым при наличии только АГ или только СД. Исследования показали, что сочетание СД и АГ приводит к большему вкладу интерстиция в состав ткани, чем наличие только одного расстройства [2]. У резистентных пациентов с АГ сопутствующий СД 2-го типа связан с большей вегетативной неустойчивостью, более низким уровнем адипонектина и повышением ИМТ [22]. В данном исследовании мы продемонстрировали увеличение массы сердца, нарушение диастолической функции и снижение ВРС у больных с контролируемой АГ и гипергликемией в 1-й час ПТТГ.
Ингибиторы ангиотензинпревращающего фермента (АПФ) часто используются в лечении АГ и различных ССЗ. Препараты этой группы не только оказывают антипролиферативный и антигипертензивный эффекты, но и улучшают действие инсулина на клеточном уровне [23, 24]. Они облегчают кровоток через микроциркуляцию в жировой и скелетной мышечной ткани [25]. Более частое использование блокаторов РААС в 1-й группе пациентов может поддерживать антидиабетические эффекты блокаторов РААС.
В современных практических руководствах диагноз СД может быть установлен у пациентов с уровнем глюкозы ≥200 мг/дл независимо от независимо от приема пищи [26]. Однако уровень глюкозы в крови в течение 1-го часа ПТТГ не входит в этот критерий. В то же время в этом исследовании мы показали серьезные предварительные результаты ДКМ у пациентов с контролируемой АГ и гипергликемическим ответом только в 1-й час ПТТГ.
Заключение
Признаки диабетической кардиомиопатии могут наблюдаться у больных с контролируемой артериальной гипертензией и диабетическим ответом в 1-й час перорального теста на толерантность к глюкозе. Для более точных результатов необходимо проведение дальнейших контролируемых исследований.



