Наличие сахарного диабета (СД) 2-го типа у больных ишемической болезнью сердца (ИБС) увеличивает вероятность развития фатальных желудочковых аритмий и наступления сердечной смерти [1]. Важную роль в развитии злокачественных аритмий при СД играет дисбаланс вегетативной нервной системы (ВНС), связанный с развитием сердечно-сосудистой автономной нейропатии [2]. Одним из методов, позволяющих оценить активность различных отделов ВНС, является изучение вариабельности ритма сердца (ВРС) [3]. Однако существуют противоречивые данные о прогностической роли показателей ВРС при диабетической нейропатии [4]. При этом с дисбалансом автономной нервной системы при СД связано удлинение интервала QT, являющегося предиктором развития фатальных желудочковых аритмий [5, 6].
Целью данного исследования явилась сравнительная характеристика показателей ВРС и интервала QT
у больных ИБС и СД 2-го типа.
Материал и методы
В исследование был включен 141 больной ИБС, из них 29 (20,6%) пациентов с нестабильной стенокардией и 112 (79,4%) с острым инфарктом миокарда, в возрасте от 30 до 69 лет (средний возраст 52,4±7,3 года). Диагноз инфаркта миокарда подтверждался положительным тропониновым тестом. У 101 (71,6%) больного наблюдался СД, средняя продолжительность которого составляла 4,8±3,1 года. У 36 (35,6%) пациентов СД был выявлен впервые. Больные СД были достоверно старше (средний возраст 55,5±6,4 против 52,1±6,9 года; p=0,006). В качестве критерия компенсации обмена
веществ при СД был использован уровень гликированного гемоглобина (HbAlc) согласно рекомендациям Европейского бюро Международной федерации по диабету и Европейского бюро Всемирной организации здравоохранения [7]. Больных СД с низким риском развития сосудистых осложнений было 44 (43,6%), с риском развития макроангиопатии — 26 (25,7%), с риском развития микроангиопатии — 31 (30,7%). Для диагностики диабетической нейропатии применяли
исследование вибрационной, тактильной и болевой чувствительности. У 53 (52,5%) больных СД выявлялась дистальная симметричная нейропатия, из них у 46 (86,8%) наблюдалось преимущественное поражение чувствительных нервов (сенсорная форма), у 7 (13,2%) комбинированное поражение нервов (сенсомоторная форма).
В качестве группы контроля в исследование были включены 29 пациентов (средний возраст 44,9±6,8 года) без достоверно верифицированной ИБС, для исключения которой выполняли электрокардиографию (ЭКГ), велоэргометрию, холтеровское мониторирование ЭКГ, эхокардиографию.
Анализ ВРС во временно`й области за 24 ч записи ЭКГ проводили с помощью программы «Astrocard
HOLTERSYSTEM-2F Elite». Изученные показатели ВРС представлены в табл. 1.
Таблица 1. Изученные показатели ВРС во временно`й области за 24 ч записи ЭКГ.
Для изучения показателей интервала QT регистрацию ЭКГ производили в 12 отведениях со скоростью 50 мм/с. Интервал QT измеряли от места перехода изоэлектрической линии сегмента PQ(R) в зубец Q(R) до места пересечения изоэлектрической линии ТР с касательной, проведенной по максимальному наклону нисходящей части волны Т. В случае невозможности точного определения зубца Т отведение исключали из анализа. При наличии зубца U за окончание интервала QT принимали самую низкую точку кривой между зубцами T и U. Интервал QT не исследовали, если число пригодных отведений не превышало 8, из них как минимум 4 грудных. В каждом отведении величину интервала QT рассчитывали как среднее из измерений в 3 последовательных циклах. Рассчитывали значение корригированного интервала QT по формуле H. Bazett, преобразованной L. Taran и N. Szilagyi [8, 9]. Корригированную
дисперсию интервала QT (DQTc) рассчитывали как разность между максимальным и минимальным значением корригированного интервала [10]. В качестве сравниваемых показателей по данным стандартной ЭКГ были использованы DQTc и максимальное корригированное значение интервала QT (QTc max), являющихся наиболее значимыми предикторами сердечной смерти из пара-
метров интервала QT [11].
Статистическую обработку данных проводили при помощи пакета программ STATISTICA 8.0. Сравнение
дискретных величин осуществляли с использованием критерия χ2 Пирсона с коррекцией по Йетсу. Для сравнения средних непрерывных величин с нормальным распределением применялся групповой t-тест, с неправильным распределением — непараметрический критерий Манна—Уитни. С целью определения основных показателей, обладающих большей полнотой связи и объединяющих различные процессы, был применен кластерный анализ. Дендрограмму иерархического кластерного анализа строили на основе невзвешенного парно-группового центроидного метода. Данные исследований представлены в виде их средних значений и стандартного отклонения (M±SD). Различия между группами считали статистически значимыми при р<0,05.
Результаты и обсуждение
При изучении ВРС выявлено, что у пациентов с ИБС без СД по сравнению с контролем были достоверно
меньше показатели TP, NN 50, LF и HF. Наличие СД у больных ИБС кроме уменьшения указанных пока-ателей приводило к дополнительному достоверному снижению SDNN, RMSSD и ULF (табл. 2). Кроме того, у пациентов с СД по сравнению с контролем были достоверно выше QTc max и DQTc. При сравнении показателей ВРС в группе больных ИБС выявлено, что у пациентов с СД наблюдаются более низкие показатели RRNN (p=0,004), LF (p=0,001) и LF/HF (p=0,01).
Таблица 2. Сравнительная характеристика показателей ВРС и интервала QT у больных ИБС и СД.
Таблица 3. Сравнительная характеристика показателей гликозилированного гемоглобина, ВРС и интервала QT у больных с СД в зависимости от риска развития сосудистых осложнений.
Таблица 4. Сравнительная характеристика уровней гликированного гемоглобина, ВРС и интервала QT у больных СД в зависимости от наличия нейропатии.
При изучении ВРС в зависимости от состояния компенсации (табл. 3), выявлено, что у пациентов ИБС
и СД с риском развития микроангиопатии наблюдалось достоверное уменьшение показателей RRNN
(p=0,03) и LF (p=0,02). Низкая мощность в диапазоне LF у больных СД обратно коррелировала с ростом
уровня гликированного гемоглобина (r=–0,25; p<0,05). У больных СД с развитием дистальной симметричной нейропатии наблюдались достоверное снижение мощности в диапазоне HF и увеличение QTc max (табл. 4). Таким образом, сопутствующий СД у больных ИБС приводит к более выраженному дисбалансу ВНС, а также негомогенности реполяризации миокарда, что отражается удлинением интервала QT. Уменьшение показателей мощности в диапазоне LF предполагает
нарушения механизмов регуляции сосудистого тонуса через барорефлекс.
В группе больных СД с риском развития микроангиопатии снижение показателей LF было максимальным и коррелировало с ростом уровня гликированного гемоглобина, что свидетельствует о важной роли
гипергликемии в нарушении симпатической регуляции. Полагают, что СД сопровождается повышением тонуса симпатической части ВНС вследствие гиперинсулинемии, которая усиливает обмен глюкозы в инсулинчувствительных клетках вентромедиального гипоталамуса и растормаживает симпатические центры ствола головного мозга [12]. Снижение при СД с наличием нейропатии HF, косвенно отражающего вагусную активность, прямо коррелировало с RMSSD (r=0,90; p<0,05), NN 50 (r=0,86; p<0,05) и LF (r=0,76; p<0,05), что свидетельствует о смещении вегетативного баланса в сторону преобладания симпатического отдела. Поскольку снижение HF наблюдалось на фоне уменьшения LF,
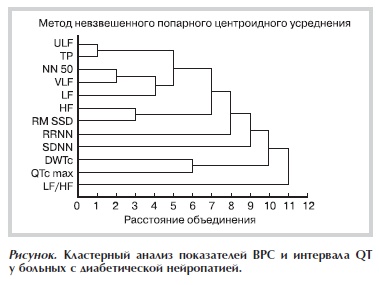
это предполагает общее снижение вегетативного тонуса. Выявленные нарушения сопровождаются удлинением интервала QT, одним из механизмов которого считается дисбаланс симпатической иннервации (снижение правосторонней симпатической иннервации) [13]. Полагают, что диабетическая вегетативная нейропатия характеризуется нейрональной дегенерацией нервных волокон как парасимпатического, так и симпатического трактов. При наличии клинических симптомов диабетической нейропатии наблюдается уменьшение мощности всего спектра частот, главным образом высоких [14]. При этом развитие диабетической нейропатии сопровождается удлинением интервала QT, величина которого может иметь даже большее прогностическое значение в оценке риска развития желудочковых аритмий, чем показатели ВРС [15]. В проведенном исследовании по данным кластерного анализа показателями, обладающими большей полнотой связи с развитием нейропатии у больных СД, являлись снижение отношения мощностей LF/HF и удлинение интервала QT (см. рисунок).
Заключение
Наличие сахарного диабета у больных ишемической болезнью сердца сопряжено со снижением тонуса вегетативной нервной системы, преимущественно за счет активности парасимпатического звена, что сопровождается нарушением реполяризации желудочков сердца.



