За последние годы в кардиохирургической практике накоплен огромный опыт выполнения операций коронарного шунтирования (КШ) пациентам с многососудистым поражением коронарного русла. Совершенствование и развитие методов искусственного кровообращения (ИК), защиты миокарда, анестезии и интенсивной терапии позволяют рассматривать КШ как достаточно безопасное хирургическое вмешательство с низким уровнем летальности, операционных и послеоперационных осложнений, а также достаточно высоким реабилитационным потенциалом. Однако характерные послеоперационные осложнения, связанные с применением ИК, в свое время привели к разработке и внедрению в клиническую практику метода КШ на работающем сердце (off-pump) — КШ-РС. Переходной технологией, направленной на улучшение результатов, стало КШ в условиях параллельной нормотермической вспомогательной перфузии (КШ-РС-НП), которая позволила проводить операции без кардиоплегии и аноксии сердца у пациентов из группы высокого риска [1, 2].
Одним из ведущих критериев оценки клинической эффективности КШ является состояние сердечной мышцы, которое традиционно оценивается преимущественно на основании клинических и биохимических показателей. Общепризнанными биохимическими маркерами повреждения миокарда служат уровень кардиоспецифичных фракций тропонина и активности цитоплазматического изофермента креатинфосфокиназы (КФК) клеток миокарда с учетом оценки изоформы фракции МВ (КФК-МВ). При этом уровень тропонина I может рассматриваться как «золотой стандарт» диагностики острого повреждения сердечной мышцы [3, 4—6]. Проведенный анализ литературы указывает лишь на единичные исследования, рассматривающие сравнительную динамику клинико-биохимических показателей состояния сердечной мышцы в раннем послеоперационном периоде после использования различных технологий КШ.
Целью нашего исследования является сравнительная клинико-биохимическая оценка состояния миокарда при применении различных технологий КШ (КШ-ИК, КШ-РС-НП и КШ-РС).
Материал и методы
Исследование выполнялось на базе ФГБУ «Центральная клиническая больница» в период с 2011 по 2014 г. Всего под наблюдением находились 100 пациентов (86% мужчин, 14% женщин) в возрасте 56—69 лет, разделенные на 3 сопоставимые по полу, возрасту, количеству пораженных коронарных артерий, состоянию миокарда и оценке хирургического риска по шкале EUROSCORE группы в зависимости от техники КШ. В 1-ю группу вошли 35 пациентов, подвергнутых КШ с ИК (КШ-ИК) и кардиоплегией, во 2-ю — 32 пациента с КШ на работающем сердце и параллельной нормотермической перфузией КШ-РС-НП, 3-ю группу составили 33 пациента после КШ-РС.
Технология проведения КШ отличалась тем, что при выполнении операции с ИК и кардиоплегией (1-я группа) реваскуляризацию миокарда проводили на остановленном сердце, в то время как у пациентов 2-й и 3-й групп реваскуляризация миокарда осуществлялась на работающем сердце. КШ во 2-й группе сопровождалось применением нормотермической вспомогательной перфузии с использованием аппарата ИК. При этом начальные этапы операции (выполнение под эндотрахеальным наркозом срединной стернотомии, системная гепаринизация, канюляция восходящей аорты и правых отделов сердца) в 1-й и 2-й группах практически не различались. Шунтирование коронарных артерий в 3-й группе происходило по классической методике off-pump с применением стабилизатора миокарда и внутренних шунтов.
 Исследование клинических показателей выполняли в 1-е сутки после КШ на основании оценки фракции выброса левого желудочка (ФВ ЛЖ) (по данным эхокардиографии). Биохимическое обследование также проводили в 1-е сутки после КШ и основывали на оценке КФК, КФК-МВ и кардиоспецифичного тропонина I в плазме крови по стандартной методике. Диагноз инфаркта миокарда (ИМ) в послеоперационном периоде устанавливали на основании повышения уровней КФК, КФК-МВ, тропонина I в сочетании с ишемическими изменениями на электрокардиограмме и появлением нарушений локальной сократимости миокарда в соответствующих зонах.
Исследование клинических показателей выполняли в 1-е сутки после КШ на основании оценки фракции выброса левого желудочка (ФВ ЛЖ) (по данным эхокардиографии). Биохимическое обследование также проводили в 1-е сутки после КШ и основывали на оценке КФК, КФК-МВ и кардиоспецифичного тропонина I в плазме крови по стандартной методике. Диагноз инфаркта миокарда (ИМ) в послеоперационном периоде устанавливали на основании повышения уровней КФК, КФК-МВ, тропонина I в сочетании с ишемическими изменениями на электрокардиограмме и появлением нарушений локальной сократимости миокарда в соответствующих зонах.
Результаты и обсуждение
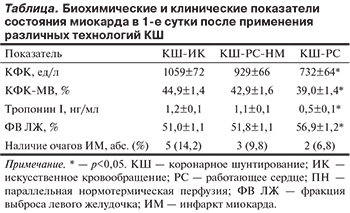
Результаты сравнительной оценки биохимических и клинических показателей состояния миокарда в 1-е сутки после проведения различных технологий КШ представлены в таблице.
Представленные в таблице данные свидетельствуют об отсутствии статистически значимых различий по исследуемым показателям между группами пациентов после КШ-ИК и КШ-РС-НП при наличии тенденции к более выраженной положительной динамике в группе пациентов, оперированных по технологии КШ-РС-НП. При этом выявлены статистически значимые различия в исследуемых показателях в группе КШ-РС по сравнению с группами КШ-ИК и КШ-РС-НП, которые выражаются снижением уровня КФК (на 21,2—30,9%; p<0,05), КФК-МВ (на 9,1—13,1%; p<0,05), тропонина I (на 0,6—0,7%; p<0,05) и повышением ФВ ЛЖ (на 9,8—11,6%; p<0,05). Наряду с этим в группе КШ-РС выявлено выраженное снижение частоты возникновения очагов ИМ (6,8%) по сравнению с группами КШ-ИК и КШ-РС-НП (14,2 и 9,8% соответственно). Дальнейший математический анализ во всех обследованных группах выявил тесную корреляцию (r=0,74—0,82; p<0,01) между биохимическими показателями и величиной ФВ ЛЖ.
Наиболее высокая клиническая эффективность операции при сравнительной оценке всех исследуемых показателей отмечалась в группе пациентов, у которых КШ выполнялось в условиях работающего сердца. Более низкие показатели наблюдались в группе КШ-ИК, что может быть объяснено использованием аппарата ИК. Применение ИК является фактором риска развития ишемии сердечной мышцы с последующей гибелью кардиомиоцитов [7—9]. Сравнительная оценка групп КШ-РС и КШ-РС-НП также показала более высокую клиническую эффективность в 1-й группе, что, по-видимому, связано с технологией КШ-РС-НП, включающей применение ИК.
Выявленная в работе тесная корреляция между биохимическими показателями и величиной ФВ ЛЖ подтверждает корректность методического подхода к оценке состояния сердечной мышцы с позиций исследования маркеров повреждения клеток миокарда (КФК, КФК-МВ, тропонин I). Клиническим подтверждением данного положения явились различия между группами по частоте возникновения очагов ИМ, которая в группе с КШ-РС была на 7,4% ниже, чем в группе КШ-ИК, и на 3% ниже, чем в группе КШ-РС-НП.
Заключение
Клиническая эффективность коронарного шунтирования с позиций состояния сердечной мышцы в 1-е сутки после операции существенно выше при технологии проведения хирургического вмешательства на работающем сердце по сравнению с технологиями применения искусственного кровообращения и на работающем сердце с параллельной нормотермической перфузией. Эти данные подтверждаются более низким уровнем биохимических маркеров повреждения миокарда и более высокими значениями клинического показателя фракции выброса левого желудочка. Однако при сравнении изложенных данных в группах коронарного шунтирования при искусственном кровообращении и коронарного шунтирования в условиях параллельной нормотермической вспомогательной перфузии отмечается наличие тенденции к более выраженной положительной динамике в группе пациентов с коронарным шунтированием в условиях параллельной нормотермической вспомогательной перфузии.



