В процессе ремоделирования левого желудочка (ЛЖ) у больных острым инфарктом миокарда (ОИМ) происходят сложные изменения не только сократительного миокарда ЛЖ, но и перестройка структур митрального клапана (МК) с развитием у некоторых пациентов ишемической митральной регургитации (ИМР).
Ремоделирование МК (изменения структуры клапана) у больных ОИМ означает процесс комплексно-
го нарушения функции клапана без морфологических изменений его створок и подклапанного аппарата в ответ на утрату части жизнеспособного миокарда ЛЖ. Взаимодействие нескольких патогенетических факторов, направленных на изменение показателей структур клапана в процессе ремоделирования, определяет характер и выраженность ишемической деформации митрального клапана (ИДМК).
Изучение последовательности изменений структур МК у больных ОИМ имеет большое значение для понимания механизмов развития ИМР и ее роли в развитии сердечной недостаточности у больных ИБС.
Цель исследования: изучить процесс ремоделирования (перестройки) структур МК у больных трансмуральным и крупноочаговым ОИМ с ИМР в острой и подострой стадии ИМ.
Материал и методы
Обследованы 160 пациентов с крупноочаговым и трансмуральным ОИМ, поступивших в отделение
кардиореанимации ГКБ № 7 Москвы (табл. 1).
Таблица 1. Клиническая характеристика обследованных больных (n=160).
У 130 обследованных пациентов был ОИМ с ИМР и у 30 пациентов, составивших группу сравнения, ОИМ без ИМР. Диагноз ОИМ основывался на критериях, рекомендованных ВОЗ (1970). Возраст пациентов составлял от 37 до 81 года (средний 60,9±10,2 года).
Пациентов включали в исследование по следующим критериям: наличие крупноочагового или трансму-
рального ОИМ, удовлетворительного окна визуализации при эхокардиографии (ЭхоКГ), структурно нормального МК, недилатированного левого предсердия (ЛП) и отсутствия нарушений ритма сердца во время исследования. Критериями исключения были: наличие других (кроме ОИМ) заболеваний сердца (органическое поражение створок клапанов, врожденные пороки сердца, заболевания перикарда, инфильтративные заболевания, пролапс МК, аортальная регургитация).
Всем пациентам проводили стандартные общеклинические, лабораторные (общий анализ крови, креатинфосфокиназа — КФК, ее фракция МВ, тропонин I), рентгенологические и электрокардиографические исследования.
На 2-е и 20-е сутки заболевания с помощью ЭхоКГ определяли количественные показатели ИМР [площадь регургитационного отверстия (SRO мм2), регургитационный объем (RV, мл), фракция регургитации (RF, %)] с использованием комбинации цветового допплеровского картирования проксимального сходящегося потока регургитации (PISA-метод, proximal isovelocity surface area method) и количественной допплер-ЭхоКГ (Q-DE-метод) [1—3].
У всех больных для оценки показателей деформации МК измеряли величину систолического верхушечного прогиба створок МК — расстояние между точкой смыкания створок и плоскостью митрального кольца (h, см) (рис. 1).
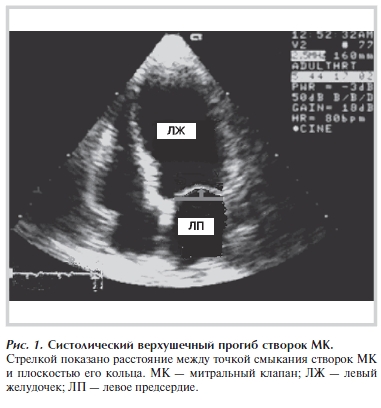
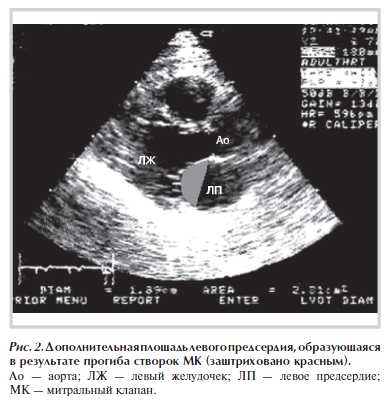
Площадь (S, см2) и дополнительный объем (V, мл) ЛП, образующиеся в результате прогиба створок МК в сторону верхушки ЛЖ в систолу, измеряли по длинной оси ЛЖ (рис. 2). Дополнительный объем ЛП оценивали по методу Симпсона. Расчитывали систолическую (Ss), диастолическую (Sd) площади митрального кольца, а также сократимость митрального кольца по формуле: C = [(Sd – Ss)/Sd] · 100%.
Статистическую обработку данных осуществляли с помощью пакета статистических программ SPSS for
Windows (версия 11.5).
Результаты и обсуждение
Сравнительный анализ показателей, характеризующих структуры МК у больных ОИМ с ИМР и без ИМР,
позволил выявить статистически значимые различия в остром периоде заболевания (2-е сутки) (табл. 2).
Таблица 2. Показатели стуктур МК у больных инфрктом миокарда в остром периоде заболевания (2 е сутки).
У пациентов с инфарктом миокарда (ИМ) и ИМР в остром периоде заболевания прогиб створок МК был
больше на 35,7%, чем у пациентов с ИМ без митральной регургитации. Дополнительные площадь и объем ЛП, образующиеся в результате систолического прогиба створок МК, превышали соответствующие показатели у пациентов с ОИМ без ИМР на 39,8 и 81,9% соответственно. Диастолическая и систолическая площади кольца МК были больше на 10,7 и 16,6% соответственно при сравнении с показателями МК у пациентов с ИМ без митральной регургитации. Сократимость
кольца МК у пациентов с ИМР, напротив, была меньше на 24,2%, чем у пациентов с ИМ без ИМР.
Таблица 3. Показатели ИДМК и ИМР у больных в остром и подостром периодах ИМ.
Таблица 4. Показатели деформации МК у пациентов с ИМ и различной степенью тяжести ИМР.
В подострой стадии заболевания в процессе формирования рубца (20-е сутки) у пациентов с ИМ и ИМР
отмечено незначительное увеличение показателей ишемической деформации структур МК при сравнении с результатами исследования структур клапана в остром периоде заболевания (p>0,05) (табл. 3). В процессе исследования изучена связь между показателями ИДМК и степенью тяжести ИМР (табл. 4). Анализируя показатели ИДМК у пациентов с различной степенью тяжести ИМР, мы отметили, что такие показатели структур МК, как величина систолического верхушечного прогиба створок МК (h, см), дополнительная площадь (S, см2) и объем (V, мл) ЛП, образующиеся в результате систолического прогиба створок МК, систолическая (Ss) и диастолическая (Sd) площади кольца достоверно и последовательно увеличиваются от легкой к тяжелой степени ИМР, а сократимость митрального кольца уменьшается.
Результаты изучения корреляции между показателями деформации МК и количественными показателями ИМР отражают прямую корреляцию средней силы между исследуемыми показателями ИДМК и ИМР. Коэффициент корреляции между фракцией регургитации и величиной смещения створок МК составил 0,628 (p<0,0001), между регургитационным объемом (RV) и дополнительным объемом ЛП — 0,52 (p<0,0001) (рис. 3).
Рисунок 3. Корреляции между фракцией регургитации и величиной смещения створок МК (А; r=0,628; p<0,0001), между регургитационым объемом и дополнительным объемом левого предсердия (Б; r=0,52; p<0,0001).
Таким образом, у больных трансмуральным и крупноочаговым ОИМ с ИМР наиболее существенные
изменения структур МК происходят в остром периоде ИМ с последующей замедленной деформацией структур МК в подострой стадии заболевания. Выявленные изменения МК у пациентов с ИМ формируются в результате взаимодействия нескольких патогенетических факторов, играющих важную роль в процессе острого ремоделирования МК и оказывающих в этом периоде заболевания наиболее существенное влияние на показатели структур МК.
Локальное изменение формы ЛЖ приводит к смещению папиллярных мышц от плоскости кольца МК
и прогибу створок клапана в сторону верхушки ЛЖ с образованием дополнительного объема в ЛП. В ряде работ [3—5] показано, что смещение папиллярных мышц является одним из основных факторов, приводящих к деформации МК и формированию ИМР. При этом существенно, в какой области миокарда ЛЖ локализуется зона инфаркта. В последние годы обнаружено, что при ИМ задней (нижней) стенки ЛЖ локальное ремоделирование ведет к нарушению поддержки задней папиллярной мышцы со смещением преимущественно задней створки МК. Степень ИМР зависит от направления натяжения митральной створки [6, 7]. Заднебоковое смещение создает максимальное натяжение хорд и смещение створки клапана в полость желудочка с образованием регургитационного отверстия (рис. 4).
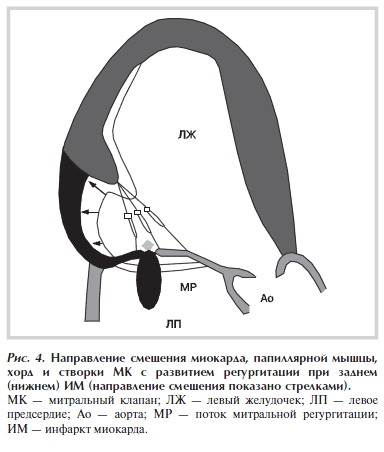
По мнению ряда авторов [8, 9] у больных с передним ИМ для возникновения ИМР необходимо также развитие глобального ремоделирования ЛЖ. Из-за нарушения положения папиллярных мышц происходит смещение точки смыкания створок МК в сторону верхушки ЛЖ. В результате формируется типичная модель деформации МК с неполным смыканием створок, что характерно для появления ИМР [6, 10].
Фиброзное кольцо МК является еще одним этиологическим компонентом ИМР у больных ИМ. В результате проведенных исследований отмечено, что у пациентов ИМ с ИМР увеличиваются систолическая и диастолическая площади фиброзного кольца МК, а также уменьшается его сократимость при сравнении с аналогичными показателями у пациентов с ИМ без ИМР.
Особенности анатомического строения фиброзного кольца имеют большое значение в развитии
ИДМК у больных ИМ. В наружных отделах фиброзного кольца коллагеновые волокна разделены большим количеством одиночных мышечных пучков [11]. Они заметны даже при макроскопическом осмотре и выглядят как мышечные мостики. Податливость этой зоны является условием, способствующим регуляции размеров левого атриовентрикулярного отверстия в различные фазы сердечного цикла [12]. Фиброзное кольцо действует как регулирующий фактор трансмитрального кровотока. Дилатация кольца, возникающая при ограничении подвижности створок вследствие смещения папиллярной мышцы, способна значительно увеличить силу ИМР [8, 13]. В процессе дилатации фиброзного кольца МК изменяются форма, размер и сфинктерная функция кольца. Выраженность деформации фиброзного кольца МК, по данным некоторых авторов, существенно
больше у пациентов с передним, чем с задним ИМ [14]. Площадь фиброзного кольца в ходе его дилатации увеличивается, а индекс сфинктерной функции уменьшается, что ведет к уменьшению степени сокращения кольца [15].
Таким образом, у больных трансмуральным и крупноочаговым ОИМ в процессе ремоделирования ЛЖ и МК происходят деформация структур клапана и развитие недостаточности МК различной степени тяжести.
Выводы
1. В процессе ремоделирования митрального клапана у больных острым инфарктом миокарда с ишемической митральной регургитацией увеличиваются систолическое верхушечное смешение точки смыкания створок клапанов на 35,7%, дополнительная площадь левого предсердия — на 39,8% и уменьшается сократимость митрального кольца на 24,2% при сравнении с показателями у больных инфарктом миокарда без ишемической митральной регургитации.
2. У больных инфарктом миокарда с ишемической митральной регургитацией отмечается прямая корреляция средней силы между показателями, характеризующими структуры деформированного митрального клапана, и количественными показателями ишемической митральной регургитации. Наиболее сильная корреляция (r=0,628; p<0,0001) наблюдается между величиной смещения точки смыкания створок митрального клапана и фракцией регургитации.
3. В остром периоде инфаркта миокарда происходят наиболее существенные изменения структур митрального клапана с последующей замедленной деформацией структур клапана в подострой стадии заболевания. Локальное изменение формы левого желудочка приводит к смещению папиллярных мышц от плоскости кольца митрального клапана, систолическому прогибу створок и точки
смыкания створок клапана в сторону верхушки левого желудочка с образованием регургитационного отверстия и дополнительного объема в левом предсердии.



